Синтез наноматериалов с использованием пав
Автор: Жеребцов Дмитрий Анатольевич
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Рубрика: Нанотехнологии и наноматериалы
Статья в выпуске: 3 т.19, 2019 года.
Бесплатный доступ
Рассмотрены методы синтеза наноматериалов с применением поверхностно-активных веществ. Приведен краткий анализ и классификация ПАВ. Одним из методов является синтез нанопористых трехмерно упорядоченных оксидных, халькогенидных или металлических наноматериалов в структуре лиотропных жидких кристаллов, формирующихся в высококонцентрированных водных растворах ПАВ. Отмечена пионерская работа 1992 г. по созданию первого мезопористого силикатного материала, послужившая инициатором широкой волны исследований в этой области. Другим методом является использование обратных мицелл ПАВ в углеводородных средах, что позволяет проводить реакции в объеме микрокапель растворов реагирующих компонентов и тем самым уменьшать размер образующихся наночастиц. Для целенаправленного использования ПАВ необходимо знание двойных и тройных диаграмм состояния вода - ПАВ и вода - масло - ПАВ, которые строятся согласно классическим представлениям физической химии о равновесии в двух- и многокомпонентных системах. В обзоре приведены наиболее подробно охарактеризованные двойные и тройные диаграммы состояния, имеющие значение для матричного синтеза. Обсуждены методы исследования диаграмм состояния. Затронуты также близко родственные системы на основе блок-сополимеров, ряд которых также может быть рассмотрен как высокомолекулярные ПАВ. Отдельно рассмотрены оксидные и оксигидроксидные наноматериалы, включающие соединения Si, Al, Ti, Zr, Hf, Nb, Ta, Mn, W, Sn, Ce и смешанных материалов, с матрицей из SiO2, на которую нанесено некоторое количество оксида другого металла: Al, V, Cr, Fe, Zr, Mo, Ni, либо металлические частицы катализаторов: Ag, Pt или Pd, полученные с применением ПАВ в процессе осаждения неорганической фазы. Приведены примеры наиболее упорядоченных мезопористых наноматериалов, образующих трехмерно периодические структуры с открытой пористостью. Предложены пути дальнейшего развития метода матричного синтеза наноматериалов с использованием ПАВ.
Поверхностно-активные вещества, наноматериалы, матричный синтез
Короткий адрес: https://sciup.org/147233927
IDR: 147233927 | УДК: 54.057 | DOI: 10.14529/met190308
Nanomaterials synthesis with the use of surfactants
This review considers the methods of nanomaterials synthesis using surfactants. It provides a brief analysis and classification of surfactants. One of the methods is the synthesis of nanoporous three-dimensional-ordered oxide, chalcogenide, or metal nanomaterials in the structure of lyotropic liquid crystals formed in highly concentrated aqueous solutions of surfactants. The 1992 pioneering work on the creation of the first mesoporous silicate material, which initiated a wide wave of research in this area, is also pointed out. Another method is the use of surfactants` reverse micelles in hydrocarbon media, which allows performing reactions in microdrops volume of reacting components` solutions and thereby reduces the size of the formed nanoparticles. For targeted use of surfactants, it is necessary to know the diagrams of the double and triple diagrams of water-surfactants and water-oil-surfactants state, which are formed according to the classical concepts of physical chemistry about equilibrium in two- and multicomponent systems. This review provides the most detailed double and triple state diagrams, which are important for matrix synthesis. The methods of the state diagrams research are discussed. Close related systems based on block copolymers, a number of which can also be considered as high-molecular surfactants, are also touched upon. Oxide and oxyhydroxide nanomaterials, including Si, Al, Ti, Zr, Hf, Nb, Ta, Mn, W, Sn, Ce and mixed materials compounds, with a matrix of SiO2, on which a certain amount of another metal oxide is deposited: Al, V, Cr, Fe, Zr, Mo, Ni, or metal particles of catalysts: Ag, Pt or Pd, obtained using surfactants in the process of inorganic phase deposition, are considered separately. The review provides examples of the most structured mesoporous nanomaterials, which form three-dimensional periodic structures with open porosity. It suggests ways of further development for the method of nanomaterials matrix synthesis using surfactants.
Текст научной статьи Синтез наноматериалов с использованием пав
Одним из первых мезопористых (нанопо-ристых) материалов, созданным и многосторонне изучаемым в настоящее время, стал MCM-41. Активное изучение мезопористых фаз на его основе началось после открытия и патентования в 1992 г. компанией Mobile Oil Corporation материала под торговой маркой МСМ-41 (Mobil Composition of Matter-41) [76, 13]. Ключевым элементом метода получения МСМ-41 является введение в раствор силиката натрия, из которого осаждают твердую фазу SiO2, поверхностно-активного вещества (бромида цетилтриметиламмония), причем концентрация ПАВ составляет от 10 до 30 мас. %. В такой системе образуется двухфазная смесь из истинного раствора и лиотропной жидкокристаллической гексагональной фазы, в которой молекулы ПАВ образуют плотноупако- ванные цилиндрические мицеллы, ориентированные параллельно друг другу. После кислотного гидролиза в межмицеллярной водной микрофазе жидкого кристалла образуется золь SiO2, который через некоторое время превращается в гель. Полученный силикагель может быть прокален на воздухе для удаления воды и ПАВ. При этом силикагель наследует структуру раствора (точнее, лиотропного жидкого кристалла), в котором он был получен. Диаметр цилиндрических пор можно изменять (от 1,5 до 10 нм), варьируя состав исходного раствора [13]. Такие размеры пор обусловливают высокую удельную площадь поверхности (400–1200 м2/г) и позволяют проникать внутрь каналов силикагеля молекулам газообразных веществ.
Материалы с монодисперсной открытой пористостью используются в качестве носи- телей катализаторов в органическом и неорганическом синтезе. Наиболее ярким примером использования МСМ-41 стало внедрение его в производство высокооктановых бензинов путем каталитической изомеризации нормальных алканов в разветвленные [111]. Это привело к увеличению доли таких бензинов, производимых из тонны нефти, и заметно приостановило потребление нефти в мире в конце 1990-х и снизило рост цен на нефть.
Этот успех показал перспективность использования ПАВ в получении наноматериалов. В дальнейшем работы по матричному синтезу привели к созданию подобных наноматериалов на основе оксидов, гидроксидов и оксигидратов других элементов.
-
1. Применение поверхностно-активных веществ для синтеза наноматериалов 1.1. Коллоидная химия как часть
нанохимии
Многие наносистемы являются термодинамически неустойчивыми, коагулируют или расслаиваются. Поэтому особого внимания заслуживают термодинамически устойчивые наносистемы; отдельное внимание в данном обзоре уделено самоорганизующимся наносистемам. К ним можно отнести лиотропные жидкие кристаллы и микроэмульсии, а также некоторые блок-сополимеры. При осаждении твердых веществ в водной фазе подобных систем можно получить наноматериалы, наследующие структуру исходных растворов ПАВ. В английском языке для подобных материалов утвердился термин «templated», то есть «построенный по шаблону», задаваемому частицами другого вещества, называемого «template», шаблон. Для систем с ПАВ, являющимися жидкими, часто используется уточняющий термин «soft template», акцентирующий внимание на их жидком состоянии, в отличие от матриц на основе твердых материалов, например, целлюлозы. В русскоязычной литературе многие исследователи используют кальку с английского произношения, называя метод и материалы «темплетными», а вещество, задающее морфологию – «темпле-том». Вместе с тем встречается и термин «матричный синтез», достаточно точно передающий содержание метода. Важной отличительной чертой самоорганизующихся наносистем является их однородность, в частности – узкое распределение размеров наночастиц по величине, высокая упорядоченность их взаимного расположения и единообразие их формы.
Для рассмотрения наноструктурирован-ных материалов и матричного синтеза необходимо начать с коллоидной и физической химии и диаграмм состояния с участием ПАВ.
Поверхностно-активные вещества (ПАВ) – это вещества, адсорбция которых на поверхность раздела фаз приводит к значительному понижению поверхностного натяжения . В наиболее общем случае молекулы ПАВ имеют дифильное строение, т. е. состоят из полярной группы и неполярного углеводородного радикала. Применение ПАВ имеет ключевое значение для синтеза наноматериалов в растворах.
ПАВ делят на четыре основных класса: анионактивные, катионактивные, неионогенные и амфотерные.
Анионактивные ПАВ содержат в молекуле одну или несколько полярных групп и диссоциируют в водном растворе с образованием длинноцепочечных анионов, определяющих их поверхностную активность.
Катионактивными называют ПАВ, молекулы которых диссоциируют в водном растворе с образованием поверхностно-активного катиона с длинной гидрофобной цепью и аниона – обычно галогенида. Преобладающими среди катионактивных ПАВ являются азотсодержащие соединения.
Неионогенные ПАВ не диссоциируют в воде на ионы. Их растворимость обусловлена наличием в молекулах гидрофильных эфирных и гидроксильных групп, чаще всего полиэтиленгликолевой цепи (рис. 1). Полярность одной оксиэтиленовой группы значительно меньше полярности групп ионогенных ПАВ.
нон НОН
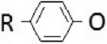
СН2СН2ОСН2СН2О -СН2СН26-йон
Рис. 1. Пример молекулы неионогенного ПАВ с гидрофобным «хвостом» R и сольватирующими молекулами воды вокруг гидрофильного полиэтиленгликольного конца молекулы
Поэтому для придания молекуле требуемой гидрофильности в зависимости от гидрофобного радикала требуется от 7 до 50 оксиэтиленовых групп. Отдельную группу неионогенных ПАВ составляют блоксополимеры этилен- и пропи-леноксидов НО(C2H4O)x(C3H6O)y(C2H4O)хH, где х и у варьируют от нескольких единиц до нескольких десятков. Наиболее изучены высокомолекулярные ПАВ в виде блок-сополимеров этиленоксида и гидрофобных групп, таких как пропиленоксид [1, 10], изопрен [132, 63], полистирол [20]. Неионогенные ПАВ менее чувствительны к солям в растворе, чем анионактивные и катионактивные ПАВ, благодаря этому они чаще используются в мат- ричном синтезе. Большинство неионогенных ПАВ являются вязкими жидкостями при комнатной температуре.
-
1.2. Диаграммы состояния систем вода – ПАВ и вода – масло – ПАВ.
Мезофазы и лиотропные жидкие кристаллы
Помимо простых диаграмм состояния с ограниченной или полной взаимной растворимостью жидкостей (типа вода–спирты), в системах вода – неионогенное ПАВ обнаруживаются промежуточные фазы или мезофазы, находящиеся по составу между водой и чистым ПАВ. Эти фазы термодинамически устойчивы, обладают дальним порядком
а)
б)
а)
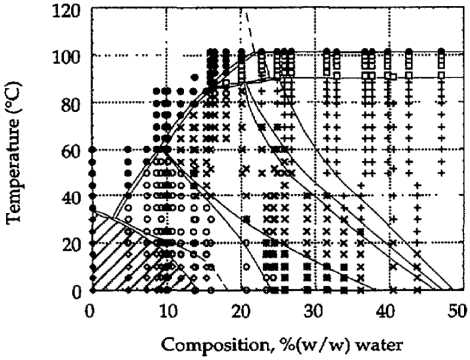
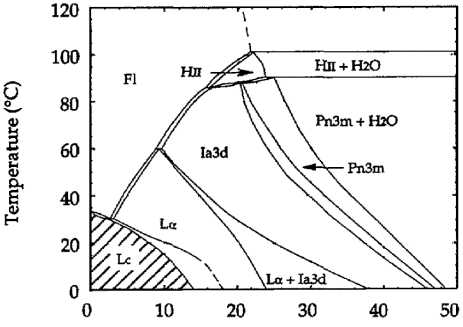
Рис. 3. Состав образцов и температуры съемки рентгенограмм (а). Полученная диаграмма состояния вода – моноолеилглицерат [19] (б): L α – ламеллярная фаза, Ia3d и Pn3m – кубические фазы, H II – обращенная гексагональная фаза, Fl – изотропная жидкость, L с – твердый моноолеилглицерат
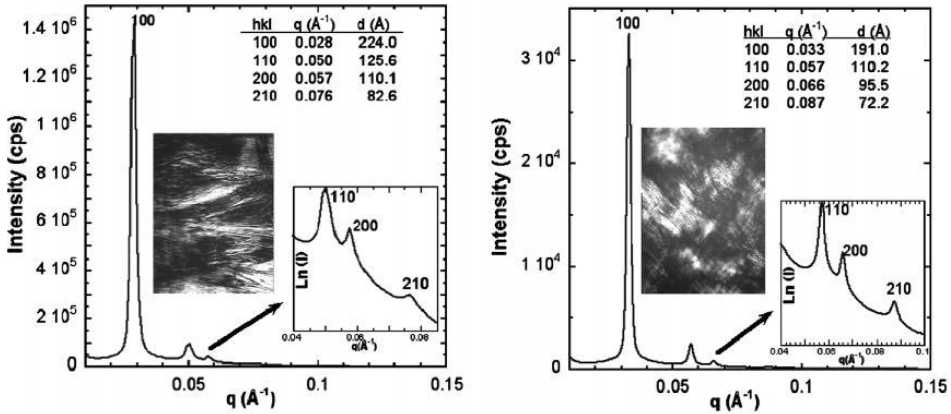
Рис. 2. Рентгенограммы малоуглового рентгеновского рассеяния мезофаз с различными ПАВ [121]: а, б – гексагональная фаза. На вставках – фотографии этих фаз (поляризационная микроскопия)
Composition, %(w/w) water
б)
структуры и называются также лиотропными жидкими кристаллами. Их структуры разнообразны и могут быть изучены рентгеновскими методами. Ввиду того, что параметры структур лежат в диапазоне 5–50 нм, их структура исследуется в первую очередь с помощью малоуглового рентгеновского рассеяния [121] (рис. 2). Известны более 20 различных пространственных групп [43], в которых могут кристаллизоваться лиотропные жидкие кристаллы.
Информацию о структуре двойных и тройных фаз получают по данным светорассеяния и поляризационной микроскопии [159, 121, 112, 155], малоуглового рассеяния рентгеновских лучей [18, 121, 112, 140, 19, 155] (рис. 2, 3) и нейтронов [49], ЭПР [158], ЯМР [18, 65, 144], электропроводности [159, 101, 18, 96, 65] и вязкости [159, 36, 155]. Постепенно увеличивается число полностью или частично построенных двойных диаграмм состояния [137, 19, 118, 91, 46, 93] (рис. 3–9)
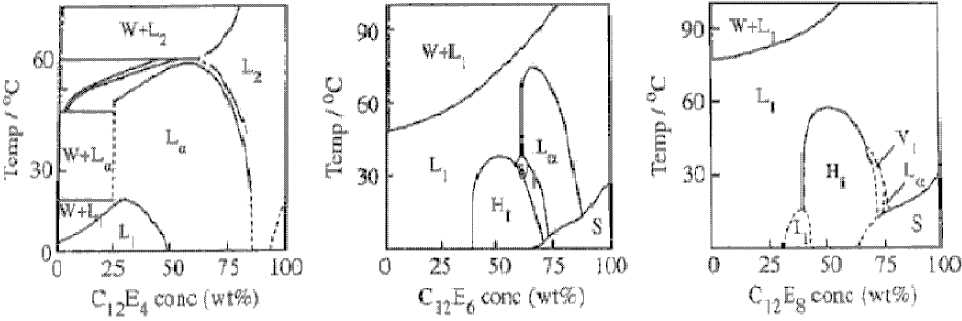
Рис. 4. Диаграммы состояния вода–полиэтиленоксидные эфиры додеканола (узкие двухфазные области не показаны) [91]: W – водная фаза, L 1 и L 2 – прямая и обращенная мицеллярная фаза, L α – ламеллярная фаза, I – кубическая фаза, V 1 – биконтинуальная фаза, S – твердая фаза, Н I – гексагональная фаза
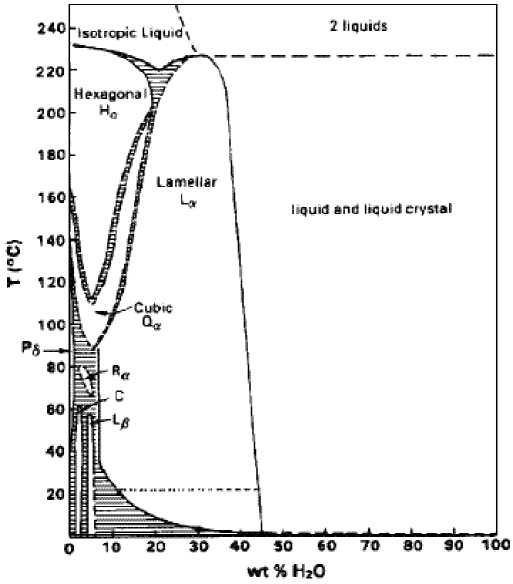
Рис. 5. Диаграмма состояния вода –яичный лецитин [118]: С – кристаллическая фаза, Н α – гексагональная фаза, L α – ламеллярная фаза, L β – ламеллярный гель, Q α – кубическая разупоря-доченная фаза, R α – ромбоэдрическая разупорядоченная фаза
а) б)

а)
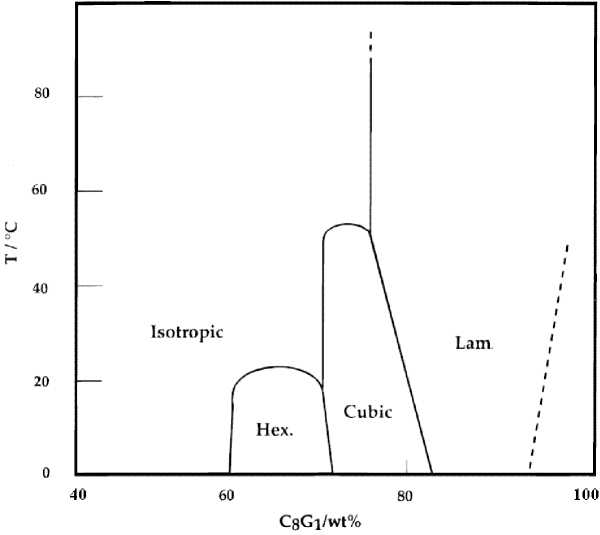
Рис. 7: а – встречная диффузия воды и н-октил-β-D-глюкозида (поляризационная микроскопия; цифры соответствуют температуре, °С). Видны двулучепреломляющие гексагональная (центральная область на фотографиях) и ламеллярная (правая область на фотографиях) фазы, между которыми находится кубическая фаза. Стрелкой показан пузырек воздуха; б – схема диаграммы состояния вода-н-октил-β-D-глюкозид [97] (узкие двухфазные области не показаны): Lam. – ламеллярная фаза, Нex. – гексагональная фаза, Isotropic – изотропная жидкость, Сubic – кубическая фаза. За штриховой линией справа – область равновесия ламеллярной фазы и гидратированных кристаллов
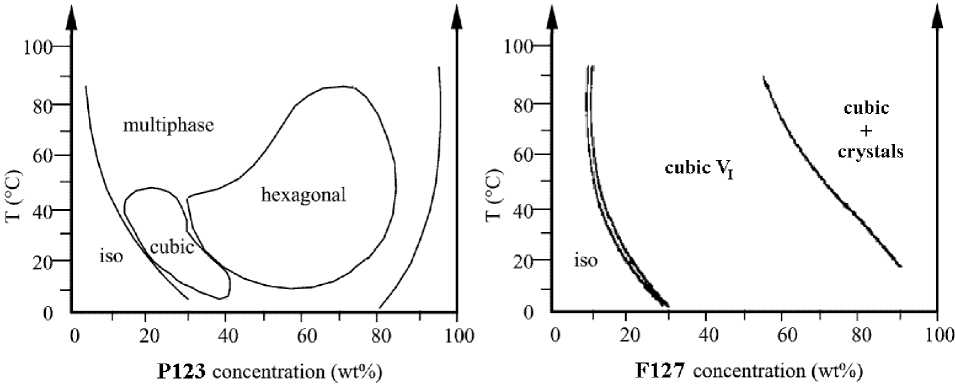
Рис. 6. Схемы диаграмм состояния вода–плюроник Р123 (EO 20 PO 70 EO 20 ) (а) и вода–плюроник F127 (EO 106 PO 70 EO 106 ) (б) [137]
б)
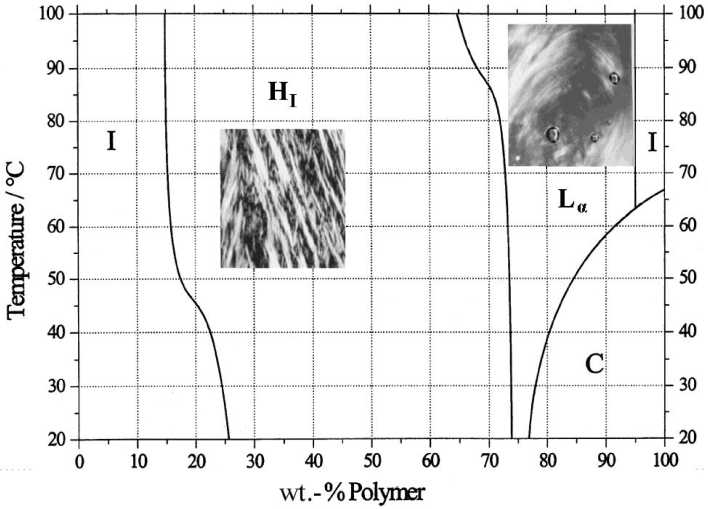
Рис. 8. Схема диаграммы состояния вода–полибутадиен-блок-полиэтиленоксид [46] (узкие двухфазные области не показаны): L α – ламеллярная фаза, Н I – гексагональная фаза, I – изотропная жидкость, С – кристаллическая фаза
а)
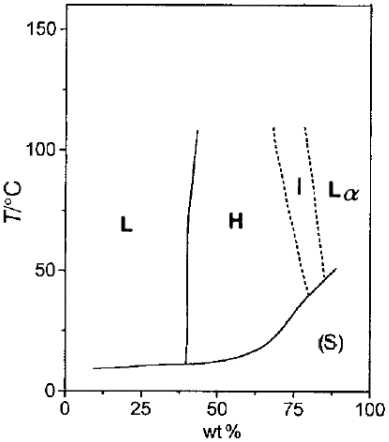
Рис. 9. Схемы диаграмм состояния вода–бромид тетрадецилтриметиламмония (а) и вода–бромид гексадецилтриметиламмония (сокращенно CTAB) (б) [73] (узкие двухфазные области не показаны): Lα – ламеллярная фаза, Н – гексагональная фаза, I – кубическая фаза, L – изотропная жидкость, S – кристаллические фазы
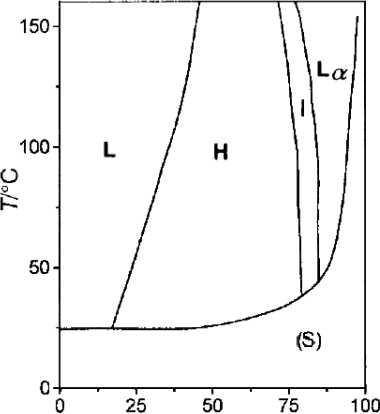
wt%
б)
и изотермических сечений тройных диаграмм [159, 143, 157, 5, 1, 119, 92, 2, 21, 142, 4, 155] (рис. 10–15). В обозначении С 12 Е n символ С 12 означает линейную молекулу спирта С 12 Н 25 ОН, а n означает число звеньев присоединенного к нему этиленоксида (Е) С 2 Н 4 О.
С появлением криогенных держателей для просвечивающих электронных микроскопов начинает развиваться прямое наблюдение структур в замороженных образцах [76, 50, 156]. Быстрое охлаждение жидким азотом позволяет избежать кристаллизации воды и перевести образец в стеклообразное состояние (рис. 16).
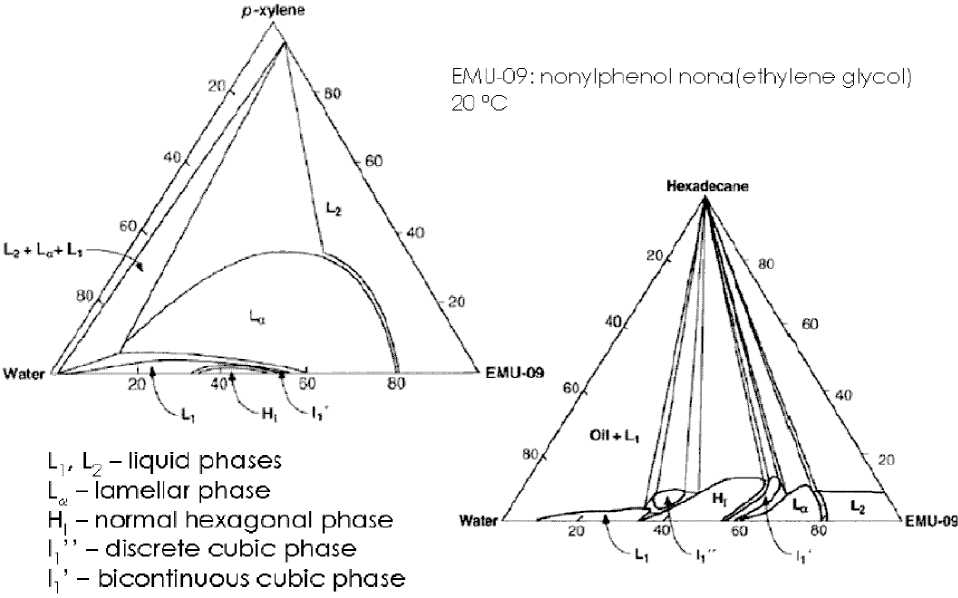
Рис. 10. Изотермические сечения диаграмм состояния вода – параксилол – ЕMU-9 и вода – гексадекан – ЕMU-9 при 20 °С [143]: ЕMU-9 – полиэтиленгликольный (9) эфир нонилфенола, L 1 , L 2 – изотропные жидкости, L α – ламеллярная фаза, Н I – прямая гексагональная фаза, I l " – дискретная кубическая фаза, I l ' – биконтинуальная кубическая фаза
C1SE5
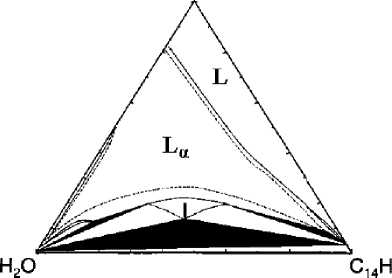
Рис. 11. Изотермическое сечение диаграммы состояния вода – С 12 Е 5 – С 14 Н 30 при 47,5 °С [142]: L – изотропная жидкость, Lα – ламеллярная фаза
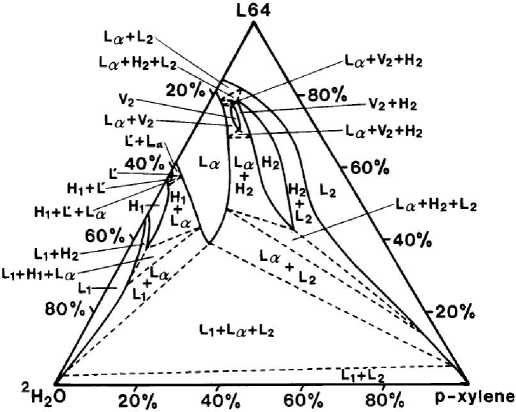
Рис. 12. Изотермическое сечение диаграммы состояния вода–параксилол–L64 при 25 °С [1]: L64 – высокомолекулярное ПАВ – EO 13 PO 30 EO 13 (ЕО и РО – этиленоксид и пропиленоксид), L 1 , L 2 – изотропные жидкости, L' – биконтинуальная жидкость, L α – ламеллярная фаза, Н 1 и Н 2 – прямая и обращенная гексагональные фазы, V 2 – биконтинуальная кубическая фаза (Ia3d, гироидная)
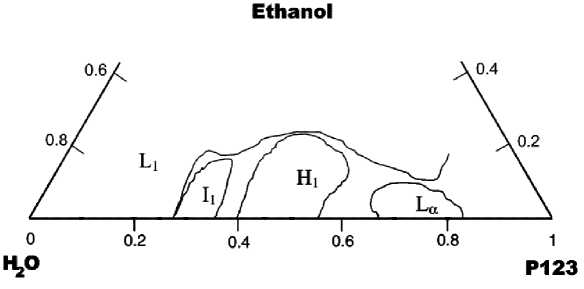
Рис. 13. Схема изотермического сечения диаграммы состояния вода – плюроник Р123 (EO 20 PO 70 EO 20 ) при 23 °С [119]: L 1 – изотропная жидкость, L α – ламеллярная фаза, Н 1 – гексагональная фаза, I 1 – кубическая фаза
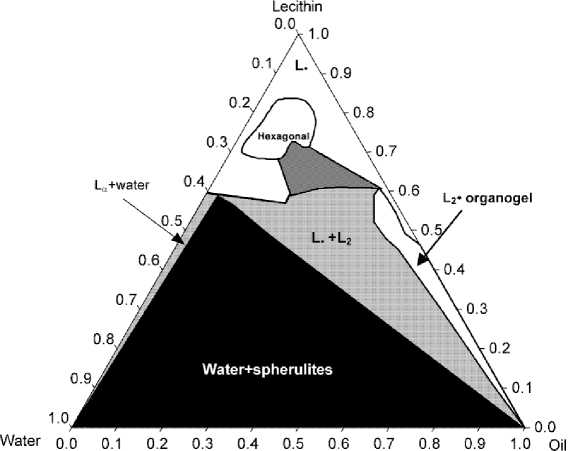
Рис. 14. Схема изотермического сечения диаграммы состояния вода–лецитин– изопропилпальмитат при 25 °С [5] (концентрации приведены в молярных долях)
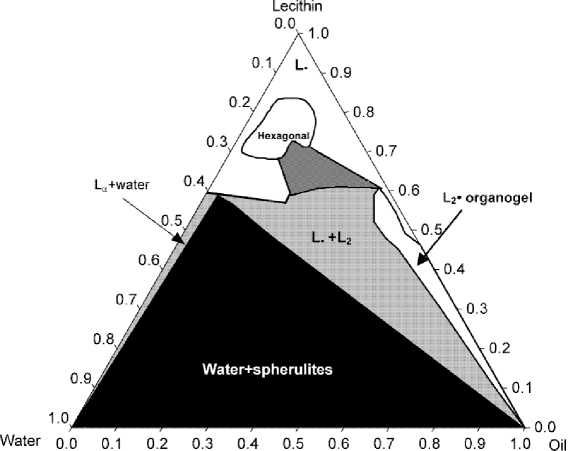
Рис. 15. Схема изотермического сечения диаграммы состояния вода–паракси-лол–P84 при 25 °С [2]: P84 – высокомолекулярное ПАВ – EO 19 PO 44 EO 19 (ЕО и РО – этиленоксид и пропиленоксид), L 1 , L 2 – изотропные жидкости, L α – ламеллярная фаза, Н 1 и Н 2 – прямая и обращенная гексагональные фазы, I 1 и I 2 – прямая и обращенная кубическая фаза (Im3m и Fd3m соответственно), V 1 и V 2 – прямая и обращенная биконтинуальные кубические фазы (обе Ia3d, гироидные)

а)
Рис. 16. Мицеллы (а) в быстрозамороженном растворе вода–плюроник F127 (5 мас. %) [76] и капли эмульсии яичного лецитина (б) в воде (1,2 мас. %) [136] (просвечивающая электронная микроскопия при 90К)
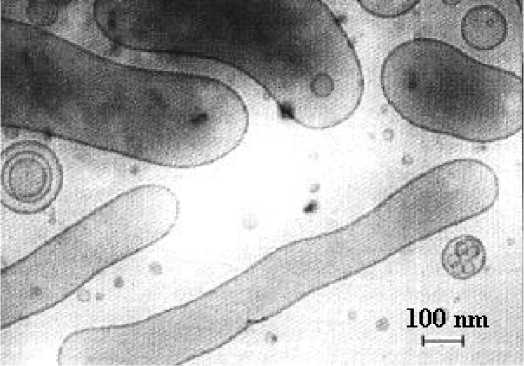
б)
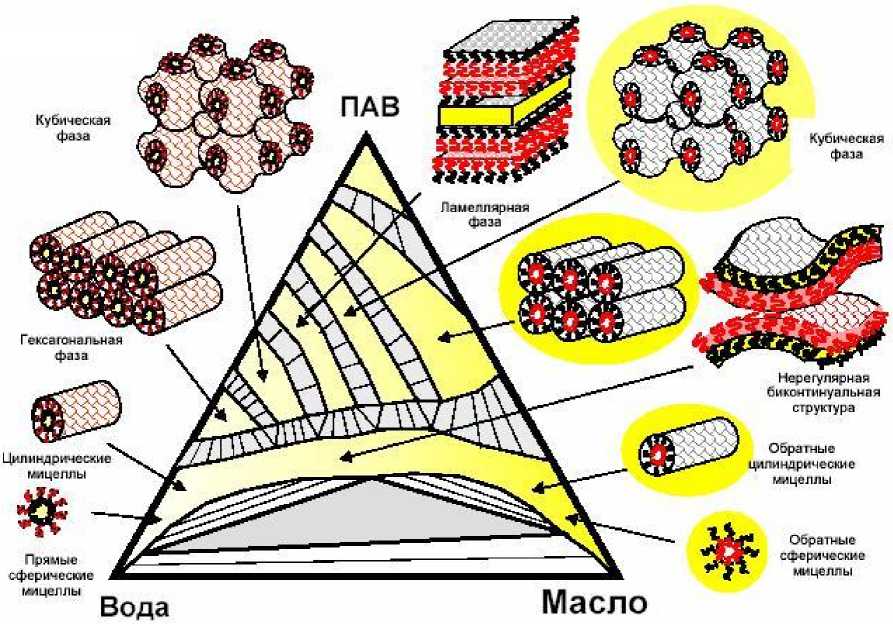
Рис. 17. Схема изотермического сечения системы вода–масло–ПАВ в общем виде [29]
В обобщенном виде рассмотренные выше варианты диаграмм состояния систем вода– масло – ПАВ представлены на рис. 17. Тем не менее следует отметить, что на схеме не обозначены все известные типы жидкокристаллических структур, которых известно более 20 [43].
В синтезе мезопористых матричных материалов наиболее часто используемыми ПАВ являются бромид цетилтриметиламмония C16H33N(CH3)3Br [33], плюроники: Р123 [10], F127 [76, 137, 78], L64 [1], Triton X-114 C8H17C6H4O(C2H4O)8H [47].
Бромид цетилтриметиламмония (CTAB) был исторически первым ПАВ, примененным для матричного синтеза, и остается наиболее употребительным и сейчас. У этого вещества есть шесть важных преимуществ, вытекаю- щих из диаграммы состояния его с водой (см. рис. 9б). Во-первых, жидкокристаллические фазы, им образуемые, устойчивы до температур более 150 °С. Это важно в случае гидротермального синтеза или гидротермальной упрочняющей обработки материалов, полученных при комнатной температуре. Во-вторых, фаза, равновесная с водным раствором, – гексагональная, и мезопористые материалы, получаемые на ее основе, имеют практически важную морфологию с открытой пористостью и высокой механической прочностью. В-третьих, эта фаза – единственная равновесная с водным раствором, что важно при проведении синтеза при нескольких температурах, когда на разных этапах тип структуры не должен изменяться.
В-четвертых, при изменении температуры концентрационные границы области гомогенности гексагональной фазы изменяются незначительно. В-пятых, область гомогенности очень широкая (30–50 % мас.), что косвенно свидетельствует о термодинамической устойчивости гексагональной фазы. И в-шестых, образование этой фазы начинается уже при 20 % мас. СТАВ в воде, что обусловливает его меньший расход и, с другой стороны, обеспечивает обилие воды в межмицеллярном пространстве. В случае матричного синтеза монолитных материалов высокая доля воды в гексагональной фазе позволяет ввести в нее больше реагентов для образования золя, которые смогут образовать более плотный и механически прочный гель.
Исходя из этих критериев, высокоперспективны для матричного синтеза гексагональных материалов и другие длинноцепочечные гомологи СТАВ, кроме них – полибу-тадиен-блок-полиэтиленоксид (см. рис. 9), а также, вероятно, другие аналоги этого блок-сополимера с участием полностью углеводородного блока и блока с высокой гидрофильностью. Блок-сополимеры пропиленоксида и этиленоксида недостаточно изучены, однако некоторая доля гидрофильности пропиленоксидной группы, по-видимому, ответственна за более узкие области гомогенности гексагональных фаз и более высокие концентрации полимера (30–60 % мас.) в воде, необходимые для существования ЖК фаз. В противоположность им полибутадиен-блок-полиэтилен-оксид образует в воде гексагональную фазу уже при его содержании 15–20 % мас., причем область ее существования простирается до
65–75 % мас., а по температуре – от 20 до 100 °С (см. рис. 8).
Блок-сополимеры различного состава имеют больше перспектив для матричного синтеза, чем низкомолекулярные ПАВ, еще и в силу их способности сохранять свою архитектуру в разнообразных растворителях. Жидкокристаллические фазы на основе низкомолекулярных ПАВ при разбавлении, к примеру этанолом, быстро теряют дальний порядок и переходят в изотропную жидкость. Полимерные ПАВ к воздействию неводных растворителей намного более устойчивы. Так, например, ряд успешных синтезов мезопори-стых материалов был проведен на основе неводных растворов [55, 146, 139, 99, 106, 70, 131, 114, 78, 32, 44, 105, 115, 84, 85]. Плюро-ники P123 или F127 растворялись в этаноле, к растворам добавлялся легко гидролизующийся хлорид металла (TiCl 4 , ZrCl 4 , SnCl 4 , TaCl 5 , WCl 6 ), после чего тонкий слой раствора (пленка) гидролизовался и гелировался при взаимодействии с влагой воздуха [146]. При использовании вместо этанола воды гидролиз этих хлоридов происходит настолько быстро и экзотермично, что никакого гомогенного раствора или золя получить не удается [78].
Многие авторы склоняются к тому, что полученные при комнатной температуре гели увеличивают свою механическую прочность и температурную устойчивость при старении в мягких гидротермальных условиях (60–120 °С) [54, 153]. Процессы упрочнения межчастичных контактов в геле при этом схожи с таковыми, происходящими при прокаливании его при 150–200 °С. Вместе с тем гидротермальная обработка при слишком высокой температуре (150–250 °С) или при слишком большой выдержке приводит к превращению аморфного или нанокристаллического мезопористого оксигидратного материала в намного более плотные и крупнокристаллические макропористые оксидные тела с потерей дальнего порядка мезопор [16]. Аналогично и прокаливание при 250–500 °С приводит к подобным результатам. Ввиду очень малых размеров зерен материала и соответственно высокой площади поверхности рекристаллизация их начинается при гораздо более низких температурах, чем крупных порошков.
-
1.3. Эмульсии и микроэмульсии
При рассмотрении возможных равновесных фаз в системах вода–масло–ПАВ нельзя обойти вниманием микроэмульсии. Микро- эмульсии – это многокомпонентные жидкие коллоидные системы (микрогетерогенные жидкости), характеризующиеся термодинамической устойчивостью. Обычно микроэмульсии прозрачны или слабо опалесцируют и образуются самопроизвольно при смешении двух жидкостей с ограниченной взаимной растворимостью (в простейшем случае – воды и углеводорода) в присутствии мицеллообразующих ПАВ. Размер частиц дисперсной фазы (микрокапель) обычно составляет 10–100 нм.
В плоскости треугольника составов (рис. 18) кривая отделяет область I существования однородной (в макроскопическом смысле) микроэмульсии от областей, где система расслаивается.
Однородная фаза может представлять собой либо равномерную смесь (ко-солюбили-зат) всех компонентов (рис. 18а), либо бикон-тинуальную микроэмульсию MI (рис. 18б). Микроэмульсия MI представляет собой на- бухшую мицеллярную систему вода–масло– ПАВ, которая в зависимости от условий (состав, температура, природа компонентов) способна равновесно сосуществовать с растворами I’ и I” (область трехфазного равновесия II).
Мицеллярные системы на основе воды и масла (области I’ и I”) хорошо описываются моделью сферических монодисперсных невзаимодействующих микрокапель, равномерно распределенных в дисперсионной среде, а микроэмульсии MI не описываются сферической моделью. Для них предложено несколько моделей, из которых наибольшее распространение получила модель губчатой структуры с хаотическим распределением микрообластей воды и масла, разделенных тончайшими пленками (бислоями) ПАВ (рис. 19).
Применение микроэмульсий обусловлено их способностью поглощать большие объемы воды и углеводородной жидкости. Микро-
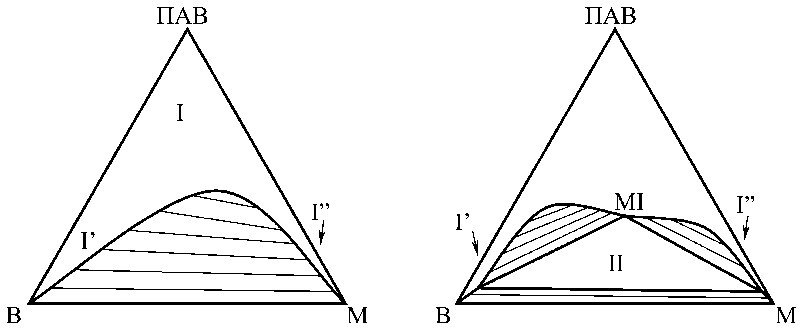
Рис. 18. Схемы изотермических сечений в системах вода–масло–ПАВ: В – вода, М – масло
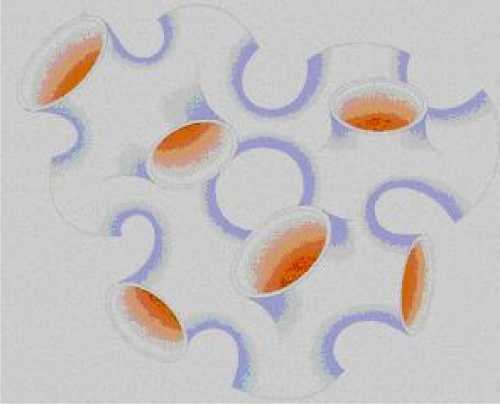
Рис. 19. Биконтинуальная модель микроэмульсии [28]
эмульсии обладают эффективным моющим действием, являются удобной формой для диспергирования лекарственных средств, растворителей, служат средой для проведения химических реакций. Ввиду большой научной и практической значимости тройные (и более сложные) системы типа вода–масло–ПАВ активно изучаются во всем мире экспериментально [157, 34, 13, 100, 160, 53, 112, 21, 40, 104, 30, 17] и теоретически [52, 28] (рис. 19, 21).
В системах, состоящих из двух несмеши-вающихся жидкостей типа вода–масло, ненулевое поверхностное натяжение между двумя жидкостями обуславливает уменьшение энергии системы с уменьшением площади поверхности, их разделяющей. Это приводит к стремлению капель приобрести сферическую форму, а также к их стремлению сливаться. В обоих случаях уменьшается удельная, приходящаяся на единицу массы, площадь границы раздела фаз.
При добавлении третьего, поверхностноактивного компонента, в системе вода– масло обычно увеличивается взаимная растворимость, уменьшается величина поверхностного натяжения. Поверхностное натяжение достигает нуля при концентрации, соответствующей полному взаимному растворению компонентов. При приближении к этой концентрации эмульсия не только не расслаивается, но и наблюдается явление самопроизвольного эмульгирования при контакте жидкостей. В системах с очень низким межфазным натяжением на форму капель эмульсии оказывают ранее не учитываемые слабые пространственные факторы, такие как форма молекул, их ассоциация в предпочтительном направлении, сольватация. Размер капель более не стремится к увеличению, принимая определенный размер (несколько единиц нанометров), а сами капли организуются в фазу микроэмульсии.
-
1.4. Блок-сополимеры
Со структурами лиотропных жидких кристаллов тесным образом связаны структуры блок-сополимеров (рис. 20, 21). Между этими двумя классами веществ сложно провести границу: высокомолекулярные ПАВ (плюро-ники), являясь в водном растворе основой для образования лиотропных жидких кристаллов, сами являются блок-сополимерами. С другой стороны, добавление к блок-сополимерам растворителей в небольших количествах не разрушает их архитектуру, а приводит к набуханию, увеличению объема одного (или обоих) из блоков. В лиотропных жидких кристаллах также в определенных пределах возможно добавлением масла (воды) увеличивать размер (диаметр, толщину) мицелл без изменения типа структуры. В обоих случаях наблюдаются достаточно широкие области гомогенности. Однако при превышении концентрации растворителя в одной из микрофаз (или изменении температуры [27, 109]) происходит образование новой архитектуры блок-сополимера [79, 125, 132, 45, 62, 63, 135, 56], чаще всего в последовательности, соответствующей схеме на рис. 20 (см. также рис. 24). Практически та же последователь-
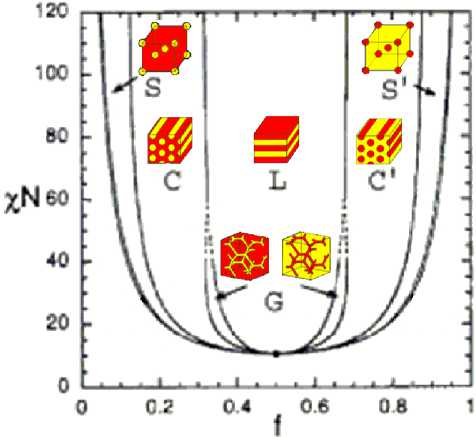
Рис. 20. Обобщенная структурная диаграмма блок-сополимеров [79]
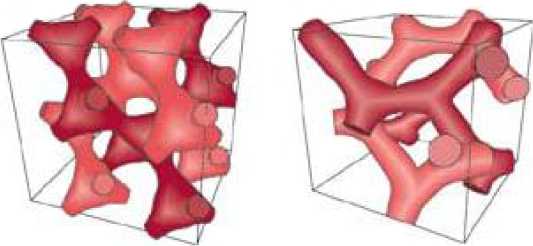
а) б)

в)
Рис. 21. Биконтинуальная двойная алмазная структура (а), биконтинуальная гироидная структура (б), наблюдаемые в блок-сополимерах и жидких кристаллах [161], и гексагональная фаза (в) в полистирол-блок-полиэтилене [88]
ность смены структуры с изменением состава наблюдается и в системах вода–ПАВ (см. рис. 17). На способности лиотропных жидких кристаллов и блок-сополимеров включать в свой состав посторонние низкомолекулярные вещества основаны методы матричного синтеза.
Разнородные блоки в блок-сополимерах стремятся образовать микродомены из звеньев одного сорта, формирующие специфическую надструктуру. На тенденцию к микросепарации влияют многие факторы, прежде всего молекулярная масса блоков, их соотношение и величина сродства друг к другу. Архитектура блоков в различных системах мономеров обнаруживает значительную схожесть (см. рис. 20). На гипотетической диаграмме блок-сополимера, состоящего из звеньев А и В, в координатах f–χN, где f – объемная доля мономера, χ – параметр, характеризующий взаимодействие А и В, N – число звеньев в молекуле, нанесены области существования гомогенного раствора (внизу), а также фаз со сферическими (S, S’), цилиндрическими (C, C’), гироидными блоками (G, G’, рис. 21) и ламеллярной (L) морфологией. Между однофазными областями существуют узкие двухфазные переходные области, на рисунке для простоты опущенные. Размеры составляющих одного блока (диаметр цилиндра или сферы, толщина ламеллы) могут составлять от 5 до 300 нм. Кроме показанных наиболее типичных структур известны и другие, например, кубическая структура, шутливо названная первооткрывателями «кошмар сантехника» (plumber nightmare) [63, 42] (рис. 22). Она состоит из бесконечных взаимно перпендикулярных «труб», идущих вдоль ребер куба и соединяющихся в его вершинах, причем материал состоит из двух таких взаимнопроникающих трехмерных сеток.

Рис. 22. Модель кубической структуры «кошмар сантехника» [63]
Структура «кошмар сантехника» образуется в многокомпонентной системе на основе блок-сополимера полиизопрен-б-полиэтилен-оксид (PI-b-PEO) и низкомолекулярных прекурсоров (INORG) неорганической основы будущего скелета (рис. 23).
Для более сложных блок-сополимеров, например, с тремя блоками А, В и С, могут наблюдаться и другие структуры [123] (рис. 24). Химия полимеров себя далеко не исчерпала и продолжает развиваться [6].
Наиболее широко для получения блок-сополимеров используют анионную или свободнорадикальную полимеризацию [3, 48, 31], например, при синтезе ПС-б-ПИ (полистирол-блок-полиизопрена) [113], ПИ-б-ПЭО (поли- изопрен-блок-полиэтиленоксида) [3], ПБ-б-ПЭО (полибутадиен-блок-полиэтиленоксида) [30], ПГМА-б-ПЭО (полигексилметакрилат-блок-полиэтиленоксида) [87]. Подобные сополимеры с характерной архитектурой используют для синтеза неорганических и гибридных ор-ганическо-неорганических материалов [125, 132, 45, 62, 63, 135, 107].
Наиболее изучены из них мезопористые силикаты. Схема синтеза представлена на рис. 25. Блок-сополимер ПИ-б-ПЭО растворяется в органическом растворителе, смешивается с эпоксидным мономером, содержащим триметоксисилановую группу, после чего растворитель испаряют, а мономер полимеризуют. В зависимости от соотношения ПИ-б-ПЭО и
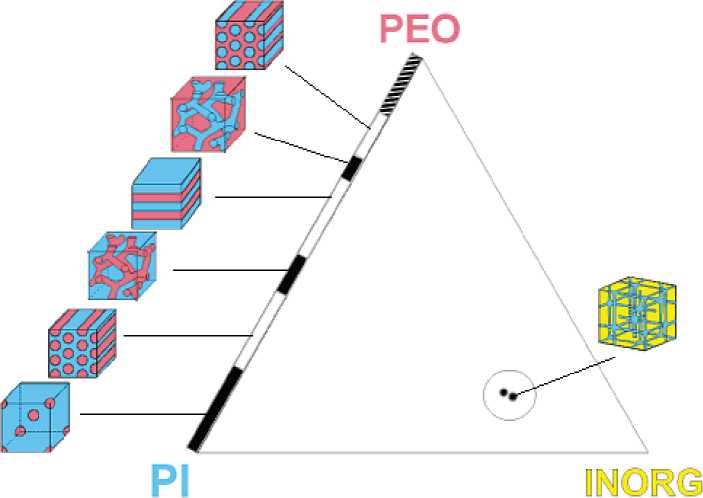
Рис. 23. Схема псевдотройной диаграммы с областью образования структуры «кошмар сантехника»

Рис. 24. Возможные структуры три-блок-сополимеров [123]
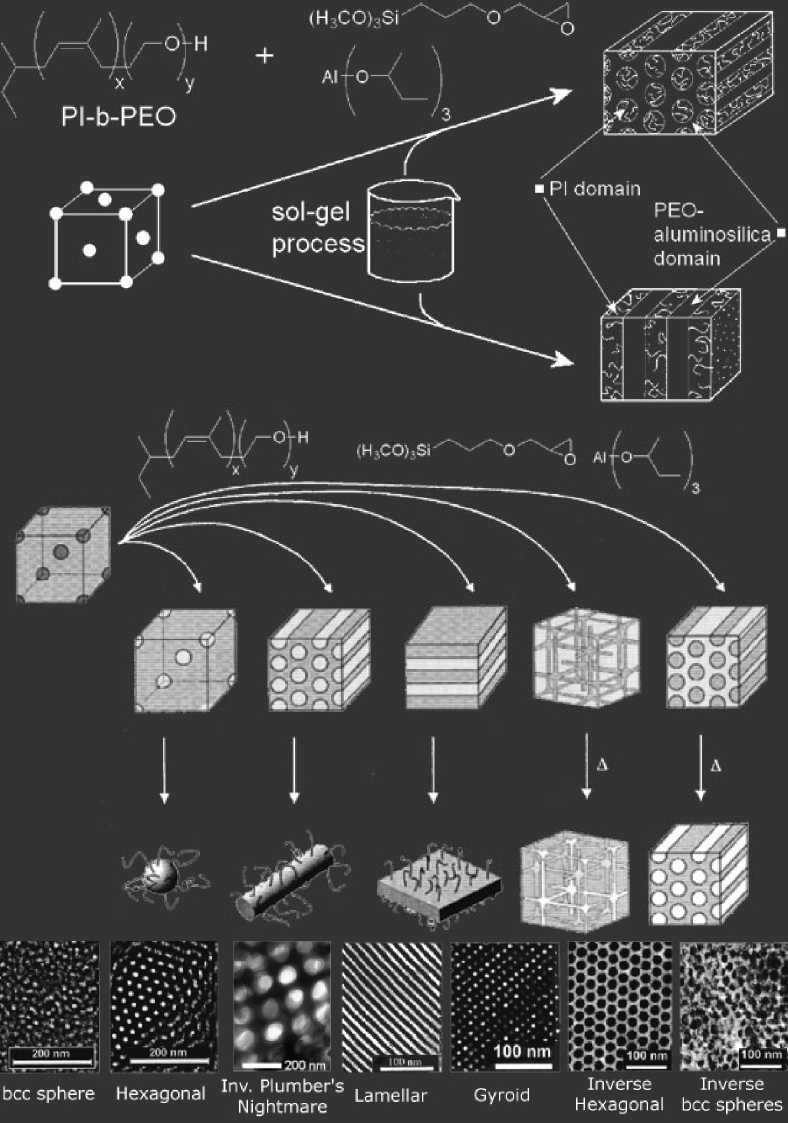
Рис. 25. Схема получения алюмосиликатных мезопористых материалов внутри блоков полиэтиленгликоля блок-сополимера полиизопрена и полиэтиленгликоля [132]
эпоксида можно получить различные структуры. В качестве дополнительного модифицирующего компонента, растворяемого в смеси, можно использовать алкоксиды алюминия. Далее материал гидролизуется во влажном воздухе. Две микрофазы, образующие теперь блок-сополимер, – это почти чистый полиизопрен и полиэтиленоксид с эпоксид- ными олигомерами с силанольными группами, способными к поликонденсации с соседними силанольными группами. Высушенная и гидролизованная пленка блок-сополимера прокаливается на воздухе при медленном нагревании до 300–500 °С для образования силикатного каркаса, наследующего морфологию блок-сополимера. Молекулы алкоксидов алюминия позволяют модифицировать кремниевые звенья и образовывать после прокаливания алюмосиликаты. Удельная площадь поверхности полученного после прокаливания материала составляет 295 м2/г.
Из материалов, перспективных для матричного синтеза, следует отметить полисти-рол-блок-полиэтиленоксид, появление которого на рынке, по мнению экспертов Евросоюза, должно было произойти в 2008 г.
Дальнейшее развитие данного направления может быть связано с получением материалов с высокоориентированной текстурой. Ориентация термотропных жидких кристаллов изучена достаточно подробно (в постоянных электрическом или магнитном поле), однако в изучении лиотропных жидких кристаллов делаются только первые шаги. Так, были предприняты малоуспешные попытки ориентирования механическим продавливанием через капилляр или вращением в зазоре между ротором и статором [41, 94, 86, 11, 102], пропусканием постоянного электрического тока через фазу на основе термотропного ЖК [69, 122]. Однако твердых наноматериалов с выраженной текстурой почти нет. В отличие от термотропных лиотропные жидкие кристаллы позволяют модифицировать свой состав, включая соли, кислоты, щелочи, органические соединения в общем количестве до 70 % мас.
Тем не менее есть положительный опыт текстурирования лиотропных фаз и материалов, получаемых на их основе. При приложении постоянного электрического поля напряженностью 150 В/мм к заключенному в тонкий капилляр (сечением 1×1 мкм) раствору ПАВ–ТЭОС–Н 2 О удалось ориентировать гексагональную фазу и выделяющийся в ней гель SiO2 в материал с величиной разориентировки доменов менее 20° [130].
В другой работе [129] приложением сильного магнитного поля (11,7 Тл) удалось ориентировать гексагональную фазу в аналогичном растворе объемом 3×5×10 мм со степенью совершенства текстуры 78 %. Для ламеллярной фазы в 50 % мас. растворе перфто-роктаноата калия в капилляре диаметром 0,5 мм удалось достичь высокой текстуры в относительно слабом поле 0,4 Тл [66].
Медленное охлаждение изотропного жидкого раствора до температуры существования жидкокристаллической фазы в сильном магнитном поле (1,4 Тл) способствует ориенти- рованию всей массы ЖК вдоль поля [64]. Иногда прибегают к многократному нагреву и охлаждению в пределах 0,5–1 °С выше и ниже температуры плавления ЖК при постоянном воздействии поля. Известен случай, когда такой метод не привел к текстурированию материала, но длительная выдержка (2 месяца) в поле ЯМР-спектрометра привела к ориентации всего объема (несколько миллилитров) гексагональной лиотропной ЖК фазы, даже несмотря на охлаждение на 26 К ниже точки ее плавления [14].
При медленном гидролизе водного раствора силиката натрия и ПАВ в сочетании с интенсивным перемешиванием была продемонстрирована возможность получать вытянутые вдоль оси гексагональной фазы жидкокристаллические «нити» диаметром 200– 300 нм [82].
Введение металлических элементов непосредственно в состав цепи блок-сополимера возможно при использовании специальных мономеров. Так был получен полистирол-блок-полиферроценилэтилметилсилан с цилиндрическими доменами последнего в матрице из полистирола [80].
Еще одним способом получения высокоупорядоченных наноматериалов служит полимеризация в кристаллах. В качестве мономера в составе лиотропной жидкокристаллической фазы могут выступать сами молекулы ПАВ, если они, например, содержат двойную углерод-углеродную связь, способную к полимеризации [110].
-
1.5. Метод матричного синтеза
Лиотропные жидкие кристаллы (и имеющие сходную пространственную архитектуру блок-сополимеры) могут быть использованы как трехмерная матрица, в домены которой возможно вводить дополнительные вещества и проводить с ними химические превращения, приводящие, в частности, к образованию твердых фаз. Твердыми фазами могут быть неорганические вещества, а также полимеры, которые наследуют морфологию исходной матрицы (жидкого кристалла, блок-сополимера или микроэмульсии). Вследствие этого метод создания таких материалов называется матричным (или темплетным) синтезом.
Одним из первых мезопористых (нанопо-ристых) матричных материалов, созданных и многосторонне изучаемых в настоящее время, стал MCM-41 [76, 13]. Полученный силикагель был прокален для удаления воды и ПАВ.
Важным оказалось то, что материал унаследовал морфологию раствора (точнее, лиотропного жидкого кристалла), в котором он был получен. Диаметром пор можно управлять (от 1,5 до 10 нм), изменяя состав исходного раствора [13]. Эти размеры обусловливают высокую удельную площадь поверхности материала (400–1200 м2/г).
В дальнейшем работы по матричному синтезу [75] привели к созданию подобных наноматериалов на основе оксидов и гидроксидов Si [82], Al [146, 26, 117, 47, 10, 147, 78, 105, 115], Ti [146, 57, 106, 148, 71, 44, 103, 128], Zr [55, 98, 146, 24, 67, 99, 57, 120, 128, 58, 84, 85], Hf [146], Nb [7, 146], Ta [8, 146], Mn [127], W [146], Sn [146], Ce [67] и смешанных материалов с матрицей из SiO 2 , на которую нанесено некоторое количество оксида другого металла: Al [83], V [38], Cr [116], Fe [77], Zr [32, 51], Zr, Mo и Ni [51], либо металлические частицы катализаторов: Ag [138], Pt или Pd [81, 90].
Сообщалось также о матричном синтезе совместным осаждением алюмосиликатных [151], алюмотитанатных [131, 134], алюмо-цирконатных [72], цирконосиликатных [124], титаносиликатных [152], титаноцирконатных [71], церийцирконатных [126, 67], титанфосфатных материалов [15].
Полученный матричным синтезом мезо-пористый Al 2 O 3 успешно модифицировали нанесением Cu 2 O [133], оксидов V [25], наночастиц Au [147], Pt [22], введением NiO [70]. На мезопористый ZrO 2 также наносили наночастицы Au [57, 58], Pd [128, 67], вводили Na 2 O [84], MnO 2 [24], V 2 O 5 [57], WO 3 /Fe 2 O 3 /Pt
[111], H 2 SO 4 [55, 108]. На TiO 2 наносили Au и V 2 O 5 [57], Pd [128].
Поверхность МСМ-41 можно модифицировать не только неорганическими, но и прививаемыми к ней органическими группами. Так, с помощью обработки триметилхлорси-ланом поверхность покрывается Si(CH 3 ) 3 -группами, что придает ей гидрофобность [149]. Обзор мезопористых материалов дан в работах [81, 90], материалов на основе Al 2 O 3 – в работе [22].
Остроумие проявили исследователи [9], применив матричный синтез на основе гомогенной гексагональной фазы для получения мезопористой платины. Создав в ЖК фазе высокую концентрацию H 2 PtCl 4 , они провели ее электрохимическое восстановление на золотом катоде. Полученная пленка платиновой губки толщиной 300 нм сохранила структуру жидкого кристалла, в котором она росла, с порами диаметром 2,5 ± 0,15 нм и толщиной стенок 2,5 ± 0,2 нм (рис. 26). Температура электроосаждения составляла 25 °C, а раствор содержал 42 мас. % C 16 E 8 , 29 мас. % воды и 29 мас. % H 2 PtCl 6 .
В свою очередь, можно сделать вывод, что гальваническое осаждение благородных металлов может служить новым методом для подтверждения структурных характеристик жидкокристаллических фаз, в которых они были получены. Альтернативой платине может быть предложено более дешевое серебро, восстановленное из нитрата, хорошо растворимого в воде и многих органических жидкостях. Еще более дешевой альтернативой может оказаться электрохимическое травление

а)
б)
Рис. 26. Платиновая губка (просвечивающая электронная микроскопия): а – вид вдоль каналов, б – вид поперек каналов
полированной поверхности анода, например, из никеля, меди, серебра или нержавеющей стали в лиотропном жидком кристалле, содержащем поваренную соль. Во всех случаях после отмывки катода (или анода) дистиллированной водой возможно изучить расположение и размеры гальванически нанесенных выступов (или ямок травления) с помощью сканирующего электронного или туннельного микроскопа.
Помимо перечисленных применений ме-зопористые темплетные материалы исследуются для применения в качестве мембран [150], сенсоров влажности [60, 12], диэлектрических покрытий для электрических и оптических микросхем [61, 74].
Известные матричные способы получения нанопористых оксидных материалов можно разделить по условиям приготовления и по типу исходных реагентов. Первые материалы типа МСМ-41 были получены специалистами по цеолитам в автоклавах при температурах до 150 °С. Многие последователи также прибегают к высоким температурам и давлениям. Однако поскольку силикагель образуется и при более низкой температуре, множество работ выполнено с использованием стандартной стеклянной посуды при комнатных температурах. Более того, при рассмотрении диаграмм состояния вода –ПАВ очевидно, что многие жидкокристаллические фазы переходят в изотропную жидкость при температуре выше 100 °С. Напротив, наибольшее число различных ЖК фаз образуется при низких температурах.
По форме образцов можно выделить работы с монолитными материалами, гелирую-щими в сосуде (пробирке, стакане, колбе, кювете), и на образцы, подготовленные для специфических физических измерений. В большинстве случаев это пленки и покрытия, получаемые окунанием стеклянной пластинки в золь.
Чтобы освободить поры полученного материала, ПАВ после окончания матричного синтеза удаляют выжиганием или выжиганием после отмывки. Во втором случае качество материала получается выше, в первую очередь по величине удельной поверхности, однородности пор по размеру, наличию дальнего порядка в расположении пор, т. е. по меньшему разрушению структуры. Действительно, известно, что при сушке гелей большие капиллярные силы, действующие на стенки пор, вызывают сжатие и коллапс исходных агрегатов дисперсной фазы и значительное уменьшение кажущегося объема геля (иногда в десятки раз). Для уменьшения разрушений воду (поверхностное натяжение 72,0 мН/м при 25 °С), присутствующую в порах, замещают промывкой на жидкость с меньшим поверхностным натяжением, например, этанол (22,0 мН/м) или ацетон (22,7 мН/м) [ХЭ]. Еще более кардинальное решение заключается в применении сверхкритической сушки геля.
Для удаления ПАВ из геля обычно применяют длительное промывание этанолом (несколько суток) в экстракторе Сокслета с обратным холодильником. Тем не менее значительная часть ПАВ (веществ, известных хорошей сорбируемостью) не удаляется полностью из гелей (веществ, известных как хорошие сорбенты). Поэтому остающиеся количества ПАВ окисляют до воды и СО2 при нагревании на воздухе до 350–500 °С, иногда в течение нескольких суток. Для более эффективного удаления органических веществ из неорганических гелей при сравнительно низких температурах 150–250 °С иногда применяют их обработку в атмосфере, содержащей озон.
По типу исходных веществ – прекурсоров твердой фазы – синтез можно разделить на проводимый из солей и из алкоксидов. В первом случае источником золя является соль соответствующего элемента (например, силикат натрия, алюминат натрия, сульфат алюминия, хлорид цирконила, нитрат марганца). При реакции с осадителем (кислотой, щелочью, раствором аммиака) выделяются необходимые оксид, гидроксид или оксигидрат, а в качестве побочного продукта – соль натрия или аммония. При последующей очистке и удалении этой соли могут возникать дополнительные сложности. Например, при промывке водой гель может пептизироваться, кроме того, многократная промывка потребует много времени, а конечная чистота все равно может оказаться недостаточной и негативно повлиять на свойства материала. В силу этих причин во многих случаях авторы стремятся использовать более дорогие соединения, как, например, тетраэтилортосиликат Si(OEt) 4 – ТЭОС [37, 60, 23, 150, 152, 151, 12, 141 95, 154, 116, 73], тетраметилортосиликат Si(OМе) 4 [73, 39, 33, 35, 145], Si(OBut) 4 [74], тетрабутоксититан Ti(OBut) 4 – ТБТ [148, 44,
103], Ti(OiPr) 4 [15, 106, 57, 131, 134, 114, 71], Ti(OEt) 4 [128], триизопропилалюминат Al(OiPr) 3 [72, 147, 83], Al(Osec-But) 3 [47, 25, 70, 131, 134, 78, 105, 115], пентаэтилтанталат [8], Zr(OPr) 4 [55, 72, 98, 99, 57, 58, 128, 51, 84, 85], Zr(OBut) 4 [71]. Продуктами гидролиза данных эфиров являются соответствующие спирты, легко удаляемые из материала при сушке. Определенным ограничением для использования данных веществ служит слишком высокая скорость реакции их с водой, приводящая к разогреву раствора (вплоть до кипения), а также к выпадению требуемых гелей слишком быстро (за доли секунды), так что относительно медленно образующаяся мицеллярная высокоупорядоченная матрица не успевает сформировать в материале дальний порядок. Понизить скорость гидролиза в ряде случаев удается разбавлением раствора нейтральным растворителем (обычно этанолом), однако это снижает устойчивость мицеллярной (ЖК) структуры вплоть до образования изотропного раствора. Иногда альтернативой может служить замена алкоголятов с короткими алкильными радикалами (метильными, этильными) на более устойчивые бутильные, трет-бутильные, фенильные. Однако единого решения для всех материалов нет и в каждом случае необходимы индивидуальные исследования. Иногда возможно применение уникальных для каждого элемента растворимых в воде исходных соединений, например, (NH 4 ) 2 [Zr(CO 3 ) 3 ] для синтеза мезопористого ZrO 2 [124].
Альтернативой алкоголятам могут быть легко гидролизующиеся до гидроксида под действием воды хлориды металлов (TiCl4, ZrCl4, SnCl4, TaCl5, WCl6 и др.) с проведением синтеза в неводных растворах, например, этанольных [146]. Однако в неводных растворителях многие низкомолекулярные ПАВ чаще всего образуют изотропные растворы без образования ЖК фаз. Поэтому в таких случаях используют высокомолекулярные ПАВ.
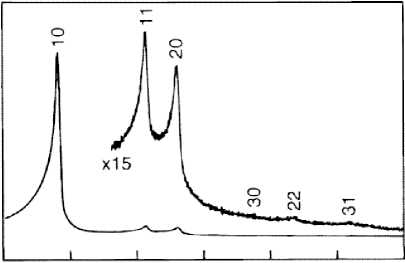
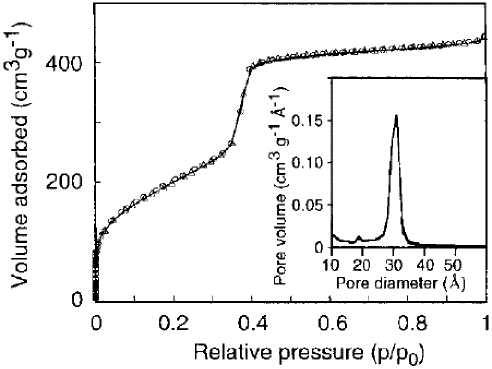
Применение вместо ТЭОС 1,2-бис(триме-токсисилил)этана [59, 89] и 1,4-бис(триэто-ксисилил)бензола [68] позволило авторам создать материал, включающий в структуру кремнийкислородного скелета прочно химически связанные с ним группы –CH 2 –CH 2 – или бензольное (пара-фениленовое) кольцо –С 6 Н 4 –. Такой материал окисляется до SiO 2 только выше 400 °С [68]. При использовании вместо ТЭОС 3-аминопропилтриэтоксисилана также может быть получен материал с привитой аминоалкильной группой [154]. Эти работы расширили класс гибридных (органическо-неорганических) материалов. Медленное проведение синтеза (более 20 ч) позволило авторам работы [59] получить высокоупорядоченный материал с четкими картинами электронной микроскопии, рентгеновской и электронной дифракции (рис. 27, 28), с характерной ступенью на кривой адсорбции, соответствующей конденсационному заполнению пор одинакового диаметра (см. рис. 28).
Морфология получаемых матричным синтезом материалов характеризуется зернами размером от 1 мкм до поликристалличе-ских монолитов 10–50 мм. Анализ составов реакционных смесей показывает, что зернистые образцы были получены в растворах с

а)
Рис. 27. Изображения материала типа МСМ-41, полученные с помощью просвечивающей (а) и растровой (б) электронной микроскопии. На врезке – данные электронной дифракции [59]

б)
1 2 3 4 5 6 7
26 (degrees) а)
б)
Рис. 28. Рентгеновская дифрактограмма материала типа МСМ-41 [59] (а) и изотерма адсорбции азота на нем при температуре кипения азота (б). На врезке – рассчитанная кривая распределения пор по размеру
низким содержанием ПАВ (1–5 м ас . %) [ 59 ] , тогда к а к мон о ли тн ые мате ри а лы п о лу че н ы в растворах с 10– 7 5 ма с . % ПАВ [ 39] . При с рав н ени и с соответс тву ющ и ми фа зов ыми д иаграммами вода – ПАВ о че в и д н о, что п ервая г руп п а ма те ри а л ов п олу че н а в д ву хфа зн ой о б ла с ти ( и зотроп ный ра ств ор + жи д к и е к ри ста ллы ) , п ри че м п ри ма лом с од е р жа н и и ЖК ф а зы и ча с то п ри н е прерыв н ом п е рем е ш и в ании, а вторая – в обла с ти, б ли зк ой к од нофаз н ой , и бе з пе ре меш и в а н ия в п ери од гелирова- н и я. Отча с ти п ри ме н е н и е п е рем еш и ван ия и н али чи е о д н оф а зног о л и отроп н ого жи дк ог о криста лл а в за и моиск л ю ч а ю т д ру г дру га , по ск оль к у в яз к ость б о льши н с тв а ЖК фа з на стольк о в ысок а , что п р и ме н е н и е меш а л ок, н апри ме р м агн итны х, не в оз мож но. Вы падение геля в ме ж м и ц е л лярном простра н с тв е е ще больше повышает вязкость.
Другая п ричи н а приме нени я раз ба в ле н н ы х рас тв оров за клю ч а етс я в том, что ме з о- п ори с ты е ма те риа лы ча ще в с е го п ре д н а зн а ч е н ы д ля и с п ыта н и я в к аче с тв е а д с о рб е н тов, ка та ли за то ров и н ос и те ле й к а т а ли за торов. Для этого предпочтительна м елк озе рн и с т ая (размер зерен 1–50 мк м ), а не мон оли тн ая ф орм а п род у к та , обе с пе чи в а ю щ а я н а ли чие круп н ых по р и б ол е е бы с трый д о с ту п жи д ко сте й и га зов ме ж ду зе рн ам и . Б ол ее того, по л у ча е ма я отн ос и те льн о в ыс ок а я мон о д и с п ерс н ос ть оса д ков п озволяе т отк а за тьс я о т о п ера ц и й раз мол а и рас с ев а п о фрак ц и ям.
Подавляющее большинство работ по матричному синтезу представляют собой попытки на основании литературных данных о со- ставах реакционных смесей и условиях синтеза получить один-два образца при каких-либо модификацированных условиях. Лишь небольшая часть работ посвящена физикохимическому исследованию зависимостей «состав исходного раствора – свойство продукта» на ряде из более чем 4 составов. И совсем немногие авторы [9, 26, 145, 17] пытаются связать результаты синтеза наноматериалов с диаграммами состояния вода –ПАВ и вода – масло– ПАВ, используемых в синтезе. Отчасти это вызвано тем, что таких диаграмм состояния построено еще очень мало.
Для образования твердых нанообъектов в растворе необходима малая растворимость введенного компонента. Высокая растворимость быстро приводит к рекристаллизации в более крупные частицы. Малая растворимость не обязательно должна быть таковой изначально. Так, при введении в воду Si(OH)4 (например, пропусканием 1%-ного раствора Na2SiO3 через катионообменную колонку в Н-форме) вначале образуется идеальный раствор Si(OH)4, в котором вскоре начинается полимеризация мономерных звеньев с образованием все более крупных молекул, имеющих все меньшую растворимость в воде и образующих глобулы золя кремниевой кислоты. Аналогично растворимость фенола и формальдегида в воде достаточно высока, однако по мере образования олигомеров и полимеров фенолоформальдегидных смол, имеющих все меньше и меньше гидрофильных групп (–OH и –CHO) на единицу массы, их растворимость в воде быстро падает, что вызывает образова- ние эмульсии. Эмульсионная полимеризация широко используется в производстве полимеров, например, поливинилацетата, водоэмульсионных красок и латексов. Во всех перечисленных случаях образование эмульсии начинается со стадии образования гомогенного раствора мономера в воде.
Наночастицами в растворах могут быть не только органические и неорганические полимеры, но и частицы любых других элементов и соединений: металлов (например, коллоидные растворы золота, серебра, платины), неметаллов (сера, получаемая кислым гидролизом тиосульфатов), солей (галогениды серебра, халькогениды кадмия), оксидов и гидроксидов. Общим критерием для синтеза наночастиц может служить величина их растворимости. Чем она меньше, тем более мелкие частицы можно получить. Как в случаях рав- новесных, так и неравновесных реакций, необходимы высокая степень пересыщения, обусловливающая высокую плотность образующихся зародышей, и малая скорость их роста, вызванная, например, низкой скоростью диффузии (высокой вязкостью среды). Обоими факторами можно управлять в широких пределах, изменяя концентрации реагентов, температуру и вязкость.
Заключение
Из обзора литературы следует высокий потенциал методов матричного синтеза нано-пористых материалов с управляемой упорядоченной структурой при использовании ПАВ и блок-сополимеров. Данное направление находится в начале развития и претерпевает подъем интереса со стороны как органической, так и неорганической химии.
Список литературы Синтез наноматериалов с использованием пав
- P. Alexandridis, U. Olsson, B. Lindman. Self-Assembly of Amphiphilic Block Copolymers: The (E0)13(P0)30(E0)13-Water-p-Xylene System // Macromolecules (1995), 28, 7700-7710. DOI: 10.1021/ma00127a016
- P. Alexandridis, U. Olsson, B. Lindman. A Record Nine Different Phases (Four Cubic, Two Hexagonal, and One Lamellar Lyotropic Liquid Crystalline and Two Micellar Solutions) in a Ternary Isothermal System of an Amphiphilic Block Copolymer and Selective Solvents (Water and Oil) // Langmuir. 14. (1998) 2627-2638. DOI: 10.1021/la971117c
- Allgaier J., Poppe A., Willner L., Richter D. Synthesis and Characterization of Poly[1,4-isoprene-b-(ethylene oxide)] and Poly[ethylene-co-propylene-b-(ethylene oxide)] Block Copolymers // Macromolecules. 30. (1997) 1582. DOI: 10.1021/ma961311q
- I. Amar-Yuli, N. Garti. Transitions induced by solubilized fat into reverse hexagonal mesophases // Colloids and Surfaces B: Biointerfaces. 43. (2005) 72-82. DOI: 10.1016/j.colsurfb.2005.03.011
- R. Angelico, A. Ceglie, G. Colafemmina, F. Lopez, S. Murgia, U. Olsson, G. Palazzo. Biocompatible Lecithin Organogels: Structure and Phase Equilibria // Langmuir. 21. (2005) 140-148. DOI: 10.1021/la047974f


