Синтез твердосплавных материалов в технологическом процессе детонационного напыления
Автор: Ганигин Сергей Юрьевич, Ибатуллин Ильдар Дугласович, Ненашев Максим Владимирович, Якунин Константин Петрович
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Надежность в машиностроении и новые конструкционные материалы
Статья в выпуске: 4-2 т.15, 2013 года.
Бесплатный доступ
В статье приведены результаты исследований процесса синтеза нитрида и карбида титана в канале ствола детонационно-газовой установки. Приводится краткое обоснование требуемых технологических режимов для протекания физико-химических превращений исходного материала – порошка титана в продуктах газовой детонации с избыточным выделением сажи и насыщением азотом. Приведены результаты морфологического и рентгенофазового анализа получаемых покрытий.
Нитрид титана, карбид титана, детонационное покрытие, азид натрия, термохимический синтез, продукты детонации
Короткий адрес: https://sciup.org/148202308
IDR: 148202308 | УДК: 658.562.3
Synthesis of solid alloy substances during detonation spraying process
The research of titanium nitride and titanium carbide synthesis in the barrel detonation-gas system are discussed in the article. A brief rationale for the required process conditions for the occurrence of physical and chemical transformations of the raw material - titanium powder in the gas detonation products with excessive release of carbon and nitrogen saturation. The results of morphological and X-ray analysis of the coatings are discussed in the article.
Текст научной статьи Синтез твердосплавных материалов в технологическом процессе детонационного напыления
Якунин Константин Петрович, кандидат технических наук, младший научный сотрудник кафедры «Технология твердых химических веществ»
Использовались следующие параметры напыления: коэффициент заполнения ствола 60%, отношение кислород/топливо – ½. Коэффициент заполнения был выбран из соображений фиксации сажевыделения именно во фронте детонации, которая проходит по всему объему газовой смеси. Выбранное соотношение кислород-топливо обусловлено стабильным режимом детонации, так как при повышении доли топлива детонационный режим становится неустойчивым. В результате были получены следовые отпечатки ячеистой структуры детонации. СЭМ-фотографии поверхности представлены на рис. 1.

Рис. 1. Сажа, образуемая в стволе установки детонационно-газового напыления
Выделяемые в процессе детонации в указанных режимах частицы сажи имеют средние размеры 60 нм. Сажа может реагировать с частицами напыляемого порошка, образуя в результате термо-химических превращений карбиды металлов. В частности, при использовании в качестве исходного продукта порошкового титана может протекать реакция типа
Ti + C → TiC. (1)
Так как размеры частиц углерода, получаемого из продуктов горения, на порядок меньше частиц порошка титана микронных размеров, при обеспечении необходимых условий будет протекать гетерогенная реакция по поверхности частиц титана с образованием карбида титана. Для оптимизации выхода в продуктах детонации карбида титана необходимо определить технологические параметры напыления, при которых реакция (1) протекает полностью. К таким параметрам относятся: соотношение компонентов газовой смеси топливо/кислород; количество газовой смеси, определяемое коэффициентом заполнения ствола; дистанция напыления, влияющая на время реакции; количество исходного порошка титана. Продуктами горения ацетилена в кислороде являются углекислый газ, оксид углерода (II) СО, сажа, вода. Приведем некоторые характерные реакции при разных соотношениях исходных газов.
С 2 Н 2 :О 2 = 2:1 – недостаток кислорода для полного сгорания ацетилена:
2С2Н2 + О2 = 4С + 2Н2О + 937,5 кДж(2)
С 2 Н 2 :О 2 = 1:1 – недостаток кислорода для полного сгорания ацетилена:
С2Н2 + О2 = С + СО + Н2О + 579,25 кДж(3)
С 2 Н 2 :О 2 = 2:3 – недостаток кислорода для полного сгорания ацетилена:
2С2Н2 + 3О2 = 4СО + 2Н2О + 1379,5 кДж(4)
С 2 Н 2 : О 2 = 2:5 – стехиометрическая реакция
2С 2 Н 2 + 5О 2 = 4СО 2 + 2Н 2 О + 2511,5 кДж (5)
Очевидно, что в реальных условиях сгорания ацетилена в кислороде при недостатке кислорода для полного окисления могут одновременно протекать различные перечисленные выше реакции, а также реакции взаимодействия с участием образующегося водяного пара или углерода, например, Н 2 О + С = СО + Н 2, СО 2 + С = 2СО. Относительное количество этих реакций в общей массе не должно быть велико, поэтому ими можно пренебречь при расчетах. К тому же эти реакции могут быть обратимыми, и направление их протекания сильно зависит от условий в момент детонации (принцип Ле-Шателье).
Как видно из приведенного выше, наибольшее количество углерода образуется при соотношении ацетилен/кислород = 2:1 (реакция 1). Но в реальности данная реакция неприменима к технологии детонационного напыления, так как в продуктах сгорания не хватает газовой фазы, а энерговыделения реакции явно недостаточно для протекания эффективного процесса кар-бидизации. По этим причинам более применима для технологии детонационного напыления реакция 2 (где С2Н2/О2 = 1 : 1).
Используя рассчитанное соотношение топлива и окислителя в технологии карбидизации титана по уравнению Ti + C = TiC (∆Нº TiC = -209 кДж/моль) в процессе детонационного напыления, можно записать суммарное итоговое уравнение (если считать, что весь углерод, образующийся при неполном сгорании ацетилена, полностью будет идти на карбидизацию титана):
С 2 Н 2 + О 2 + Ti = СО + Н 2 О + TiC (5)
Энерговыделение данной реакции ∆Н = ∑ Н прод. -∑ Н реаг. = –788,25 кДж, то есть реакция карбиди-зации титана в условиях детонации ацетиленкислородной смеси будет экзотермическая.
Количество по массе реагирующих веществ для данной реакции определяли, задаваясь известным количеством газовой смеси на основе объема ствола, равного произведению коэффициента заполнения ствола на объем ствола и известных молярных масс компонентов. В результате была определена масса титанового порошка для полного протекания реакции карбидизации m (Ti) = 0,0214 г. Объем требуемого количества титана равен V (Ti) = m (Ti) / ρ Ti = 0,0047 см3. Это значение определяет геометрические размеры челнока дозатора для ввода порошка в ствол детонационной установки. В экспериментах использовался челнок дозатора с лункой для порошка прямоугольной формы с размерами сторон: ширина 8 мм, длина 1,5 мм и стандартной глубина 0,4 мм.
Для повышения производительности целесообразно смещать реакцию горения в сторону восстановительного пламени, повышая выход углерода. Однако это требует тщательных расчетов тепловыделения для выполнения условий плавления используемого порошка титана. В эксперименте выполнялось 1000 выстрелов порошком титана по стальному образцу. На рис. 2 представлен рентгенофазовый анализ полученного покрытия. Структура полученного покрытия представлена на рис. 3. В полученном покрытии присутствуют кристаллические фазы карбида титана. Увеличение выхода карбида титана можно обеспечить путем повышения температуры реагирующих компонентов.

Рис. 3. Структура полученного покрытия в результате синтеза карбида титана при разном увеличении
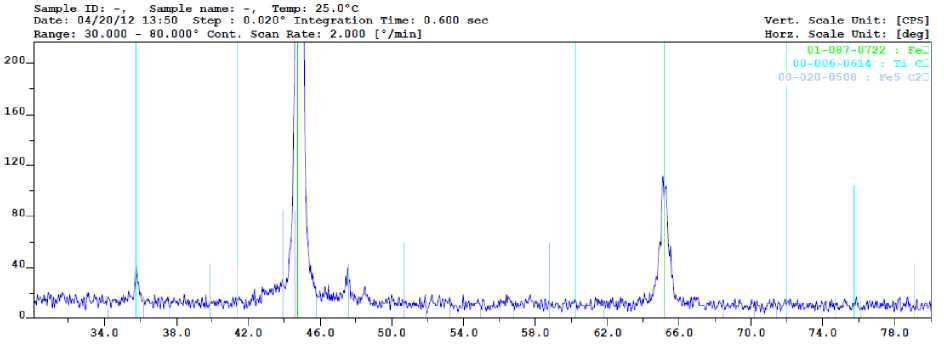
Рис. 2. Дифрактограмма рентгенофазового анализа полученного покрытия в результате синтеза карбида титана на стальной подложке
В ходе исследований установлена возможность протекания в стволе детонационной установки реакций синтеза нитридов металлов на примере нитрида титана. Для осуществления реакции образования нитрида использовался азот, выделяемый в процессе термического разложении азида натрия NaN3 → Na + N2 + N [1]. Считая, что на протекание реакции идет только азот, выделяющийся при разложении азида натрия, определяли массы компонентов, вступающих в реакцию с образованием нитрида титана TiN по уравнению:
3Ti + NaN 3 = 3TiN + Na (6)
Исходные компоненты титан и азид натрия загружаются в челнок дозатора. Необходимая масса порошка титана оказалась равной m (Ti) = 0,0478 г. Таким образом, механическую смесь порошков готовили исходя из соотношения m (Ti)/ m (NaN 3 ) = 3,15. Далее на медную подложку выполняли 300 выстрелов. Для снижения влияния воздушной среды ствол детонационной установки заполняли азотом под избыточным давлением 1,1 атм. Полученное покрытие имело толщину 40 мкм. Масса образованного слоя равна 300 мг. Цвет покрытия черный с налетом желтого цвета. Был проведен рентгенофазовый анализ полученного покрытия (рис. 4).
Из рентгенограммы видно, что побочные продукты типа оксида и гидроксида натрия в нитридах отсутствуют. На данном этапе исследований представленные результаты рентгенофазового анализа подтверждают возможность создания промышленных технологий формирования слоев покрытий нитридов металлов. Топография поверхности покрытия нитрида титана, синтезированного по уравнению реакции (6), представлена на рис. 5.
В целом все возможные гомофазные и гетерофазные реакции так или иначе влияют на весь ход процесса образования конечного продукта – нитрида титана, что приводит к изменению реального выхода конечного продукта от теоретического расчетного количества. Ход этих возможных перечисленных выше реакций обычно трудно предсказуем, но очевидно, что на протекание их оказывают значительное влияние такие параметры системы, как давление, температура, концентрации тех или иных веществ.
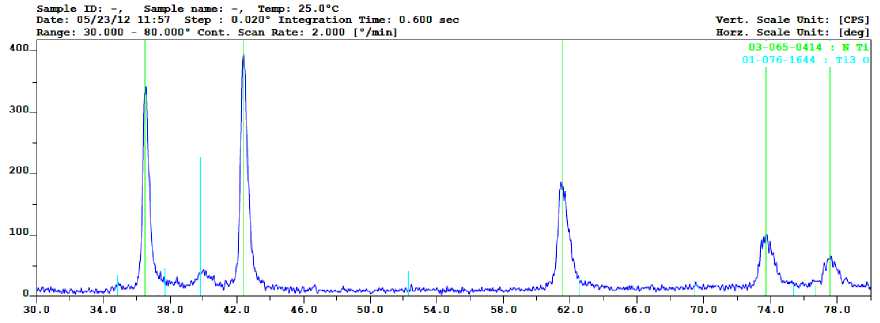
Рис. 4. Рентгенограмма полученного покрытия нитрида титана

Рис. 5. Структура покрытия нитрида титана
Выводы: очевидно, что получение нитридов методом газовой детонации принципиально возможно, но они неизбежно будут загрязнены оксидами металлов (Ti, Na), титанатами, сажей, причем доля получаемых нежелательных продуктов будет весьма значительной в массе покрытия.
Работа проводилась при финансовой поддержке Министерства образования и науки Российской Федерации.
Список литературы Синтез твердосплавных материалов в технологическом процессе детонационного напыления
- Бичуров, Г.В. Азидная технология самораспространяющегося высокотемпературного синтеза микро-и нанопорошков нитридных композиций: монография/Г.В. Бичуров, Л.А. Шиганова, Ю.В. Титова. -М.: Машиностроение-1, 2012. 657 с


