Системная склеродермия, клинические варианты течения
Автор: Муркамилов И.Т., Айтбаев К.А., Юсупов Ф.А., Райимжанов З.Р., Юсупова З.Ф., Юсупова Т.Ф., Хакимов Ш.Ш., Солижонов Ж.И., Хабибуллаев К.К.
Журнал: Бюллетень науки и практики @bulletennauki
Рубрика: Медицинские науки
Статья в выпуске: 2 т.11, 2025 года.
Бесплатный доступ
Системная склеродермия (ССД) - одно из наиболее распространенных аутоиммунных заболеваний среди женщин, с пиком заболеваемости в возрасте 44-55 лет. В ревматологии выделяют несколько клинических форм ССД: диффузную, ограниченную (лимитированную), ювенильную (с началом до 16 лет) и перекрестную (особую) формы. ССД - классическое гетерогенное заболевание с разнообразными клиническими проявлениями и вариантами течения. Наиболее частым первичным симптомом является синдром Рейно, который может быть как первичным, так и вторичным. Развитие ССД в пожилом возрасте требует тщательного лабораторного обследования для исключения онкологических причин. Представлен клинический случай ССД с периодами обострений и ремиссий. У пациентки 58 лет заболевание дебютировало с синдрома Рейно и повышенной активности воспалительных маркеров. Спустя год целенаправленное обследование выявило серологические маркеры ССД, при этом, несмотря на прогрессирование синдрома Рейно, воспалительные маркеры не были повышены.
Системная склеродермия, синдром рейно, кожные изменения, указательные пальцы
Короткий адрес: https://sciup.org/14132076
IDR: 14132076 | УДК: 616-004.616-008.616-07 | DOI: 10.33619/2414-2948/111/27
Systemic scleroderma, clinical variants of the course
Systemic scleroderma (SSc) is one of the most common autoimmune diseases among women, with a peak incidence between the ages of 44 and 55. Rheumatology distinguishes several clinical forms of SSc: diffuse, limited (localized), juvenile (onset before 16 years), and overlap (mixed) forms. SSc is a classic heterogeneous disease with a wide range of clinical manifestations and varied courses. The most frequent initial symptom is Raynaud’s syndrome, which can be either primary or secondary. The onset of SSc in older adults requires thorough laboratory investigations to rule out oncological causes. This article presents a clinical case of SSc with periods of exacerbations and remissions. The 58-year-old patient’s disease began with Raynaud’s syndrome and elevated inflammatory markers. A year later, targeted testing revealed serological markers of SSc, while inflammatory markers were not elevated despite the progression of Raynaud’s syndrome.
Текст научной статьи Системная склеродермия, клинические варианты течения
Бюллетень науки и практики / Bulletin of Science and Practice
УДК 616-004.616-008.616-07
Системная склеродермия (ССД) в последние годы привлекает значительное внимание в ревматологии, поскольку характеризуется прогрессирующим течением, ранней утратой трудоспособности и высоким уровнем смертности [1].
Социально-экономическое бремя ССД связано с ухудшением качества жизни пациентов, изменениями контуров тела вследствие выраженных кожных изменений, а также ранним поражением внутренних органов [2].
Различают несколько клинических форм ССД: диффузную, ограниченную (лимитированную), ювенильную (начало до 16 лет) и перекрестную (особую) [3, 4]. Последняя, известная как “Overlap – Syndrome” в зарубежной литературе, объединяет признаки ССД с проявлениями других аутоиммунных заболеваний. Заболеваемость ССД варьирует от 3,7 до 19 случаев на 1 миллион населения ежегодно [5].
В США этот показатель достигает 19,3 на 1 миллион, тогда как в Кыргызской Республике точная распространенность ССД остается неопределенной. Ограниченная форма ССД встречается гораздо чаще — 45 случаев на 100 тысяч населения [6].
Пик заболеваемости ССД приходится на возраст 44-55 лет, причем женщины болеют в 5-7 раз чаще мужчин [7, 8].
В недавнем исследовании описан случай подострого течения диффузной формы ССД у молодого мужчины [5].
За последние годы во всем мире отмечается рост заболеваемости ССД [9, 10].
Широкий спектр клинических проявлений заболевания вызывает как клинический, так и академический интерес.
Цель исследования – анализ научных публикаций по ССД и описание клинического случая.
Согласно исследованиям, проведенным в Научно-исследовательском институте ревматологии им. В. А. Насоновой, ССД представляет собой классическое гетерогенное заболевание с разнообразными клиническими формами и течением [2, 11, 12]. Механизмы развития ССД связаны с нарушениями клеточной и гуморальной иммунорегуляции, которые играют ключевую роль в патогенезе и прогнозе болезни [12]. Основу заболевания составляет поражение соединительной ткани с преобладанием фиброза и сосудистых изменений по типу облитерирующего эндартериолита [13].
Существует четкая корреляция между лабораторными показателями и клиническими проявлениями ССД. Для болезни характерны специфические изменения кожи, внутренних органов и обширные вазоспастические нарушения.
Синдром Рейно . Наиболее часто диагностируемым проявлением системной склеродермии (ССД) является синдром Рейно, который встречается у значительной части пациентов и характеризуется вазоспастическими нарушениями [14].
На ранних стадиях ССД первыми проявлениями выступают нарушения микроциркуляции и повторяющиеся эпизоды вазоспазмов мелких периферических артерий [2].
Частота и продолжительность этих эпизодов варьируют от 15 до 20 минут и сопровождаются восстановлением кровотока и исчезновением необычной окраски кожи [15].
Исследователи отмечают, что такие сосудистые нарушения стимулируют развитие системных аутоиммунных и воспалительных процессов, которые приводят к активации фиброзирующих изменений и развитию облитерирующей васкулопатии [16]. В дебюте ССД синдром Рейно регистрируется в 90% случаев [17].
Некоторые работы указывают, что возраст начала синдрома Рейно у женщин ниже, чем у мужчин [18].
Практически все пациенты отмечают, что провоцирующими факторами синдрома Рейно являются низкие температуры и психоэмоциональный стресс. Эти наблюдения подтверждаются данными, свидетельствующими о большей частоте синдрома Рейно в странах с холодным климатом [18]. Частота вазоспастических эпизодов также выше зимой, чем летом. Анализ происхождения и клинических проявлений синдрома Рейно подробно представлен в исследовании [18].
Синдром Рейно подразделяется на первичную и вторичную формы. Первичный синдром чаще встречается у молодых людей. При ССД регистрируется вторичный синдром Рейно, который может развиваться в результате приема определенных лекарственных средств и часто выявляется у пациентов с ССД и системной красной волчанкой [19].
Длительное течение заболевания, особенно более 5 лет, приводит к дигитальному ангииту и трофическим нарушениям. Пациенты часто жалуются на онемение, покалывание и боль [20].
Первоначально нарушения наблюдаются в кистях и стопах, но с прогрессированием могут затрагивать сосуды головного мозга, почек, сердца, легких и других органов. В исследовании [21] описан случай поражения сосудов головного мозга у 45-летней пациентки с ССД, что указывает на связь генерализованной формы синдрома Рейно с тяжелым течением заболевания и неблагоприятным прогнозом.
Синдром Рейно может сочетаться с эндокринными заболеваниями, такими как патологии щитовидной железы, паращитовидных желез, надпочечников, гипофиза и сахарный диабет [22].
Существуют данные, что синдром Рейно может отмечаться у родственников первой линии [20].
В некоторых случаях он является единственным симптомом эндокринных нарушений [14]. Кроме того, он может сопровождаться другими аутоиммунными заболеваниями. Описан случай синдрома Рейно у 77-летней пациентки, у которой онемение пальцев рук, утренняя скованность и болезненность в крупных суставах протекала долгие годы, а диагноз ССД был установлен достаточно поздно, после того, как обнаружили высокие титры антител к Scl70 [23]. Эти данные подтверждают, что синдром Рейно – это мультидисциплинарная проблема, требующая участия специалистов различных профилей, таких как сосудистые хирурги, терапевты, ревматологи, эндокринологи и нефрологи.
Ограниченная (лимитированная) форма ССД часто имеет хроническое течение и проявляется синдромом Рейно. Плотный отек кожи кистей считается ранним симптомом ССД, а индурация кожи сигнализирует о прогрессировании заболевания. Со временем кожа становится плотнее, толще, теряет эластичность, появляются участки гипер- и диспигментации, а затем развивается атрофия [16].
У пациентов с длительным течением болезни формируются характерные изменения лица и кистей, включая акроостеолиз, что сопровождается укорачиванием и деформацией пальцев [24].
Практически у всех пациентов со стойким синдромом Рейно развивается склеродактилия вследствие фиброза кожи и околосуставных тканей, а также часто наблюдаются дигитальные язвы, рубцы и контрактуры [25].
Интерстициальное поражение легких. С увеличением продолжительности системной склеродермии (ССД) возрастает частота поражения легких, что сопровождается снижением их диффузионной способности. В литературе описан случай сочетания ССД и ревматоидного артрита у 57-летней пациентки, где поражение легких предшествовало развитию синдрома Рейно с кожными и суставными проявлениями [26]. Этот случай представляет практический интерес, поскольку легочные поражения доминировали в клинической картине, в то время как остальные симптомы были маловыраженными. В микропрепарате кожи у пациентки с ССД были выявлены атрофия эпидермиса, склероз всех слоев дермы с атрофией кожных придатков и мононуклеарная инфильтрация поверхностных слоев дермы [26].
Одним из наиболее серьезных проявлений поражения легких при ССД является интерстициальное поражение легких (ИПЛ), которое наблюдается примерно у 30% пациентов и часто становится причиной смертности [2, 27]. На ранних стадиях ССД легочные симптомы могут отсутствовать. Нередко у таких пациентов развивается неспецифическая интерстициальная пневмония, которая требует госпитализации и выявляется при компьютерной томографии органов грудной клетки [28]. По другим данным, частота ИПЛ при ССД достигает 65-70% [29].
Следует отметить, что ИПЛ чаще встречается у афроамериканцев, а также у пациентов с диффузной кожной формой ССД или в присутствии антител к топоизомеразе 1 (Scl-70). Исследования показывают, что ИПЛ при ССД проявляется, как правило, одышкой, малопродуктивным кашлем и неспецифической интерстициальной пневмонией, диагностируемой с помощью компьютерной томографии [27]. Важно проводить дифференциальную диагностику между ИПЛ, обусловленным ССД, и идиопатическим легочным фиброзом, поскольку тактика лечения в этих случаях различна [26].
Работа Л. П. Ананьевой (2018) подчеркивает, что инфекционные осложнения при ССД возникают реже, чем при других иммуновоспалительных ревматических заболеваниях [30]. Особый интерес вызывает повышенная частота развития рака легких на фоне склеродермического пневмосклероза. В одном из когортных исследований установлено, что рак легких чаще встречается у мужчин с ССД, а также у пациентов с иммуноглобулин G-антителами к антигену Scl-70 [31]. Таким образом, риск развития злокачественных новообразований легких у пациентов с ССД в 3–5 раз выше, чем в общей популяции.
Ранее О. А. Цветкова и соавт. (2014) описали клинический случай 63-летнего пациента с ССД, у которого заболевание изначально проявлялось синдромом Рейно, а затем присоединились респираторные симптомы [32].
Многие исследователи отмечают, что благодаря современным методам терапии тяжелое поражение почек при ССД стало встречаться реже, в то время как легочные изменения стали более заметными в клинической картине [33]. В настоящее время продолжаются клинические исследования, направленные на оценку течения ИПЛ при ССД [34].
Поражение почек. Прогрессирующее течение системной склеродермии (ССД) приводит не только к необратимым фиброзным изменениям кожи, но также к поражению почек, сердца, желудочно-кишечного тракта и других органов. Согласно данным отдельных авторов, поражение почек при ССД выявляется у 19% пациентов [35].
Морфо-функциональные изменения почек, особенно в случае ранней фатальной формы, известной как «истинная склеродермическая почка», являются одной из основных причин смерти у больных с быстро прогрессирующей формой заболевания [36]. Описаны случаи, когда резкое ухудшение функции почек потребовало экстренного, а затем и программного гемодиализа [37].
Склеродермический почечный криз может проявляться такими симптомами, как внезапно возникшая ретинопатия, артериальная гипертензия, клубочковая гематурия, протеинурия, рецидивирующий отек легких, олигурия или анурия [38,39]. При этом, снижение фильтрационной функции почек может наблюдаться даже при отсутствии явных признаков мочевого синдрома [40]. В некоторых случаях поражение почек и легких может быть первым проявлением ССД, что подтверждают описанные клинические случаи, включая недавно описанный случай атипичного почечного криза у 63-летней пациентки [41].
Отмечается также высокий риск развития острого повреждения почек у пациентов с ССД [42]. Важно учитывать, что такие изменения, как изолированное снижение фильтрационной функции почек, ренального функционального резерва и увеличение индекса сопротивляемости междольковых артерий, указывают на прогрессирование хронической болезни почек [43]. Ухудшение функции почек значительно снижает общую выживаемость пациентов с ССД.
В последние годы активно обсуждается роль сосудисто-эндотелиальной дисфункции в патогенезе поражения почек при ССД. Также следует учитывать, что на развитие дисфункции почек могут влиять длительный прием лекарственных средств, таких как D-пеницилламин и нестероидные противовоспалительные препараты (НПВП).
Поражение сердца. На ранних стадиях системной склеродермии (ССД) сердечные изменения часто остаются недиагностированными, что затрудняет точную оценку частоты кардиоваскулярных осложнений. По данным предыдущих исследований, частота поражения сердца при ССД варьируется от 15% до 35% [44].
Целенаправленные исследования показали, что клинические проявления поражения сердца при ССД включают фиброз миокарда желудочков, нарушения возбудимости и/или проводимости, миокардит, перикардит и сердечную недостаточность [43].
Клинически поражения пищевода при ССД проявляются изжогой, отрыжкой, дисфагией и загрудинной болью. В ряде исследований, при эндоскопическом обследовании, сниженный тонус нижнего пищеводного сфинктера обнаружен у всех пациентов с рефлюкс-эзофагитом, а также у 64% пациентов без клинических жалоб [47].
В работе А. Е. Каратеева и соавторов (2014) описаны клинические, эндоскопические и морфологические проявления поражения пищевода при ССД [48].
В исследовании 479 пациентов (93,7% женщины, 6,3% мужчины), эзофагит выявлен более чем у половины пациентов. У 20% больных наблюдались эрозии и язвы слизистой оболочки пищевода, а длительное течение заболевания повышало риск развития значительной структурной перестройки слизистой [48]. Кроме того, те же исследователи установили частоту пищевода Барретта у пациентов с ССД на уровне 20,1% [49].
Зарубежные данные также указывают на кишечную метаплазию у 18% пациентов с ССД [50].
Современные исследования сосредоточены на изучении нарушений моторно-эвакуаторной функции пищевода при ССД [51].
Нарушения моторики пищевода коррелируют с тяжестью течения ИПЛ, а степень снижения тонуса пищевода связывается с возникновением кишечной метаплазии [53].
В проспективном исследовании установлено, что риск развития рака пищевода у пациентов с пищеводом Барретта составляет 3% в год в течение трёхлетнего периода наблюдения [31].
Ранее считалось, что опухолевые формы ССД встречаются редко. Однако, при их сочетании можно рассматривать различные сценарии: развитие заболеваний может происходить независимо; склеродермия может быть индуцирована опухолью или наоборот; опухолевый процесс может быть следствием иммуносупрессивной терапии [54].
Следовательно, пациенты с ССД в пожилом возрасте должны проходить тщательное обследование для исключения злокачественных новообразований [55].
Наряду с поражениями ЖКТ, интерес вызывает связь ССД с состоянием костной ткани. Исследования Р. Т. Алекперова и Н. В. Торопцовой демонстрируют, что снижение минеральной плотности костей у пациентов с ССД варьирует от 32 до 77%, а частота остеопоротических переломов — от 2% до 38% [56].
К факторам риска остеопороза при ССД относятся возраст, менопауза, избыточный вес, высокие уровни С-реактивного белка (СРБ), фибриногена, интерлейкина-6, длительный прием глюкокортикоидов, ингибиторов протонной помпы и дефицит витамина D [57, 58].
Приводим описание клинического случая. Пациентка А., 58 лет, жительница сельской местности, обратилась в клиническую базу кафедры факультетской терапии Кыргызская государственная медицинская академия им. И. К. Ахунбаева. Жалобы при поступлении: прогрессирование изменений кожи и усиление онемения кистей рук (Рисунок 1).
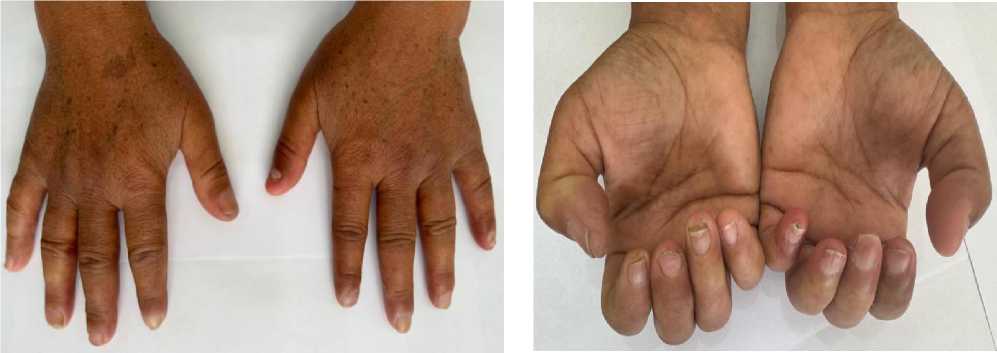
Рисунок 1. Уплотнение, пигментации, цианоз кожи кистей. Начальный остеолиз концевых фаланг. Фото из архива И. Т. Муркамилова
Анамнез заболевания. В течение 3-х лет страдает суставным синдромом с болями преимущественно в мелких суставах, купируемыми приемом НПВП. На протяжении 2 лет отмечает утреннюю скованность длительностью 1–1,5 часа. Ранее обращалась к терапевту и ангиохирургу, где был выявлен синдром Рейно. Периодически принимала трентал и ацетилсалициловую кислоту с положительным эффектом.
Обследования. Декабрь 2023 г.: повышение СОЭ (60 мм/ч), анемия (Hb 115 г/л), гиперфибриногенемия (5,6 г/л), повышение СРБ (10,6 мг/л). Ревматоидный фактор не повышен. Отрицательные маркеры вирусных гепатитов и сифилиса. ЭКГ и рентгенография органов грудной клетки без особенностей. УЗДГ пальцевых артерий: выраженный вазоспазм. Апрель 2024 г.: повышение СРБ (48 мг/л), СОЭ 36 мм/ч, картина вазоспазма пальцевых артерий при УЗДГ. Hb 124 г/л.
Анамнез жизни: 4 беременности, все протекали без осложнений, роды самостоятельные. Климакс наступил в 38 лет. Профессиональная деятельность — художница на протяжении 20 лет.
Физикальное обследование: рост 160 см, вес 65 кг, ИМТ 25,3 кг/м². Радиальные кожные складки вокруг рта, гиперпигментация, диффузное уплотнение кожи, дигитальные язвы, сгибательные контрактуры пальцев кистей, уплотнение и пигментация кожи голеностопных суставов (Рисунок 2). Периферических отеков нет. Артериальное давление 100/60 мм рт. ст., ЧСС 72 уд/мин.
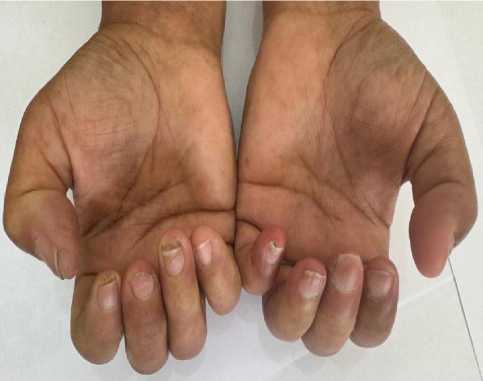
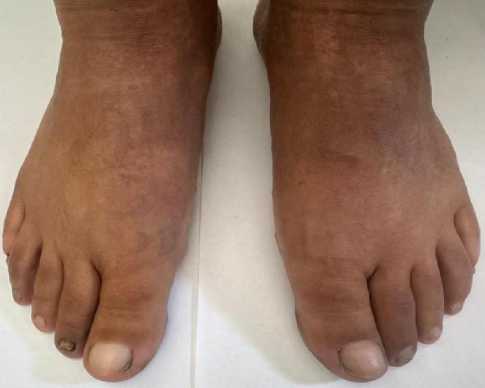
Рисунок 2. Уплотнение, пигментации, цианоз кожи кистей и стоп. Начальный остеолиз концевых фаланг и стоп. Фото из архива И. Т. Муркамилова
Лабораторные данные (при обращении): Hb 120 г/л, СОЭ 17 мм/ч, тромбоциты, лейкоциты в норме. Печеночные трансаминазы, электролиты, креатинин, липидный профиль – в пределах нормы. Уровень витамина D – 22,4 нг/мл (умеренный дефицит). Паратгормон – 100 пг/мл (норма до 75 пг/мл). Антиядерные антитела на клетках HEP-2: центромерное свечение, Т>1:640, центромерный пептид CENP-B положительный (++).
Инструментальные исследования: УЗДГ сосудов кистей: картина вазоспазма. ЭКГ и рентген грудной клетки – без особенностей.
На основании изложенных выше данных пациентке выставлен клинический диагноз: Системная склеродермия, диффузная форма, хроническое течение, активность II степени. Склеродактилия, кальциноз мягких тканей кистей и стоп, акростеолиз. Фиброзная сгибательная контрактура II-III пальцев кистей, гиперпигментация кожи, телеангиоэктазии, синдром Рейно II ст.
Рекомендованная терапия: Глюкокортикоиды, вазоселективные блокаторы кальциевых каналов, антиагреганты.
Заключение. Клинический случай интересен тем, что системная склеродермия дебютировала суставным синдромом и синдромом Рейно. Отмечено значительное снижение воспалительных маркеров после обследования, но сохранялись вазоспастические нарушения. Это демонстрирует вариабельность течения заболевания, которое может протекать с обострениями и ремиссиями
Информированное согласие на публикацию описания клинического случая и использования медицинских данных в научных целях получено.
Исследование не имело спонсорской поддержки. Конфликт интересов отсутствует.
Авторы несут полную ответственность за предоставление окончательной версии рукописи в печать. Все авторы принимали участие в разработке концепции статьи и написании рукописи. Окончательная версия рукописи была одобрена всеми авторами.
Список литературы Системная склеродермия, клинические варианты течения
- Ананьева Л. П. Новые направления в лечении системной склеродермии (системного прогрессирующего склероза) // Доктор.Ру. 2021. Т. 20. №7. С. 32–39. https://doi.org/10.31550/1727-2378-2021-20-7-32-39
- Насонов Е. Л. Российские клинические рекомендации. Ревматология. М.: ГЭОТАР-Медиа, 2017. 464 с.
- Adigun R., Goyal A, Hariz A. Systemic Sclerosis (Scleroderma). StatPearls: StatPearls Publishing, 2024.
- Makris A., Panagiotopoulos A., Distler O., Sfikakis P. P. Systemic Sclerosis Sine Scleroderma: A Time of Reappraisal // The Journal of Rheumatology. 2024. V. 51. №11. P. 1060-1068. https://doi.org/10.3899/jrheum.2023-1113
- Трофимова А. С., Шохин А. А., Трофимов Е. А. Клинический случай системной склеродермии у мужчины: гендерные различия и возможности капилляроскопии // Современная ревматология. 2024. Т. 18. №1. P. 84–89. https://doi.org/10.14412/1996-7012-2024-1-84-89.
- Гурский Г. Э., Гребенников В. А., Хоронько В. В. Современные представления о склеродермии // Клиническая дерматология и венерология. 2012. Т. 10. №2. С. 4-9.
- Мазуров В. И. Клиническая ревматология. М.: Е-ното, 2021. 696 с.
- Di Ciaula A., Covelli M., Berardino M. Gastrointestinal symptoms and motility disorders in patients with systemic scleroderma // BMC Gastroenterol. 2008. V. 8. P. 7. https://doi.org/10.1186/1471-230X-8-7
- Beydon M., McCoy S., Nguyen Y. Epidemiology of Sjögren syndrome // Nat Rev Rheumatol. 2024. V. 20. №3. P. 158-169. https://doi.org/10.1038/s41584-023-01057-6
- Yen T. H., Chen Y. W., Hsieh T. Y. The risk of major adverse cardiovascular events in patients with systemic sclerosis: a nationwide, population-based cohort study // Rheumatology (Oxford). 2024. V. 63. №8. P. 2074-2081. https://doi.org/10.1093/rheumatology/kead464
- Гусева Н. Г. Системная склеродермия: ранняя диагностика и прогноз // Научно-практическая ревматология. 2007. V. 1. P. 39-45.
- Ананьева Л. П., Александрова Е. Н. Аутоантитела при системной склеродермии: спектр, клинические ассоциации и прогностическое значение // Научно-практическая ревматология. 2016. V. 54. №1. P. 86-99.
- Гусева Н. Г., Невская Т. А., Старовойтова М. Н. Проблема активности при системной склеродермии // Современная ревматология. 2013. №2. C. 18-24.
- Паневин Т. С., Алекперов Р. Т., Мельниченко Г. А. Синдром Рейно в практике эндокринолога // Ожирение и метаболизм. 2019. Т. 16. №4. С. 37–45. https://doi.org/10.14341/omet10245
- Путилина М. В. Феномен Рейно в практике врача-интерниста // Фарматека. 2015. №20. С. 24-31.
- Ананьева Л. П. Лечение системной склеродермии с учетом национальных рекомендаций и рекомендаций Европейской лиги по борьбе с ревматизмом (EULAR) // Фарматека. 2014. Т. 10. №283. С. 79-86.
- Leroy U., Sarah R., Francisco C. Prevalence of Barrett's Esophagus in Female Patients With Scleroderma // The American Journal of Gastroenterology. 2021. https://doi.org/10.14309/ajg.0000000000001109
- Алекперов Р. Т., Старовойтова М. Н. Синдром Рейно в практике терапевта // РМЖ. 2010. №27. С. 1695.
- Ахметшина Л. А., Токранова Л. В., Фатыхова Э. З. Феномен Рейно в ранней диагностике системной склеродермии // Терапия. 2019. Т. 5. №8. С. 151-156.
- Herrick A. L., Clark S. Quantifying digital vascular disease in patients with primary Raynaud's phenomenon and systemic sclerosis // Ann Rheum Dis. 1998. Т. 57. №2. P. 70-8. https://doi.org/10.1136/ard.57.2.70
- Горячкина Л. Н., Носкова Л., Злобина Т. И. Генерализованный синдром Рейно при системной склеродермии // Байкальский медицинский журнал. 2001. Т. 24. №1. С. 76-78.
- Martini G., Foeldvari I., Russo R. Juvenile Scleroderma Working Group of the Pediatric Rheumatology European Society. Systemic sclerosis in childhood: clinical and immunologic features of 153 patients in an international database // Arthritis Rheum. 2006. V. 54. №12. P. 3971-8. https://doi.org/10.1002/art.22207
- Сильченко В. В., Чикина С. Ю. Несвоевременная диагностика генерализованной формы системной склеродермии (клинический случай) // Новогодние встречи на Петроверигском: Материалы конференции. Кардиоваскулярная терапия и профилактика. 2024. Т. 23. №5S. С. 1-106. https://doi.org/10.15829/1728 8800-2024-5S
- Zargaran M., Rostamian A., Malek M., Rostamian A. A patient with scleroderma associated with severe acro-osteolysis: A case report // J Scleroderma Relat Disord. 2022. V. 7. №2. P. NP1-NP3. https://doi.org/10.1177/23971983211070117
- Guerra M. G., Rodrigues M., Águeda A. Osteolysis in Systemic Sclerosis: A Scoping Review // J Rheumatol. 2023. V. 50.№7. P. 863-872. https://doi.org/10.3899/jrheum.220626
- Морова Н. А., Кропотина Т. В., Шелягина Е. С. Легочный фиброз как первое проявление перекрестной формы системной склеродермии // Терапевтический архив. 2016. V. 88. №5. P. 77-78.
- Perelas A., Silver R. M., Arrossi A. V. Systemic sclerosis-associated interstitial lung disease // Lancet Respir Med. 2020. V. 8. №3. P. 304-320. https://doi.org/10.1016/S2213-2600(19)30480-1
- Chatterjee S., Perelas A., Yadav R. Viewpoint: a multidisciplinary approach to the assessment of patients with systemic sclerosis-associated interstitial lung disease // Clin Rheumatol. 2023. V. 42. №3. P. 653-661. https://doi.org/10.1007/s10067-022-06408-4
- Сосновская А. В., Фомин В. В., Попова Е. Н. Гастроэзофагеальнорефлюксная болезнь и взаимосвязь с выраженностью поражения легких при системной склеродермии // Клиническая нефрология. 2016. №1. C. 24-28.
- Ананьева Л. П. Диагностика и лечение интерстициального поражения легких при системной склеродермии // Современная ревматология. 2018. Т. 12. №2. С. 12–21.
- Colaci M., Giuggioli D., Sebastiani M. Lung cancer in scleroderma: results from an Italian rheumatologic center and review of the literature // Autoimmun Rev. 2013. V. 12. №3. P. 374–9. https://doi.org/10.1016/j.autrev.2012.06.003
- Цветкова О. А., Воронкова О. О., Рогова Е. Ф. Системная склеродермия. Висцеральная форма с преимущественным поражением легких, легочная гипертензия, синдром Рейно. Клиническое наблюдение // РМЖ. 2014. №5.С. 397.
- Биличенко Т. Н. Диагностика и лечение поражения легких при системной склеродермии // Клиническая медицина. 2020. Т. 98. №3. С. 185–196. https://doi.org/10.30629/0023-2149-2020-98-3-185-196
- Scheidegger M., Boubaya M., Garaiman A. Characteristics and disease course of untreated patients with interstitial lung disease associated with systemic sclerosis in a real-life two-centre cohort // RMD Open. 2024. V. 10. №1. P. e003658. https://doi.org/10.1136/rmdopen-2023-003658
- Ferri C., Valentini G., Cozzi F. Systemic Sclerosis Study Group of the Italian Society of Rheumatology (SIR-GSSSc). Systemic sclerosis: demographic, clinical, and serologic features and survival in 1,012 Italian patients // Medicine (Baltimore). 2002. V. 81. №2. P. 139-53. https://doi.org/10.1097/00005792-200203000-00004
- Чотчаева Ф. Р., Зыкова А. С., Новиков П. И. Диагностика и лечение системной склеродермии // Клиническая фармакология и терапия. 2018. Т. 27. №1. С. 66-73.
- Steen V. D. Scleroderma renal crisis // Rheum Dis Clin North Am. 2003. V. 29. №2. P. 315-33. https://doi.org/10.1016/s0889-857x(03)00016-4
- Гусева Н. Г., Аникина Н. В., Щербаков А. Б. Применение капотена при системной склеродермии // Терапевтический архив. 1992. №5. С. 100–2.
- Cole A., Ong V. H., Denton C. P. Renal Disease and Systemic Sclerosis: an Update on Scleroderma Renal Crisis // Clin Rev Allergy Immunol. 2023. V. 64. №3. P. 378-391. https://doi.org/10.1007/s12016-022-08945-x
- Farrukh L., Steen V., Shapiro L. Spectrum of renal disease in scleroderma other than scleroderma renal crisis: A review of the literature // Clin Nephrol. 2024. V. 102. №2. P. 97-106. https://doi.org/10.5414/CN111243
- Lalwani A., Amin S., Yousaf Z. A Case of Atypical Scleroderma Renal Crisisn// Eur J Case Rep Intern Med. 2024. V. 11. №8. P. 004706. https://doi.org/10.12890/2024_004706
- Wajid S., Shapiro L, Farrukh L Acute Kidney Injury in Systemic Sclerosis Beyond Scleroderma Renal Crisis: A Case-Control Study // J Clin Rheumatol. 2024. V. 30. №6. P. 219-222. https://doi.org/10.1097/RHU.0000000000002108
- Захарова А. Ю., Гордеев А. В., Мутовина З. Ю. Системная склеродермия и хроническое поражение почек // Терапия. 2017. №4.С. 69-74.
- Maidman S. D., Birjiniuk J., Donnino R. Rapidly Progressive Primary Scleroderma Cardiomyopathy in a Young Adult Characterized by Multimodality Imaging // CASE (Phila). 2023. V. 7. №9. P. 349-353. https://doi.org/10.1016/j.case.2023.03.006
- Ханин А. Л., Варин А. А., Филатова Л. Д. Туберкулёз лёгких на фоне системной склеродермии, дебютирующей инфарктом миокарда и рецидивирующим плевритом (случай из практики) // Туберкулез и болезни легких. 2010. V. 87. №9. P. 57-61.
- Thonhofer R., Siegel C., Trummer M. Early endoscopy in systemic sclerosis without gastrointestinal symptoms // Rheumatol Int. 2012. V. 32. №1. P. 165-8. https://doi.org/10.1007/s00296-010-1595-y
- Lahcene M., Oumnia N., Matougui N. Esophageal dysmotility in scleroderma: a prospective study of 183 cases // Gastroenterol Clin Biol. 2009. V. 33. №6-7. P. 466-9. https://doi.org/10.1016/j.gcb.2009.01.014
- Каратеев А. Е., Мовсиян М. М., Ананьева Л. П. Клинические, эндоскопические и морфологические проявления поражения пищевода при системной склеродермии // Клиническая медицина. 2014. V. 92. №6. P. 67-74.
- Каратеев А. Е., Movsisyan M. M., Ананьева Л. П. Патология пищевода при системной склеродермии: данные клинико-эндоскопического обследования // Научно-практическая ревматология. 2012. V. 50. №1. P. 54-59. https://doi.org/10.14412/1995-4484-2012-505
- Santos-Navarro R. R., Méndez-del-Monte R., del Real-Calzada C. Manifestaciones de esclerosis sistémica en el aparato digestivo. Clínicas, endoscópicas y por manometría // Rev Med Inst Mex Seguro Soc. 2008. V. 46. №5. P. 503-10.
- Kaniecki T., Hughes M., McMahan Z. Managing gastrointestinal manifestations in systemic sclerosis, a mechanistic approach // Expert Rev Clin Immunol. 2024. V. 20. №6. P. 603-622. https://doi.org/10.1080/1744666X.2024.2320205
- Сосновская А. В., Фомин В. В., Лебедева М. В. Взаимосвязь гастроэзофагеальной рефлюксной болезни и интерстициального поражения легких при системной склеродермии // Consilium Medicum. 2015. V. 17. №12. P. 73–76.
- Leroy U., Sarah R., Francisco C. Prevalence of Barrett's Esophagus in Female Patients With Scleroderma // The American Journal of Gastroenterology. 2021. https://doi.org/10.14309/ajg.0000000000001109
- Егоров И. В. Трудный пациент: overlap-синдром, паранеопластический синдром или случайная полиморбидность? // Доктор.Ру. 2020. Т. 19. №11. С. 46–51. https://doi.org/10.31550/1727-2378-2020-19-11-46-51
- Шостак Н. А., Клименко А. А, Демидова Н. А. Склеродермия как паранеопластический синдром и опухоли, ассоциированные со склеродермией // Клиницист. 2020. Т. 14. №1–2. С. 55–61. https://doi.org/10.17650/1818-8338-2020-14-1-2-55-61
- Алекперов Р. Т., Торопцова Н. В. Системная склеродермия и остеопороз // Альманах клинической медицины. 2015. №43. С. 90-99. https://doi.org/10.18786/2072-0505-2015-43-90-99
- Garcia S., Fernandes B. M., Ganhão S. Bone mineral density and fracture risk in a cohort of Portuguese systemic sclerosis patients // ARP Rheumatol. 2022. V. 1. №2. P. 179-180.
- Schulz N., Dischereit G., Henke L. Prevalence and effects of Vitamin D receptor polymorphism on bone mineral density and metabolism in patients with systemic sclerosis: a preliminary study // Clin Exp Med. 2024. V. 24. №1. P. 121. https://doi.org/10.1007/s10238-024-01385-1


