Системные проявления первичного остеоартроза коленных суставов у пациентов на ранней стадии его развития
Автор: Белова С.В., Гладкова Е.В., Зубавленко Р.А., Ульянов В.Ю.
Журнал: Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье @vestnik-reaviz
Рубрика: Клиническая медицина
Статья в выпуске: 2 (50), 2021 года.
Бесплатный доступ
Цель исследования - изучение системных проявлений первичного остеоартроза коленных суставов у пациентов на ранней стадии его развития. При обследовании 42 пациентов без клинической симптоматики, находившихся в группе риска развития остеоартроза коленных суставов, и 12 доноров без патологии опорно-двигательной системы, было установлено, что уже на ранней стадии развития первичного остеоартроза имелись нарушения системного характера, заключающиеся в негативном изменении клеточного звена иммунитета на фоне активации провоспалительных цитокинов, что могло способствовать развитию аутоиммунного ответа с последующей воспалительной реакцией, приводящей к возникновению и прогрессированию деструктивных изменений в соединительнотканных структурах коленных суставов, подтвержденных повышенным содержанием олигомерного матриксного хрящевого белка и хрящевого гликопротеина-39.
Первичный остеоартроз, ранняя стадия, коленные суставы, системные проявления
Короткий адрес: https://sciup.org/143176798
IDR: 143176798 | УДК: 003.8:616-092 | DOI: 10.20340/vmirvz.2021.2.CLIN.5
Systemic symptoms of primary knee osteoarthrosis in patients with the early stage of the disease
The research was aimed at the investigation of systemic symptoms of primary knee osteoarthrosis in patients with the early stage of the disease. We examined 42 patients with no clinical symptoms but at high risk of knee osteoarthrosis, and 12 donors with no musculoskeletal pathologies. It was established that systemic abnormalities featured by the negative change in the cell immunity along with pro-inflammatory cytokine activation were detectable even in the early stage of primary osteoarthrosis. These had probably facilitated the progress of the immune response followed by the inflammatory reaction that led to the progress of destructive changes in the connective tissue structures of the knees4 the process was proven by the increase in cartilage oligomeric matrix protein as well as cartilage glycoprotein-39.
Текст научной статьи Системные проявления первичного остеоартроза коленных суставов у пациентов на ранней стадии его развития
УДК 003.8:616-092
С позиций современной ревматологии остеоартроз (ОА) объединяет гетерогенную группу заболеваний с различными постоянно меняющимися клиникопатогенетическими фенотипами, приводящими к общим клиническим проявлениям [1, 2]. ОА является результатом взаимодействия биологического и механического факторов, приводящих к дисбалансу между синтетическими и деградационными процессами экстрацеллюлярного матрикса суставного хряща и субхондральной кости [3]. Возникновение и прогрессирование данной патологии могут обусловливать эволюционные, генетические, травматические и метаболические факторы [3], вызывающие молекулярные изменения клеток и состояния экстрацеллюлярного матрикса, приводящие к разволокнению, ульцерации, истончению хрящевого слоя, а также к остеосклерозу с утолщением и уплотнением кортикального слоя субхондральной кости, к образованию субхондральных кист и остеофитозу. Локальные изменения при ОА со временем принимают системный характер. Развитие молекулярной биологии и открытие способности растворимых провос-палительных медиаторов увеличивать синтез матричных металлопротеиназ и коллагеназ хондроцитами позволили выдвинуть предположение об участии иммунной системы в патогенезе ОА и обосновать «воспалительную» теорию возникновения и развития данного заболевания [4].
В научной литературе имеются сведения о важной роли адаптивного и врожденного иммунитета в патогенезе ОА [1], при этом именно последнему уделяется особое внимание в развитии раннего ОА [5]. Клеточные и внеклеточные факторы (TLR фагоцитирующие клетки, хондроциты, компоненты системы комплемента и NK-клетки) врожденного иммунитета принимают активное участие в возникновении воспалительного процесса в суставных тканях. Позднее к развитию воспаления в соединительнотканных структурах присоединяются факторы адаптивного иммунитета в силу того, что в синовиальной среде сустава (синовиальная жидкость и синовиальная оболочка) у пациентов с ОА имеются клетки, принимающие участие в гуморальном и клеточном иммунном ответе, а также благодаря высвобождающимся антигенным детерминантам хрящевого матрикса в результате воздействия факторов риска и активации катаболических процессов, что приводит к хронизации воспалительных процессов [1].
Цель исследования: изучение системных проявлений первичного остеоартроза коленных суставов у пациентов на ранней стадии его развития.
Материалы и методы
В исследовании приняли участие 42 пациента без клинической симптоматики, находящиеся в группе риска развития ОА коленных суставов (возраст, пол, генетические заболевания соединительной ткани), включенные в исследование методом случайной выборки, среди которых было 19 (45,2 %) мужчин и 23 (54,8 %) женщин в возрасте 49,2 ± 4,4 года. Группу контроля составили 12 доноров (5 мужчин и 7 женщин) без патологии опорно-двигательной системы аналогичного возраста. В исследование не включались лица, имевшие сопутствующую соматическую патологию.
Все пациенты были обследованы с помощью клинических, инструментальных и лабораторных методов исследования. Клиническая картина заболевания складывалась из определения клинической симптоматики и состояния системы опорнодвигательного аппарата. Инструментальное обследование включало в себя проведение УЗИ, рентгенографии и МРТ крупных суставов. Проведение оценки иммунологических реакций заключалось в определении количественного и качественного состава клеточных популяций лимфоцитов по их иммунофенотипу (CD3+, CD3+CD8+, CD3+CD4+, CD16+CD56+, CD19+) методом ла- зерной проточной цитофлюориметрии на цитометре BD FACSCantoll (США), а также по уровню неоптерина, низкомолекулярного производного гуанозинтрифосфата и основного продуцента макрофагов, определяемого методом твердофазного иммунофер-ментного анализа на многофункциональном фотометре Epoch (Bio Tek, CША). Аналогичным методом определяли содержание про-воспалительных цитокинов (ТNF-α, IL-1, IL-6, «Вектор Бест», Россия), а также содержание олигомерного матриксного хрящевого белка и хрящевого гликопротеина-39, характеризующие состояние хрящевой ткани. Определение вышеуказанных параметров осуществлялось на фоне проведения таких стандартных биохимических тестов как альбумин, глюкоза, фракции билирубина, трансаминазы, холестерин, мочевина, креатинин, С-реактивный протеин на биохимическом анализаторе «Сапфир-400», Япония.
Весь цифровой материал подвергался статистической обработке с помощью программ Microsoft Excel 2010, Statistica 6.0. с применением непараметрического критерия Манна – Уитни. Результаты были представлены в виде медиан (Ме) с указанием квартильных размахов (нижний (25 %) и верхний (75 %) квартили). Результаты считались достоверно значимыми при р < 0,05.
От обследуемых пациентов было получено добровольное информированное согласие на проведение комплексных медицинских мероприятий, осуществляемых согласно стандартам Хельсинской декларации Всемирной медицинской организации.
Результаты
У обследованных пациентов жалобы, в основном, отсутствовали. Исключение составили 4 пациента, отмечавшие периодически возникающие боли в коленном суставе после физических нагрузок.
По данным инструментальных методов исследования у 24 пациентов была установлена нулевая стадия при отсутствии рентгенологических признаков поражения и у 18 – первая стадия заболевания с имеющимися остеофитами на поверхности сустава в незначительном количестве. При этом отмечалось некоторое утолщение синовиальной оболочки, снижение толщины гиалинового хряща, дегенеративные изменения в медиальном мениске (по данным УЗИ), а также незначительное сужение суставной щели (рентгенографическое исследование) и наличие участков патологически измененных тканей с утратой трехмерной высокоупорядоченной структуры хрящевого матрикса (МРТ-исследование).
У данных пациентов были обнаружены изменения в клеточном звене иммунной системы. Было достоверно снижено содержание Т-лимфоцитов (табл. 1), при этом имелось незначительное снижение Т-хелперов (CD3+CD4+), Т-супрессоров (CD3+CD8+) и В-лимфоцитов (CD19+) (табл. 1). Уровень NK-клеток (CD16+CD56+) имел тенденцию к повышению (табл. 1).
При исследовании активности провос-палительных цитокинов было установлено достоверно (р < 0,05) повышенное содержание IL-1 β , TNF- α и несущественное (р > 0,05) понижение уровня IL-6 в сравнении с группой контроля (рис. 1).
Изучение основного продуцента макрофагов – неоптерина показало несущественное повышение его содержания [8,7 (8,1; 9,2)] ммоль/л по сравнению с показателями контрольной группы [7,6 (6,8; 7,6)] ммоль/л на фоне повышенного содержания С-реактивного протеина [4,7 (4,2; 5,0)] мг/л по сравнению со значениями у доноров [3,1 (2,2; 3,4)] мг/л.
Таблица 1. Показатели клеточного иммунитета
Table 1. Indicators of cellular immunity
|
Показатели |
Контрольная группа (n = 11) |
Пациенты с первичным ОА коленных суставов (n = 24) |
Значение р |
|
Т-лимфоциты CD3+ (абс.) |
1672,5 (1562,1; 1782,3) |
1510,1 (1359,6; 1636,7) |
0,025181* |
|
Т-лимфоциты CD3+ (относит.) |
72,2 (71,5; 72,3) |
71,2 (70,4; 72) |
0,046605* |
|
Т-супрессоры CD3+CD8+ (абс.) |
689,9 (653,8; 714,9) |
675,8 (660,5; 695) |
0,594032 |
|
Т-супрессоры CD3+CD8+ (относит.) |
27,2 (22,5; 28,7) |
23,1 (20,9; 24,8) |
0,00855* |
|
Т-хелперы CD3+ CD4+ (абс.) |
991,3 (945,5; 994) |
982,9 (974; 991,5) |
0,915106 |
|
Т-хелперы CD3+ CD4+ (относит.) |
48,7 (41,5; 49,3) |
46,4 (41,8; 48,8) |
0,455545 |
|
Естественные киллеры CD16+CD56+ (абс.) |
230,5 (210,1; 248,3) |
242,5 (215,4; 260,5) |
0,569672 |
|
Естественные киллеры CD16+CD56+ (относит.) |
13,2 (11,1; 16,1) |
14,5 (11,3; 14,7) |
0,943345 |
|
В-лимфоциты CD19+ (абс.) |
272,1 (237,9; 275,5) |
268,1 (235,9; 292,9) |
0,83117 |
|
В-лимфоциты CD19+ (относит.) |
13,7 (11,7; 14,2) |
12,7 (11; 15,2) |
0,423999 |
Примечание: р – показатель различий исследуемых показателей между донорами и пациентами с первичным ОА коленных суставов на ранней стадии, * – достоверная значимость, n – количество обследуемых.
Кроме того, у данного контингента были достоверно (р < 0,05) повышены метаболиты хрящевой ткани в сыворотке крови: олигомерный матриксный хрящевой белок был повышен у пациентов [852,1 (759,3; 917,8)] нг/л по сравнению с значениями в группе контроля [582,0 (418,5; 629,3)] нг/л; уровень хрящевого гликопротеина-39 у пациентов составил [64,7 (62,2; 71,2)] нг/мл против значений доноров [17,2 (16,6; 17,3)] нг/мл.
Обсуждение
Результаты проведенного нами исследования показали, что у пациентов с первичным ОА коленных суставов без клинической симптоматики уже на ранней стадии его развития имелись нарушения системного характера.
Анализ результатов иммунологического исследования выявил отклонения в состоянии клеточного иммунитета у пациентов с ранним первичным ОА коленных суставов по сравнению со значениями в контрольной группе. Изменения касались как количественного, так и качественного состава субпопуляций лимфоцитов: Т-лимфоциты, В-лимфоциты, NK-клетки, аутентифицированные с помощью цветных моноклональных антител. Анализ значений Т-лимфоцитов, активность которых направлена на распознавание и уничтожение патологических клеток с чужеродным антигеном, свидетельствовал о достоверно значимом снижении их абсолютного и относительного содержания (табл. 1). Отмечалось незначительное снижение Т-хелперов (CD3+CD4+) и Т-супрессоров (CD3+CD8+) (табл. 1). Изменение В-лимфоцитов(CD19+), обеспечивающих гуморальный иммунитет, было аналогичным изменению Т-хелперов (табл. 1). Что касается значений NK-клеток (CD16+CD56+), то их уровень имел тенденцию к повышению (табл. 1). NK-клетки относят к лимфоцитам врожденного иммунитета, способных немедленно, без предварительной иммунизации реагировать на чужеродный агент, а также на собственные деформированные клетки без молекул основного комплекса гистосовместимости I класса (МНС-I) автономно от системы комплемента и антител. К повышению NK-клеток в крови приводит их быстрое реагирование на клеточный стресс, инфекционный и воспалительный агенты, что отмечалось и в нашем исследовании. По литературным источникам у женщин с ОА коленного сустава III стадии, в отличие от наших пациентов с 0-I стадиями, определение содержания NK-клеток в периферической крови также показало тенденцию к их повышению по сравнению со значениями в контрольной группе [6]. В исследовании иностранных авторов было установлено наличие корреляционных взаимосвязей между повышенным уровнем провоспалительных цитокинов и присутствием естественных киллеров с фенотипом CD56brightCD16- в синовиальной жидкости, представляющей собой важную составляющую сустава и отражающую картину происходящих изменений в синовиальной оболочке и хрящевой ткани, при этом быстро реагирующей на негативные изменения в суставной среде. Данное обстоятельство могло способствовать возникновению и прогрессированию хронического воспалительного процесса в структурных компонентах сустава [7].
Цитокины относятся к биологическим медиаторам межклеточных и системных взаимодействий. При соединительнотканной патологии у пациентов с ОА четыре класса (регуляторные, деструктивные, ингибирующие, анаболитические факторы роста) этих биологически активных компонента оказывают разнонаправленное воздействие практически на все структурные элементы сустава, включая синовиальную оболочку, хрящевую и костную ткани. В нашей работе при изучении провоспали-тельных цитокинов была определена повышенная продукция IL-1 β и TNF- α на фоне незначительного понижения уровня IL-6 в сравнении с группой контроля (рис. 1). При определении провоспалительного цитокина
IL-1 β , отвечающего за активацию остеокластов, реструктуризацию коллагеновой сети и деминерализацию костной ткани, был установлен его достоверно повышенный уровень (р < 0,05) в сравнении со значениями в контрольной группе. Определение провоспалительного цитокина TNF- α – основного медиатора воспаления, оказывающего подавляющее действие на синтез клеточных элементов экстрацеллюлярного матрикса и стимулирующего дегенеративные процессы в нем, также показало его достоверное повышение (р < 0,05). Данный цитокин отличает разнообразие иммуномодулирующих и провоспалительных свойств, как считают некоторые авторы, большинство их этих характерных свойств TNF- α могут приобретать фундаментальное значение в иммунопатологических процессах при воспалительных ревматических заболеваниях [8]. Определение содержания провоспалительного цитокина IL-6, основного индуктора синтеза острофазовых белков, показало его незначительное снижение (р > 0,05) в сравнении с группой контроля. В исследовании И.В. Ширинского с соавт. (2015) уровень IL-6 прямо коррелировал с рядом функциональных показателей тяжести заболевания у пациентов с диабет-ассоциированным ОА [9].
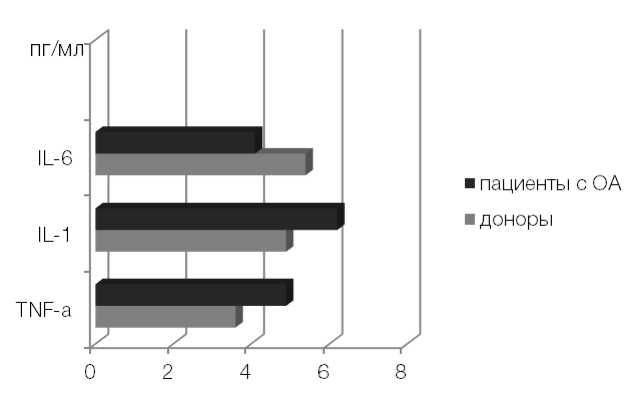
Рис. 1. Содержание провоспалительных цитокинов у доноров и пациентов с первичным ОА коленных суставов на ранней стадии
Fig. 1. Content of pro-inflammatory cytokines in donors and patients with early primary knee OA
Установленные в нашем исследовании изменения экспрессии провоспалительных цитокинов могут способствовать инициации развития дегенеративных явлений в соединительнотканных компонентах сустава в силу того, что они являются биологически активными медиаторами, активирующими выработку протеолитических ферментов хондроцитами, клетками хрящевой ткани. Протеолитические ферменты, индуцируя деструкцию коллагеновых волокон и молекул протеогликанов, приводят к нарушению соединительнотканных структур, что активирует аутоиммунные механизмы и вызывает воспалительную реакцию в суставных тканях.
Помимо изучения компонентов клеточного звена иммунитета и активности цитокинов, в данной работе исследовался основной продуцент макрофагов – неоптерин, производимый гуанозинтрифосфатом. Установленное несущественное повышение содержания неоптерина по сравнению с показателями контрольной группы косвенно указывало на некоторую возрастающую секреторно-синтетическую активность иммунокомпетентных клеток под влиянием на них растворимого цитокина интерферона-гамма (IFN- γ ) и фактора некроза опухоли-альфа (TNF- α ). Кроме того, повышенное содержание неоптерина могло свидетельствовать и о воспалительной составляющей. Данное положение подтверждает и повышенное содержание С-реактивного протеина по сравнению со значениями у доноров, что отмечалось и в другом исследовании у пациентов с ОА, ассоциированным с метаболическим синдромом [10]. Повышенная продукция С-реактивного протеина, относящегося к белкам острой фазы, может быть объяснена тем, что на границе суставного хряща и синовиальной оболочки, в зоне повышенного риска развития деструктивных процессов, синтезируемые клетками синовиальной мембраны некоторые цитокины приводят к повышенному образованию продукции данных острофазовых белков.
В последнее время для оценки состояния хрящевой ткани многими авторами используется определение олигомерного матриксного хрящевого белка, относящегося к внеклеточному белку семейства тромбоспондина-5, выполняющему связывание полимерных коллагеновых волокон в экстрацеллюлярном матриксе соединительной ткани. Имеются данные, указывающие на связь между уровнем этого белка и развитием деструктивных изменений в соединительнотканных структурах суставов [11] . Интерес к представленному белку появился после открытия в его гене мутаций, приводящих к таким аутосомнодоминантным заболеваниям соединительной ткани, как множественная эпифизарная дисплазия I типа и псевдохондроплазия. В нашей работе содержание олигомерного матриксного хрящевого белка у пациентов с первичным ОА коленных суставов на ранней стадии его развития было достоверно (p < 0,05) повышено в сыворотке крови [852,1 (759,3; 917,8)] нг/л по сравнению со значениями в группе контроля [582,0 (418,5; 629,3)] нг/л. Из научных источников известно влияние изменений в структуре олигомерного матриксного хрящевого белка на структурно-функциональное состояние связочного аппарата. Генные мутации в данном белке могут приводить к возникновению гипермобильности суставов, что можно отнести к факторам риска развития раннего ОА [12].
Кроме исследования маркера хрящевой ткани – олигомерного матриксного хрящевого белка, нами был изучен еще один показатель, характеризующий метаболизм хрящевой ткани – хрящевой гликопротеин-39, свойства которого изучены не в полной мере, однако, определенная направленность изменений и характер имеющихся взаимосвязей с развитием ряда патологий дают основание предположить его важную роль в ремоделировании тканевых структур. У обследованных нами пациентов содержание данного гликопротена-39 было отлично от нормы (p < 0,05) и соответствовало [64,7 (62,2; 71,2)] нг/мл против значений доноров [17,2 (16,6; 17,3)] нг/мл. Аналогичные результаты были получены в научном исследовании, в котором у больных ОА с кардиоваскулярной патологией уровень гликопротена-39 также был повышен, кроме того, была установлена взаимосвязь клинических особенностей течения ОА у пациентов с преимущественным поражением коленных суставов и продукта деградации хрящевой ткани сустава – хрящевого гликопротеина-39, свидетельствовавшего о наличии воспалительного процесса и характеризующего тяжесть течения заболевания [3].
Заключение
Резюмируя, можно утверждать, что у пациентов с первичным ОА коленных суставов без клинической симптоматики уже на ранней стадии его развития имелись нарушения системного характера. Исследование иммунологических реакций у данного контингента выявило некоторые изменения в состоянии клеточного звена иммунитета на фоне активации провоспалитель-ных цитокинов. Данное обстоятельство, как правило, способствует развитию аутоиммунного ответа с последующей воспалительной реакцией, о чем свидетельствует повышенное содержание С-реактивного протеина, что в итоге приводит к возникновению и прогрессированию деструктивных изменений в соединительнотканных структурах коленных суставах, подтверждающихся повышенным содержанием олигомерного матриксного хрящевого белка и хрящевого гликопротеина-39 в биологической среде организма.
Список литературы Системные проявления первичного остеоартроза коленных суставов у пациентов на ранней стадии его развития
- Shirinskij V.S., Kazygasheva E.V., Shhirinskij I.V. Vospalenie i immunitet: rol' v patogeneze osteoartrita. Medicinskaya immunologiya. 2019;21(1):39-48. (In Russ).
- Castaneda S., Roman-Blas J.A., Largo R. et al. Osteoarthritis: a progressive disease with changing pheno-types. Rheumatology. 2014;53(6):1-3. https://doi.org/10.1093/rheumatology/ket247.
- Kczoeva A.A. Rol' xryashhevogo glikoproteina-39 u bol'ny'x osteoartrozom kolennogo sustava v sochetanii s ishemicheskoj boleznyu serdcza, arterial'noj gipertenziej i dislipidemiej. Terapiya. 2018;3(21):72-77. (In Russ).
- Kragstrup T.W., Sohn D.H., Lepus C.M. et al. Fibroblast-like synovial cell production of extra domain A fi-bronectin associates with inflammation in osteoarthritis. BMC Rheumatol. 2019;2(3).Art. № 46. https://doi.org/10.1186/s41927-019-0093-4.
- Kandahari A.M., Yang X., Dighe A.S. et al. Recognition of immune response for the early diagnosis and treatment of osteoarthritis. J. Immunol. Res. 2015. Art. ID 192415. https://doi.org/10.1155/2015/192415.
- CHepeleva M.V., CHegurov O.K., Kuznecova E.I. Koncentracii citokinov v perifericheskoj krovi i sinovial'noj zhidkosti pacientov s deformiruyushchim osteoartrozom kolennogo sustava v zavisimosti ot velichiny defekta vnutrennego myshchelka bol'shebercovoj kosti. Genij Ortopedii. 2017;23(4):450-454. (In Russ).
- Jaime P., Garcia-Guerrero N., Estella R. et al. CD56+/CD16- natural killer cells expressing the inflammatory protease granzyme A are enriched in synovial fluid from patients with osteoarthritis. Osteoarthritis cartilage. 2017;25(10):1708-1718. https://doi.org/10.1016/j.joca.2017.06.007.
- Nasonov E.L., Aleksandrova E.N., Novikov A.A. Autoimmunnye revmaticheskie zabolevaniya - problemy im-munopatologii i personificirovannoj terapii. Vestnik RAMN. 2015;70(2): 169-182. https://doi.org/10.15690/vramn.v70i2.1310 (In Russ).
- SHirinskij I.V., Kalinovskaya N.YU., SHirinskij V.S. Kliniko-immunologicheskaya harakteristika diabet-associirovannogo osteoartrita. Medicinskaya immunologiya. 2015;17(1):87-92. https://doi.org/10.15789/1563-0625-2015-1-87-92 (In Russ).
- Vasil'eva L.V., Lahin D.I. Vliyanie metabolicheskogo sindroma na klinicheskuyu kartinu osteoartroza. Medicin-skij vestnik Severnogo Kavkaza. 2017;12(1):8-10. http://doi.org/10.14300/mnnc.2017.12002 (In Russ).
- Belova YU.S. Karyakina E.V. Hryashchevoj protein pri razlichnyh tipah displazii. Russkij medicinskij zhurnal. 2017;25(19):1352-1355. (In Russ).
- Tyurin A.V. Klinicheskie osobennosti i molekulyarno-geneticheskie aspekty osteoartroza u bol'nyh s displaziej soedinitel'noj tkani: avtoref. dis. ... kand. med. nauk. Moscow; 2015. 23 c. (In Russ).


