Системы критериев оценки ответа солидных опухолей при лечении иммуноонкологическими препаратами
Автор: Юдин Денис Иванович, Лактионов Константин Павлович, Саранцева Ксения Андреевна, Черненко Полина Андреевна, Арзуманян Алла Леонидовна
Журнал: Злокачественные опухоли @malignanttumors
Рубрика: Диагностика и лечение опухолей. Оригинальные статьи
Статья в выпуске: 1 (22), 2017 года.
Бесплатный доступ
Иммунотерапия активирует иммунную систему пациента с развитием противоопухолевого иммунного ответа. В настоящее время иммуноонкологические препараты широко и успешно применяются для лечения различных видов опухолей. Критерии эффективности, применяемые при оценке химиотерапевтических препаратов, могут привести к значительным сложностям и ошибкам интерпретации ответа на иммунотерапию. Учитывая это, очень важно выбрать соответствующие критерии оценки. Целью этого обзора является освещение этой темы.
Иммунотерапия, системы критериев оценки ответа солидных опухолей
Короткий адрес: https://sciup.org/140223023
IDR: 140223023 | DOI: 10.18027/2224-5057-2017-1-46-46
Systems of response evaluation criteria in solid tumors in immunooncology treatment
Immunotherapies enhance patients' endogenous immune system function of attacking tumor cells, and are being widely and successfully used in the field of immuno-oncology. Adoption of assumptions based on more traditional chemotherapy-based responses can lead to significant operational difficulties and inaccurate interpretation of responses seen. It is therefore important to choose the appropriate clinical response criteria. These topics are addressed in this white paper.
Текст научной статьи Системы критериев оценки ответа солидных опухолей при лечении иммуноонкологическими препаратами
Наиболее часто в клинической практике мы используем качественную оценку результатов лекарственного лечения – «отрицательная/положительная динамика». Однако для получения адекватных, сравнимых результатов в клинических исследованиях новых препаратов появилась необходимость в количественной оценке. В 1981 г. ВОЗ была принята клиническая классификация степеней ответа опухоли, основанная на изменении линейных размеров новообразования, определяемых лучевыми методами исследования [1]. В 2000 г. она была пересмотрена и представлена как критерии оценки ответа солидных опухолей (Response Evaluation Criteria In Solid Tumors – RECIST), в которой стали использовать двухмерные измерения вместо трехмерных, уменьшено количество измеряемых очагов [2]. Дальнейшая эволюция RECIST привела к созданию в 2009 г. ее новой версии 1.1, которая отличается как граничными значениями количественных показателей, так и увеличением количества оцениваемых параметров, ранжировки их значимости [3]. Эта система была внедрена в клиническую практику для оценки эффективности терапии химиотерапевтическими и таргетными препаратами.
В последние годы активно развивается и внедряется в клиническую практику новый подход к терапии злокачественных опухолей – иммуноонкология. Препараты, блокирующие контрольные точки иммунного ответа, показали свою эффективность в лечении различных солидных опухолей, таких как меланома, немелкоклеточный рак легкого, почечно-клеточный рак и др. [4, 5]. Однако эти препараты обладают совсем другим механизмом действия, по сравнению с химиотерапевтическими и таргетными агентами. Иммуно-онкологические препараты активируют иммунную систему, вследствие чего иммунные T-клетки начинают атаковать опухолевые клетки с развитием противоопухолевого ответа [6]. Учитывая косвенное действие препаратов, развитие ответа на лечение может занять от нескольких недель до нескольких месяцев. Иногда может развиться процесс, называемый псевдопрогрессирование, для которого характер- но временное увеличение размера опухоли или появление видимых новых очагов в связи с инфильтрацией опухоли активными иммунными клетками [7]. Игнорирование формальных признаков неэффективности по критериям RECIST позволило продолжить эффективное лечение у ряда пациентов с формальным прогрессированием (псевдопрогрессирование). Таким образом, ответ на иммунотерапию может развиваться по четырем основным направлениям: уменьшение размеров существующих очагов без возникновения новых; длительная стабилизация размеров опухоли с последующим уменьшением её в размерах; уменьшение в размерах опухоли после первоначального её увеличения; уменьшение в размерах некоторых очагов при появлении новых.
Учитывая вышеперечисленное, стало актуальным внедрение новых критериев оценки эффективности иммуноонко-логических препаратов [8]. Целью данного обзора литературы является осветить некоторые новые моменты в оценке ответа на лекарственное лечение солидных опухолей.
КРИТЕРИИ ОЦЕНКИ ОТВЕТА СОЛИДНЫХ ОПУХОЛЕЙ – RECIST 1.1
Критерии оценки ответа солидных опухолей, опубликованные в 2000 году и пересмотренные в 2009 году, стали наиболее широко применяемой системой в клинической практике и в клинических испытаниях, своеобразным «золотым стандартом». Это наиболее стандартизированный и практически удобный метод для оценки ответа и прогрессирования в разделе лечения солидных опухолей, за исключением злокачественной лимфомы [3].
Ключевые понятия RECIST 1.1 включают в себя:
-
1. Целевые (таргетные) очаги (не более 5, не более 2 на орган и наиболее воспроизводимые)
-
2. Измеримые очаги (размер не менее 10 мм для солидного очага, патологический лимфоузел более 15 мм по короткой оси, литический или смешанный очаг в кости с мягкотканым компонентом не менее 10 мм)
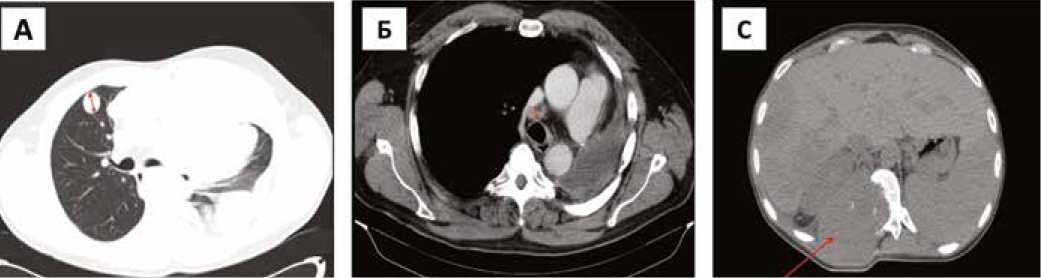
Рис. 1. Примеры измерения очагов в системе RECIST 1.1
А. Оценка солидного очага в легком; В. Измерение претрахеального лимфоузла в средостении; С. Метастаз в позвонок с внекостным компонентом
-
3. Неизмеримые очаги (остеобластические очаги, поражение мозговых оболочек, плевральный и перикардиальный выпот, асцит и перитонеальные метастазы и лимфогенный карциноматоз).
Ключевые правила измерения в RECIST 1.1 включают в себя следующие понятия (рис.1):
– в солидном очаге оценивается только наиболее длинный диаметр
– в лимфоузле оценивается только наиболее короткий диаметр
– в костном очаге оценивается только солидный компонент.
В системе RECIST при выполнении КТ исследования обязательно использование внутривенного контрастирования с единой методикой постконтрастного сканирования. Для сливающихся/разделившихся очагов сравнивается наиболее длинный диаметр общего очага с суммой наиболее длинных размеров новых очагов. Сумму диаметров всех выбранных таргетных очагов считаем точкой отсчета для дальнейших изменений и оценки эффекта. Все другие очаги считаем не-таргетными и учитываем их в дальнейшем как таковые.
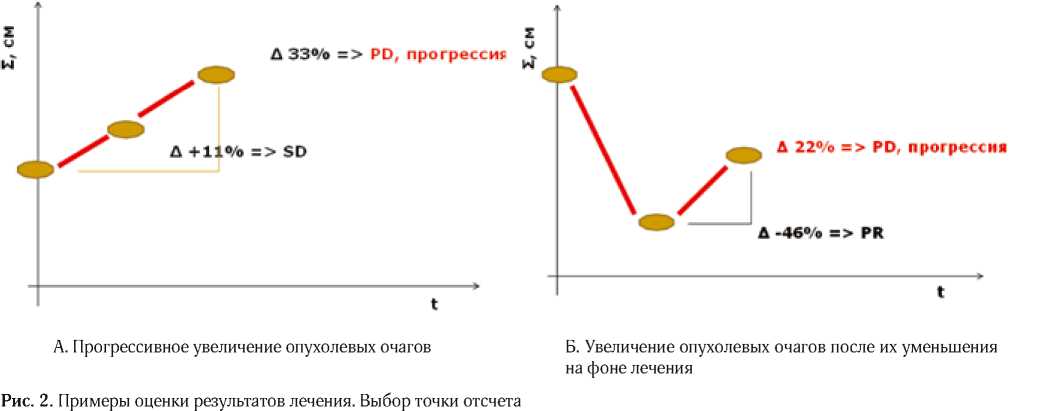
На основании результата исследований делается заключение об эффективности терапии: полный ответ (ПО), частичный ответ (ЧО), стабилизация заболевания (СЗ) и прогрессия заболевания (ПЗ). Критерии, на основании которых делается заключение об эффективности, представлены в таблице 1. Необходимо отметить, что непосредственная эффективность лечения оценивается по динамике размера и количества опухолевых очагов, поэтому очень важно правильно выбрать «точку отсчета» (рис.2). Оценка производится каждые 6–8 недель.
Тем не менее, несмотря на преимущества, учитывая, что критерии RECIST были разработаны для оценки ответа на лечение цитотоксическими химиопрепаратами, существуют некоторые ограничения в их применении для оценки эффективности иммуноонколо-гических препаратов. Например, раннее увеличение размера опухоли или появление новых очагов, класси-
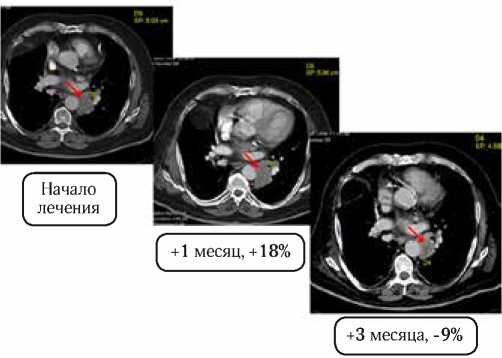
Рис. 3. Первоначальное увеличение размеров опухолевого узла на фоне эффективной иммунотерапии
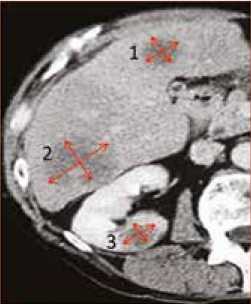
Очаг 1: 3 х 2 см
Очаг 2: 4 х 3 см
Очаг 3: 1,5 х 1 см
Опухолевая масса = сумма произведений 2 max перпендикулярных размеров
(3 х 2) + (4 х 3)+ (1,53 х 1) = 19,5
Рис. 4. Измерение опухолевой массы таргетных очагов в IrRC фицируется как прогрессирование заболевания. Однако клинический опыт показал, что полный и частичный ответ или стабилизация заболевания могут быть достигнуты после первоначального увеличения опухоли при применении иммуноонкологических препаратов (рис. 3). Для того чтобы преодолеть ограничения RECIST 1.1, были разработаны другие критерии оценки [8, 9, 10].
КРИТЕРИИ ОЦЕНКИ ОТВЕТА НА ИММУНОТЕРАПИЮ (IMMUNE-RELATED RESPONSE CRITERIA) – IRRC
Новизна IrRC проявилась в появлении понятия «опухолевой массы» и требовании подтверждения прогрессирования заболевания при последующей оценке, примерно через четыре недели. IrRC появился в ответ на необходимость оценки эффективности ипилимумаба у пациентов с диссеминированной меланомой в клинических протоколах [10]. Позднее эта система оценки была внедрена в другие исследования в области имму- нотерапии по изучению применения новых иммуноон-кологических препаратов при различных злокачественных опухолях.
КЛЮЧЕВЫЕ ПОНЯТИЯ IRRC
Целевыми (таргетными) очагами, поддающимися измерению, считаются новые очаги – не более 5 на орган, до 10 виcцеральных и 5 кожных. Измеряемыми очагами являются очаги с размерами не менее 5 Х 5 мм. В понятие неизмеряемые очаги включены: остеобластические очаги, поражение мозговых оболочек, плевральный и перикардиальный выпот, асцит и перитонеальные метастазы, лимфогенный карциноматоз и образования без четких контуров. Введено понятие «опухолевая масса», которая рассчитывается по формуле:
опухолевая масса = сумма произведений 2 max перпендикулярных размеров.
При каждой последующей оценке производится суммирование опухолевой массы показательных и новых (!) поддающихся измерению очагов. Пример оценки опухолевой массы в Ir RC представлен на рис. 4.
Оценка эффективности терапии по IrRC включает те же параметры, что и RECIST 1.1 и представлена в таблице 1. Принципиально важным является то, что появление новых очагов не является прогрессированием. Размеры перпендикуляров max диаметров новых очагов прибавляются к общей опухолевой массе (>5 Х 5 мм). Окончательная оценка ответа опухоли требует подтверждения через 4 недели. При этом датой прогрессирования будет считаться дата исследования, где оно первоначально было зафиксировано, а не дата подтверждения.
КРИТЕРИИ ОЦЕНКИ ОТВЕТА СОЛИДНЫХ ОПУХОЛЕЙ НА ИММУНОТЕРАПИЮ
(IMMUNE-RELATED RESPONSE EVALUATION CRITERIA IN SOLID TUMORS) – IRRECIST
Несмотря на возможно наиболее адекватную оценку результатов иммунотерапии, система IrRC довольно громоздка, особенно по сравнению с универсальной RECIST 1.1. Данное противоречие привело к попытке объединения двух систем оценки и появлению критериев оценки ответа солидных опухолей на иммунотерапию (IrRECIST) в 2013 году [11]. В IrRECIST постарались сохранить преимущества RECIST 1.1, преодолев ее недостатки, связанные с оценкой эффективности иммунотерапии. Предполагается, что данная система оценки будет наибо- лее адекватна для исследований иммуноонкологических препаратов и, что принципиально, совместима с наиболее распространенной системой RECIST. Правила измерения и оценки результатов аналогичны RECIST 1.1, за исключением некоторых принципиальных моментов: появление новых очагов не является прогрессированием, размеры диаметров новых очагов прибавляются к общей сумме таргетных очагов, окончательная оценка ответа опухоли требует подтверждения через 4 недели. Принципиальные отличия в рассматриваемых системах оценки ответа опухоли на проводимую терапию представлены в таблице 1.
ЗАКЛЮЧЕНИЕ
Появление новых иммунотерапевтических препаратов произвело настоящую революцию в онкологии. Текущие исследования уже показали, что иммунотерапевтические агенты могут значительно улучшить не только общую выживаемость, но и качество жизни больных с различными злокачественными новообразованиями на поздних стадиях, когда выбор эффективной терапии ограничен и клинических прогноз у этих пациентов длительное время оставался крайне неблагоприятным [4, 5]. Однако необходимо учитывать, что иммуноонкологические препараты не являются в классиче- ском понимании противоопухолевыми препаратами. Механизм действия ингибиторов контрольных точек направлен на иммунную систему, происходит активация собственного Т-клеточного иммунитета, который впоследствии и формирует противоопухолевый ответ. То время, которое требуется иммунной системе на развитие ответа, несколько отодвигает время начала противоопухолевого ответа и в некоторых случаях опухолевые очаги успевают увеличиться в размерах, либо появляются новые очаги. В дальнейшем после активации иммунного ответа все очаги, в том числе и новые, уменьшаются в размерах, однако традиционные критерии оценки не способны учесть эти особенности иммуноонколо-гических препаратов. Понимание специфических механизмов действия иммунотерапевтических препаратов диктует необходимость изменения требований к критериям оценки эффективности лечения. Адаптация критериев RECIST 1.1 в IrRECIST и создание IrRC является эволюционным шагом на пути к дальнейшей оптимизации подхода к оценке эффективности лечения у пациентов, получающих иммунотерапию. При правильной оценке эффективности иммуноте-рапевтичеких препаратов сократится число случаев раннего и необоснованного прекращения лечения пациентов современными эффективными препаратами и смене режимов терапии на менее эффективные и в большинстве случаев более токсичные схемы химиотерапии.
Список литературы Системы критериев оценки ответа солидных опухолей при лечении иммуноонкологическими препаратами
- Miller A. B., Hoogstraten B., Staquet M., Winkler A. Reporting results of Cancer treatment. Cancer 1981; 47:207-14.
- Therasse P., Arbuck S. G. et al.: New Guidelines to Evaluate the Response to Treatment in Solid Tumors. Journal of the National Cancer Institute 2000 92(3):205-216.
- Eisenhauer E. A., Therasse P., Bogaerts J. et al.: New response evaluation criteria in solid tumours: revised RECIST guideline (version 1.1). In: Eur. J. Cancer. 45, Nr. 2, Januar 2009, S. 228-47.
- Laktionov K. K., Sarantseva K. A., Breder V. V. et al. Immunotherapy for non-small cell lung cancer treatment. Malignant Tumours 2016; 3: 18-26.
- Park J., Kwon M., Shin E. C. Immune checkpoint inhibitors for cancer treatment. Arch Pharm Res. 2016 Nov; 39(11):1577-1587.
- Sarantseva K. A., Laktionava L. V., Reutova E. V., Chernenko P. A., Breder V. V. Immunology: immune response as leading protectionfactor against cancer. Malignant Tumours 2016; 2: 5-14.
- Chiou V. L., Burotto M. Pseudoprogression and Immune-Related Response in Solid Tumors. J Clin Oncol. 2015 Nov 1; 33(31):3541-3.
- Wolchok J. D., Hoos A., Bohnsack O. et.al. Guidelines for the Evaluation of Immune Therapy Activity in Solid Tumors: Immune-Related Response Criteria, Clin Cancer Res 2009; 15(23) December 1, 2009.
- Nishino M. et al. Developing a common language for tumor response to immunotherapy: immune-related response criteria using unidimensional measurements. Clin Cancer Res. 2013 Jul 15; 19(14):3936-43.
- Nishino M., Gargano M., Suda M., Ramaiya N. H., Hodi F. S. Optimizing immune-related tumor response assessment: does reducing the number of lesions impact response assessment in melanoma patients treated with ipilimumab? J Immunother Cancer. 2014; 2: 17 DOI: 10.1186/2051-1426-2-17
- Mizuki Nishino, Nikhil H. Ramaiya, Emily S. Chambers, et al. Immune-related response assessment during PD-1 inhibitor therapy in advanced non-small-cell lung cancer patients. J Immunother Cancer. 2016; 4: 84.


