SNP и InDel маркеры хлоропластной и ядерной ДНК для анализа генетического разнообразия растений чая Camellia sinensis (L.) Kuntze на производственных плантациях и в базовой коллекции
Автор: Самарина Л.С., Шхалахова Р.М., Малюкова Л.С., Бобровских А.В., Малюченко О.П., Конинская Н.Г., Маляровская В.И., Гвасалия М.В., Цатурян Г.А., Шуркина Е.С., Рындин А.В.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Молекулярное маркирование
Статья в выпуске: 1 т.61, 2026 года.
Бесплатный доступ
Характеристика геноресурсов субтропических культур в нетипичных регионах произрастания может пролить свет на молекулярные механизмы адаптации растений в неблагоприятных условиях и использоваться в селекционных программах. Северо-Западный Кавказ России как один из самых северных регионов промышленного чаеводства в мире может быть источником наиболее морозостойких форм чая. Однако до сих пор отсутствует понимание генетического разнообразия местных чайных плантаций, их молекулярно-генетическое описание, неизвестно происхождение местных сортов и форм. В представленном исследовании выявлены эффективные SNP- и InDel-маркеры для ядерного и хлоропластного геномов чайного растения, характеризующиеся высоким уровнем внутривидового полиморфизма. Из восьми универсальных пар праймеров к хлоропластному геному цветковых растений, наиболее эффективными оказались 23S, 4.5S/5S, 16S, rpl23/rpl2.l, rpoC1 intron, trnE-UUC/trnT-GUU, которые позволили выявить геномный полиморфизм среди отечественных сортов и форм чая. Отобранные эффективные маркеры ядерной и хлоропластной ДНК были секвенированы по Сэнгеру. С использованием этих маркеров проведена оценка генетического разнообразия растений чая, произрастающих на четырех производственных плантациях и в коллекции ФИЦ СНЦ РАН (г. Сочи). Внешними контролями служили образцы с промышленных плантаций из Республики Абхазия и Шри-Ланки. Для ядерных маркеров SNPs (наибольшая дискриминационная способность D = 0,90-0,92) уровень полиморфизма в среднем по всем популяциям составил P = 83 %, для хлоропластных маркеров SNPs/InDel (наибольшая дискриминационная способность D = 0,36-0,68) — в среднем P = 62 %. Самое высокое разнообразие установлено в селекционной коллекции чая (уровень полиморфизма Р = 100 %, h по хлоропластной и ядреной ДНК соответственно 0,330 и 0,335) и в популяции производственных плантаций п. Калиновое озеро (Р = 100 %, h соответственно 0,346 и 0,401). Выявлено сходство коллекционных генотипов и образцов из производственных популяций с контрольными образцами, контрастными по реакции на холодовое воздействие (сорт Колхида и форма А2019). Показана вариабельность генетического разнообразия внутри популяций чая с разной географической локализацией. Полученные результаты являются важным этапом в описании генетического разнообразия Camelliasinensis (L.) Kuntze во влажных субтропиках России и разработке современных селекционных программ по сохранению зародышевой плазмы перспективных генотипов. Выявленные генотип-специфичные SNP и InDel-маркеры также могут быть использованы для молекулярной паспортизации перспективных сортов и форм чая.
Camellia sinensis, коллекция геноресурсов, генотипирование, однонуклеотидный полиморфизм, SNP, InDel
Короткий адрес: https://sciup.org/142247332
IDR: 142247332 | УДК: 633.72:577.22:577.2 | DOI: 10.15389/agrobiology.2026.1.89rus
SNP and InDel markers of chloroplast and nuclear DNA for the analysis of genetic diversity in tea plants Camellia sinensis (L.) Kuntze from commercial plantations and a core collection
Characterization of genetic resources of subtropical crops in atypical growing regions can shed light on the molecular mechanisms of plant adaptation to unfavorable conditions and can be used in breeding programs. The Northwestern Caucasus of Russia, as a northernmost region of commercial tea Camellia sinensis (L.) Kuntze cultivation in the world could be a source of the most frost-resistant tea forms. However, an understanding of the genetic diversity of local tea plantations, their molecular genetic characterization, and the origin of local cultivars and forms is still lacking. In this study, we identified effective SNP and InDel markers for the nuclear and chloroplast genomes of the tea plants, characterized by a high level of intraspecific polymorphism. Among eight universal primer pairs for the chloroplast genome of flowering plants, 23S.4.5S/32S.5S, 16S, rpl23/rpl2.l, rpoC1 intron, and trnE-UUC/trnT-GUU the most effective and enabled the detection of genomic polymorphism among domestic tea cultivars and forms. DNA fragments that contain the selected effective nuclear and chloroplast DNA markers were sequenced by Sanger’s method. With these markers, we assessed the genetic diversity of tea plants from four commercial plantations and from the core collection of the Federal Research Centre the Subtropical Scientific Centre RAS (Sochi). Specimens from commercial plantations of the Republic of Abkhazia and from Sri Lanka served as external controls. For nuclear SNP markers, the highest discriminatory power was D = 0.90-0.92, and the average polymorphism level identified based on population samples was P = 83 %. For chloroplast SNP/InDel markers, the highest discriminatory power was D = 0.36-0.68, and the average polymorphism level was P = 62 %. The greatest genetic diversity was found in the tea core collection, the polymorphism level was P = 100 %, h values for chloroplast and nuclear DNA were 0.330 and 0.335, respectively, and in populations of commercial plantations from Kalinovoye Ozero settlement, with P = 100 % and h values of 0.346 and 0.401, respectively. We revealed phylogenetic similarities of collection and commercial genotypes to the control cv. Kolkhida and form A2019 contrasting in their response to cold stress. We also found variation in genetic diversity within tea populations growing in different geographic regions. The data obtained reveal the genetic diversity of C. sinensis in the humid subtropics of Russia, which will allow for the improvement of conservation programs for this promising gene pool. The identified genotype-specific SNP and InDel markers can also be used for molecular certification of tea cultivars and forms.
Текст научной статьи SNP и InDel маркеры хлоропластной и ядерной ДНК для анализа генетического разнообразия растений чая Camellia sinensis (L.) Kuntze на производственных плантациях и в базовой коллекции
Camellia sinensis (L.) Kuntze (чай) — одна из важнейших многолетних вечнозеленых субтропических культур, общая площадь чайных плантаций достигла 5 318 000 га при 2-кратном увеличении мирового производства за последние 5 лет (1). В первую десятку стран-производителей чая в 2023 году входили Китай, Индия, Кения, Шри-Ланка, Вьетнам, Индонезия, Мьянма, Турция, Бангладеш и Уганда, на долю которых приходится 94,19 % площадей чайных плантаций в мире (1).
На Кавказе интродукция чайного растения началась около 150 лет назад в Гурии (историческая область на западе Грузии, 41,9443°N, 42,0458°W). В XIX веке семена чайных растений были привезены из Китая и Индии, а
∗ Анализ генетического разнообразия растений чая выполнен за счет средств гранта РНФ ¹ 23-46-00002. Апробация универсальных праймеров выполнена за счет средств ГЗ ФИЦ СНЦ РАН ¹ FGRW-2024-0005, регистрационный номер 124022000092-4. Коллекция чая предоставлена в рамках реализации ГЗ ФИЦ СНЦ РАН ¹ FGRW-2024-0003, регистрационный номер 124022000093-1.1.
также из Японии, Шри-Ланки, Вьетнама и Индонезии и высажены в Гурии, представляя большое генетическое разнообразие гибридов (2, 3). Далее коммерческое выращивание чайного растения распространилось на юг Турции, а также в более северные регионы Северо-Западного Кавказа. Важным этапом в распространении чайного растения на Северо-Западном Кавказе стало появление сорта Колхида. Этот сорт, признанный лучшим, был выведен в 1939 году грузинскими селекционерами М.В. Колелейшвили и Т.Д. Мутовкиной (4) методом клоновой селекции на основе китайской крупнолистной разновидности. Сорт имеет крупные светло-зеленые листья, относится к южной разновидности чая, характеризуется ранней весенней вегетацией, высокой урожайностью (около 8870 кг/га, что на 50 % больше, чем у других районированных в Российской Федерации сортов) (5).
Коллекции зародышевой плазмы сельскохозяйственных культур за пределами основных регионов выращивания служат ценным материалом для селекции на повышение устойчивости к различным агроклиматическим условиям (6, 7). Изучение зародышевой плазмы чая и анализ генетического разнообразия этой культуры в регионах Северо-Западного Кавказа могут прояснить механизмы адаптации растений в нетипичных условиях произрастания и необходимы для надлежащего использования генетических ресурсов (8-10).
За последнее десятилетие в мировых исследованиях по структурной геномике чайного растения достигнуты значительные успехи. На сегодняшний день доступны последовательности референсных ядерных (11-14) и хлоропластных (15-18) геномов чайного растения и создано несколько геномных баз данных (19-21). Эти результаты способствуют разработке надежных генетических маркеров и углубленному описанию мировых генетических ресурсов чайного растения, что, в свою очередь, позволит усовершенствовать стратегии селекции для обеспечения устойчивого развития чайной промышленности и распространения культуры в новых экологических условиях (22, 23). Для характеристики генетического разнообразия коллекций чая разработаны и применяются различные наборы молекулярных маркеров (24).
Северо-Западный Кавказ России как один из самых северных регионов промышленного чаеводства в мире может быть источником наиболее морозостойких форм чая. Однако до сих пор отсутствует понимание генетического разнообразия местных чайных плантаций, их молекулярно-генетическое описание, неизвестно происхождение местных сортов и форм. Велика потребность в расширении и поддержании местных коллекций гермоплазмы, их морфобиологического и молекулярно-генетического описания.
Ранее мы оценили генетическое разнообразие коллекции перспективных сортов и мутантных форм чая, произрастающих в нашем регионе, на основе различий в длине амплифицированных фрагментов при использовании SSR (Simple Sequence Repeat) и SCoT (Start Codon Target Polymorphism) маркеров (6). Однако некоторые авторы считают, что структурные полиморфизмы (Single Nucleotide Polymorphisms — SNPs, InDels) обладают более высоким потенциалом и надежностью при анализе генетического разнообразия и разработке паспортов селекционных форм чая по сравнению с полиморфизмами длин амплифицированных фрагментов (11, 25). Кроме того, в связи с высокой гетерозиготностью чайного растения (11) более эффективной может быть разработка молекулярных паспортов на основе пластидного генома (26). Генетическая информация, присутствующая в пластидной ДНК, представляет большой интерес для популяционной генетики, в основном из-за неменделевского способа наследования этих геномов (27). Кольцевая молекула хпДНК структурно высококонсервативна, что позволило разработать так называемые универсальные пары праймеров, которые могут амплифицировать некодирующие области у большинства растений (28). Сложность этого приема генотипирования и паспортизации может быть связана с поиском подходящего локуса в пластидном геноме с достаточным уровнем внутривидового полиморфизма, что позволило бы дифференцировать и идентифицировать отдельные сорта в пределах одного вида (26).
В настоящем исследовании нами впервые установлены праймеры для хлоропластного генома, которые эффективны при анализе внутривидовых полиморфизмов чайного растения; выполнен анализ генетического разнообразия базовой коллекции и местных производственных плантаций чая; выявлены генотип-специфичные полиморфизмы для характеристики ценных сортов. Полученные результаты будут способствовать разработке современных программ селекции чая и будущих стратегий сохранения зародышевой плазмы чайного растения.
Цель работы — определить информативность SNP и InDel маркеров при выявлении структурных полиморфизмов в ядерной и хлоропластной ДНК для оценки биоразнообразия отечественной популяции растений чая.
Методика . Растительный материал и выделение тотальной ДНК. Исследования были выполнены в 2024 году. Растительный материал для анализа отбирали из базовой коллекции гермоплазмы ФИЦ СНЦ РАН, г. Сочи, Россия (44 растения — г. Сочи, п. Уч-Дере, 1 растение — Республика Адыгея, п. Цветочный) и на четырех производственных плантациях чая (9-15 растений на каждой плантации) (агломерации г. Сочи). Российские производственные плантации были заложены в 1930-х годах семенами, привезенными в основном из Грузии и Китая, и поддерживаются путем естественного восстановления при перекрестном опылении (не исключено, что и при самоопылении) (29). Дополнительно анализировали образцы с промышленных плантации в Республике Абхазия (9 растений) и на Шри-Ланке (20 растений). Каждое выбранное для исследования растение в пределах одной популяции (базовая коллекция, плантация) располагалось на расстоянии не менее 10 м от другого выбранного растения. С каждого такого растения брали один зрелый здоровый лист из верхней части кроны (одно растение — один лист/образец) для выделения полногеномной ДНК.
Образцы из Республики Абхазия и Шри-Ланки получали в высушенном виде. Остальные образцы до выделения ДНК хранили при +4 °С не более 1 нед. Листовой материал (50-100 мг) растирали в жидком азоте с последующей экстракцией по протоколу CTAB (30). Качество полученных образцов ДНК проверяли с помощью электрофореза в агарозном геле и спектрофотометрически по OD 260/280 (BioDrop ^Lite, «Biodrop, Ltd.», Великобритания). Образцы ДНК разводили DEPC-водой для ПЦР до концентрации 20 нг/мкл и хранили при -20 °С.
Праймеры для амплификации фрагментов ядерной и хлоропластной ДНК и условия ПЦР. Праймеры для ядерной ДНК были разработаны нами на основе геномов образцов из базовой коллекции — сорта Колхида (г. Сочи, п. Уч-Дере) и формы A2019 (адыгейская морозостойкая форма, Республика Адыгея, п. Цветочный) , . Учитывали следующие критерии: пара праймеров должна выявлять полиморфизмы, различающие A2019 и сорт Колхида, обеспечивать формирование одной четкой полосы, соответствующей ожидаемому размеру ПЦР-фрагмента при гель-электро-форезе (500-900 п.н., что оптимально для секвенирования по Сэнгеру). Во всей выборке растений праймеры должны обеспечивать высокое качество получаемых сиквенсов и выявлять полиморфные сайты. Из шести разработанных пар праймеров пара SNP3A (F 5´-AGGTCATTCCAAACAACCCCT-3´, R 5´-TGACATTTACCGCAATGATCCTC-3´) соответствовала всем этим требованиям, генерировала фрагмент размером 606 п.н. и была выбрана для амплификации фрагментов геномной ДНК всех исследуемых образцов.
Для анализа полиморфизмов хлоропластной ДНК тестировали 8 пар универсальных праймеров для генотипирования цветковых растений:
Пара праймеров [Нуклеотидная последовательность 5' ^ 3'| Размер продукта, п.н. | Ссылка
|
23S,4.5S/32S, 5S |
F TCTCCTCCGACTTCCCTAG; R ACCATGAACGAGGAAAGGC |
400-430 |
(25) |
|
16S |
F ATTGCGTCGTTGTGCCTGG; R GATACGTTGTTAGGTGCTCC |
350-370 |
(25) |
|
petB/petD |
F TAGGGGGAATTACACTTAC; R CATTAACATGAATACGGCAG |
490-500 |
(25) |
|
rpl23/rpl2.l |
F GAAGAAGCTTGTACAGTTTGG; R TTTACTTACGGCGACGAAG |
490-500 |
(25) |
|
rpl2 intron |
F ATTGAGTTCAGTAGTTCCTC; R CCAAACTGTACAAGCTTCTTC |
430-520 |
(25) |
|
rpoC1 intron |
F GAGTAACATGAAGCTCAG; R GTTTCCTTTCATCCGGCT |
540-670 |
(25) |
|
trnK intron |
F GTCTACATCATCGGTAGAG; R CAACCCAATCGCTCTTTTG |
430-500 |
(25) |
|
trnE-UUC/trnT-GUU |
F TCCTGAACCACTAGACGATG; R ATGGCGTTACTCTACCACTG |
834 |
(16) |
ПЦР-смесь объемом 50 мкл состояла из 25 мкл 2½ HS-TaqPCR реакционного буфера (ООО «Биолабмикс», Россия), содержащего Hot Start Taq-полимеразу, 0,5 мкл каждого праймера (10 мкМ), 2 мкл ДНК матрицы (20 нг/мкл) и DEPC-воды для ПЦР. Амплификацию (термоциклер LightCycler® 96, «Roche», Германия) проводили в следующем режиме: начальная денатурация при 95 °С в течение 4 мин; 30 циклов — плавление при 94 °С 30 с, отжиг при 58 °С для хлоропластной ДНК и 60 °С для ядерной ДНК в течение 30 с, элонгация при 72 °С 30 с; финальная элонгация при 72 °C 7 мин. Полученные ПЦР-продукты визуализировали с помощью электрофореза в 2 % агарозном геле в 1 % буфере TAE при 90 В в течение 2 ч для подтверждения наличия четких одиночных полос.
Очистка и секвенирование по Сэнгеру, анализ данных. Ферментативную очистку ампликонов проводили с использованием экзонуклеазы I (ExoI) и щелочной фосфатазы (Sap). По 1 ед. каждого фермента добавляли к образцу и инкубировали 15 мин при 37 °С, затем ферменты инактивировали при 85 °С в течение 15 мин.
Секвенирование проводили на генетическом анализаторе ABI3500xl («ThermoFisher Scientific», США) с использованием набора BrilliantDye v3.1 («NIMAGEN», Нидерланды) в соответствии с инструкциями к набору. Полученные последовательности анализировали с помощью программы mafft add с опцией выравнивания полноразмерных последовательностей с MSA . Парное выравнивание между сортом Колхида и формой A2019 рассматривали как существующее выравнивание, последовательности остальных генотипов добавляли к указанному выравниванию в качестве новых с опцией сохранения длины выравнивания. Затем полученное выравнивание обрабатывали с помощью gblocks с мягкими параметрами . Для менее строгого отбора использовали следующие опции: разрешить меньшие длины конечных блоков, разрешить пробелы внутри конечных блоков, разрешить менее строгие позиции фланкирования. Последовательности низкого качества с длинными пробелами удаляли из полученных выравниваний с помощью MEGA-X .
После преобразования данных в файл fasta выполняли анализ методом главных компонент (PCA) и кластеризацию k-средних на основе алгоритма Neighbor Joining в программе Past .
Качество маркеров также оценивали с помощью инструментов GeneAlex 6.5 (31) и IMEC (32). Для каждого выявленного полиморфизма были рассчитаны следующие параметры информативности h, PIC и D. Генетическое разнообразие h = 1 - (p2 + q2), где p — частота полиморфизма и q = 1 - p. Для полиморфизмов ядерной ДНК показатель h соответствует ожидаемой гетерозиготности, для хлоропластных (гаплоидных) полиморфизмов отражает гаплотипическое разнообразие. PIC (polymorphism information content) = 1 - E p i 2 - EE p i 2 p / 2 ; PIC выражает вероятность того, что генотип потомка по этому маркеру позволит установить (при отсутствии кроссинговера), какой из двух аллельных вариантов маркера он унаследовал от каждого из родителей. Дискриминирующая способность D (discriminatory power) = 1 - E p i [(Np i - 1)/(N - 1)]; D представляет собой вероятность того, что две случайно выбранные особи имеют разные паттерны аллелей и, таким образом, отличаются друг от друга (32).
Результаты . Материалом для исследования послужили листья коллекционных растений чая и растений с длительно эксплуатируемых местных производственных плантаций (рис. 1, табл. 1). Внешними контролями были высушенные листья растений чая, полученные с промышленных плантаций в Республике Абхазия, то есть находящихся на относительно небольшом географическом удалении, и на Шри-Ланке. В качестве внутренних контрольных генотипов выступали эталонный местный сорт Колхида (г. Сочи, п. Уч-Дере) и морозостойкая форма А2019 (Республика Адыгея, п. Цветочный) из базовой коллекции ФИЦ СНЦ РАН.
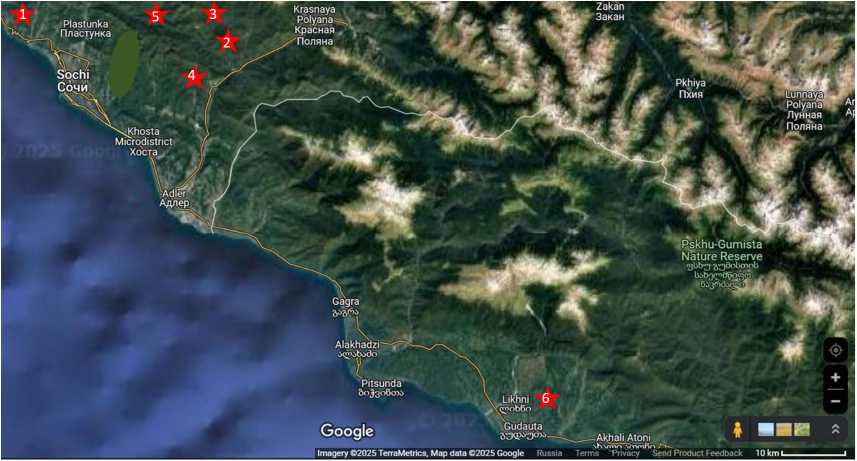
Рис. 1. Расположение популяций чая Camellia sinensis (L.) Kuntze, включенных в исследование (отмечены звездочками, номера соответствуют номеру популяции в таблице 1).
1. Географическое положение популяций чая Camellia sinensis (L.) Kuntze, включенных в исследование (2024 год)
|
¹ популяции |
Место произрастания |
Число образцов |
Тип гермоплазмы |
Координаты места сбора образцов |
1 ФИЦ СНЦ РАН г. Сочи п. Уч-Дере (базовая коллекция) Адыгейский филиал ФИЦ СНЦ РАН, Республика Адыгея, п. Цветочный (базовая коллекция)
2 г. Сочи, п. Калиновое озеро (нижние тер расы, производственная плантация ¹ 1)
44 Вегетативно размно- 43°40'59"N 39°38'12"W женные сорта и формы
1 Вегетативно размно- 44°29'45"N 40°08'18"W женная формыа
-
3 г. Сочи, п. Калиновое озеро (верхние тер
расы, производственная плантация ¹ 2)
-
4 г. Сочи, с. Прогресс (производственная
плантация ¹ 3)
-
5 г. Сочи, с. Семеновка (производственная
плантация ¹ 4)
-
6 Абхазия (Гудаутский район, с. Лыхны)
-
7 Шри-Ланка (г. Нувара Элии)
|
Продолжение таблицы 1 |
||
|
15 |
Гибриды от свободного опыления |
43°37'29"N 39°52'18"W |
|
10 |
Гибриды от свободного опыления |
43°36'19"N 39°49'28"W |
|
15 |
Гибриды от свободного опыления |
43°11'45"N 40°38'21"W |
|
9 |
Гибриды от свободного опыления |
43"ir46"N 40°38'21"W |
|
20 |
Гибриды от свободного опыления |
7°08'13"N 81°03'43"E |
Базовая коллекция чая (вегетативно размноженная) высажена в 1980-х годах и представлена местными сортами, гибридами и мутантными формами (рис. 2, табл. 2).

Рис. 2. Базовая коллекция гермоплазмы чая ФИЦ СНЦ РАН (г. Сочи, 2024 год) , включенная в исследование. На фото типичный зрелый лист каждого генотипа.
2. Характеристика базовой коллекции гермоплазмы чая Camellia sinensis (L.) Kuntze ФИЦ СНЦ РАН (2024 год)
|
Образец |
Происхождение |
Площадь листа, см2 |
Стандартное отклонение ± SD |
Содержание 2С ДНК, пг |
|
Форма ¹ 502 |
γ -Радиомутант сорта Колхида |
57,7 |
6,3 |
5,7 |
|
Форма ¹ 69 |
Клоновая селекция |
66,5 |
7,3 |
5,8 |
|
Форма ¹ 1385 |
γ -Радиомутант |
83,8 |
9,2 |
6,2 |
|
Форма ¹ 35 |
Клоновая селекция |
35,2 |
3,9 |
6,5 |
|
Форма ¹ 19 |
Клоновая селекция |
35,7 |
3,9 |
6,6 |
|
Форма ¹ 121 |
Клоновая селекция |
34,7 |
3,8 |
6,6 |
|
Форма ¹ 507 |
γ -Радиомутант |
40,8 |
4,5 |
6,6 |
|
Форма ¹ 536 |
γ -Радиомутант |
68,7 |
7,6 |
6,6 |
|
Форма ¹ 4605 |
γ -Радиомутант |
52,7 |
5,8 |
6,7 |
|
Форма ¹ 3986 |
γ -Радиомутант |
58,2 |
6,4 |
6,8 |
|
Форма ¹ 36 |
Клоновая селекция |
59,1 |
6,5 |
6,9 |
|
Форма ¹ 125 |
Клоновая селекция |
85,2 |
9,4 |
6,9 |
|
Форма ¹ 551 |
Форма/ γ -радиомутант |
65,6 |
7,2 |
6,9 |
|
Форма ¹ 855 |
Химический мутант |
55,6 |
6,1 |
6,9 |
|
Форма ¹ 57 |
Клоновая селекция |
70,0 |
7,7 |
7,0 |
|
Форма ¹ 837 |
γ -Радиомутант |
66,6 |
7,3 |
7,0 |
|
Форма ¹ 3574 |
γ -Радиомутант |
46,1 |
5,1 |
7,0 |
|
Сорт Колхида |
Клоновая селекция |
65,3 |
7,2 |
7,0 |
|
Сорт Сочи |
Сорт/клоновая селекция |
52,1 |
5,7 |
7,0 |
|
Продолжение таблицы 2 |
||||
|
Сорт Грузинский 15 |
Контролируемая гибридизация |
34,2 |
4,2 |
7,0 |
|
Форма А2019 |
Клоновая селекция |
33,6 |
4,5 |
7,0 |
|
Форма ¹ 316 |
γ -Радиомутант, п. Кимынь |
97,3 |
10,7 |
7,1 |
|
Форма ¹ 1018 |
γ -Радиомутант |
52,7 |
5,8 |
7,1 |
|
Форма ¹ 1877 |
γ -Радиомутант |
70,6 |
7,8 |
7,1 |
|
Форма ¹ 582 |
γ -Радиомутант |
71,0 |
7,8 |
7,3 |
|
Форма ¹ 527 |
γ -Радиомутант |
57,4 |
6,3 |
7,3 |
|
Форма ¹ 1405 |
γ -Радиомутант |
69,8 |
7,7 |
7,3 |
|
Форма ¹ 53 |
Клоновая селекция |
63,3 |
7,0 |
7,4 |
|
Форма ¹ 62 |
Клоновая селекция |
68,8 |
7,6 |
7,4 |
|
Форма ¹ 2264 |
Химический мутант |
52,4 |
5,8 |
7,4 |
|
Сорт Каратум |
Клоновая селекция |
83,3 |
9,2 |
7,4 |
|
Форма ¹ 2697 |
γ -Радиомутант, п. Кимынь |
112,3 |
12,4 |
7,5 |
|
Форма ¹ 1467 |
γ -Радиомутант |
74,9 |
8,2 |
7,7 |
|
Форма ¹ 1484 |
γ -Радиомутант |
34,3 |
3,8 |
7,7 |
|
Форма ¹ 321 |
γ -Радиомутант |
70,3 |
7,7 |
7,8 |
|
Форма ¹ 1102 |
γ -Радиомутант |
92,4 |
10,2 |
7,8 |
|
Форма ¹ 1292 |
γ -Радиомутант |
75,0 |
8,3 |
7,9 |
|
Форма ¹ 3509 |
γ -Радиомутант |
54,9 |
6,0 |
8,0 |
|
Форма ¹ 212 |
Клоновая селекция |
84,6 |
9,3 |
8,1 |
|
Форма ¹ 501 |
γ -Радиомутант семян сорта Колхида |
71,0 |
7,8 |
8,1 |
|
Форма ¹ 50 |
Клоновая селекция |
71,0 |
7,6 |
8,3 |
|
Форма ¹ 56 |
Клоновая селекция |
73,1 |
8,0 |
8,5 |
|
Форма ¹ 1326 |
γ -Радиомутант |
70,1 |
7,7 |
8,6 |
|
Сорт Кубанский |
Клоновая селекция |
36,6 |
4,0 |
8,7 |
|
Форма ¹ 619 |
γ -Радиомутант семян сорта Колхида |
149,1 |
16,4 |
10,8 |
Тестирование универсальных праймеров для хлоропластного генома цветковых растений. Для анализа использовали тестовую выборку из 12 образцов, в которую вошли 9 коллекционных, включая сорт Колхида и форму A2019 (внутренние группы сравнения), а также два образца из Шри-Ланки (внешняя группа сравнения) (рис. 3, табл. 3).
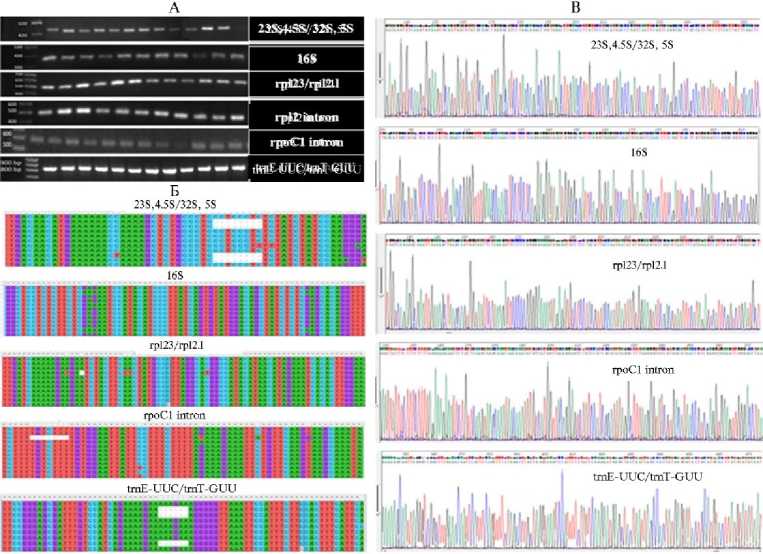
Рис. 3. Результаты амплификации, секвенирования фрагментов хлоропластной ДНК и поиска полиморфизмов у растений чая Camellia sinensis (L.) Kuntze при использовании разных праймеров .
А: ампликоны слева направо — образцы ¹ 619, ¹ 582, ¹ 2697, сорт Сочи, сорт Кубанский, сорт Колхида, ¹ 316, сорт Грузинский 15, Шри-Ланка 1, Шри-Ланка 2, сорт Каратум, форма A2019.
Б: файлы выравнивания показывают примеры найденных сайтов полиморфизма у пяти наиболее эффективных пар хлоропластных праймеров.
В: фрагменты хроматограмм представлены для образца ¹ 2697, который характеризовался наибольшим числом уникальных полиморфизмов (г. Сочи, 2024 год).
3. Эффективность амплификации и число полиморфизмов во фрагментах хлоропластной ДНК в тестовой выборке образцов чая Camellia sinensis (L.) Kuntze ( n =12, г. Сочи, 2024 год)
|
Пара праймеров |
Длина фрагмента, п.н. |
Число сайтов |
Число уникальных сайтов |
Доля образцов с полиморфизмами, % |
||
|
SNPs |
InDel |
SNPs |
InDels |
|||
|
23S,4.5S/32S, 5S |
358 |
7 |
2 |
6 |
1 |
44 |
|
16S |
321 |
3 |
1 |
0 |
1 |
30 |
|
rpl23/rpl2.l |
443 |
7 |
2 |
7 |
2 |
18 |
|
rpl2 intron |
433 |
0 |
0 |
0 |
0 |
0 |
|
rpoC1 intron |
526 |
10 |
0 |
2 |
0 |
45 |
|
trnE-UUC/trnT-GUU |
504 |
1 |
3 |
0 |
0 |
60 |
Примечание. Представлены результат для образцов ¹ 619, ¹ 582, ¹ 2697, сорт Сочи, сорт Кубанский, сорт Колхида, ¹ 316, сорт Грузинский 15, Шри-Ланка 1, Шри-Ланка 2, сорт Каратум, форма A2019.
Указана длина фрагмента после удаления некачественных прочтений.
Из восьми пар универсальных праймеров для хлоропластной ДНК только с шестью были получены продукты амплификации. Исключение составили пары праймеров PetB/PetD и TrnK intron. Из шести пар праймеров пять пар позволили выявить структурные полиморфизмы внутри вида C. sinensis (см. рис. 3, табл. 3).
Наибольшее число фрагментов с полиморфизмами генерировала пара праймеров trnE-UUC/trnT-GUU, в этом варианте доля образцов с выявленными полиморфизмами в тестовой выборке составила 60 % (см. табл. 3). У сорта Каратум были обнаружены уникальные InDel полиморфизмы при использовании праймеров 16S и rpl23/rpl2.l. У образца ¹ 2697 с помощью пары праймеров 23S,4.5S/32S, 5S был обнаружен уникальный InDel полиморфизм и пять уникальных SNPs. У сорта Сочи праймеры rpoC1 intron позволили обнаружить уникальный SNP. У образца ¹ 582 один уникальный SNP полиморфизм найден с помощью праймеров 23S,4.5S/32S, 5S, второй — с праймерами rpoC1 intron. В связи с тем, что пара праймеров trnE-UUC/trnT-GUU оказалась наиболее эффективной на тестовой выборке из 12 образцов, ее использовали в дальнейшем при анализе расширенных выборок, включающих образцы из базовой коллекции и популяций производственных плантаций.
Распределение и характеристика полиморфизмов, выявляемых с ядерными и хлоропластными праймерами в выборке растений чая из базовой коллекции и производственных плантаций. Сформированная выборка состояла из 110 образов, взятых из базовой коллекции и с плантаций (табл. 4). На основе данных для 89 образцов с помощью пары праймеров для ядерной ДНК (фрагмент 606 п.н.) было выявлено восемь SNPs. Среди них четыре SNPs были специфичны для сорта Колхида (позиции 210A/G, 355T/C, 369A/C, 582T/G) (см. дополнительные материалы на сайте , остальные четыре SNPs были полиморфными в анализируемой выборке (позиции 98T/C, 240A/G, 305G/A, 357C/T). Для полиморфизмов 98T/C, 305G/A и 357C/T анализ показал наиболее высокие значения h и D (h = 0,41-0,43, D = 0,90-0,92). Для полиморфизма 240A/G значения h и D оказались наименьшими — соответственно 0,086 и 0,089 (см. табл. 4).
При анализе 110 образцов с помощью хлоропластных праймеров trnE-UUC/trnT-GUU (генерация фрагмента 504 п.н.) обнаружили три полиморфизма, включая два InDel — с делецией одного нуклеотида Т (T/Del1) и с делеций 5 нуклеотидов Т (T/Del5), а также один SNP (А/G). Среди них полиморфизм T/Del1 показал самый высокий индекс дискриминационной способности D = 0,68.
Значение PIC для всех выявленных полиморфизмов варьировало в диапазоне от 0,4 до 0,6. При этом следует отметить, что значения PIC для хлоропластных маркеров в целом были выше, чем для маркеров ядерной ДНК (см. табл. 4).
4. Параметры информативности полиморфизмов, выявленных с помощью наиболее эффективных праймеров ядерной и хлоропластной ДНК в базовой коллекции и в популяциях производственных плантаций чая Camellia sinensis (L.) Kuntze (г. Сочи, 2024 год)
|
Полиморфизм |
1 h 1 |
PIC 1 |
D |
|
Фрагмент ядер |
ной ДНК |
||
|
Позиция SNP: |
|||
|
98T/C |
0,42267 |
0,40840 |
0,91037 |
|
240A/G |
0,08584 |
0,49404 |
0,08836 |
|
305G/A |
0,41358 |
0,41220 |
0,91701 |
|
357C/T |
0,43126 |
0,40474 |
0,90347 |
|
Ф |
рагмент хлороп |
ластной ДНК |
|
|
T/Del1 |
0,49190 |
0,49442 |
0,68457 |
|
T/Del5 |
0,20843 |
0,59368 |
0,22335 |
|
SNPA/G |
0,32000 |
0,56420 |
0,36147 |
Примечание. h — уровень генетического/гаплотипического разнообразия, PIC — информационное содержание полиморфизма, D — дискриминационная способность маркера. Для анализа хлоропластной ДНК использовали пару праймеров trnE-UUC/trnT-GUU, проанализировано 110 образцов, взятых из базовой коллекции и с плантаций; для анализа ядерной ДНК использовали разработанные нами праймеры SNP3A, проанализировано 89 образцов из той же выборки.
Внутрипопуляционное генетическое разнообразие у изученных образцов растений чая. Для понимания генетического разнообразия внутри каждой популяции, оценивали на основании доли полиморфных локусов (P, %) и величины h (табл. 5, качество сиквенсов ядер-ной ДНК для образцов из Шри-Ланки оказалось недостаточным для включения в анализ). Средний уровень полиморфизма в исследованных популяциях составил P = 83 % (для фрагментов ядерной ДНК) и P = 62 % (для фрагментов хлоропластной ДНК). Наибольший полиморфизм (P = 100 % как по ядерным полиморфизмам, так и по хлоропластным) был выявлен в образцах базовой коллекции и на производственных плантациях в п. Калиновое озеро (нижняя и верхняя террасы). Это свидетельствует о сохранении высокого генетического разнообразия в указанных локациях. Наименьшей генетической вариабельностью отмечены плантации в с. Прогресс и в Республике Абхазия, где для хлоропластной ДНК параметры P и h равнялись нулю, а для ядерной ДНК оставались самыми низкими (P = 75 %, h = 0,093 для с. Прогресс; P = 50 %, h = 0,204 для Республики Абхазия). Это может объясняться разными способами наследования маркеров. Хлоропластная ДНК наследуется унипарентально (материнская линия), и если все растения в популяции происходят от одного материнского растения (например, при вегетативном размножении), то гаплотипы будут идентичны, что дает низкое генетическое разнообразие. Ядерная ДНК наследуется бипарентально и может сохранять некоторый уровень разнообразия за счет рекомбинации, даже если популяция основана небольшим числом родительских особей.
5. Внутрипопуляционное генетическое разнообразие растений чая Camellia sinensis (L.) Kuntze, выявляемое на основании полиморфизмов ядерной и хлоропластной ДНК (2024 год)
|
Популяция |
Ядерная ДНК |
Хлоропластная ДНК |
|
n P, % п h |
n P, % и h |
ФИЦ СНЦ РАН г. Сочи, п. Уч-Дере
(базовая коллекция) 33 100 0,335 32 100 0,330
г. Сочи, п. Калиновое озеро (нижние тер расы, производственная плантация ¹ 1) 9 100 0,401 9 100 0,346
Продолжение таблицы 5
г. Сочи, п. Калиновое озеро (верхние тер-
|
расы, производственная плантация ¹ 2) |
15 |
100 |
0,286 |
15 |
100 |
0,267 |
|
г. Сочи, с. Прогресс (производственная плантация ¹ 3) |
10 |
75 |
0,093 |
10 |
0 |
0,000 |
|
г. Сочи, с. Семеновка (производственная плантация ¹ 4) |
15 |
75 |
0,305 |
15 |
67 |
0,201 |
|
Республика Абхазия (Гудаутский район, с. Лыхны) |
7 |
50 |
0,204 |
9 |
0 |
0,000 |
|
Шри-Ланка (г. Нувара Элии) |
Нет данных |
20 |
67 |
0,139 |
||
|
M ± SEM |
83±8 |
0,271±0,036 |
62±17 |
0,183±0,041 |
||
Примечание. n — размер выборки, P — уровень полиморфизма в группе, h — уровень генетического разнообразия в группе, M — среднее значение, ± SEM — стандартная ошибка среднего значения. Для анализа хлоропластной ДНК использовали пару праймеров trnE-UUC/trnT-GUU, для анализа ядерной — разработанные нами праймеры SNP3A. Качество сиквенсов образцов из Шри-Ланки для анализа ядерной ДНК было неудовлетворительным для дальнейшего анализа.
Построение филогенетических древ изученных популяций чая Camellia sinensis (L.) Kuntze и их распределение в координатах PCA. С помощью полиморфизмов, выявленных с помощью праймеров для хлоропластной ДНК (trnE-UUC/trnT-GUU, три полиморфизма) и ядерной ДНК (SNP3A, четыре полиморфизма) (см. табл. 4), был проведен анализ генетического разнообразия изученных популяций чая во влажных субтропиках России. Методом Neighbor Joining на основе трех полиморфизмов хлоропластной ДНК выявили две большие группы образцов. Половина выборки всех генотипов, включая образцы с производственных плантаций, образцы из Республики Абхазия и из с. Прогресс, сформировали одну группу, в которой генетические дистанции между образцами практически отсутствуют (рис. 4, вверху слева). Вторая группа разделилась на три основные подгруппы. Первая подгруппа включала образцы из Шри-Ланки и семь образцов из базовой коллекции ФИЦ СНЦ РАН (¹ 527, ¹ 2697, ¹ 582, ¹ 212, ¹ 507, ¹ 3823, ¹ 837). Вторая подгруппа объединила морозоустойчивую форму A2019 и 12 образцов с коммерческих плантаций с. Семеновка, п. Калиновое озеро и 5 образцов из базовой коллекции (¹ 19, ¹ 35, ¹ 1467, ¹ 316 и ¹ 1385). В третьей подгруппе объединились сорт Колхида и 12 других образцов из базовой коллекции (¹ 855, ¹ 2254, ¹ 502, ¹ 501, ¹ 855, ¹ 1326, ¹ 321, ¹ 1877, ¹ 157, сорт Грузинский 15, ¹ 619 и ¹ 546). Пять образцов из Шри-Ланки также попали в эту подгруппу. Кроме того, образцы из базовой коллекции ¹ 136, ¹ 4605 и два образца из п. Калиновое озеро располагались отдельно от всех остальных.
На основе четырех полиморфизмов ядерных ДНК с помощью метода Neighbor Joining все образцы были также разделены на две ветви. Одна показала более высокое разнообразие и включала в основном образцы из п. Калиновое озеро, а также несколько образцов из с. Прогресс, Республики Абхазия и базовой коллекции (сорта Колхида, Грузинский 15; формы ¹ 3823, ¹ 502, а также морозостойкая форма A2019). Остальные генотипы сформировали вторую ветвь с низким уровнем разнообразия (см. рис. 4, вверху по центру).
При объединении данных по полиморфизмам хлоропластного и ядерного фрагментов геномов для анализа, часть последовательностей удаляли из-за низкого качества прочтений. Построение филогенетического дерева, с учетом одновременно ядерных и хлоропластных полиморфизмов показало, что большинство образцов из Республики Абхазия схожи друг с другом, но генетически далеки от генотипов насаждений чая, расположенных в агломерации г. Сочи (с. Прогресс, с. Семеновка, п. Калиновое озеро). Наибольшее сходство наблюдалось у образцов из с. Прогресс, наименьшее — в производственных насаждениях в п. Калиновое озеро и с. Семеновка.
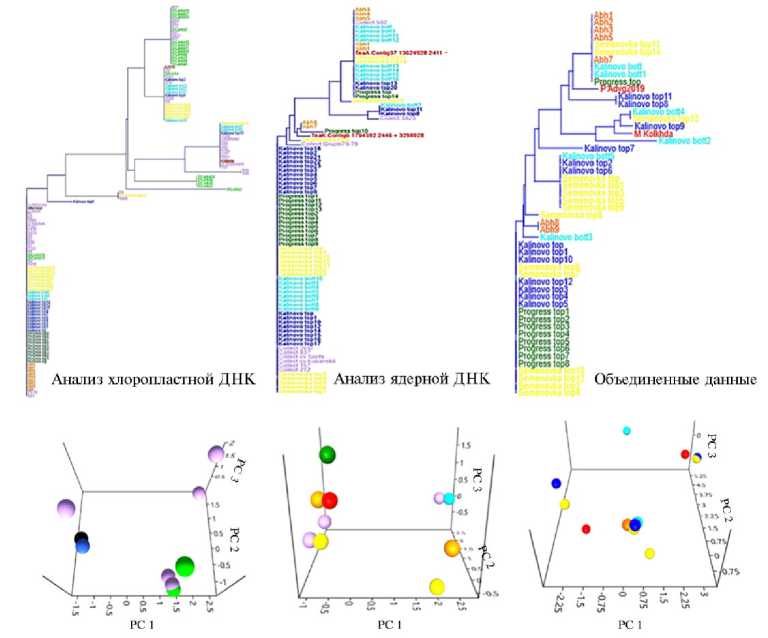
Рис. 4. Кластеризация образов из исследованных популяций растений чая Camellia sinensis (L.) (2024 год) на основе полиморфизмов фрагментов ядерной и хлоропластной ДНК : сверху — филогенетическое дерево, построенное по методу Neighbor Joining для каждого типа маркеров и их сочетания; снизу — соответствующие результаты PCA-анализа популяций растений чая, включенных в исследование. Описание популяций см. в таблицах 1 и 5. Разные цвета показывают разные популяции чая и отображаются на филогенетических деревьях и на PCA-диаграммах: оранжевый цвет — образцы из Республики Абхазия, желтый — с. Семеновка, голубой — п. Калиновое озеро (нижние террасы), синий — п. Калиновое озеро (верхние террасы), зеленый — с. Прогресс, сиреневый — базовая коллекция, салатовый — образцы из Шри Ланки. Красным цветом обозначены элитный сорт Колхида (г. Сочи) и морозостойкий генотип А2019 (Республика Адыгея, п. Цветочный) (внутренние контроли).
Данные PCA-анализа (см. рис. 4) согласуются с результатами кластеризации методом Neighbor Joining. В частности, на основе данных о полиморфизмах хлоропластной ДНК выявлены значимые генетические дистанции между образцами в базовой коллекции гермоплазмы, что свидетельствует о разных материнских линиях, от которых получены эти генотипы. Эти результаты подтверждаются анализом полиморфизма фрагментов геномной ДНК. Кроме того, популяции из п. Калиновое озеро и с. Семеновка по данным PCA-анализа показали наибольший уровень генетического разнообразия.
Полученные нами результаты представляют собой первое сообщение о генетическом разнообразии коммерческих чайных плантаций на Западном Кавказе — северной границе промышленного возделывания культуры. Самое высокое разнообразие, выявленное в популяциях п. Калиновое озеро (P = 100 % по обоим типам маркеров), может быть следствием как исходной гетерогенности посадочного материала, так и длительным возделыванием, которое могло сопровождаться накоплением соматических мутаций или спонтанной гибридизацией. Поддержание такого разнообразия имеет важное значение для адаптивного потенциала культуры в условиях меняющегося климата и для будущих селекционных программ, поскольку служит источником ценных аллелей (29). Обращает на себя внимание генетическая близость образцов из Республики Абхазия к части сочинских производственных популяций при их низком разнообразии (с. Прогресс) по данным полиморфизма хлоропластной ДНК. Это может указывать на общее происхождение материнских линий, вероятно, связанное с историей интродукции чая в регион. В то же время гетерогенность образцов из Шри-Ланки, распределившихся по разным подгруппам при кластерном анализе хлоропластной ДНК, отражает сложную генетическую структуру популяций Camellia sinensis на острове. Формирование цейлонского генофонда происходило на основе нескольких интродукций из Китая и Индии (Ассам), что привело к накоплению генетического разнообразия (33, 34). В нашем опыте отсутствие генетического сходства образцов из Шри-Ланки с большинством местных популяций подтверждает, что интродукционный материал для Черноморского побережья Кавказа имел иное, скорее всего китайское, происхождение.
Для анализа структурных полиморфизмов в амплифицированных фрагментах ядерной и хлоропластной ДНК растений мы использовали наиболее надежный метод секвенирования по Сэнгеру. Большая часть праймеров, используемых в нашей работе, были разработаны для высококонсервативных регионов в 42 локусах, которые фланкируют более изменчивые внутренние участки. Универсальность амплификации была первоначально подтверждена на 48 видах из таксономически различных семейств высших растений (25). По данным этих исследователей (25), семь праймеров наиболее вариабельны (16S, 23S,4.5S/32S, 5S, PetB/PetD, rpl23/rpl2.l и rpl2 intron), а два других (intron rpoC1 и intron TrnK) предложены как наиболее эффективные универсальные праймеры для дальнейшего изучения. Эти авторы использовали в исследовании температуру отжига всех хлоропластных праймеров 50-55 °C, но в нашей работе использовали отжиг при 58 °C, возможно, по этой причине две пары праймеров (intron TrnK) из восьми не обеспечили амплификацию. Несмотря на небольшой размер выборки в нашей работе, большая часть праймеров характеризовалась наличием нескольких внутривидовых полиморфизмов, что открывает перспективы для использования в качестве инструмента паспортизации отечественных сортов чая.
В исследовании S.C. Lee с соавт. (35) использовали универсальные праймеры хпДНК (trnL, trnL-trnF) и ядерной ДНК; секвенировали ампликоны, полученные для 113 образцов растений чая из Тайваня. Авторы делают вывод, что ядерные праймеры позволяют выявить больше полиморфизмов, чем хлоропластные, следовательно, больше подходят для создания базы данных штрих-кодов ДНК чайного растения (35). Однако наши результаты показали, что у растений чая полиморфизмы хлоропластной ДНК более надежны из-за высокой гетерозиготности ядерной ДНК, которая влияет на качество секвенирования и замедляет обработку полученных данных, увеличивает погрешность анализа и усложняет пробоподготовку ампликонов для секвенирования.
В работах L. Li с соавт. (16) показано, что эволюционные изменения хлоропластного генома Camellia sinensis состояли из повторов и вставок-деле-ций (InDels), а распределение повторов, InDels и SNPs достоверно коррелировало. Китайский (CSS) и индийские (CSA) подвиды чая показали значительные различия в структурных характеристиках хлоропластного генома (16). Полученные результаты также показали, что полиплоидизация влияет на изменение хлоропластной ДНК. Согласно нашим данным, сорта и формы чая с измененной плоидностью, такие как сорт Каратум, формы ¹ 619 и ¹
2697, характеризовались большей частотой структурных полиморфизмов во фрагментах хлоропластной ДНК по сравнению с диплоидными сортами и формами чая. В целом, анализ хлоропластной ДНК выявил три основных гаплотипа в базовой коллекции ФИЦ СНЦ РАН, один из которых был характерен для большей части генотипов из Шри-Ланки. Результаты анализа хлоропластной ДНК указывают на то, что изучаемый набор зародышевой плазмы произошел от трех различных материнских генотипов.
Отметим, что ядерные SNP маркеры успешно использовали другие исследователи для описания коллекций зародышевой плазмы чайного растения. Например, X. Wang c соавт. (36) проанализировали 117 китайских сортов чая, использовав 45 SNP маркеров, чтобы выявить те из них, которые дискриминируют формы CSS и CSA популяций. Они подтвердили, что в Китае подвид CSA в основном распространен в провинции Юньнань, в то время как подвид CSS, вероятно, происходит из Восточного Китая (36). Кроме того, S. Liu с соавт. (37) проанализировали полногеномные полиморфизмы у двух сортов — Shuchazao ( Camellia sinensis var. sinensis ) и Yunkang 10 ( Camellia sinensis var. assamica ) и разработали 48 полиморфных маркеров InDel со средним PIC = 0,457, что сопоставимо с нашими результатами. Исследование этих авторов подтвердило, что генетическая структура зародышевой плазмы, как правило, связана с географическим происхождением образцов (37). Кроме того, C. Lee с соавт. (38) использовали 47 SNPs для анализа генетического разнообразия 137 образцов чая из местной коллекции (гора Ушань, Юго-Западный Китай) и соседних регионов. Отмечено, что местные формы генетически отличаются от местных культурных сортов (38). В другом исследовании 10 маркеров InDel использовались для выяснения происхождения 32 местных сортов чая из Флориды (США) и выбора лучших комбинаций скрещивания для селекции (39).
Таким образом, в результате проведенного нами исследования впервые получены данные о генетическом разнообразии растений чая в зоне влажных субтропиков России. Впервые отмечена эффективность универсальных праймеров хлоропластной ДНК для обнаружения внутривидового полиморфизма у чайного растения, изучены распределение SNPs и InDels во фрагментах хлоропластной и ядерной ДНК и генетическое разнообразие чайных растений в базовой коллекции, а также на производственных плантациях Северо-Западного Кавказа. Впервые выявлены эффективные праймеры для хлоропластной ДНК (trnE-UUC/trnT-GUU, 16S и rpl23/rpl2.l, 23S,4.5S/32S, 5S), позволяющие идентифицировать отечественные сорта чая. Для оценки меж- и внутрипопуляционного генетического разнообразия в производственных насаждениях чая мы впервые применили секвенирование по Сэнгеру для анализа структурных полиморфизмов в амплифициро-ванных фрагментах ДНК. Общий уровень генетического полиморфизма для производственных насаждений в регионе составил около 83 % (для ядерной ДНК) и 62 % (для хлоропластной ДНК). Значение PIC всех выявленных полиморфизмов варьировало от 0,4 до 0,6, при этом значения PIC для хлоропластных ДНК маркеров были выше, чем для ядерных. Полученные результаты дают новые знания о генетическом разнообразии гаплотипов в базовой коллекции ФИЦ СНЦ РАН и в популяциях производственных плантаций чая в самом северном регионе выращивания. Продолжение исследований на большей выборке с расширенным набором молекулярных маркеров будет полезно для разработки молекулярных паспортов форм и сортов отечественной коллекции растений чая. Результаты полного геномного секвенирования для A2019 и сорта Колхида доступны в базах данных (в сборке), а также в arch/project/CNP0004163/ (исходные прочтения), последовательности ампликонов представлены в дополнительных материалах на сайте
1 ФГБНУ Федеральный исследовательский центр Субтропический научный центр РАН,


