Содержание тяжелых металлов в осоке водяной (Carex aquatilis Wahlenb.) прибрежно-водных биоценозов природного парка "Нумто"
Автор: Мурашко Ю.А., Кравченко И.В.
Журнал: Вестник Красноярского государственного аграрного университета @vestnik-kgau
Рубрика: Биологические науки
Статья в выпуске: 8, 2017 года.
Бесплатный доступ
Интерес к исследованию содержания тяже-лых металлов в зеленой массе растений обу-словлен значительной ролью этих элементов в естественных процессах метаболизма рас-тений. В статье представлены результаты исследования количественного содержания тяжёлых металлов (Cr, Mn, Fe, Ni, Cu, Zn, Cd, Pb) в пробах воды реки Казым, пойменных и водораздельных озёр, расположенных в грани-цах особо охраняемой территории Белоярско-го района Ханты-Мансийского автономного округа - Югры - Природного парка «Нумто», а также прибрежно-водной растительности обследованных водоёмов. Пробы воды и при-брежно-водной растительности собраны в ходе комплексной экспедиции на территории природного парка в июле-августе 2016 года на пробных площадках прибрежной зоны модель-ных водоемов с низким уровнем техногенного воздействия. Исследование фонового содер-жания выбранных металлов в водных объек-тах и зеленой массе осоки Carex aquatilis Wahlenb. проводили методом атомной абсорб-ции. Установлено, что Carex aquatilis проявля-ет резистивные свойства по отношению к высоким естественным концентрациям желе-за в окружающей среде, а по отношению к ни-келю наблюдается эффект аккумулирования. Превышение предельно допустимой концен-трации (ПДК) в пробах воды по железу вплоть до 17,8 ПДК не приводит к увеличению его со-держания в зеленой массе Carex aquatilis. При низком содержании растворенного в воде ни-келя (не выше 0,03 ПДК) отмечен эффект его аккумуляции в зелёной массе растений. Наи-большее превышение содержания никеля в фитомассе по сравнению с водой соответст-вующего водоема составляет 5,6 раза.
Тяжелые металлы, вод-ные объекты, прибрежно-водная раститель-ность, аккумуляция, природный парк "нумто"
Короткий адрес: https://sciup.org/140224246
IDR: 140224246 | УДК: 502.4(571.122):574.5:54
The content of heavy metals in Carex aquatilis Wahlenb. of coastal water biocenoses of natural park "Numto"
The interest in the research of heavy metals content in the vegetation is caused by a significant role of these elements in natural processes of plants metabolism. The results of the research of heavy metals quantitative content (Cr, Mn, Fe, Ni, Cu, Zn, Cd, Pb) in the water sampling of the Kazym river, inundated and water separate lakes located in borders of especially protected territory of Beloyarsky Region of Khanty-Mansy Autonomous Area Yugra Natural park “Numto” and also coastal and water vegetation of the analyzed reservoirs are presented in the study. Water and coastal-water vegetation sampling are done during complex ex-pedition on the territory of the natural park in July-August, 2016 on trial platforms of the model reser-voirs coastal zone with the low level of technogenic influence. The research of the background content of the chosen metals in the water bodies and vege-tation of Carex aquatilis Wahlenb. was carried out by the atomic absorption method. It has been es-tablished that Carex aquatilis reveals resistive properties in relation to high natural concentration of iron in the environment and the effect of accumu-lation in relation to nickel. The excess of maximum permissible concentration (MPC) in the iron water tests up to 17.8 the maximum permissible concen-tration limits doesn't lead to the increase in the con-tents of Carex aquatilis herbage. At low content of nickel dissolved in water (not higher than 0.03 max-imum concentration limits), the effect of its accumu-lation in vegetation is noted. The greatest excess of nickel content in the plants biomass in comparison with the water of corresponding reservoir is 5.6 times.
Текст научной статьи Содержание тяжелых металлов в осоке водяной (Carex aquatilis Wahlenb.) прибрежно-водных биоценозов природного парка "Нумто"
Введение. Обязательное присутствие в растениях небольших количеств некоторых тяжелых металлов обусловлено их участием в целом ряде естественных процессов метаболизма, роста и развития. В качестве микроэлементов тяжелые металлы, в частности, могут входить в состав естественных биологических ферментов, которые регулируют белковый, углеводный и жировой обмен, участвовать в синтезе нуклеиновых кислот. Однако при избытке тяжелых металлов в окружающей среде динамическое равновесие нарушается, и те же химические элементы, попадая в растение в значительно больших количествах, уже могут вызывать сильное токсическое действие [3, 4, 9].
Тяжелые металлы поглощаются растениями, произрастающими на суше, водными растениями и растениями, обитающими на «пограничных» территориях водоемов в разных количествах и с разной интенсивностью. Условия обитания, так или иначе, определяют механизм процесса поглощения тяжелых металлов, его длительность и быстроту. Растения, находящиеся на суше, поглощают подвижные формы тяжелых металлов, в основном за счет своего корневого питания из почвы, либо попадающие на поверхность растений из атмосферы в составе сезонных осадков, пыли и т.д. Подвижные формы тяжелых металлов, которые растворены в воде, поглощаются значительно легче, и поэтому виды растений, имеющие длительный контакт с водными объектами, в большей степени подвержены риску возникновения повышенного содержания металлов. Однако растения, постоянно находящиеся в воде и не прикрепленные к грунту, лишены возможности поглощать тяжелые металлы из донных отложений или минералов почвы и могут потреблять эти элементы только из водной среды. Растения, располагающиеся на границе водоемов или в прибрежной зоне, имеющие постоянный контакт с водой и развитую корневую систему, имеют возможность поглощать тяжелые металлы как из почвы, так и из водной среды. Кроме того, прибрежная растительность, находясь в более комфортных условиях, способна образовывать достаточно плотные заросли, превращающиеся в своеобразный накопитель веществ, которые переносятся в форме различных потоков с поверхности суши в водоем либо (в период сезонных паводков) из воды на сушу. Роль накопителя усиливается, когда в составе задерживаемых веществ находятся поллютанты разной природы. Часто в составе загрязняющих веществ присутствуют источники тяжелых металлов. Следовательно, растения, формирующие прибрежный буфер, потенциально могут находиться в условиях наиболее длительного их воздействия. В связи с этим важным является изучение степени накопления тяжелых металлов прибрежно-водной растительностью и выявление ее видов, способных к высокой аккумуляции этих элементов.
Осока является типичным представителем прибрежной растительности, и на ее примере целесообразно рассматривать степень влияния повышенного содержания тяжелых металлов в окружающей среде на их содержание в зеленой массе. Чтобы корректно оценивать фактор воздействия повышенных концентраций тяжелых металлов на растения, необходимо иметь представление о границах нормального содержания этих элементов в растениях чистых «фоновых» территорий.
В качестве чистых мест удобно использовать особо охраняемые природные территории Ханты-Мансийского автономного округа, например
Природный парк «Нумто», расположенный в Белоярском районе Югры. Прибрежно-водные биоценозы водных объектов парка «Нумто» находятся на значительном удалении от крупных промышленных объектов, транспортных магистралей и больших городских поселений и не подвержены риску техногенного загрязнения.
Цель исследования . Оценить содержание тяжелых металлов в зеленой массе надводной части прибрежно-водной растительности водных объектов на территории Природного парка «Нумто».
Задачи исследования : установить присутствие и определить концентрацию подвижных форм тяжелых металлов (хрома, марганца, никеля, железа, меди, цинка, кадмия, свинца) в водных объектах и оценить степень их загрязнения данными элементами; изучить характер накопления тяжелых металлов в органах травянистых прибрежно-водных растений на примере осоки водяной ( Carex aquatilis Wahlenb.) Природного парка «Нумто».
Теоретическая и практическая значимость. С теоретической точки зрения полученная информация об устойчивости Carex aquatilis Wahlenb. к различным естественным концентрациям тяжелых металлов (Cr, Mn, Fe, Ni, Cu, Zn, Cd, Pb) может представлять интерес при исследовании механизма обмена микроэлементами растения с окружающей средой, установлении лимитирующих стадий этого процесса и особенностей переноса тяжелых металлов внутри растения. Индифферентное отношение Carex aquatilis к естественным для водоемов Югры концентрациям тяжелых металлов (Cr, Mn, Cu, Zn, Cd, Pb), ее резистивные свойства к повышенному содержанию растворимых форм железа и эффект аккумулирования по отношению к никелю позволяют лучше понять особенности движения и накопления перечисленных химических элементов в природных объектах. С практической точки зрения представленные результаты исследования могут использоваться при проведении экологического мониторинга водных объектов Природного парка «Нумто», организации рационального управления территорией, планировании и проведении природоохранных мероприятий.
Объекты и методы исследования. Объектом исследований служила осока водяная
( Carex aquatilis Wahlenb.), формирующая прибрежную полосу растительности водоемов с разным гидродинамическим режимом Природного парка «Нумто» Белоярского района Ханты-Мансийского автономного округа.
Отбор растений для анализа проводился на пробных площадках (ПП), располагающихся непосредственно вдоль р. Казым (ПП 6) и вблизи двух типов озер (ПП 1–5) в границах Природного парка «Нумто» (рис.). Озера первого типа имели каналы сообщения с основным руслом реки (ПП 2–5), и прибрежная растительность могла подвергаться затоплению при сезонных паводках так же, как и береговая растительность самой реки. Озера второго типа распола- гались на надпойменной террасе (ПП 1), на коренном берегу не имели прямого сообщения с основным руслом реки и занимали понижения на границе верховых болот и соснового бора. Прибрежная полоса растений таких озер находилась в более стабильных гидрологических условиях, так как было исключено затопление паводковыми водами реки, а их водная подпитка осуществлялась за счет болотных вод и сезонных осадков.
Из водоемов, вблизи которых были выбраны пробные площадки сбора осоки, были также отобраны пробы воды для анализа содержания в ней тяжелых металлов.
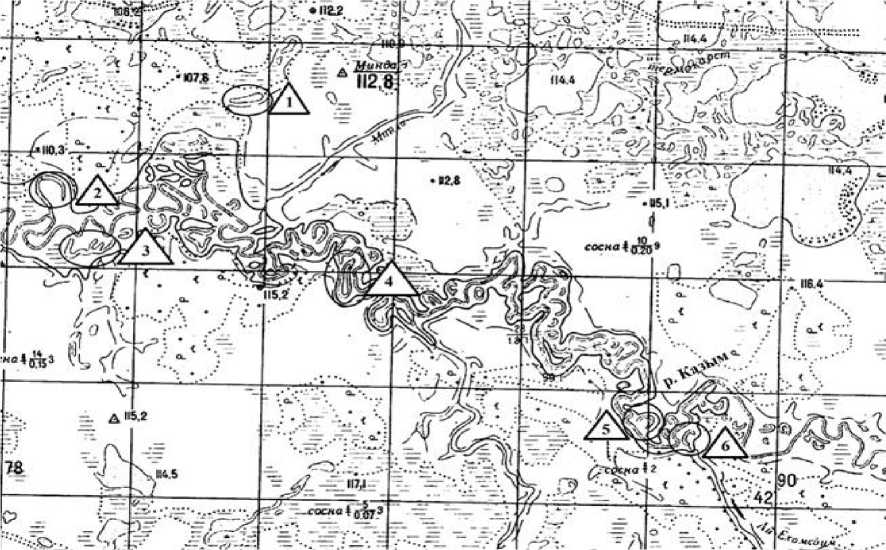
Карта-схема участка Природного парка «Нумто» с указанием мест отбора проб
Отбор проб воды из водных объектов проводили с глубины 30–100 см согласно ГОСТу [1]. Фиксацию мест отбора проб воды и растений осуществляли с помощью навигатора Garmin.
Отбор растительных образцов выполнен по существующим правилам отбора проб [8]. Анализ содержания подвижных форм тяжелых металлов (Cr, Mn, Fe, Ni, Cu, Zn, Cd, Pb) в пробах воды и в растительном сырье проводили методом атомной абсорбции на приборе МГА-915 МД [2, 5] в научной лаборатории биохимии и комплексного мониторинга окружающей среды Научно-исследовательского института экологии Севера Сургутского государственного университета. Анализ фитомассы осуществляли после ее сухого воздушного озоления при температуре 550 °С и растворения золы в азотной кислоте [2].
Результаты исследования и их обсуждение. Количественные результаты содержания тяжелых металлов в воде и в сухой массе Carex aquatilis представлены в таблице.
Содержание тяжёлых металлов в воде (мкг/дм3) и Carex aquatilis (мкг/г) водных объектов поймы р. Казым на территории Природного парка «Нумто» Ханты-Мансийского автономного округа - Югры
|
Номер ПП |
Объект |
Cr |
Mn |
Fe |
Ni |
Cu |
Zn |
Cd |
Pb |
|
1 |
Вода |
0,40±0,02 |
7,75±0,07 |
72,83±3,15 |
0,15± 0,01 |
0,35±0,01 |
32,77±1,71 |
0,03±0,001 |
0,19±0,01 |
|
Осока |
0,12±0,01 |
0,81±0,03 |
- |
0,35±0,01 |
0,21±0,01 |
12,19±0,38 |
0,02±0,001 |
0,12±0,01 |
|
|
2 |
Вода |
0,81±0,04 |
6,66±0,08 |
1779,35±68,07 |
0,17±0,01 |
0,34±0,01 |
8,09±0,71 |
0,03±0,001 |
0,24±0,01 |
|
Осока |
0,12±0,01 |
0,63±0,01 |
44,19±2,69 |
0,64±0,01 |
0,27±0,01 |
16,77±0,25 |
0,01±0,001 |
0,06±0,01 |
|
|
3 |
Вода |
0,35±0,01 |
2,76±0,08 |
451,89±17,79 |
0,09±0,01 |
0,21±0,01 |
13,27±0,53 |
0,03±0,001 |
0,34±0,01 |
|
Осока |
0,13±0,01 |
0,68±0,02 |
147,55±5,48 |
0,50±0,01 |
0,15±0,01 |
9,35±0,23 |
0,01±0,001 |
0,11±0,01 |
|
|
4 |
Вода |
0,26±0,01 |
12,68±0,77 |
41,60±0,75 |
0,28±0,01 |
0,15±0,01 |
- |
0,03±0,001 |
0,11±0,01 |
|
Осока |
0,07±0,01 |
0,54±0,02 |
36,02±1,26 |
0,14±0,01 |
0,08±0,01 |
12,32±0,40 |
0,01±0,001 |
0,07±0,01 |
|
|
5 |
Вода |
0,60±0,02 |
4,66±0,24 |
261,67±1,49 |
0,35±0,01 |
0,32±0,01 |
4,76±0,16 |
0,04±0,001 |
0,31±0,01 |
|
Осока |
0,08±0,01 |
0,43±0,01 |
35,33±2,42 |
0,85±0,01 |
0,27±0,01 |
8,07±0,23 |
0,01±0,001 |
0,04±0,01 |
|
|
6 |
Вода |
0,68±0,02 |
7,10±0,03 |
1657,64±59,53 |
0,34±0,01 |
0,28±0,01 |
18,08±0,93 |
0,07±0,002 |
0,50±0,01 |
|
Осока |
0,11±0,01 |
0,43±0,01 |
70,90±1,19 |
0,33±0,01 |
0,20±0,01 |
11,51±0,46 |
0,10±0,002 |
0,05±0,01 |
'прочерк в таблице означает отсутствие данных.
гГя^рн atfyuahmovongj
Анализ присутствия и количественного содержания тяжелых металлов в воде исследованных водных объектов и растениях (табл.) показал, что все перечисленные тяжелые металлы в разных количествах присутствуют как в воде, так и в зеленой массе растений. При этом содержание в воде растворимых форм Cr, Mn, Ni, Cu, Cd и Pb было значительно ниже нормативных значений предельно допустимых концентраций, а концентрации Zn и Fe превышали установленные нормы для 50 и 67 % исследованных водоемов соответственно [6].
При исследовании содержания тяжелых металлов в зеленой массе осоки установлено, что по отношению к Cr, Mn, Cu, Cd и Pb эффект аккумулирования не выражен или выражен очень слабо. Содержание этих элементов в зеленой массе растений во всех случаях ниже, чем в водной среде водоема (табл.).
Диапазон содержания железа в воде исследованных водоемов достаточно широк (72,83– 1779,35 мкг/дм3) (табл.). Однако, как в случае низких концентраций, так и при высоком содержании растворенного железа в водной среде (max 17,8 ПДК), это не приводит к существенному увеличению элемента в фитомассе Carex aquatilis. Среднее содержание железа в зеленой массе растения составляет 66,79 мкг/г.
Среднее содержание цинка в зеленой массе осоки составляет 11,7 мкг/г, при этом отмечено некоторое превышение содержания элемента в растении при его концентрации в воде ниже нормативов ПДК. При увеличении концентрации цинка в воде выше норматива (до 3,3 ПДК) увеличения его содержания в растении не наблюдается. Такое поведение растений по отношению к цинку можно объяснить его ограниченным переходом в надземную массу фитоценозов [7].
При исследовании растений на содержание никеля зафиксировано существенное превышение количества металла в растении по сравнению с водной средой. Установленный факт можно объяснить способностью Carex aquatilis накапливать высокие концентрации этого металла в течение жизни и выступать в роли биохимического барьера по отношению к этому элементу [7].
Выводы. Получена информация о фоновом содержании Cr, Mn, Fe, Ni, Cu, Zn, Cd и Pb в зеленой массе осоки Carex aquatilis, произра- стающей в прибрежной зоне исследованных водоемов Природного парка «Нумто» Белоярского района Ханты-Мансийского автономного округа – Югры, которые не подвергались техногенному воздействию. Установлено, что по отношению к высоким естественным концентрациям железа в водной среде Carex aquatilis проявляет резистивные свойства, а по отношению к подвижным формам никеля наблюдается эффект аккумулирования.
Список литературы Содержание тяжелых металлов в осоке водяной (Carex aquatilis Wahlenb.) прибрежно-водных биоценозов природного парка "Нумто"
- ГОСТ Р 51592-2000. Вода. Общие требова-ния к отбору проб. -М.: Стандартинформ, 2008. -45 с.
- ГОСТ 30178-96. Сырье и продукты пище-вые. Атомно-абсорбционный метод опре-деления токсичных элементов. -М.: Стан-дартинформ, 2010. -10 с.
- Ильин В.Б., Сысо А.И. Микроэлементы и тяжелые металлы в почвах и растениях Новосибирской области. -Новосибирск: Изд-во СО РАН, 2001. -229 с.
- Кабата-Пендиас А., Пендиас Х. Микроэле-менты в почвах и растениях. -М.: Мир, 1989. -439 с.
- Количественный химический анализ вод. Методика измерений массовой концентра-ции алюминия, бария, бериллия, ванадия, железа, кадмия, кобальта, лития, марганца, меди, молибдена, мышьяка, никеля, свин-ца, селена, серебра, стронция, титана, хрома, цинка в пробах природной и сточных вод атомно-абсорбционным методом с электротермической атомизацией с исполь-зованием атомно-абсорбционного спектро-метра модификации МГА-915, МГА-915 М, МГА-915 МД. ПНД Ф 14.1:2.253-09 (М 01-46-2013). -М.: НПФ «Люмэкс», 2009. -36 с.
- Об утверждении нормативов качества воды водных объектов рыбохозяйственного зна-чения, в том числе нормативов предельно допустимых концентраций вредных ве-ществ в водах водных объектов рыбохо-зяйственного значения: Приказ Федераль-ного агентства по рыболовству от 18 янва-ря 2010 года № 20//Российская газета. Федеральный выпуск. -2010. -5 марта.
- Тарабрин В.П. Физиология устойчивости древесных растений в условиях загрязне-ния окружающей среды тяжелыми метал-лами//Микроэлементы в окружающей сре-де. -Киев: Наукова думка, 1980. -С. 17-28.
- Титова В.И., Дабахова Е.В., Дабахов М.В. Агро-и биохимические методы исследова-ния состояния экосистем: учеб. пособие для вузов. -Н. Новгород: Изд-во ВВАГС, 2011. -170 с.
- Hall J., Williams E. Transition metal transport-ers in plants//J. Exp. Bot. -2003. -Vol. 54. -P. 2601-2613.


