Соединения лейцина с катионами меди (II) в водных растворах
Автор: Бондарева Л.П., Русина Е.В., Овсянникова Д.В.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Химическая технология
Статья в выпуске: 4 (74), 2017 года.
Бесплатный доступ
Строение альфа-аминокислот обусловливает возможность образования большого количества форм координационных соединений с катионами металлов. В реакциях комплексообразования с катионами металла могут участвовать все формы аминокислоты: протонированные образуют с ионами металлов аддукты за счет координации с неподеленными электронными парами атомов кислорода карбоксильной группы, константы устойчивости таких комплексов невелики, и они обычно подобны сольватокомплексам; биполярная и депротонированная формы образуют не только аддукты, но и внутрикомплексные соединения. Изучение равновесий в системе аминокислота-катион металла наиболее часто проводят потенциометрическими и спектрофотометрическим методами, позволяющими быстро, с хорошей воспроизводимостью определять равновесные концентрации и состав раствора без смещения химического равновесия. В литературе достаточно подробно изучено хелатное соединение лейцина с катионами меди (II), образующееся в щелочной среде, с показателями констант устойчивости 7,89 и 6,45. В настоящей работе проведено изучение условий комплексообразования в нейтральных водных растворах в системе, содержащей алифатическую аминокислоту L, D лейцин и катионы меди (II). Различие в длинах волн, соответствующих максимальной оптической плотности, свидетельствует об изменении состава водного раствора и присутствии соединений лейцината меди. Спектрофотометрическим методом изомолярных серий доказано существование комплексного соединения между биполярными ионами лейцина и катионами меди (II) в нейтральных водных растворах состава (СuLеu4)2+. Для определения констант устойчивости использовали метод Я. Бьеррума со следующими допущениями: аминокислота рассматривалась как одноосновная слабая кислота, константа устойчивости комплексного соединения рассчитывалась, как среднее значение для всех функциональных групп лейцина. Определенный в работе показатель константы устойчивости протонированного соединения состава (СuLеu4)2+ равен 4,27 ± 0,21.
D лейцин, катионы меди(ii), константа устойчивости, протонированные комплексы
Короткий адрес: https://sciup.org/140229899
IDR: 140229899 | DOI: 10.20914/2310-1202-2017-4-175-180
The compounds of leucine with copper (II) cations in aqueous solutions
The structure of alpha-amino acids offers the possibility of the formation of a large number of forms coordination compounds with cations of metals All forms of amino acids can participate in complexation reactions with metal cations: protonated form with metal ions adducts by coordinating with unshared electron pairs of oxygen atoms of carboxyl groups, the stability constants of such complexes are small and they usually like solvate complexes; bipolar and deprotonated forms not only adducts, but also chelation. The study of equilibrium in the system of amino acid - metal cation are most often carried out potentiometric and spectrophotometric methods, allowing fast, with good reproducibility to determine the equilibrium concentration and composition of the solution without displacement of the chemical equilibrium. In the literature, a chelate compound of leucine with copper (II) cations, formed in an alkaline medium with stability constants of 7.89 and 6.45, has been studied in sufficient detail. This paper presents a study of the conditions of complex formation in neutral aqueous solutions in the system containing aliphatic amino acid L, D-leucine and copper cations (II). The difference in the wavelengths corresponding to the maximum optical density indicates a change in the composition of the aqueous solution and the presence of copper leucinate compounds. The existence of a complex compound between bipolar leucine ions and copper (II) cations in neutral aqueous solutions of the composition (СuLеu4)2+ was proved by the spectrophotometric method of isomolar series. For the determination of stability constants using the method of J. Bjerrum with the following assumptions: an amino acid was regarded as monobasic weak acid, the stability constant of complex compounds was calculated as the average of all functional groups of leucine. Defined in the work a measure of stability constants protonated compounds composition (СuLеu4)2+ is equal to 4.27.
Текст научной статьи Соединения лейцина с катионами меди (II) в водных растворах
Большинство органических лигандов, являющихся аналогами природных соединений, способны взаимодействовать с катионами переходных металлов, имеют в своем составе кислород- и/или азот – содержащие группы, за счет которых и возможна координация. При этом координация может осуществляться различными способами, что связано как со строением молекулы лиганда, так и с влиянием условий
протекания реакции комплексообразования, в частности с рН среды или соотношение концентраций металл – лиганд [1–2].
Строение α-аминокислот обуславливает возможность образования большого количества форм координационных соединений с катионами металлов. Согласно данным рентгеноструктурного анализа карбоксильная группа может давать девять форм связывания молекулы аминокислоты с катионом металла [3].
В реакциях комплексообразования с катионами металла могут участвовать все формы аминокислоты. Протонированные образуют с ионами металлов аддукты за счет координации с неподеленными электронными парами атомов кислорода карбоксильной группы, константы устойчивости таких комплексов невелики, и они обычно подобны сольватокомплексам. Биполярная и депротонированная формы образуют не только аддукты, но и внутрикомплекс-ные соединения. Депротонированная форма при комплексообразовании, как правило, не доступна из-за протекания при рН > 6 гидролиза ионов d – элементов. Однако хелатообразование может приводить к смещению равновесия в сторону депротонированной формы, кроме того, некоторые катионы переходных металлов способны вытеснять ионы водорода. Самым распространенным типом координации аминокислот без дополнительных донорных групп с d-элементами в твердых комплексах является глицин-подобный (через атом азота α-амино-группы и атом кислорода карбоксильной группы) пятичленный хелатный узел [4–7]. Другим способом координации катионов металлов аминокислотами без дополнительных донорных групп является связь через биден-татно-мостиковую карбоксильную группу, в то время как атом азота не участвует в координации. При этом образуются димерные, тримерные, тетрамерные и полимерные соединения [8].
Для определения состава и устойчивости комплексов можно использовать практически любое, функционально связанное с комплексообразованием, свойство металла, лиганда или системы в целом. Изучение равновесий в системе аминокислота – катион металлов наиболее часто проводят потенциометрическими и спектрофотометрическим методами, позволяющими быстро, с хорошей воспроизводимостью определять равновесные концентрации и состав раствора без смещения химического равновесия. Полученные экспериментальные данные дают возможность рассчитывать константы равновесия реакций в указанных системах.
Кроме того, в сточных и природных водах могут одновременно содержаться катионы переходных металлов и органические соединения, способные связываться между собой. Данное обстоятельство затрудняет контроль содержания тяжелых металлов в воде [9]. В связи с этим, целью работы стало определение состава и устойчивости аминокислотного комплекса лейцина с катионами меди (II) в нейтральном водном растворе.
Материалы и методы исследования
Изучение условий комплексообразования в нейтральных водных растворах проводили на примере системы, содержащей алифатическую аминокислоту L, D-лейцин и нитрат меди(II).
Лейцин (2-амино-4-метилпентановая кислота) ограниченно растворяется в воде (растворимость в 100 г. воды при 25 °C – 2,19 г.). Значения характеризующие кислотные свойства карбоксильной группы лейцина – рK а 1 = 2,4; характеризующие кислотность аминогруппы – рK а 2 = 9,6, изоэлектрическая точка – 6,0.
Достаточно подробно изучено комплексное соединение лейцина с катионами меди (II), образующееся в щелочной среде, и имеющее показатели константы устойчивости lgβ 1 = 7,89 и lgβ 2 = 6,45 [10].
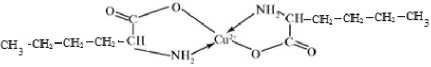
Исследование образования аминокислотного комплекса проводились спектрофотометрическим и потенциометрическим методами.
Для определения состава соединения лейцина с медью использовали спектрофотометрический метод изомолярных соотношений, основанный на определении отношения концентраций реагирующих веществ, соответствующих образующемуся комплексному соединению . Спектры электронного поглощения исследуемых растворов получали на спектрофотометре UV-mini 1240 (Shimadzu, Япония) при длинах волн 190–1100 нм в кварцевых кюветах с толщиной оптического слоя 10 мм. Спектры поглощения раствора лейцина и раствора лейцина с внесенным раствором Cu(NО 3 ) 2 получали относительно раствора сравнения – бидистиллированной воды.
Для определения устойчивости соединения лейцина с медью использовали потенциометрический метод. Кривые титрования, полученные при одинаковых концентрациях иона водорода и лиганда в присутствии и в отсутствии ионов металла, наиболее наглядно отражают протекание равновесных реакций и представляют весомую информацию о составе и ряде устойчивости образующихся комплексов. Потенциометрическое титрование проводили на рН-метре «рН-150 М». Титровали исходный раствор лейцина и раствор комплексного соединения лейцина с медью установленного состава. Для этого в стакан вносили 25 см3 лейцина с концентрацией 0,1 моль/дм3, из градуировочной бюретки последовательно вводили по 0,5 см3 раствора NаОН с концентрацией 0,05 моль/дм3. После введения каждой порции раствора NаОН и перемешивания определяли значение рН раствора до установления постоянного значения. Затем проводили в тех же условиях титрование лейцина раствором НСl с концентрацией 0,05 моль/дм3. При рН-метри-ческом титровании комплексного соединения в стакан вносили 10 см3 раствора лейцина с концентрацией 0,1 моль/дм3 и 10 см3 раствора нитрата меди(II) с концентрацией 0,05 моль/дм3.
Результаты и обсуждение
Для установления возможности существования соединений лейцина с катионами меди (II) в нейтральных растворах, получили спектры поглощения в интервале рН от 2 до 6 (рисунок 1) .
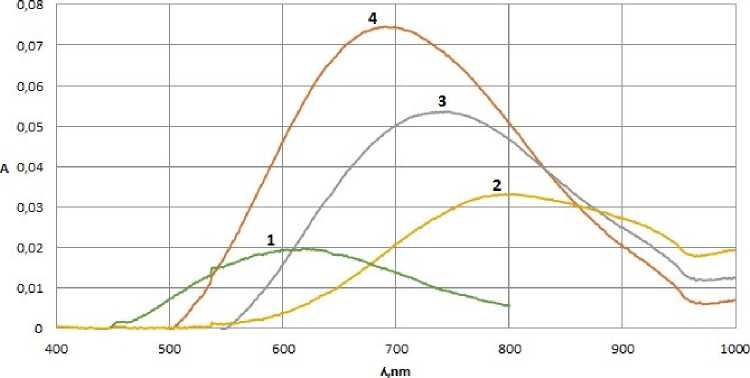
Рисунок 1. Спектры поглощения водных растворов лейцина с нитратом меди, при различных рН: 1 – при рН 2,06; 2 – рН 4,00; 3 – рН 5,00; 4 – рН 6,00
Figure 1. Absorption spectra of aqueous solutions of leucine with copper nitrate at various рН: 1 – at a рН of 2.06; 2 – рН 4,00; 3 – рН 5.00; 4 – рН 6,00
В спектре поглощения алифатической аминокислоты, не содержащей хромофорных и ауксохромных групп, характеристическая длинноволновая полоса поглощения отсутствует. Максимумы поглощения возникают лишь в присутствие окрашенных катионов меди. Различие в длинах волн, соответствующих максимальной оптической плотности, свидетельствует об изменении состава водного раствора и присутствии соединений лейцината меди [11].
Для определения состава соединений лейцина с ионами меди (II) применен спектрофотометрический метод и получены спектры поглощения водных растворов с рН 6,0 лейцина с нитратом меди при различном соотношении Leu: Сu2+. Установлено, что при соотношениях от 1:1 до 1:10 наблюдаемый максимум поглощения одинаков. Для определения состава комплексного соединения строили его кривую насыщения при длине волны 763 нм, представленную на рисунке 2.
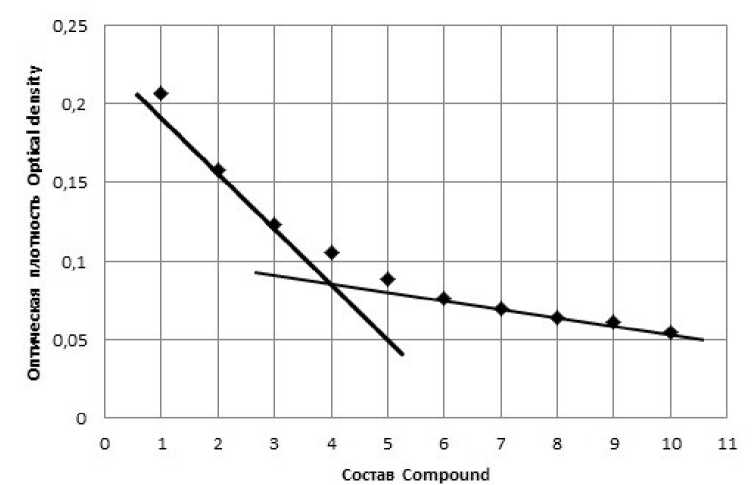
Рисунок 2. Кривая насыщения комплексного соединения [Cu(II)] / [Leu], при λ = 763 нм
Figure 2. Saturation curve of the complex compound [Cu (II)] / [Leu], at λ = 763 nm
Соотношение компонентов в комплексе определили проведением перпендикуляра из точки пересечения касательных в области максимума на кривой изомолярной серий. Согласно рисунку 2, в нейтральном растворе образуется неустойчивое комплексное соединение состава [Сu2+]: [Leu] = 1:4.
Для определения устойчивости протонированного комплекса лейцина с ионами меди в водных растворах проведены потенциометрические исследования и построены кривые потенциометрического титрования растворов лейцина и его комплексов с медью в широком диапазоне рН. Полученные кривые титрования лейцина и лейцината меди(II), представлены на рисунке 3.
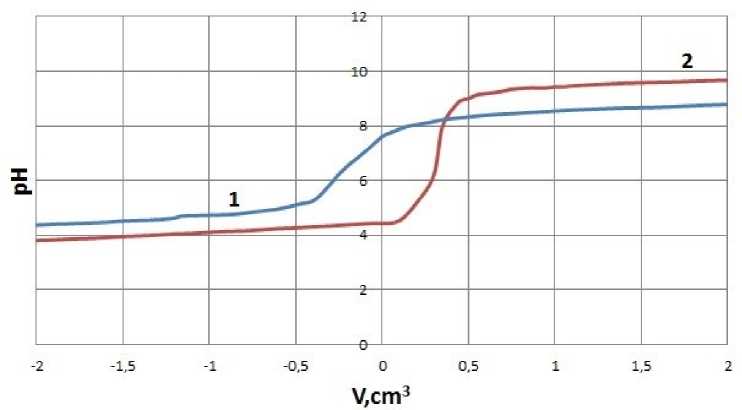
Рисунок 3. Кривые титрования лейцина и лейцината меди (II): 1 – лейцин; 2 – лейцинат меди(II)
Figure 3. Curves titration of leucine and copper (II) leucinate: 1 – leucine; 2 – leucinate of copper (II)
Для определения констант устойчивости использовали метод Я. Бьеррума. Данный метод требует расчета двух функций: свободной концентрации лиганда [L] и функции образования Я. Бьеррума ñ. Следует отметить, что при использовании данного метода приняты следующие допущения: аминокислота рассматривалась как одноосновная слабая кислота, и константа устойчивости комплекса рассчитывалась как среднее значение для всех функциональных групп лейцина.
Процесс комплексообразования ионов металла с биполярным ионом лейцина может быть выражен в общем виде следующим образом:
Меz++ 4L± ↔ [МеL 4 ]2+ (1)
Для оценки значение константы устойчивости, необходимо учесть кислотно-основное равновесие лейцина
-
L- + H+ ↔ LH (2)
Константа равновесия данной реакции соответствует константе устойчивости комплекса и может быть выражена уравнением
СC
К уст. = -7^ , (3)
CHL где СН+ – равновесная концентрация замещенных металлом ионов Н+, исходя из значения рН в каждой точке титрования; СL- – равновесная концентрация свободного (незакомплексованного) лиганда; СНL – концентрация связанного с протоном лиганда.
Причём по уравнению материального баланса с учётом степени диссоциации α для нахождения С НL применялось выражение:
C hl = (1 - а) С 0 - + а С 0- , (4)
где С 0_ - начальная концентрация лейцина.
Рассчитывали степень диссоциации, исходя из закона разбавления Освальда (с учётом принятого допущения):
К д =
а 2 С 0
1 - а
где К д – константа диссоциации лейцина равная 2,4 [12].
С помощью математических преобразований из формулы (5) получено квадратное уравнение вида
α2 + 2,4α – 2,4 = 0 (6)
С учётом того, что α не может быть отрицательной величиной, из двух корней квадратного уравнения был выбран корень, равный 0,9611.
Далее рассчитывали концентрацию свободного лиганда С L -в системе «лейцин – катионы металла». Для этого выражали С L - из уравнения (3), а затем подставляли в полученное выражение формулу (4). Таким образом, полученное уравнение для расчёта С L - имеет вид:
К
CL -= , ((1 - a) С0L-+ aCH +). (7) СН+ где Сн + - концентрация ионов Н+, определяемая из значений рН в каждой точке титрования системы «лейцин – катион металла».
Расчёт концентрации лиганда – лейцина проводили по формуле (7), зная исходные концентрации аминокислоты и соли металла.
Согласно методу Я. Бьеррума константу устойчивости комплексного соединения К n можно рассчитать из значения C , по полуцелому значению среднего координационного числа (n), то есть при ñ = n – 0,5, если отношения двух последовательных констант устойчивости достаточно велики:
К n
C
L / при Я = n - 0,5
где n – число лигандов в комплексе.
Логарифмируя выражение (8),
получить:
lgK n = lg
Ct
L V при я = n - 0,5
можно
=- lg (C L-) . = p (C J . 05
L при n = n - 0,5 L при n = n - 0,5
После сделанных преобразований строили график зависимости Я = f ( pC r) ,
так называемую кривую образования, и при значении ñ = n – 0,5 экстраполяцией на ось абсцисс определяли значение рК уст комплексного соединения лейцина.
Кривая образования комплексного соединения лейцина с нитратом меди состава (СuLеu 4 )2+ приведена на рисунке 4.
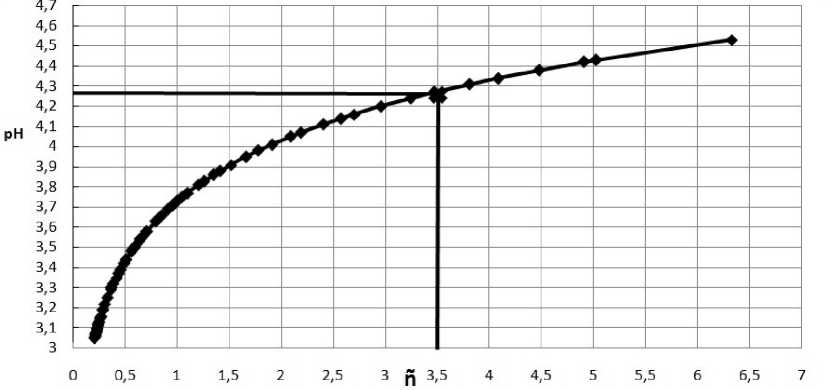
Рисунок 4. Кривая образования комплексного соединения (СuLеu 4 )2+
Figure 4. Curve formation of a complex compound (СuLеu4) 2+
Полученная кривая образования плавная, не имеющая ступеней, что подтверждает образование малоустойчивого комплексного соединения. Значения рК уст. получены экстраполяцией на ось абсцисс значения на оси ординат, равного ñ = 4 – 0,5 = 3,5. Таким образом, определено, что показатель константы устойчивости рК уст. равен 4,27 ± 0,21.
Список литературы Соединения лейцина с катионами меди (II) в водных растворах
- Скопенко В.В., ?Цивадзе А.Ю., ?Савранский А.И. Координационная химия. М.: ИКЦ «Академкнига», 2009. 325 с.
- Sigel H. Metal ions in biological systems. Vol. 2. N.Y.; London: Marcel Dekker, 2014. 360 р.
- Панюшкин В.Т., Буков Н.Н., Болотин С.Н. Координационная химия природных аминокислот. М.: Наука, 2007. 247 с.
- S?vag?, I. Critical survey of the stability constants of complexes of aliphatic amino acids//Pure and Applied Chemistry. 2015. V. 65. № 5. P. 1029-1080.
- Chidambarm M.V., Bhattacharya P.K. Studies on mixed amino acid and metal chelates//Acta Chimica. 2012. V.75. № 2. Р. 123-128.
- Reddy G., Sotyanarayana S. Formation constant of complex of some djyvalent metal ions//Indian J. Chem. 2010. V. 28. № 4. Р. 337-339.
- Li N.C. Study of ternary complexes of Cu(II) involving aliphatic carboxylic acids and amino acids//J. Am. Chem. Soc. 2005.V.77. P.5225-5229
- Панюшкин В.Т., Неудачина Л.К. Физико-химические основы применения координационных соединений. Екатеринбург: Издво Урал. ун-та, 2014. 124 с.
- Бондарева Л.П., Селеменев В.Ф. Комплексообразование фосфорорганических биологически активных соединений: монография. Воронеж: ИПЦ «Научная книга», 2012. 232 с.
- Яцимирский К.Б., Крисс Е.Е. Константы устойчивости комплексов металлов с биолигандами. Киев: Наукова Думка, 1979. С. 31-57
- Григорова Е.В., Бондарева Л.П., Корниенко Т.С. Равновесия метионина в водных растворах//Журнал общей химии. 2010. Т. 80. № 12. С. 1988-1992.
- Berthon G. The Stability Constans of Metal Complexes of Amino Acids with Polar Side Chains.//Pure &App. Chem. 1995. V. 67. №. 7. Р. 1117-1240


