Сократительная активность и энергетический метаболизм постинфарктного сердца на фоне диабетического поражения в эксперименте
Автор: Кондратьева Д.С., Афанасьев С.А., Егорова М.В., Реброва Т.Ю., Попов С.В.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 2-1 т.26, 2011 года.
Бесплатный доступ
Цель работы: исследовать сократительную активность и энергетический метаболизм постинфарктного миокарда крыс на фоне диабета. Сократительную активность оценивали по реакции папиллярных мышц на экстрасистолические воздействия. В группы сравнения включали интактных животных, животных с постинфарткным кардиосклерозом, крыс с сахарным диабетом (стрептозотоцин, 60 мг/кг), а также животных с постинфарктным кардиосклерозом на фоне сахарного диабета. Было обнаружено, что при постинфарктном кардиосклерозе и диабете в отдельности возбудимость миокарда крыс повышается, тогда как при сочетании этих патологий возбудимость остается в пределах контрольных значений. Постэкстрасистолическое сокращение миокарда крыс с постинфарктным кардиосклерозом и диабетом в отдельности угнеталось. При сочетанной патологии постэкстрасистолическая потенциации миокарда крыс сохранялась на уровне контрольных значений. Состояние процессов окислительного фосфорилирования кардиомиоцитов крыс наиболее близко к контрольным значениям в группе с сочетанной патологией. Авторы считают, что гипергликемия на стадии формирования постинфарктного ремоделирования повышает адаптивные возможности миокарда, что способствует сохранению ритмоинотропных реакций миокарда, а также способствует менее выраженному нарушению энергетического метаболизма.
Сократимость, постинфарктное и диабетическое ремоделирование миокард крысы, саркоплазматический ретикулум, экстрасистолические и постэкстрасистолические сокращения
Короткий адрес: https://sciup.org/14919438
IDR: 14919438 | УДК: 616.127-004
Contractile activity and energetic metabolism of postinfarction heart against diabetic damage in experiment
The aim of this study was to investigate contractility and energetic metabolism of postinfarction myocardium rats with diabetes. Contractility was estimated using a method of reaction of papillary muscles on extrasystolic impulses. Comparison groups included intact animals, rats with postinfarction cardiosclerosis, rats with a diabetes (streptozotocine, 60 mg/kg), and also animals with postinfarction cardiosclerosis in combination with diabetes. It was revealed that during postinfarction cardiosclerosis and diabetes separately excitability of rat's myocardium raises, whereas during the combination of these pathologies excitability remains within control values. Postextrasystolic contraction of myocardium of rats with postinfarction cardiosclerosis and diabetes separately was depressed. With combination of postinfarction and diabetic lesion the postextrasystolic contraction of rat myocardium was preserved within the control values. Condition of oxidative phosphorylation processes of rat cardiomyocytes was closer to control values in the group with combine pathology. Authors consider that hyperglycemia in postinfarction remodeling develops raises the adaptive possibilities of myocardium that promotes preservation rhythmoinotropic myocardium reactions, and also promotes less expressed damage of an energetic metabolism.
Текст научной статьи Сократительная активность и энергетический метаболизм постинфарктного сердца на фоне диабетического поражения в эксперименте
Как известно, сочетание ишемической болезни сердца и сахарного диабета повышает вероятность сосудистых катастроф. Развитие сократительных дисфункций при диабетическом поражении миокарда связано как с ремоделированием клеточных мембран кардиомиоцитов [1], так и с нарушением энергетического метаболизма. Снижение содержания и доступности АТФ для метаболических процессов служит дополнительным фактором дисбаланса гомеостаза Са2+ в кардиомиоцитах. Одной из ключевых энергозависимых структур кардиомиоцитов, отвечающих за внутриклеточный гомеостаз Са2+, и соответственно, за инотропный ответ клетки, является сар- коплазматический ретикулум (СР). Показано, что нарушение функций этой внутриклеточной структуры при сердечной недостаточности сопровождается инверсией ритмоинотропных реакций миокарда [2, 3]. Причиной этого является зависимость функционального состояния СР, в частности, активности его Са2+-транспортирующих систем от энергетической обеспеченности отдельных кардиомиоцитов [4]. Вместе с тем механизмы развития инотропных нарушений, связанных с ремоделированни-ем кальций-транспортируюших систем, а также состояние окислительного фосфорилирования кардиомиоцитов при сердечной недостаточности на фоне сахарного диабета недостаточно изучены.
Цель исследования: оценить сократительную активность и энергетический метаболизм постинфарктного сердца на фоне диабетического поражения.
Материал и методы
Работа выполнена на 45 половозрелых крысах-самцах линии Вистар. Животных разделили на 4 группы: I группу составили интактные животные (n=12), II группу – крысы с постинфарктным кардиосклерозом (ПИКС), (n=11), III группу – животные с индуцированным сахарным диабетом (n=8), и IV группу – крысы, которым через 2 недели после коронароокклюзии моделировали диабет (n=8). Инфаркт миокарда моделировали путем окклюзии левой нисходящей коронарной артерии [2]. Сахарный диабет моделировали однократным введением стрептозотоцина (Sigma, США) в дозе 60 мг/кг, внутрибрюшинно, разведенного в 0,01 моль/л цитратном буфере (рН 4,5) [5, 6]. Крыс IV группы брали в эксперимент через 4 недели после индукции диабета. Концентрацию глюкозы в сыворотке крови определяли ферментно-ко-лорометрическим тестом (Biocon Diagnostic, Германия). В сердцах крыс II и IV групп оценивали размер постинфарктных рубцов методом планиметрии [7].
В день эксперимента животных, находящихся под легким эфирным наркозом, обездвиживали смещением шейного отдела позвоночника. Извлекали сердце из грудной полости и промывали его в проточной камере через аорту раствором Кребса–Хензеляйта следующего состава (в мМ): NaCl – 120; KCl – 4,8; CaCl2 – 2,0; MgSO4 – 1,2; KH2PO4 – 1,2; NaHCO3 – 20,0; глюкоза – 10,0 (Sigma, США). Выделенные папиллярные мышцы помещали в термостабилизированную проточную камеру. Один конец мышцы фиксировали к стенке камеры, а второй – закрепляли на штоке изометрического датчика (6МХ1С). Перфузию мышц осуществляли при 36,5 °С оксигенированным (О2 – 95%, СО2– 5%) раствором Кребса–Хензеляйта. Стимуляцию мышц проводили электрическими импульсами прямоугольной формы длительностью 5 мс при частоте 0,5 Гц. Регистрировали кривые изометрического сокращения папиллярных мышц. Экстрасистолическое воздей- ствие оказывали при помощи однократного нанесения внеочередного электрического импульса через 0,2–1,5 с от начала регулярного цикла [2]. Измеряли амплитуду эк-страсистолического (ЭС) и постэкстрасистолического (ПЭС) сокращения и выражали ее в процентах к амплитуде регулярного цикла.
Митохондрии сердца получали методом дифференциального центрифугирования в стандартной сахарозной среде, содержащей (мМ) 300 сахарозу, 10 ЭДТА, 8 трис, рН 7.4. Митохондрии суспендировали в 250 мМ растворе сахарозы. Скорость поглощения кислорода митохондриями определяли полярографически с помощью электрода Кларка. Измерение проводили в среде, содержащей (мМ) 300 сахарозу, 10 КСl, 5 КН2РО4, 5 сукцинат (или 5 малат + 5 глутамат), 1 ЭДТА, 5 трис, рН 7.4. Измерения проводили в термостатируемой ячейке объемом 1 мл при температуре 27 °С и постоянном перемешивании при помощи магнитной мешалки. Регистрировали скорость поглощения кислорода без АДФ и в присутствии 100 мкМ АДФ. Ингибирование фосфолипазы А2 проводили при помощи бром-фенацилбромида Реакцию начинали добавлением суспензии митохондрий (2 мг белка). Концентрацию белка в пробе определяли методом Лоури. В работе использовали реактивы фирм Sigma и ICN. Скорость потребления кислорода приведена в нМ О2 в мин на 1 мг белка.
Полученные данные обработаны общепринятыми методами вариационной статистики, представлены как M± σ , статистическую значимость различий показателей оценивали с использованием t-критерия Стьюдента и U Манна–Уитни.
Результаты и обсуждение
Проведенные исследования показали, что ремоделирование миокарда после коронароокклюзии во II группе сопровождалось снижением массы тела на 18,8% и гипертрофией сердца на 90% по сравнению с I группой (табл. 1). Индукция диабета через 4 недели в III группе вызывала снижение массы тела на 56% (р<0,01), тогда как в IV группе отмечалось снижение массы тела только на 26%. Повышение концентрации глюкозы в крови наблюдалось в III и IV группах, что свидетельствует о развитии сахарного диабета в этих группах.
Исследование инотропной реакции на ЭС воздействия показало, что амплитуда ЭС сокращения миокарда животных II группы после ЭС интервала длительностью 0,25 с была выше на 8% (р<0,01) по сравнению с I группой, при этом с увеличением длительности ЭС интервала эта разница увеличивалась и достигала 16% (р<0,01), рисунок 1.
Повышение амплитуды ЭС сокращений во II группе свидетельствует об увеличении внутриклеточного содержания ионов кальция, участвующих в ЭС сокращении. Как известно, ишемическое поражение сердца характеризуется угнетением синтеза АТФ, что приводит к нарушению работы АТФ–зависимых ионных насосов и, соответственно, к повышению внутриклеточной концентрации Na+ и Са2+ [8]. Экстрасистола в III группе появлялось уже после нанесения электрического стимула через 0,225 с, тогда
Таблица 1
Изменение веса тела и сердца крыс
|
Группы |
n |
mТ, г |
Глюкоза, моль/л |
mС/mТ, мг/г |
mЛЖ/m C, мг/мг |
Площадь зоны рубца,% |
|
I |
12 |
298±23,7 |
6±0,37 |
3,29±0,21 |
0,645±0,013 |
- |
|
II |
11 |
242±11,17*# |
7±0,13# |
6,27±0,33*# |
0,687±0,016* |
51,3±8,9 |
|
III |
8 |
160±14,8* |
27±2,75* |
3,77±0,31 |
0,676±0,014 |
- |
|
IV |
8 |
221±4,51* |
18±1,79* |
3,37±0,11 |
0,673±0,019 |
46,1±2,7 |
Примечание: n – количество животных, mС – масса сердца, mТ – масса тела, mЛЖ – масса левого желудочка. * p<0,01 статистическая значимость различий по сравнению с I группой, # – р<0,01 статистическая значимость различий по сравнению с IV группой.
как ЭС сокращение миокарда животных в остальных группах возникало только при воздействии электрическим стимулом через 0,25 с. Как известно, экстрасистоличес-
кий стимул вызывает инотропный ответ только в случае, если воздействие попадает в фазу относительной реф-рактерности [9]. Из этого следует, что развитие диабета
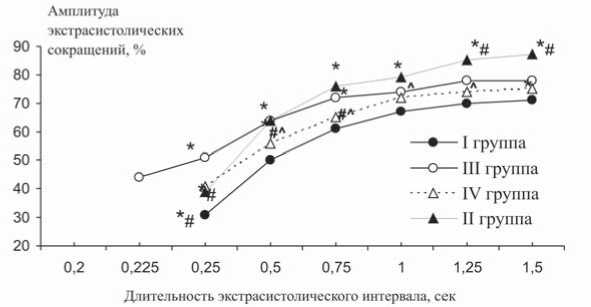
Рис. 1. Динамика экстрасистолических сокращений миокарда крыс с постинфарктным кардиосклерозом и диабетическим поражением.
Примечание: по оси ординат – амплитуда сокращений в процентах по отношению к регулярным сокращениям; по оси абсцисс – длительность ЭС интервала в секундах; * – p<0,001 в сравнении с I группой, # – p<0,01 в сравнении с III группой, h – p<0,01 в сравнении со II группой; здесь и далее.
приводит к укорочению фазы абсолютной рефрактерности и повышению возбудимости клеток сердца. Кроме того, амплитуда ЭС сокращений III группы после коротких ЭС интервалов была на 20% выше, чем в I группе (рис. 1). Динамика экстрасистолического сокращения миокарда животных IV группы была сходна с реакцией I группы (рис. 1). Как видно из полученных результатов, сочетание ишемического и диабетического поражения миокарда парадоксально способствует уменьшению выраженности изменений динамики ЭС сокращений, полученных на фоне ПИКС и диабета в отдельности.
Как известно, внеочередной электрический импульс инициирует дополнительное поступление внеклеточных ионов кальция в миоплазму кардиомиоцитов. Эти дополнительные Са2+ аккумулируются в СР и участвуют в первом ПЭС сокращении, амплитуда которой превышает значение регулярного цикла [9]. Как видно из рисунка 2, ПЭС потенциация во II группе практически не наблюдалась.
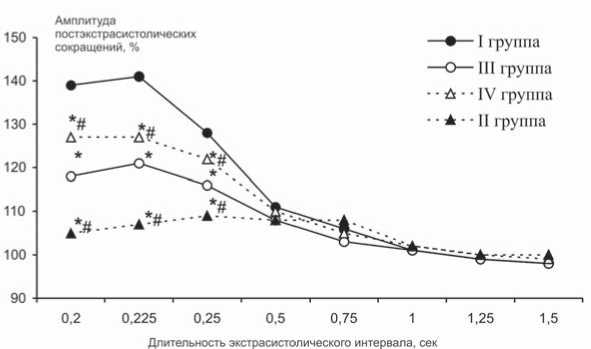
Рис. 2. Постэкстрасистолические сокращения миокарда крыс с постинфарктным кардиосклерозом и диабетическим поражением
Амплитуда ПЭС сокращений в таком миокарде была чуть больше исходных значений вне зависимости от длительности ЭС интервала. Этот факт свидетельствует о значительном снижении депонирующей функции СР. Скорее всего, это связано с тем, что в условиях постинфарктного ремоделирования миокарда крыс в кардиомиоцитах нарушается работа систем СР, ответственных за реализацию функций захвата и выброса ионов кальция [10]. В III группе ПЭС потенциация миокарда была достоверно меньше в сравнении с I группой (рис. 2). ЭС воздействие с короткими интервалами вызывало повышение ПЭС сокращения на 27–19% в IV группе (рис. 2), что свидетельствует о лучшем сохранении Са2+ – депонирующей способности СР.
Таблица 2
Скорость потребления кислорода и дыхательный контроль митохондрий сердца крыс в различных экспериментальных моделях
|
Группы |
Скорость потребления кислорода, нМО /мин на мг белка |
ДК |
|
|
Исходно |
На фоне бромфенацилбромида |
||
|
I |
10,5±1,8 |
10,6±1,4 |
3,4 |
|
II |
44,7±2,8* |
38,0±1,7*# |
2,0 |
|
III |
35,2±3,5* |
21,1±2,4*# |
1,9 |
|
IV |
20,9±1,5* |
11,6±1,5*# |
2,3 |
Примечание: в скобках указана степень снижения величины ДК по отношению к ДК интактных животных; * – р<0,01 различия по отношению к I группе; # – р<0,01 различия в каждой группе между исходным показателем и на фоне бромфенацил-бромида; ДК – дыхательный контроль.
Исследование скорости дыхания митохондрий кардиомиоцитов показало, что скорость исходного поглощения кислорода II, III и IV групп значительно превышала значения I группы (табл. 2). Наблюдаемое увеличение потребления кислорода может быть обусловлено протонофорным действием жирных кислот [11] и разобщением окисления и фосфорилирования в митохондриях. Действительно, при добавлении в среду измерения АДФ мы получили выраженное снижение величины дыхательного контроля II и III групп. Однако в IV группе при добавлении АДФ величина дыхательного контроля оказалась наиболее близкой к значениям I группы. Как известно, при сердечно-сосудистых патологиях отмечается повышение активности эндогенных фосфолипаз и, как следствие, накопление свободных жирных кислот [12], которое провоци- рует разобщение процессов окисления и фосфорилирования [11]. Ингибирование фосфолипазы А2 при помощи бромфенацилбромида не изменило скорость дыхания митохондрий в I группе, однако в остальных группах этот показатель достоверно снижался (табл. 2). Это подтверждает факт повышения активности фосфолипазы А2 при развитии патологических состояний. Полученные данные свидетельствуют о том, что нарушение процессов энергетического метаболизма кардиомиоцитов наименее выражено в группе животных с сочетанной патологией.
Результаты исследований позволяют говорить о том, что индукция диабета на фоне формирования постинфарктного ремоделирования сердца парадоксально способствует сохранению в кардиомиоцитах функциональной активности систем ионного транспорта, отвечающих, в частности, за работу СР как внутриклеточного депо Са2+, а также способствует лучшему сохранению энергетического метаболизма. Возможно, это связано с гликозилированием мембран кардиомиоцитов в условиях гипергликемии, что приводит к увеличению ригидности мембран и препятствует избыточному притоку Са2+ в миоплазму [13]. Другой фактор, обеспечивающий адаптивные реакции при сочетанном развитии постинфарктных и диабетических нарушений миокарда, может быть связан с особенностями внутриклеточного энергетического метаболизма. Видимо, повышение уровня глюкозы на начальных стадиях развития ПИКС стимулирует процессы гликолиза в кардиомиоцитах. Известно, что положительный эффект глюкозы на работу сердца при экспериментальной ишемии миокарда связан с повышением гликолитической продукции АТФ [14]. Вероятно, в результате сдвига энергетического метаболизма в сторону гликолитической продукции АТФ сохраняется функциональная активность Са2+-транспортирующих насосов СР, поскольку АТФ, образующаяся в процессе гликолиза, является незаменимым источником энергии для Са2+-АТФазы ионного насоса СР [14]. Вместе с тем установленные нами данные согласуются с результатами об ишемической резистентности миокарда животных с небольшим сроком стрептозотоцин-индуцированного диабета [6, 15].
Таким образом, в эксперименте индукция сахарного диабета на стадии формирования постинфарктного ремоделирования повышает адаптивные возможности миокарда, что способствует сохранению ритмоинотропных реакций миокарда, связанных с работой кальций-транс-портирующих систем СР, а также способствует менее выраженному нарушению энергетического метаболизма.
Работа подготовлена по материалам исследований, финансируемых Министерством образования и науки в рамках ФЦП “Исследования и разработки по приоритетным направлениям развития научно-технологического комплекса России на 2007–2012 годы” (ГК № 02.527.11.0007) и гранта 7 Рамочной программы Рос-сия-ЕС (№ 241558).
Список литературы Сократительная активность и энергетический метаболизм постинфарктного сердца на фоне диабетического поражения в эксперименте
- Ziegelhoffer-Mihalovicova B., Waczulikova I., Sikurova L. et al. Remodelling of the sarcolemma in diabetic rat hearts: the role of membrane fluidity//Mol. Cell Biochem. -2003. -Vol. 249 (1-2). -P. 175-82.
- Кондратьева Д.С., Афанасьев С.А., Фалалеева Л.П. и др. Инотропная реакция миокарда крыс с постинфарктным кардиосклерозом на экстрасистолические воздействия//Бюл. экспер. биол. -2005. -Т. 130 (6). -C. 613-616.
- Кондратьева Д.С., Афанасьев С.А., Евтушенко А.В. и др. Сравнительная оценка инотропной реакции изолированного миокарда пациентов с ишемической и ревматической болезнью сердца после кратковременных периодов покоя на фоне амиодарона//Кардиология. -2008. -Т. 10. -С. 45-50.
- Marengo F.D., Marquez M.T., Bonazzola P. et al. The heart extrasystole: an energetic approach//Am. J. Physiol. -1999. -Vol. 276(1). -P. H309-H316.
- Дубилей Т.А., Бадова Т.А., Мигован С.А. и др. Влияние ишемии/реперфузии на функцию изолированного сердца у крыс разного возраста со стрептозотоциновым диабетом//Проблемы старения и долголетия. -2007. -Т. 16 (1). -С. 11-20.
- Satoh N., Sato T., Shimada M. at al. Lusitropic effect of MCC-135 is associated with improvement of sarcoplasmic reticulum function in ventricular muscles of rats with diabetic cardiomyopathy//J. Pharmacol. Exp. Ther. -2001. -Vol. 298 (3). -P. 1161-1166.
- Усачева М.А., Попкова Е.В., Смирнова Е.А. и др. Адаптация сердечно-сосудистой системы к постинфарктному кардиосклерозу у крыс с разной врожденной адренореактивностью миокарда//Бюл. экспер. биол. -2007. -Т. 144 (12). -С. 624-628.
- Sniecinski R., Liu H. Reduced efficacy of volatile anesthetic preconditioning with advanced age in isolated rat myocardium//Anesthesiology. -2004. -Vol. 100 (3). -P. 589-597.
- Vassallo D.V., Lima E.Q., Campagnaro P. et al. Mechanisms underlying the genesis of post-extrasystolic potentiation in rat cardiac muscle//Braz. J. Med. Biol. Res. -1995. -Vol. 28(3). -P. 377-383.
- Sen L., Cui G., Fonarow G.C., Laks H. Differences in mechanisms of SR dysfunction in ischemic vs. idiopathic dilated cardiomyopathy//Am. J. Physiol. Heart Circ. Physiol. -2000. -Vol. 279. -P. H709-H718.
- Мохова Е.Н., Хайлова Л.С. Участие анионных переносчиков внутренней мембраны митохондрий в разобщающем действии жирных кислот//Биохимия. -2005. -Т. 70, № 2. -С. 197-202.
- Молчанов С.Н., Люсов С.А., Говорин А.В. и др. Сывороточные липиды при различных стадиях и морфофункциональных типах сердечной недостаточности у больных, перенесших инфаркт миокарда//Рос. кардиол. журнал. -2005. -№ 2. -С. 10-17.
- Waczulikova I., Ziegelhoffer A., Orszaghova Z. et al. Fluidising effect of resorcylidene aminoguanidine on sarcolemmal membranes in streptozotocin_diabetic rats: blunted adaptation of diabetic myocardium to Ca2+ overload//J. Physiol. Pharmacol. -2002. -Vol. 53 (4). -P. 727-739.
- Vanoverschelde J.L., Janier M.F., Bakke J.E. et al. Rate of glycolysis during ischemia determines extent of ischemic injury and functional recovery after reperfusion//Am. J. Physiol. -1994. -Vol. 267(5 Pt 2). -P. H1785-H1794.
- Chen H., Shen W.L., Wang X.H. et al. Paradoxically enhanced heart tolerance to ischaemia in type 1 diabetes and role of increased osmolarity//Clin. Exp. Pharmacol. Physiol. -2006. -33 (10). -P. 910-916.


