Сопоставимость показателей перфузии сетчатки при сквозных макулярных разрывах по данным различных оптических когерентных томографов-ангиографов
Автор: Докторова Т.А., Суетов А.А., Бойко Э.В., Сосновский С.В.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4S1 т.18, 2023 года.
Бесплатный доступ
Обоснование. В разных моделях ОКТ-ангиографов используются различные алгоритмы визуализации сосудистого сигнала. Сопоставимость показателей перфузии при наблюдении заболеваний макулы, включая сквозные макулярные разрывы (СМР), остается малоизученной.
Сквозной макулярный разрыв, окта, оптическая когерентная томография-ангиография, поверхностное капиллярное сплетение, фовеальная аваскулярная зона, фаз
Короткий адрес: https://sciup.org/140303502
IDR: 140303502 | DOI: 10.25881/20728255_2023_18_4_S1_13
The comparison of retinal perfusion indicators in full-thickness macular holes according to data from various OCT angiography devices
Background. Different optical coherence tomography angiography (OCT-A) devices use various vascular signal visualization algorithms. Comparability of perfusion parameters in the monitoring of macular diseases, including full-thickness macular hole (FTMH) remains poorly understood.
Текст научной статьи Сопоставимость показателей перфузии сетчатки при сквозных макулярных разрывах по данным различных оптических когерентных томографов-ангиографов
Актуальность
Сквозной макулярный разрыв (СМР) – частый вариант патологии витреомакулярного интерфейса, характеризующийся формированием сквозного полнослойного дефекта в зоне фовеа [1; 2]. При этом в сетчатке вокруг зоны разрыва развивается интраретинальный отек с кистозными изменениями на уровне внутренного ядерного и наружного плексиформного слоев, а также изменяется перфузия как в поверхностном, так и в глубоком капиллярном сплетении [3–7]. При хирургическом закрытии

Докторова Т.А., Суетов А.А., Бойко Э.В., Сосновский С.В.
СОПОСТАВИМОСТЬ ПОКАЗАТЕЛЕЙ ПЕРФУЗИИ СЕТЧАТКИ ПРИ СКВОЗНЫХ МАКУЛЯРНЫХ РАЗРЫВАХ ПО ДАННЫМ РАЗЛИЧНЫХ ОПТИЧЕСКИХ КОГЕРЕНТНЫХ ТОМОГРАФОВ-АНГИОГРАФОВ
СМР ранее описано восстановление капиллярной перфузии с уменьшением площади фовеальной аваскулярной зоны [7]. Тем не менее, значение регистрируемого изменения кровоснабжения макулярной области при СМР, в том числе для прогнозирования результатов хирургического лечения, остается недостаточно изученным.
Разработка и внедрение в клиническую практику оптической когерентной томографии-ангиографии (ОКТА) сделали возможным оценку микроциркулятор-ного русла сетчатки, при этом, в отличие от ангиографии с внутривенным введением красителей, исследование не является инвазивным, занимает меньше времени и позволяет количественно анализировать микроциркуляцию в различных слоях сетчатки [8]. Для проведения ОКТА используются различные ОКТ-машины, в которых выделение сосудистого сигнала на последовательных Б-сканах реализуется посредством алгоритмов контрастирования, основанных, например, на эффектах допплеровского сдвига, дисперсии спеклов, дисперсии фаз, усиленного контраста спеклов, оптической микроангиографии [9]. Но отличие в разных моделях томографов алгоритмов визуализации сосудистого сигнала и методов автоматической сегментации слоев затрудняет корректное сопоставление количественных результатов исследований при наблюдении заболеваний макулы, включая СМР.
Цель
Изучить взаимосвязь количественных показателей ретинальной перфузии, регистрируемых с помощью различных ОКТ-ангиографов, при сквозных макулярных разрывах.
Материалы и методы
Проведено исследование 25 пациентов (25 глаз) с диагнозом СМР (19 женщин и 6 мужчин) в возрасте 63,5±5,43 года (диапазон от 54 до 73 лет). Критерии включения в исследование: наличие диагноза СМР, отсутствие в анамнезе и на момент осмотра воспалительных заболеваний органа зрения, глаукомы, сосудистых заболеваний сетчатки, дистрофических заболеваний макулы, макулярной неоваскуляризации, аномалий рефракции свыше 3 дптр, качество сигнала при сканировании не ниже Q8 и прозрачные оптические среды.
Всем пациентам в условиях медикаментозного мидриаза (Тропикамид 0,5%) с использованием протокола 3х3 мм и 6х6 мм ОКТА-сканирование на томографах Solix (Optovue, США), Сirrus HD OCT (Carl Zeiss Meditec, США) и DRI OCT Triton plus (Topcon, Япония).
В томографе Solix для проведения ОКТА система AngioVueTM использует источник лазерного излучения с длиной волны 840 нм при скорости сканирования 120 000 А-сканов в секунду и аксиальном разрешении 5 мкм, выделение сосудистого сигнала происходит посредством алгоритма амплитудной декорреляционной ангиографии с разделением спектра (split-spectrum amplitude decorrelation angiography, SSADA). Для минимизации артефактов при получении изображений в томографе предусмотрен алгоритм Dual Track, а протокол сканирования HD OCT angio предусматривает последовательное выполнение 4 сканов, каждый из которых включает 2 ортогональных паттерна, с их усреднением, при этом скан 3x3 мм имеет разрешение 400x400 пикселей.
Сканирование в томографе Сirrus HD OCT (Carl Zeiss Meditec, США) происходит с помощью источника лазерного излучения с длиной волны 840 нм со скоростью сканирования 68 000 А-сканов в секунду, аксиальное разрешение составляет 5 мкм. Программное обеспечение прибора AngioplexTM для выделения сигнала использует алгоритм ОКТ-микроангиографии (OCT-microangiography complex algorithm, OMAG). Для минимизации артефактов движения предусмотрена технология FastTrac. Скан 3x3 мм имеет разрешение 245x245 пикселей, при этом протокол сканирования предусматривает дистанцию между последовательными сканами 12,2 мкм, а каждый B-скан повторяется 4 раза в одной и той же позиции [10].
В томографе DRI OCT Triton plus (Topcon, Япония) предусмотрена система SS OCT AngioTM с использованием источника лазерного излучения с большей длиной волны – 1050 нм, скорость сканирования составляет 100 000 А-сканов в секунду, аксиальное разрешение 8 мкм. Контрастирование сосудов происходит с помощью алгоритма OCTARATM (OCT Angiography Ratio Analysis), а для минимизации артефактов используется система трекинга SMARTTrack с 4-кратным получением каждого скана в каждой позиции [11].
Анализировали вычисляемые автоматически программным обеспечением приборов площадь и периметр фовеальной аваскулярной зоны (ФАЗ), плотность капилляров в поверхностном капиллярном сплетении (ПКС) в зоне фовеа и перифовеа, в соответствии с ETDRS.
Статистическая обработка результатов исследования проводилась с использованием программы Statistica 12.0 (StatSoft Inc., США). Все количественные данные представлены в формате M±SD и Me (Q1;Q3). Оценку нормальности распределения в анализируемых выборках проводили с помощью теста Колмогорова-Смирнова. Сравнение показателей между группами выполнялось с помощью непараметрического U-критерия Манна-Уитни. Для определения связи между параметрами в группах использовали расчет рангового коэффициента корреляции. Статистически значимыми считали результаты с уровнем значимости p<0,05.
Результаты
В исследуемой группе среднее значение максимально корригированной остроты зрения составило 0,31±0,17 при средней рефракции (сфероэквивалент) -0,67±1,93 дптр и ПЗО 23,48±1,02 мм. В 2 случаях глаза с СМР были артифакичными. По данным структурной ОКТ, апикальный диаметр разрыва составил 412,72±129,42 мкм, базальный 835,38±129,43 мкм, во всех случаях вокруг зоны разрыва присутствовал кистозный отек нейроретины.

Докторова Т.А., Суетов А.А., Бойко Э.В., Сосновский С.В.
СОПОСТАВИМОСТЬ ПОКАЗАТЕЛЕЙ ПЕРФУЗИИ СЕТЧАТКИ ПРИ СКВОЗНЫХ МАКУЛЯРНЫХ РАЗРЫВАХ ПО ДАННЫМ РАЗЛИЧНЫХ ОПТИЧЕСКИХ КОГЕРЕНТНЫХ ТОМОГРАФОВ-АНГИОГРАФОВ
Плотность капилляров в ПКС в перифовеа, %
Плотность капилляров в ПКС в фовеа, %
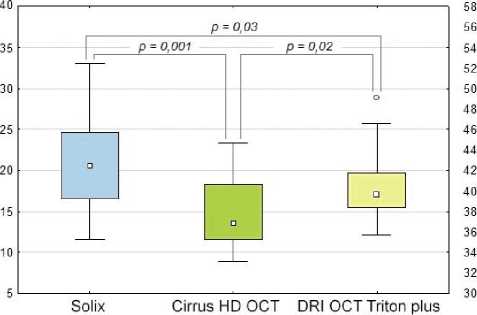
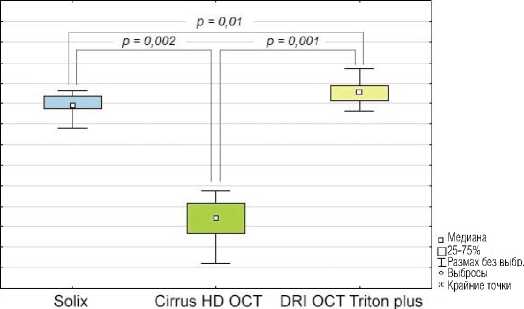
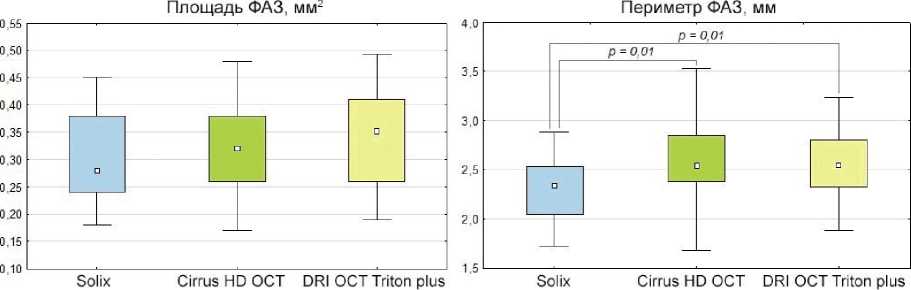
Рис. 1. Сопоставление показателей перфузии макулярной области, измеренных на различных ОКТ-ангиографах, при сквозных макулярных разрывах.
Среднее значение площади ФАЗ значимо не отличалось между приборами и составило для Solix 0,28 (0,24;0,38) мм2, Сirrus HD OCT 0,32 (0,26;0,38) мм2 и DRI OCT Triton plus 0,35 (0,26;0,41) мм2 (p>0,05; Рис. 1), при этом выявлена значимая корреляция значений площади ФАЗ между сравниваемыми ОКТ-ангиографами (R>0,9, p = 0,001).
Показатели периметра ФАЗ составили для Сirrus HD OCT 2,54 (2,38;2,85) мм и DRI OCT Triton plus 2,55 (2,32;2,81) мм (p>0,05). На Solix регистрировали значимо более низкие показатели в сравнении с остальными ОКТ-ангиографами (2,34 (2,05;2,53) мм, p = 0,01; Рис.1), что может быть связано с более правильной формой построения границ зоны ФАЗ. Значимая корреляция значений периметра ФАЗ выявлена между всеми сравниваемыми приборами: для пары Solix и Сirrus HD OCT R = 0,79 (p = 0,001), для пары Сirrus HD OCT и DRI OCT Triton plus R = 0,82 (p = 0,001) и для пары Solix и DRI OCT Triton plus R = 0,66 (p = 0,001).
В зоне фовеа среднее значение плотности капилляров в ПКС составило для Solix 20,54 (16,56;24,63)%, Сirrus HD OCT 13,60 (11,60;18,30)% и DRI OCT Triton plus 17,04 (15,44;19,75)%, при этом показатели значимо отличались между всеми ОКТ-ангиографами (p<0,02; Рис. 1). Значимая корреляция значений в зоне фовеа выявлена между всеми сравниваемыми приборами: для пары Solix и Сirrus HD OCT R = 0,67 (p = 0,01), для пары Сirrus HD OCT и DRI OCT Triton plus R = 0,71 (p = 0,01) и для пары Solix и DRI OCT Triton plus R = 0,76 (p = 0,01).
В зоне перифовеа среднее значение плотности капилляров в ПКС составило для Solix 47,80 (47,50; 48,80)%, Сirrus HD OCT 36,90 (35,30; 38,30)% и DRI OCT Triton plus 49,15 (48,35; 49,78)%, при этом показатели значимо отличались между всеми ОКТ-ангиографами (p<0,01; Рис. 1) и не было выявлено значимой корреляции между ними.
Заключение
При проведении ОКТА в глазах с СМР на приборах Solix, Сirrus HD OCT и Triton plus наибольшее соответствие значений выявлено для показателей площади и периметра ФАЗ. Показатели плотности капилляров в ПКС в сетчатке, окружающей разрыв, при измерении на разных приборах значимо отличаются и не согласуются между собой.
Источник финансирования: исследовательская работа проведена на личные средства авторского коллектива.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).

Докторова Т.А., Суетов А.А., Бойко Э.В., Сосновский С.В.
СОПОСТАВИМОСТЬ ПОКАЗАТЕЛЕЙ ПЕРФУЗИИ СЕТЧАТКИ ПРИ СКВОЗНЫХ МАКУЛЯРНЫХ РАЗРЫВАХ ПО ДАННЫМ РАЗЛИЧНЫХ ОПТИЧЕСКИХ КОГЕРЕНТНЫХ ТОМОГРАФОВ-АНГИОГРАФОВ
Список литературы Сопоставимость показателей перфузии сетчатки при сквозных макулярных разрывах по данным различных оптических когерентных томографов-ангиографов
- Самойлов А.Н., Хайбрахманов Т.Р., Фазлеева Г.А., Самойлова П.А. Идиопатический макулярный разрыв: история и современное состояние проблемы // Вестник офтальмологии. — 2017. — Т.133. — №6 — С. 133–137. [Samoylov AN, Khaibrakhmanov TR, Fazleeva GA, Samoylova PA. Idiopathic macular hole: history and status quo review. Vestnik oftal’mologii. 2017;133(6):131–137. (In Russ).] https://doi.org/10.17116/oftalma20171336131-137.
- Файзрахманов Р.Р., Павловский О.А., Карпов Г.О. Патогенетические механизмы макулярных разрывов: обзор текущих исследований. Российский офтальмологический журнал. 2023;16(2):183-187. [Fayzrakhmanov RR, Pavlovsky OA, Karpov GO. Pathogenetic mechanisms of macular holes: a review of recent research work. Russ Ophthalmol J 2023;16:183–7. (In Russ).] https://doi.org/10.21516/2072-0076-2023-16-2-183-187.
- Докторова Т.А., Суетов А.А., Бойко Э.В., Сосновский С.В. Влияние ретинальной перфузии на биоэлектрическую активность сетчатки при сквозных макулярных разрывах // Офтальмологические ведомости. – 2022. – Т. 15. – №4. – C. 7-14. [Doktorova TA, Suetov AA, Boiko EV., Sosnovskii SV. The effect of retinal perfusion on the bioelectric activity of the retina in full-thickness macular holes. Ophthalmol J 2022;15:7–14. (In Russ).] https://doi.org/10.17816/OV111903.
- Kim YJ, Jo J, Lee JY, Yoon YH, Kim JG. Macular capillary plexuses after macular hole surgery: An optical coherence tomography angiography study. Br J Ophthalmol 2018;102:966–70. https://doi.org/10.1136/bjophthalmol-2017-311132.
- Nair U, Sheth JU, Indurkar A, Soman M. Intraretinal cysts in macular hole: A structure-function correlation based on en face imaging. Clin Ophthalmol 2021;15:2953–62. https://doi.org/10.2147/OPTH.S321594.
- Rizzo S, Savastano A, Bacherini D, Savastano MC. Vascular features of full-thickness macular hole by OCT angiography. Ophthalmic Surg Lasers Imaging Retin 2017;48:62–8. https://doi.org/10.3928/23258160-20161219-09.
- Шкворченко Д.О., Крупина Е.А., Фомин А.В. ОКТ-ангиография в оценке результатов хирургического лечения макулярных разрывов. Офтальмология. 2019;16(3):310-316. [Shkvorchenko DO, Krupina EA, Fomin A V. OCT angiography in evaluation of the macular holes treatment results. Oftalmologiya 2019;16:310–6. (In Russ).] https://doi.org/10.18008/1816-5095-2019-3-310-316.
- Spaide RF, Fujimoto JG, Waheed NK, Sadda SR, Staurenghi G. Optical coherence tomography angiography. Prog Retin Eye Res 2018;64:1–55. https://doi.org/10.1016/j.preteyeres.2017.11.003.
- Sampson DM, Dubis AM, Chen FK, Zawadzki RJ, Sampson DD. Towards standardizing retinal optical coherence tomography angiography: a review. Light Sci Appl 2022;11. https://doi.org/10.1038/s41377-022-00740-9.
- Rosenfeld PJ, Durbin MK, Roisman L, Zheng F, Miller A, Robbins G, et al. ZEISS AngioplexTM Spectral Domain Optical Coherence Tomography Angiography: Technical Aspects. Dev Ophthalmol 2016;56:18–29. https://doi.org/10.1159/000442773.
- Stanga PE, Tsamis E, Papayannis A, Stringa F, Cole T, Jalil A. Swept-Source Optical Coherence Tomography AngioTM (Topcon Corp, Japan): Technology Review. Dev Ophthalmol 2016;56:13–7. https://doi.org/10.1159/000442771.


