Сорбционная очистка модельных растворов от ионов железа и кремния с применением оксигидроксида алюминия
Автор: Мачехина Ксения Игоревна, Грязнова Елена Николаевна, Меринова Лилия Рашидовна, Абрамова Полина Владимировна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Неорганическая химия
Статья в выпуске: 1 т.14, 2022 года.
Бесплатный доступ
Исследованы процессы сорбции ионов железа (III) и кремния из модельного раствора с применением сорбента - нановолокнистого оксигидроксида алюминия, полученного методом окисления порошка алюминия водой при постоянной температуре в диапазоне от 60 до 75 °С, с удельной поверхностью 196,16 м2/г, диаметром пор от 2 до 15 нм и длиной до 1 мкм. Порошок алюминия получен методом электрического взрыва проводника в аргоне. Изучены процессы сорбции ионов железа и кремния из модельного раствора, содержащего ионы железа (III), кремний и органические вещества гумусового происхождения на оксигидроксиде алюминия и активированном угле. Установлено, что степень извлечения ионов железа и кремния составила 82 % и 41 % соответственно для сорбента оксигидроксида алюминия при исходной концентрации железа 6,7 мг/л и кремния 25,6 мг/л. Для активированного угля - это 25 и 9 % при одной и той же массе навески сорбента. Время сорбции составило 4 часа. Значение максимальной сорбционной емкости оксигидроксида алюминия по отношению к ионам железа составило 10 мг/г, к ионам кремния 38 мг/г из модельного раствора. Полученный нановолокнистый оксигидроксид алюминия можно использовать на стадии доочистки для удаления железа, связанного с кремнийорганическими соединениями из подземных вод, в которых содержание железа в коллоидном состоянии не превышает 2 мг/л, при содержании кремния не выше 12,4 мг/л и органических веществ до 6,2 мг/л.
Оксигидроксид алюминия, сорбция, железо, кремний, водоподготовка
Короткий адрес: https://sciup.org/147236627
IDR: 147236627 | УДК: 546.62+546.05 | DOI: 10.14529/chem220109
Sorption purification of model solutions from iron and silicon ions using aluminum oxyhydroxide
The sorption processes of iron(III) and silicon ions from a model solution have been investigated using nanofibrous aluminum oxyhydroxide as a sorbent, obtained by oxidizing aluminum powder with water at a constant temperature in the range from 60 to 75 °C; its surface area is 196.16 m2/g, the pore diameters are from 2 to 15 nm, and the lengths are up to 1 μm. Aluminum powder was obtained by electric explosion of a conductor in argon. The adsorption processes have been studied for iron and silicon ions on aluminum oxyhydroxide and activated carbon from a model solution containing iron(III) ions, silicon, and organic substances of humic origin. The degrees of extraction of iron and silicon ions have been 82% and 41%, respectively, for the aluminum oxyhydroxide sorbent, at the initial concentration of iron 6.7 mg/L and 25.6 mg/L of silicon. For activated carbon, these have been 25% and 9% at the same weight of the sorbent sample. The sorption time is 4 hours. The value of the maximum sorption capacity of aluminum oxyhydroxide with respect to iron ions is 10 mg/g, and 38 mg/g for silicon ions from the model solution. The nanofibrous aluminum oxyhydroxide can be used at the post-treatment stage to remove iron associated with organosilicon compounds from groundwater, where iron substances are present in the colloid form and their concentration does not exceed 2 mg/L and the concentration of silicon does not exceed 12.4 mg/L, with organic substances up to 6.2 mg/L.
Текст научной статьи Сорбционная очистка модельных растворов от ионов железа и кремния с применением оксигидроксида алюминия
Сорбционная очистка является одним из методов для глубокой очистки сточных, природных и технических вод для многих сфер производства. Среди существующих технологий водоподготовки процесс сорбции имеет ряд преимуществ: низкая стоимость, простота конструкций и удобство эксплуатации. Кроме этого сорбционные методы очистки могут быть использованы на стадии доочистки или для очистки вод, содержащих примеси в коллоидном состоянии. Примером таких вод являются подземные воды северных районов Сибири [1], которые характеризуются повышенной заболоченностью. Особенностью вод этого региона являются примеси, содержащие гидроксид железа (III), которые благодаря соединениям кремния и органическим веществам гумусового происхождения находятся в воде во взвешенном состоянии, обеспечивая повышенную мутность и цветность воды [2, 3]. При обработке вод такого состава снижается эффективность работы установок [4] и возникают проблемы получения питьевой воды, соответствующей Сан-ПиН 2.1.4.1074-01 «Питьевая вода. Гигиенические требования к качеству воды». Основными методами удаления примесей в коллоидном состоянии, которые применяются в водоподготовке, являются мембранные технологии на стадии доочистки, использование коагулянтов и сорбционные методы. Процессы ультра- и нанофильтрации примесей в коллоидном состоянии были исследованы авторами в работе [5]. Результаты показали, что только использование нанофильтра-ционных мембран приводит к снижению концентрации ионов железа и кремния в растворе до значений ПДК. При этом наблюдается низкая производительность.
Исследования в области создания композиционных материалов, применение которых в технологиях водоподготовки позволило бы увеличить эффективность и производительность существующих установок, ведутся постоянно [6–10]. Наиболее распространенным сорбентом является активированный уголь ввиду его большой удельной поверхности (от 500–1500 м2/г), которая активизирует углерод и идеально подходит для адсорбции [11, 12]. В настоящей работе в качестве эталонного сорбента использовали активированный уголь (PAC) Norit SA UF производства фирмы Norit.
Проведенные нами ранее исследования примесей в коллоидном состоянии на модельной системе, состоящей из соединений железа, кремния и органических веществ гумусового происхождения, показали, что частицы имеют отрицательный заряд поверхности [13]. Поэтому сорбционный процесс наиболее эффективно протекает при использовании сорбента, поверхность которого заряжена положительно.
Работы в области получения сорбентов с высокой удельной поверхностью ведутся постоянно [14–18]. Одним из таких сорбентов является оксигидроксид алюминия.
Цель работы – изучить сорбционные свойства нановолокнистого оксигидроксида алюминия для удаления ионов железа и кремния из модельных растворов.
Экспериментальная часть
Современные способы получения нановолокнистого оксигидроксида алюминия (AlOOH) достаточно разнообразны [19–22]. В работе [23] описаны преимущества и недостатки основных методов их получения. Нами выбран метод окисления нанопорошка алюминия, полученного методом электрического взрыва проводника (ЭВП) в аргоне, водой при постоянной температуре в диапазоне от 60 до 75 °С, по методике, описанной в [24]. Морфологические характеристики сорбента исследовали методом просвечивающей электронной микроскопии с использованием электронного микроскопа JEM-2100F (JEOL, Япония). Образцы для просвечивающей электронной микроскопии предварительно подготавливали путем помещения их в спирт, после чего получали однородную суспензию в ультразвуковом поле частотой 23 кГц и мощностью 400 Вт. Из полученной суспензии микропипеткой отбирали аликвоту и помещали на медную сетку для электронной микроскопии с предварительно нанесенной формваровой пленкой.
Спецификация сорбента, выбранного в качестве эталонного, приведена в табл. 1.
Таблица 1
Спецификация сорбента Norit SA UF
|
Производитель |
Norit |
|
Название |
Norit SA UF |
|
Удельная площадь поверхности, м2/г |
1200 |
|
Средний диаметр частиц, мкм |
7 |
|
Размер частиц > 180 мкм, макс. % от общей массы |
0,1 |
|
Насыпная плотность, кг/м3 |
160 |
|
Влажность, макс., % |
5 |
Для определения сорбционной активности сорбентов использовали модельный раствор, который состоял из трех основных компонентов, таких как ионы железа (III), ионы кремния и органические вещества гумусового происхождения. Методика приготовления модельного раствора описана авторами в работе [25]. Концентрация органических веществ в модельном растворе составляла 2,2 мг О 2 /л, ионов железа (III) – 6,7 мг/л и ионов кремния – 25,6 мг/л.
Сорбционные свойства сорбентов определяли статическим методом. Для эксперимента готовили семь одинаковых растворов: в колбу объемом 250 мл помещали навеску сорбента и добавляли модельный раствор. Затем колбы с раствором и сорбентом ставили в устройство для перемешивания Lab-Shaker 110. Скорость вращения составляла 180 об/мин. С момента начала перемешивания засекали время и убирали по одной колбе через 15, 30, 60, 120, 180, 240 и 1440 минут соответственно. Для отделения раствора от адсорбента полученную смесь фильтровали через мембрану фирмы Millpore (США). Размер пор мембраны составлял 400 нм. Далее в пробах определяли содержание органических веществ, ионов железа и кремния.
Содержание органических веществ в воде оценивали по величине химического потребления кислорода (ХПК). ХПК определяли фотометрическим методом с использованием фотометрического анализатора «Флюорат-02-3М» фирмы «Люмекс» согласно ГОСТ 31859-2012. «Вода. Метод определения химического потребления кислорода». Сущность метода заключается в обработке пробы воды серной кислотой и бихроматом калия при заданной температуре в присутствии сульфата серебра и определении значений ХПК в заданном диапазоне концентраций путем измерения оптической плотности исследуемого раствора при заданном значении длины волны.
Содержание ионов железа и кремния в растворе определяли фотоколориметрически с использованием спектрофотометра ПЭ-6100УФ фирмы ПРОМЭКОЛАБ. Для определения кремния использовали методику согласно РД 52.24.433-2005, для железа общего – ГОСТ 4011-72.
Сорбционный эксперимент состоял из двух основных этапов: построение кинетики и изотермы сорбции. Экспериментально величину адсорбции (А) растворенных веществ на твердом сорбенте при различных концентрациях компонентов в модельном растворе вычисляли по урав- нению:
(С -С УК
A =
исх равн р-ра
, mсорб где Cисх и Cравн – исходная и равновесная концентрация ионов в растворе; mсорб – масса сорбента;
V р-ра – объем раствора.
Обсуждение результатов
Структура полученного оксигидроксида алюминия характеризуется таким понятием, как пористость, которая представлена в основном мезопорами. Площадь удельной поверхности полученного оксигидроксида алюминия, определённая методом тепловой десорбции азота с помощью прибора «Сорбтометр-М» (Россия), составила 196,16 м2/г, имея при этом диаметр от 2 до 15 нм, а длину до 1 мкм. Содержание металлического алюминия менее 0,5 мас. %. Микрофотография полученного сорбента представлена на рис. 1.

Рис. 1. Микрофотография нановолокнистого оксигидроксида алюминия
Состав модельного раствора выбирали исходя из данных мониторинга подземных вод Сибири. Анализ подземных вод указанного региона ведется коллективом авторов около 15 лет. Процесс водоподготовки таких вод осложняется в значительной степени одновременным присутствием в воде соединений железа и кремния в коллоидном состоянии, поэтому кинетические зависимости строили отдельно для каждого компонента.
На рис. 2 (а и б) приведены кинетические кривые сорбции ионов железа и кремния на оксигидроксиде алюминия. Для сравнения на графиках представлены кинетические кривые сорбции ионов железа и кремния на активированном угле.
Из рис. 2 видно, что степень извлечения ионов железа и кремния составляет 82 и 41 % соответственно для сорбента оксигидроксида алюминия. Для активированного угля – это 25 и 9 % при одной и той же массе навески. Определено время сорбции, которое составило 4 часа. В дальнейшем сорбционный эксперимент для получения изотермы сорбции проводили 4 часа. Для по- лучения изотермы сорбции концентрацию компонентов модельного раствора оставляли постоянной (см. табл. 1). Объем модельного раствора составлял 250 мл. Массу сорбента оксигидроксида алюминия изменяли от 2,5 мг до 750 мг.
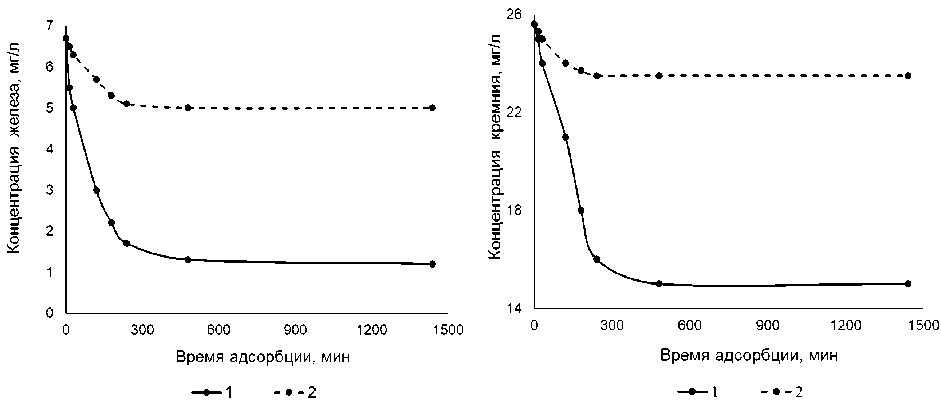
Рис. 2 б. Кинетика адсорбции ионов кремния из модельного раствора: 1 – на AlOOH;
2 – на активированном угле Norit SA UF
Рис. 2 а. Кинетика адсорбции ионов железа из модельного раствора: 1 – на AlOOH;
2 – на активированном угле Norit SA UF
Для получения количественных характеристик процессов сорбции построили изотермы сорбции ионов железа (III) (рис. 3, а) и кремния (рис. 3, б) на оксигидроксиде алюминия.
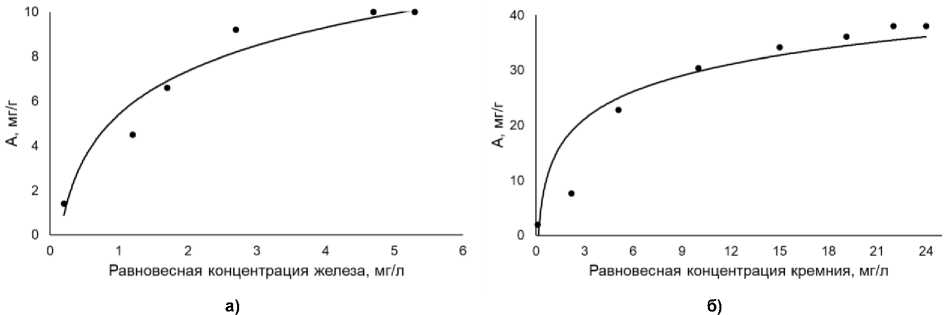
Рис. 3. Изотерма адсорбции на оксигидроксиде алюминия: а – ионов железа (III); б – адсорбции ионов кремния
Исходя из анализа полученных экспериментальных результатов по сорбции ионов железа и кремния, установили, что процесс протекает в соответствие с уравнением Ленгмюра:
CC 1
-
—--1--,
A Am AmKi где A – количество вещества, адсорбированного 1 м² поверхности (или 1 г) адсорбента (удельная адсорбция вещества), г/м² или г/г; Am – количество вещества, адсорбированного 1 м² поверхности (или 1 г) адсорбента при максимальном ее заполнении, г/м² или г/г; С – равновесная концентрация вещества в газовой фазе или растворе; Kl – константа адсорбционного равновесия, характеризующая энергию взаимодействия адсорбата и адсорбента.
Значение максимальной сорбционной емкости оксигидроксида алюминия по отношению к ионам железа составило А m = 10 мг/г, к ионам кремния А m = 38 мг/г. Для активированного угля полученные значения составили Аm = 0,5 мг/г для ионов железа и Аm = 1 мг/г для ионов кремния.
Сравнение сорбционных свойств активированного угля и оксигидроксида алюминия по отношению к ионам железа и кремния, показало, что на активированном угле ионы железа и кремний практически не сорбируется в сравнении с оксигидроксидом алюминия. Высокую сорбционную емкость по сравнению с активированным углем можно объяснить тем, что оксигидроксид алюминия имеет положительный электрокинетический потенциал, равный +60 мВ [23], определенный методом динамического светорассеяния по электрофоретической подвижности частиц. Исследования физико-химических свойств модельного раствора [26] показали, что электрокинети-ческий потенциал коллоидных частиц модельного раствора составляет –32 мВ, что связано со строением дисперсной фазы. Ядром выступает гидроксид железа (III), который окружен потен-циалопределяющими ионами из гидроксокатионов железа, органических молекул гуминовых веществ и силикат-ионов. Сорбция отрицательно заряженных коллоидных частиц идет за счет межмолекулярного взаимодействия (cил Ван-дер-Ваальса).
Для области средних концентраций в диапазоне 1,0–3,2 мг/л для ионов железа (см. рис. 3, а) и 2,0–15,0 мг/л для ионов кремния (см. рис. 3, б) построили изотермы сорбции в координатах линейной формы уравнения Ленгмюра. Экстраполяция зависимости до оси ординат дает отрезок, равный . Полученные значения констант сорбционного равновесия по отношению к ионам AmK железа и кремния составили 0,7 и 0,09 соответственно. Значения констант свидетельствуют о слабом латеральном взаимодействии адсорбата и адсорбента.
Полученный нановолкнистый оксигидроксид алюминия апробировали в качестве сорбента на реальной подземной воде, отобранной в с. Майское (Томская область). Перед экспериментом воду аэрировали кислородом воздуха для окисления железа (II), а затем отстаивали в течение 1 ч для осаждения гидроксида железа (III), которое не связано в кремнийорганические соединения, и фильтрования через фильтр 400 нм. Результаты проведенных исследований представлены в табл. 2.
Таблица 2 Химический состав воды с. Майское (Томская область)
|
Показатели |
Химический состав воды, мг/л |
ПДК |
||
|
исходной |
после окисления и отстаивания и фильтрования |
после сорбции на AlOOH |
||
|
ХПК (мг O 2 /л) |
6,3 |
6,2 |
2,0 |
5,0 |
|
Al |
0,045 |
0,045 |
0,045 |
0,5 |
|
Fe |
6,1 |
2,0 |
0,2 |
0,3 |
|
Si |
12,4 |
12,4 |
6,3 |
10,0 |
Из анализа табличных данных следует, что сорбционная очистка с применением нановолок-нистого оксигидроксида алюминия целесообразна для удаления железа, связанного с кремнийор-ганическими веществами, которые не удаляются при очистке по классической технологии, которая включает аэрацию, отстаивание и фильтрование. Степень извлечения ионов железа составила 90 %, а кремния – 49 %.
Заключение
Определены основные параметры сорбции ионов железа и кремния из модельного раствора на оксигидроксиде алюминия с удельной поверхностью 196,16 м2/г, диаметром пор от 2 до 15 нм и длиной до 1 мкм. Установлено, что степень извлечения ионов железа увеличивается в 3,3 раза и ионов кремния в 4,5 раза по сравнению с активированным углем. Время сорбции составило 4 часа. Значение максимальной сорбционной емкости оксигидроксида алюминия по отношению к ионам железа составило 10 мг/г, к ионам кремния 38 мг/г из модельного раствора.
Полученный нановолокнистый сорбент можно использовать на стадии доочистки для удаления железа, связанного с кремнийорганическими соединениями из подземных вод, в которых содержание железа в коллоидном состоянии не превышает 2 мг/л, при содержании кремния не выше 12,4 мг/л и органических веществ до 6,2 мг/л.
Список литературы Сорбционная очистка модельных растворов от ионов железа и кремния с применением оксигидроксида алюминия
- Видяйкина, Н.В. Обеспечение экологической безопасности при использовании сельским населением подземных вод для питьевых целей на примере Томской области и Ханты-Мансийского автономного округа: дис. … канд. геол.-минерал. наук / Н.В. Видяйкина. – Томск, 2010. – 153 с.
- Geochemical Groundwater Peculiarities of Paleogene Sediments in S-E Western Siberia Artesian Basin / А.А. Balobanenko, V.A. L'gotin, E.M. Dutova et al. // IOP Conf. Series: Earth and Environmen-tal Science. – 2016. – V. 43. – P. 012030. DOI: 10.1088/1755-1315/43/1/012030.
- Цветность подземных вод Западно-Сибирского региона / Л.В. Сериков, Л.Н. Шиян, Е.А. Тропина и др. // Известия Томского политехнического университета. – 2009. – Т. 314, № 3. – С. 54–58.
- Iron Oxidation in Different Types of Groundwater of Western Siberia / L.V. Serikov, E.A. Tropi-na, L.N. Shiyan et al. // J. Soils Sediments. – 2009. – V. 9, № 2. – P. 103–110. DOI: 10.1007/s11368-009-0069-x
- Изучение процессов ультра и нанофильтрования коллоидных растворов железа / К.И. Мачехина, Л.Н. Шиян, Е.А. Тропина и др. // Известия Томского политехнического университета. – 2011. – Т. 318, № 3. – С. 27–30.
- Тарнопольская, М.Г. Физико-химические основы очистки воды угольным сорбентом МИУ-С / М.Г. Тарнопольская // Водоснабжение и санитарная техника. – 2006. – № 7. – С. 35–39.
- Кахраманлы, Ю.Н. Сорбент на основе пенаполиамида для очистки водной поверхности от нефти и нефтепродуктов / М.Г. Кахраманлы, Н.Т. Алиева // Вода: химия и экология. – 2011. – № 6. – С. 70–75.
- Артѐменко, С.Е. Гибридные композиционные материалы / С.Е. Артѐменко, Ю.А. Кадыкова // Химические волокна. – 2008. – № 6. – С. 5–7.
- Марченко, Л.A. Сорбционная доочистка сточных вод / Л.A. Марченко, Т.Н. Биковикова, A.C. Шабанова // Экология и промышленность России. – 2007. – Октябрь. – С. 53–55.
- Kardash, M.M. Problems of Wastewater Treatment and Methods of Solving them / M.M. Kar-dash, A.A. Fedorchenko, N.B. Fedorchenko // Fibre Chemistry. – 2003. – V. 35, № 1. – P. 79–82. DOI: 10.1023/A:1023844226989
- Тарнопольская, М.Г. Сравнение сорбента МИУ-С с различными активными углями с помощью экспресс-метода контроля метиленового голубого / М.Г. Тарнапольская, Е.А. Соловьева // Вода: химия и экология. – 2011. – № 3. – С. 52–57.
- Сорбция ионов меди активированным углем марки БАУ-А / О.Д. Линников, И.В. Родина, И.В. Бакланова и др. // Сорбционные и хроматографические процессы. – 2018. – Т. 18, № 4. – С. 554–562. DOI: 10.17308/sorpchrom.2018.18/563
- Мачехина, К.И. Устойчивость коллоидов железа в природных водах / К.И. Мачехина, Л.Н. Шиян, Е.А. Тропина // Журнал прикладной химии. – 2012. – Т. 85, № 7. – С. 1182‒1185.
- Сорбционная очистка растворов от ионов тяжелых металлов с применением цеолита, модифицированного углеродными нанотрубками / Т.Ю. Дьячкова, И.А. Макарова, Е.С. Ваганова и др. // Вестник ЮУрГУ. Серия «Химия». – 2019. – Т. 11, № 2. – С. 16–27. DOI: 10/14529/chem190202.
- Буянтуев, С.Л. Исследование удельной поверхности углей, обработанных электродуговой плазмой, с помощью модели полимолекулярной адсорбции Брунауэра, Эммета, Теллера / С.Л. Буянтуев, А.С. Кондратенко // Вестник Бурятского госуниверситета. – 2012. – № 3. – С. 226–230.
- Boehm, H.P. Surface Oxides on Carbon and their Analysis: a Critical Assessment / H.P. Boehm // Carbon. – 2002. – № 40. – P. 145–149. DOI: 10.1016/S0008-6223(01)00165-8
- Kongsuwan, A. Binary Component Sorption of Cu(II) and Pb(II) with Activated Carbon from Eucalyptus Camaldulensis Dehn Bark / A. Kongsuwan, P. Patnukao, P. Pavasant // J. Ind. Eng. Chem. – 2009. – № 15. – P. 465–470. DOI: 10.1016/j.jiec.2009.02.002
- Statistical Optimization of the Synthesis of Highly Microporous Carbons by Chemical Activation of Kraft Lignin with NaOH / V. Torné-Fernández, J. Mateo-Sanz, D. Montané et al. // J. Chem. Eng. – 2009. – № 54. – P. 2216–2221. DOI: 10.1021/je800827n
- Hydrothermal Synthesis and in situ Surface Modification of Boehmite Nanoparticles in Super-critical Water / T. Mousavand, S. Ohara, M. Umetsu et al. // J. Supercrit. Fluids. – 2007. – V. 40. – P. 397–401. DOI: 10.1016/j.supflu.2006.07.021
- Mahmoodi, K. Fast and Facile Synthesis of Boehmite Nanofibers / K. Mahmoodi, B. Alinejad // Powder Technol. – 2010. – V. 199. – P. 289–292. DOI: 10.1016/j.powtec.2010.01.019
- Ksapabutra, B. Sol–gel Transition Study and Pyrolysis of Alumina-based Gels Prepared from Alumatrane Precursor / B. Ksapabutra, E. Gularib, S. Wongkasemjita // Colloids and Surfaces A: Physi-cochem. Eng. Aspects. – 2004. – V. 233. – P. 145–153. DOI: 10.1016/j.colsurfa.2003.11.019
- Hydrothermal Synthesis and Characterization of Core/Shell AlOOH Microspheres / L. Zhang, W. Lu, L. Yan et al. // Microporous Mesoporous Mater. – 2009. – V. 119. – P. 208–216. DOI: 10.1016/j.micromeso.2008.10.017
- Грязнова, Е.Н. Технология получения модифицированного ионами марганца (II) оксигидроксида алюминия нановолокнистой структуры и материалов на его основе: дис. … канд. техн. наук / Е.Н. Грязнова. – Томск, 2015. – 135 с.
- Влияние процесса модифицирования на свойства нановолокон оксогидроксида алюминия / Е.Н. Грязнова, Л.Н. Шиян, Н.А. Яворовский, В.В. Коробочкин // Журнал прикладной хи-мии. – 2013. – Т. 86, № 3. – С. 389–394.
- Пат. 2502556 Российская Федерация. Способ приготовления модельного коллоидного раствора / В.А. Власов, Е.Н. Грязнова, К.И. Мачехина, Е.А. Тропина, Л.Н. Шиян; заявитель и патентообладатель Национальный исследовательский Томский политехнический университет. – № 2502556; заявл. 12.07.2012; опубл. 27.12.2013, Бюл. № 11. – 5 с.
- Мачехина, К.И. Процесс очистки подземных вод от коллоидных соединений железа и его аппаратурное оформление: дис. … канд. техн. наук / К.И. Мачехина. – Томск, 2013. – 121 с.


