Сорбционное концентрирование ионов серебра сетчатыми сополимерами 1-винил-1,2,4-триазола с дивинилсульфидом
Автор: Шаулина Людмила Павловна, Ермакова Тамара Георгиевна, Кузнецова Надежда Петровна, Прозорова Галина Фирсовна, Андреева Алена Игоревна
Журнал: Вестник Бурятского государственного университета. Философия @vestnik-bsu
Рубрика: Химия
Статья в выпуске: 3, 2015 года.
Бесплатный доступ
Исследованы условия извлечения, механизм взаимодействия и сорбционные характеристики сетчатых сополимеров 1-винил-1,2,4-триазола с дивинилсульфидом различного состава.
Сетчатые сополимеры, 1-винил-1, 4-триазол, дивинилсульфид, сорбция, сорбционная емкость, коэффициент распределения, условия элюирования
Короткий адрес: https://sciup.org/148182883
IDR: 148182883 | УДК: 546.42
Sorbtion concentration of silver ions by cross-linked copolymers 1-vinyl-1,2,4-triazole with divinylsulfide
Sorbtion conditions, the mechanism of interaction and sorption characteristics of cross-linked copolymers of 1-vinyl-1,2,4-triazole with divinylsulfide with various ratio of components were determined.
Текст научной статьи Сорбционное концентрирование ионов серебра сетчатыми сополимерами 1-винил-1,2,4-триазола с дивинилсульфидом
Сорбционное извлечение благородных металлов, в частности серебра, связано с выделением его из растворов сложного состава, анализом низких концентраций, использованием агрессивных технологических растворов. Избирательность сорбционного извлечения обеспечивается кислотностью рас- твора. В ряде работ показано, что эффективное извлечение комплексообразующими сорбентами возможно из растворов с концентрацией 1–3М [1–3].
Ведущая роль в сорбционном концентрировании и выделении ионов комплексообразующими сорбентами принадлежит функциональным группам, содержащим активные атомы [4, 5]. На свойства соединений, их сорбционную активность значительное влияние оказывает природа мономеров и сшивающих агентов. Последние обеспечивают определенную структуру сополимера, делают ее пористой, увеличивают общую поверхность [4]. В работах [6, 7] в качестве сшивающего агента использовали дивинилсульфид. Наряду с созданием пространственно сшитого соединения, которое имеет высокую химическую прочность, с сомономером вводятся донорные атомы серы, способные к образованию координационной связи с ионами металлов.
Целью данной работы является исследование сорбционных свойств сополимеров 1-винил-1,2,4-триазола с дивинилсульфидом разного состава по отношению к иону серебра и выяснение возможности их использования в качестве сорбентов.
Сополимеры 1-винил-1,2,4-триазола (ВТ) с дивинилсульфидом (ДВС) синтезировали радикальной полимеризацией сомономеров в массе в присутствии ДАК при 60 оС в течение 6 ч. Структурная формула сополимера (сорбент С) представлена на схеме:
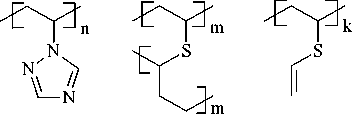
Сополимеры представляют собой стеклообразные блоки светло-желтого цвета, нерастворимые в кислотах, щелочах, органических растворителях. Состав и структуру сополимеров определяли по данным элементного анализа и ИК-спектроскопии. Сополимеры обогащены звеньями ДВС независимо от соотношения сомономеров в реакционной смеси (табл. 1).
В ИК-спектрах сополимеров наблюдаются полосы поглощения, отвечающие частотам валентных и деформационных колебаний триазольного цикла, см-1: (1503, 1429, 1275, 1120, 1000, 660), и дивинилсульфидного фрагмента, см-1: 670-750. В сополимерах присутствуют в небольших количествах двойные связи тиовинильной группы ДВС. Последний выступает в реакции сополимеризации одновременно как сомономер и как сшивающий агент.
Таблица 1
Элементный анализ и состав сополимеров
|
Сорбент |
Состав исходной смеси, мол. % |
Элементный анализ, % |
Состав сополимера, мол. % |
|||
|
ВТ |
ДВС |
N |
S |
ВТ |
ДВС |
|
|
С1 |
30 |
70 |
10.64 |
28.14 |
22 |
75 |
|
С2 |
50 |
50 |
16.39 |
19.37 |
35 |
65 |
|
С3 |
70 |
30 |
25.01 |
10.97 |
56 |
46 |
|
С4 |
97 |
3 |
35.83 |
2.72 |
80 |
20 |
Известно, что сополимер ВТ является комплексообразователем за счет донорных свойств атома азота в четвертом положении гетерокольца [8, 9]. Вместе с тем протонизация в кислых средах делает этот сополимер анионообменником [6].
Сорбционные свойства исследовали в статических условиях. Концентрации ионов металлов контролировали атомно-абсорбционным методом.
Изучено влияние природы и концентрации кислот в интервале 1-7М на извлечение ионов серебра. В зависимости, представленной на рис. 1, отмечается тенденция к уменьшению сорбции с увеличением концентрации кислот. Извлечение несколько выше в сернокислом растворе.
Возможная причина этого заключается в том, что серебро в растворе находится как в катионной форме, так и в виде анионных комплексов [Ag(SO4)]- и [Ag(SO4)2]3-. Извлечение катионной формы серебра из растворов кислот осуществляется по координационному механизму. Снижение сорбции обеспечивается протеканием конкурирующей реакции с ионами водорода (схема 1).
Но из раствора серной кислоты по ионообменному механизму возможно извлечение комплексного аниона, для которого характерна конкурирующая реакция с анионом кислоты (схема 2). Установление характеристик далее проводили из 1М растворов кислот.
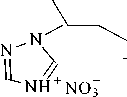
Ag+
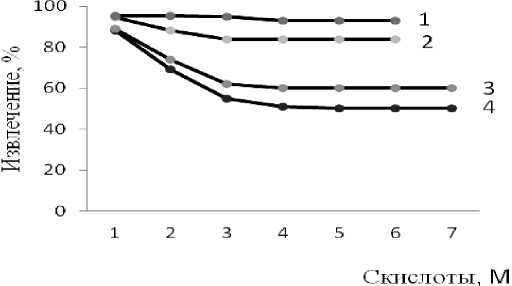
Рис. 1. Влияние природы и концентрации кислот на извлечение ионов серебра сорбентами С1 (1, 2) и С4 (3, 4); 1,3 – H 2 SO4; 2,4 – HNO 3
Схема 1
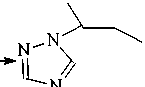
Ag+NO 3 -
Схема 2
NH+[Ag(SO 4 )]-
Для доказательства взаимодействия использовали данные ИК-спектроскопии образцов сорбентов, обработанных 1М растворами кислот, и образцов, содержащих ионы серебра. В спектрах образцов происходят изменения полос, связанных с состоянием атома азота (4): для наиболее интенсивной полосы 1505 отмечается сдвиг до 1516 см-1.
Извлечение характеризуется высокой скоростью: время установления равновесия составляет 20– 30 мин при времени полусорбции τ 1/2 = 8–15 мин.
Основными характеристиками сорбентов являются сорбционная емкость и коэффициенты распределения. Для определения этих характеристик изучали равновесное распределение серебра от его концентрации в 1М растворах азотной и серной кислот (рис. 2).
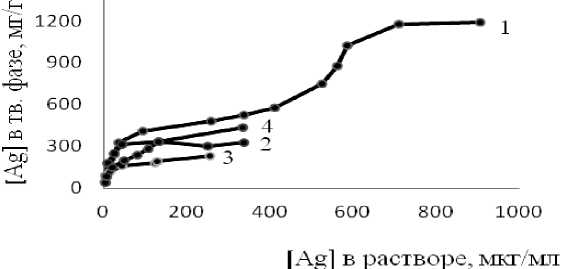
Рис. 2. Кривые равновесного распределения ионов серебра для сополимеров C2 (3, 4) и C4 (1, 2): 1, 4 – H 2 SO 4 , 2, 3 – HNO 3
Значения сорбционной емкости сополимеров и коэффициентов распределения серебра представлены в табл. 2.
Анализируя данные табл. 2, следует отметить, что, несмотря на небольшую разницу в суммарном содержании активных атомов ( ∑ ), значение сорбционной емкости возрастает с увеличением количества атомов азота (триазольных циклов). Для сорбента с наибольшим содержанием атомов серы наблюдается меньшее значение емкости, что является подтверждением неучастия атомов серы в сорбционном взаимодействии.
Таблица 2
Значения сорбционной емкости (СЕ) и коэффициентов распределения (D) серебра в растворах кислот для сополимеров ВТ-ДВС
|
Сорбент |
Содержание гетероатомов, % |
СЕ, мг/г; D, см3/г |
|||
|
N |
S |
∑ |
HNO 3 |
H 2 SO 4 |
|
|
C1 |
10.64 |
28.14 |
38.78 |
120; 1.9 ·103 |
134; 1.2∙103 |
|
C2 |
16.39 |
19.37 |
35.76 |
180; 2.4 ·103 |
325; 2.2∙103 |
|
C3 |
25.01 |
10.97 |
35.98 |
560; 1.3 ·104 |
520; 1.5∙104 |
|
C4 |
35.83 |
2.72 |
38.55 |
- |
1184; 1.0∙104 |
Изотерма для сополимера С4 имеет S-образный характер (рис. 2, кривая 1). Объяснить это можно тем, что сорбент отличается от других по его способности к набуханию (меньшее количество сшивающего агента). Следовательно, если сначала осуществляется сорбция за счет химического взаимодействия, то вторая ступень связана с проникновением ионов сорбата внутрь набухшей гранулы (физическая сорбция).
Установлено, что из 1М растворов кислоты не извлекаются ионы железа и цветных металлов, за исключением ионов меди.
Для регенерации сорбентов использовали 3 %-ный раствор тиомочевины в 1М соляной кислоте, которая образует с ионами серебра водорастворимый бесцветный комплекс [Ag(NH 2 ) 2 CS] 3 +, используемый в атомно-абсорбционном определении. При комнатной температуре в течение 60 мин элюируется из фазы сорбента до 83 % серебра, при 60 оС - до 97 %. Сополимеры не теряют своей сорбционной активности в двух циклах: сорбция – десорбция. Сополимеры можно рекомендовать для извлечения ионов серебра из кислых, сложных по составу растворов.
Список литературы Сорбционное концентрирование ионов серебра сетчатыми сополимерами 1-винил-1,2,4-триазола с дивинилсульфидом
- Шаулина Л.П., Скушникова А.И., Домнина Е.С. Изучение сорбции ионов благородных металлов сетчатыми полимерами винилимидазолов с акриловой кислотой//Журн. приклад. химии. -1991. -Т. 64, вып. 1. -C. 194-196.
- Сорбция серебра (1) силикагелями, химически модифицированными меркаптопропильными и дипропилдисульфидными группами/В.Н. Лосев //Журн. неорг. химии. -2006. -Т. 51, № 4. -С. 565-568.
- Chakrapani G., Mahanta P.L., Murty D.S.R., Gomathy B. Preconcentration of traces of gold, silver and palladium on activated carbon and its determination in geological samples by flame AAS after wet ashing//Talanta. -2001. -Vol. 53. -P. 1139-1147.
- Салдадзе К.М., Копылова-Валова В.Д. Комплексообразующие иониты (комплекситы). -М.: Химия, 1980. -336 с.
- Цизин Г.И. Развитие методов концентрирования микрокомпонентов в России (1991-2010 гг.)//Журн. аналит. химии. -2011. -Т. 66, вып. 11. -С. 1135-1143.
- Сополимер дивинилсульфида и 4-винилпиридина -эффективный сорбент ртути/Н.С. Шаглаева //Журн. приклад. химии. -2005. -Т. 78, вып. 8. -С. 1296-1298.
- Трофимов Б.А., Амосова С.В. Дивинилсульфид и его производные. -Новосибирск: Наука, 1983. -264 с.
- Строение комплексов поли-1-винил-1,2,4-триазола и поли-1-винилимидазола с ионами меди (II)/А.И. Кокорин //Высокомолек. соедин. -1985. -Т. 27А, № 9. -С. 1834-1838.
- Slovokhotov Yu.L., Struchkov Yu.T., Polinsky A.S., Pshezhetsky V.S., Ermakova T.G. Dichloro-bis-(1-ethyl-1,2,4-triazole)copper(II)//Cryst. Struct. Commun. -1981. -№. 10. -P. 577-582.


