Состояние гемостаза при замещении дефектов костей свода черепа
Автор: Сбродова Л.И., Дьячков А.Н., Гордиевских Н.И.
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 3, 2005 года.
Бесплатный доступ
Работа выполнена на 15 взрослых беспородных собаках обоего пола в возрасте от года до трех лет, которым моделировали, а затем устраняли методом чрескостного дистракционно-компрессионного остеосинтеза патологию плоских костей свода черепа. Установлено, что после наложения аппарата на голову и резекции фрагмента костей черепа происходят изменения свертывающей активности крови. Установлено, что свертываемость крови повышается в связи с потреблением еѐ факторов на регенераторные процессы и восстанавливается только после снятия аппарата.
Череп, резекция, дефект, гемостаз, эксперимент
Короткий адрес: https://sciup.org/142120828
IDR: 142120828
The hemostasis status in filling the defects of skull vault bones
The work was made using 15 adult mongrel dogs of both sexes at the age of 1-3 years which were subjected to modeling and to subsequent elimination the pathology of skull vault flat bones by the method of distraction-and-compression osteosynthesis. The changes in blood coagulating activity were determined to occur after fixator application to the head and resection of the fragment of skull bones. It was established that blood coagulation increased in connection with intensive involvement of its factors in regenerative processes and it only recovered after the fixator removal.
Текст научной статьи Состояние гемостаза при замещении дефектов костей свода черепа
Применение чрескостного остеосинтеза для замещения дефектов костей свода черепа, к тому же стимулирующего мозговое кровообращение за счет образования экстра- и интракраниальных анастомозов, позволило добиться положительных результатов при лечении больных с последствиями травм головного мозга и нарушениями мозгового кровообращения.
Из литературных источников известно, что система гемостаза, как одна из наиболее лабильных систем организма, при черепномозговой травме резко изменяет свою актив- ность. В то же время крайне мало публикаций, посвященных изучению свертывающей системы крови при дистракционном остеосинтезе. Тем более, нет исследований, раскрывающих состояние гемостаза при замещении дефектов костей черепа методом дозированной дистракции.
В связи с этим нами проведено изучение свертывающей и фибринолитической систем крови при замещении дефектов костей свода черепа путем дозированного перемещения в нем полнослойного костного фрагмента на питающей ножке.
МАТЕРИАЛ И МЕТОДЫ
Работа выполнена на 15 взрослых беспородных собаках обоего пола в возрасте от года до трех лет, которым моделировали, а затем устраняли методом чрескостного дистракционнокомпрессионного остеосинтеза дефект костей свода черепа.
Методика операции. На голову собаки накладывали кольцо аппарата Илизарова, производили разрез мягких тканей головы по сагиттальной линии, слева отслаивали мышцы и резецировали участок костей свода черепа в среднем 2,6 15 см. От заднего края дефекта формировали полнослойный костный фрагмент длиной около 1,2 см и шириной 1,3 см, сохраняющий связи с окружающими мягкими тканями за счет мышечной ножки, и фиксировали его у заднего края дефекта двумя тракционно-направляющими спицами. Сохраняли твердую мозговую оболочку. Через 7 дней после операции на кольцо аппарата Илизарова устанавливали тракционный узел и начинали дозированное перемещение костного фрагмента с темпом 0,5-1 мм в сутки до смещения фрагмента к переднему краю дефекта.
Отмечено, что в первые дни после операции состояние животных было, как правило, средней тяжести. Вставать и активно передвигаться по клетке, собаки начинали через сутки. Через одну неделю поведение их практически не отличалось от поведения здоровых животных.
Исследования проводили до операции, перед началом дистракции, в ходе ее, в периоде фиксации и после снятия аппарата.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ОБСУЖДЕНИЕ
При анализе развернутых коагулограмм (таблица) до операции в группе обследованных животных не выявлено каких-либо отклонений в системе свертывания крови, однако её фибринолитическая активность была повышена до 27,2±0,8 %, что, возможно, объясняется сезонными изменениями и гиподинамией [16]. Исходная картина мазков периферической крови животных до оперативного вмешательства была «спокойной» (рис. 1).
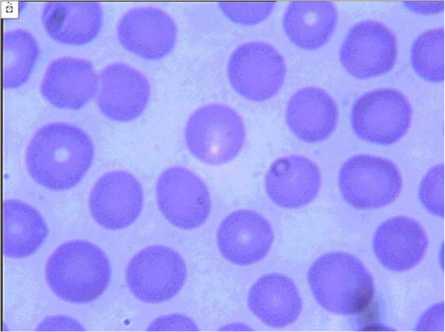
Рис. 1. Картина периферической крови животного до операции
В первые сутки после операции прослеживались изменения свертывающего потенциала крови во всех его фазах. Отмечалось некоторое удлинение времени свертывания крови; повышение её тромбопластиновой активности, на что указывало укорочение времени потребления протромбина с 26,7±0,8 с до 22,8±1,54 с (р<0,05) и повышение толерантности плазмы к гепарину на 23,4 % (р<0,05). Угнеталась антитромбиновая и гепариновая активность - тромбиновое время укорачивалось с 20,6±0,37 с до 16,1±1,36 с (р<0,05), свободного гепарина с 5,8±0,42 с до 3,8±0,8 с (р<0,01). Количество фибриногена увеличивалось в два раза. Вместе с тем, фибриназа, принимающая участие в процессе полимеризации фибриновой молекулы, понижалась на 31 % (р<0,05), определялись продукты деградации фибриногена/фибрина - этаноловая проба выражалась 4+, снижался фибринолиз на 6,2 %. Было совершенно очевидно, что активность кровяных пластинок, определяемая в раннем послеоперационном периоде, менялась, увеличивался их количественный состав на 17 %. Множество тромбоцитов находилось в конгломератах (агрегация) и прослеживалась адгезия, тромбоциты выбрасывали псевдоподии (рис. 2). Адгезия и агрегация тромбоцитов инициировали выход тромбопластических и антигепарино- вых субстанций. Отмеченный нами тромбоцитоз и увеличенная тромбоцитарная адгезивность согласовывались с гиперкоагуляцией, выявленной и по другим показателям коагулограммы.
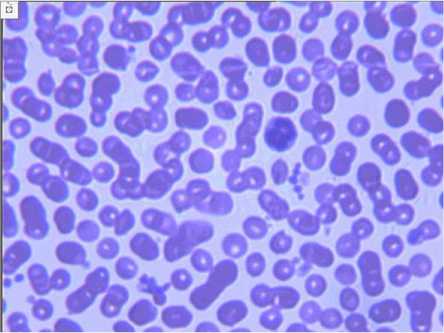
Рис. 2. Щадящая компенсаторная анемия, агрегат тромбоцитов, сегментоядерный лейкоцит. Первые сутки после операции
В последующие дни число кровяных пластинок и адгезивность нарастали (рис. 3, 4, 5). Показано, что помимо участия тромбоцитов в биохимических процессах, необходимых для коагуляции крови, они, благодаря свойству адгезивности, играют и механическую роль в образовании тромба [4, 5]. Результаты гистологического исследования показали, что через 7 дней после операции в дефекте и первоначальном диастазе между фрагментом и задним краем дефекта содержалась свернувшаяся кровь, в которую на глубину 0,5-1 мм проникали тяжи соединительной ткани и капилляры [3].
К началу дистракции - через 7 суток с момента операции - свертывание крови понижалось, отмечалась заметная адаптация к стрессорному воздействию (операции и наложению аппарата) со стороны системы гемостаза. Понижалась на 62 % тромбопластиновая активность: время потребления протромбина удлинялось и на 18,9 % понижалась резистентность плазмы к гепарину по отношению к исходному уровню. Стимулировался на 6 % фибринолиз. В этот период наблюдалась активизация сосудисто-тромбоцитарного гемостаза. По всей вероятности, под влиянием напряжения натяжения спиц в аппарате значительно изменялась электрическая активность самого сосуда. Выделяющийся при этом адреналин - один из неспецифических раздражителей -изменял потенциал сосуда в сторону увеличения отрицательного заряда интимы и вызывал изменения коагуляционных свойств [12, 15]. Возбуждение вегетативной нервной системы, симпати- ческого ее отдела, приводило к увеличению проницаемости эндотелия с одновременным выбросом в кровоток тканевых факторов, способных стимулировать свертывание крови и фибринолиз. Под действием возбуждений увеличивалась и определяемая нами концентрация тромбина -второго неспецифического раздражителя, который в результате биохимического взаимодействия повышал чувствительность хеморецепторов сосудистых стенок, вследствие чего включался рефлекторный акт, способный вызывать снижение антитромбиновой (на 14 %) и гепариновой активности (на 29,3 %) [4, 9]. Напротив, при малой концентрации тромбина наблюдалось бы повышение этой активности. На большую концентрацию тромбина указывало и увеличение количества фибриногена почти в 2 раза. Количество тромбоцитов при этом возрастало на 23 %.
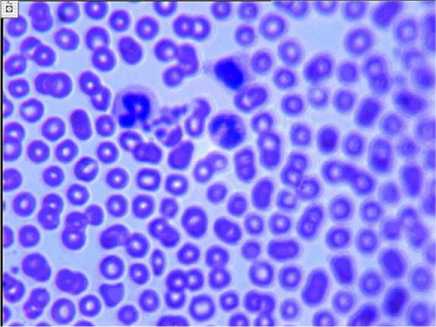
Рис. 3. Выраженная анемия, активированные тромбоциты, моноцит, нейтрофилы. 7 суток дистракции
Через одну неделю дистракции гиперкоагуляция сохранялась ускорение общей свертывающей активности крови составляло до 23,4 %. Увеличивались по отношению к предыдущему сроку наблюдения тромбопластиновая (на 34 %) и антитромбиновая (на 13 %) активность. Концентрация фибриногена была высокая, в пределах предыдущего срока наблюдения, вместе с этим, его фибриназа была снижена на 20 %. Фибринолиз уменьшался до 17 %. Уровень свободного гепарина восстанавливался.
Во вторую неделю дистракции антитромбо-пластиновая и антитромбиновая активность возрастали на 33 % и 29 %, соответственно; снижались количество фибриногена и его XIII фактор, этаноловая проба была менее выражена (3+). Содержание гепарина увеличивалось до 141 %. Время свертывания крови ускорялось на 29,4 %, а фибринолиз снижался на 10,5 %. Заметим, что при нормализации количества тромбоцитов в мазках крови прослеживались их агрегаты (рис. 4).
В третью неделю дистракции в I и II фазах свертывающей системы крови преобладала гиперкоагуляция. В мазках крови определялось скопление палочкоядерных нейтрофилов
(рис. 5), которые за счет своих субстанций принимают немаловажное участие в регенераторных процессах [11]. Из собственных наблюдений замечено, что при чрескостном остеосинтезе именно в данный период происходит активный выход из костного мозга, подчеркиваем, палочкоядерных нейтрофилов.
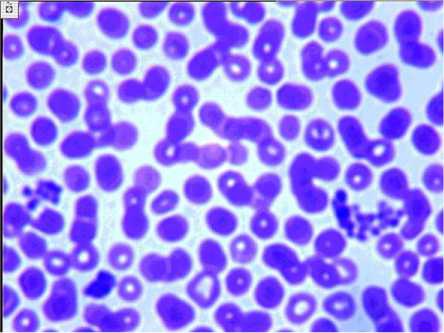
Рис. 4. Выраженная агрегация тромбоцитов, палочкоядерный нейтрофил. 14 суток дистракции
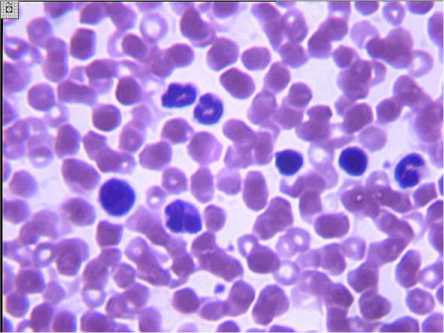
Рис. 5. В поле зрения скопление клеток белого ряда. 21 сутки дистракции
В четвертую неделю в большинстве коагулограмм время рекальцификации несколько удлинялось. Устойчивость плазмы к гепарину в этот период дистракции и вплоть до её окончания оставалась на уровне 90 %, что означало постепенное восстановление тромбопластической активности. Об этом свидетельствовал и ряд других показателей утилизация протромбина и уменьшение количества фибриногена до 138 %, которое вплоть до конца дистракции практически не менялось. Все вышеперечисленное является хорошим прогностическим признаком. Более того, количество тромбоцитов, фибриназа и фибринолиз крови восстанавливались. Оставались сниженными антитромбин и антигепарин.
На пятую неделю преобладала тенденция к гипокоагуляции: время свертывания крови и рекальцификации плазмы были удлинены на 9 % и 45 %, соответственно; растормаживание фибринолиза приводило к снижению фибриназы. Концентрация тромбина возвращалось к доопера- цонному периоду. Снижались продукты паракоагуляции (этаноловая проба 2+) и объем гепарина. Тромбопластиновая активность снижалась вплоть до конца периода дистракции. Количество тромбоцитов увеличивалось на 14 %. Увеличение кровяных пластинок мы связываем со снижением их адгезивно-агрегационных свойств и восстановлением при этом сосудистого русла. Мотивы повышения кровяных бляшек могли быть и другими. Во-первых, во избежание кровотечения и предотвращения срывов адаптации при активации фибринолиза крови и снижении ее фибриназы, возможно, организм выбрасывал в кровоток из своего резерва дополнительные свободные тромбоциты. Возможно, изменение потенциала сосудистой стенки приводило к ослаблению адгезивно-агрегационной активности тромбоцитов.
К концу периода дистракции (на 42-е сутки) свертываемость крови понижалась на 27 % от исходного значения. Другой, более чувствительный показатель, также отвечающий за общую свертывающую активность крови, время рекальцификации плазмы (74,3±2,3 с) возвращался к доопе-рационному уровню (79,5±4,07 с). Фибринолиз имел ту же тенденцию, что в целом приводило к выравниванию обеих систем. Концентрация фибриногена и фибриназы превышали норму на 46 % и на 19,3 %, соответственно. Одновременно с этим отмечено снижение количество тромбоцитов на 18,5 %, тромбина – на 5 %, а эндогенного гепарина – на 8,6 % от исходного уровня. Выраженная этаноловая проба указывала на латентную тенденцию к внутрисосудистому свертыванию.
Через месяц фиксации по многим показателям коагулограммы: антитромбиновой, антиге- париновой, фибриназной активности, этаноловой пробе, количеству тромбоцитов наблюдалась нормализация. Вместе с тем, время потребления протромбина удлинялось на 71 %, фибриноген повышался на 32 %. Параллельное снижение свертывающего и фибринолитического потенциала крови в целом предотвращало срыв в системе гемостаза. И только после снятия аппарата происходило восстановление свертывающей и фибринолитической активности крови.
Таким образом, установлено, что после наложения аппарата на голову и резекции фрагмента костей черепа происходят изменения со стороны свертывающей активности крови. Через одну неделю после операции активность её свертывания несколько понижалась и сопровождалась повышением фибринолитической активности, в результате включения адаптационных и приспособительных механизмов организма. Выявленная нами гиперкоагуляция в периоде дистракции являлась следствием рефлекторного повышения уровня прокоагулянтов (тромбина, фибриногена) и снижения уровня антикоагулянтов (гепарина). Установлено, что свертываемость крови оставалась повышенной в связи с потреблением факторов свертывания на регенераторные процессы и восстанавливалась только после снятия аппарата.
Полученные нами данные могут быть использованы для дифференцированной диагностики развивающихся изменений гемокоагуляции и коагуологического контроля за эффективностью производимой терапии.
Таблица 1
Изменения в свертывающей и фибринолитической активности крови при замещении дефектов костей свода черепа М±m
|
Показатели |
Исходные |
1-3 сут. п/о |
7 сут. п/о |
1 нд |
2 нд |
3 нд |
4 нд |
5 нд |
6 нд |
1мф |
1м б/а |
|
ВСК (с) |
439,4± |
474,3± |
373,9± |
387,43± |
309,7*± |
292,3*± |
475,8± |
478,3± |
558,75*± |
546,1*± |
504,4*± |
|
28,47 |
80,1 |
40,9 |
30,1 |
32,3 |
36,9 |
57,7 |
7,3 |
67,4 |
45,09 |
43,09 |
|
|
ВРП (с) |
79,5± |
63,3± |
61,36*± |
60,9*± |
66,7± |
54,8*± |
84,2± |
115,2*± |
74,3± |
120,3*± |
101,3*± |
|
4,07 |
5,9 |
5,9 |
4,7 |
3,3 |
3,83 |
11,2 |
5,2 |
2,3 |
2,6 |
3,5 |
|
|
ПП (с) |
26,67± |
22,75*± |
43,25**± |
28,6± |
35,3*± |
30,25± |
34,5± |
30,25± |
29,7± |
45,7*± |
27,3± |
|
0,84 |
1,54 |
6,1 |
0,75 |
5,29 |
6,0 |
5,6 |
4,2 |
2,7 |
2,3 |
1,45 |
|
|
ТГП (с) |
317,8± |
243,3*± |
377,8*± |
251,3*± |
265,3± |
226,6*± |
280,7± |
288,3± |
276,75± |
298,7± |
337,7± |
|
16,6 |
8,9 |
31,6 |
12,4 |
6,7 |
6,9 |
6,9 |
10,09 |
9,9 |
9,8 |
8,25 |
|
|
ФГ (г/л) |
2,132± |
4,172**± |
4,143**± |
4,29**± |
3,535*± |
3,363*± |
2,928*± |
2,84± |
3,107*± |
2,81*± |
2,22± |
|
0,237 |
0,30 |
0,292 |
0,391 |
0,153 |
0,272 |
0,178 |
0,227 |
0,182 |
0,391 |
0,247 |
|
|
ТВ (с) |
20,6± |
16,1**± |
17,8*± |
20,1± |
26,5± |
22,2± |
15,66**± |
18,8± |
19,6± |
21,3± |
22,3± |
|
0,37 |
1,36 |
0,8 |
1,24 |
3,47 |
2,85 |
0,76 |
1,29 |
0,3 |
0,88 |
1,2 |
|
|
СГ (с) |
5,8± |
3,8**± |
4,1*± |
6,0± |
8,2**± |
3,3**± |
4,08*± |
3,8**± |
5,3± |
5,67± |
5,7± |
|
0,42 |
0,8 |
0,39 |
0,58 |
1,43 |
0,38 |
0,37 |
0,37 |
0,33 |
0,33 |
0,88 |
|
|
XIII ф (с) |
46,3± |
31,9*± |
41,5± |
37,2± |
31,3*± |
40,7± |
45,2± |
37,7± |
55,25*± |
53,3*± |
47,3± |
|
4,24 |
3,47 |
3,18 |
5,05 |
1,20 |
2,3 |
5,07 |
5,3 |
4,38 |
6,84 |
8,19 |
|
|
ФА (%) |
27,2± |
20,8*± |
33,2*± |
16,6*± |
17,5*± |
20,3*± |
28,3± |
30,7± |
26,3± |
16,6*± |
21,1± |
|
0,8 |
4,7 |
4,6 |
2,72 |
2,18 |
2,02 |
2,4 |
2,1 |
2,4 |
3,5 |
1,53 |
|
|
PTL 109 |
332,7± |
388,3± |
408,8*± |
409,0*± |
332,9± |
380,8± |
306,2± |
379,1± |
271,25*± |
346,7± |
330,3± |
|
10,15 |
26,72 |
26,57 |
13,4 |
24,3 |
19,97 |
35,56 |
26,29 |
17,37 |
10,14 |
5,77 |
|
|
Этанол |
2,0 + |
4,0 + |
4,0 + |
4,0 + |
3,0 + |
4,0 + |
3,0 + |
2,0 + |
3,0 + |
4,0 + |
2,0 + |
Примечание: * p<0,05; ** p<0,001. Список сокращений: ВСК – время свертывания крови; ВРП – время рекальцификации плазмы; ПП – потребление протромбина; ТГП – толерантность гепаринизированной плазмы; ФГ – фибриноген; ТВ – тромбиновое время; СГ – свободный гепарин; ХIII ф – тринадцатый фактор, фибриназа; PTL – тромбоциты; Этанол – этаноловая проба; с – секунда.


