Совершенствование параметрической базы, необходимой для термодинамического моделирования огневого рафинирования меди
Автор: Михайлов Геннадий Георгиевич, Самойлова Ольга Владимировна, Трофимов Евгений Алексеевич, Макровец Лариса Александровна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Статья в выпуске: 34 (210), 2010 года.
Бесплатный доступ
Используя приближение теории субрегулярных ионных растворов, рассчитаны диаграммы состояния двойных силикатных систем Cu2O-SiO2 и NiO-SiO2. Посредством термодинамических расчётов описаны равновесия, реализующиеся в системе Cu-Si-O в условиях существования медного расплава. Уточнены и сведены воедино значения необходимых для расчета термодинамических параметров. Проведено сравнение результатов расчёта диаграмм состояния с литературными данными.
Термодинамическое моделирование, теория субрегулярных ионных растворов, диаграммы состояния
Короткий адрес: https://sciup.org/147156663
IDR: 147156663 | УДК: 669.33+541.123
Adjustment of thermodynamical parameter base for modeling copper melt fire refining
Phase diagrams of Cu2O-SiO2 and NiO-SiO2 binary silicate systems have been calculated, using the theory of subregular ionic solutions. Equilibria in the Cu-Si-O system in presence of copper melt have been described by means of thermodynamic calculations. Thermodynamic parameters necessary for the calculation have been improved and adjusted to each other. Results of phase diagram calculation were compared with literature data.
Текст научной статьи Совершенствование параметрической базы, необходимой для термодинамического моделирования огневого рафинирования меди
Термодинамическое моделирование процессов огневого рафинирования меди в настоящее время развито недостаточно. Это связано и с отсутствием необходимой для этого базы термодинамических данных, а также и с тем, что окончательное рафинирование меди проводится при электролизе. Управление процессом огневого рафинирования с целью получения анодов оптимального состава позволит повысить качество анодов, экономить электроэнергию. Помимо этого термодинамическое моделирование, несомненно, полезно при анализе получения сплавов с медью.
Настоящая работа направлена на получение термодинамических характеристик процессов рафинирования черновой меди от кремния и никеля и пополнения базы термодинамических данных для этих процессов.
Оксиды Cu2O, SiO2, NiO, FeO являются основными компонентами медерафинировочных шлаков. Создание термодинамической модели таких шлаков требует уточнения значений термодинамических параметров, характеризующих фазовые равновесия, реализующиеся в двойных оксидных системах: Cu2ONiO, Cu2O SiO2 и MiO-SiO2. Ранее [1], ис пользуя приближение теории субрегулярных ионных растворов, нами была проанализирована система Cu2O-NiO и рассчитаны координаты линий ликвидус диаграммы состояния этой системы. В настоящей работе ставится задача аналогичным образом проанализировать двойные силикатные системы Cu2O-SiO2 и NiO-SiO2, определить значения модельных параметров и рассчитать диаграммы состояния этих систем.
Приближение теории субрегулярных ионных растворов, используемое для описания термодинамических параметров расплавов Cu2O-SiO2 и NiO-SiO2, предполагает расчёт активностей компонентов двухкомпонентных оксидных расплавов по формулам [2]:
lg^ = v1lgxI+—^—(г1Гзх!2х|йп2 +
+ Х]Х2 (2 — Зх1)5п22 + Х2 (1 -ЗХ] )5122г]) i (1) lgo-2 = v2lgx2+ —™(v2R (1-Зх2)Й112 + + х{х2 (2-Зх2)й122 +3xfx2 61222 1) ■ (2)
Здесь У] и а2 - активности компонентов шлакового расплава; vt и v2 - стехиометрические коэффициенты (для Cu2O v = 2, для SiO2 или NiO v = 1); xt и х2 - ионные доли для оксидных пар (Cu2O-SiO2 и NiO-SiO2); Q - энергетические параметры теории, Дж/моль; R - универсальная газовая постоянная (R = 8,314 Дж/(моль-К)); Т - температура, К.
На первом этапе, используя координаты реперных точек (в качестве которых избраны точки эвтектических и монотектических равновесий), были подобраны значения энергетических параметров теории.
Для определения координат реперных точек для системы Cu2O-SiO2 использовались экспериментальные данные по диаграмме состояния этой системы, полученные в работе [3], согласно которым, в частности, координаты точки низкотемпературной эвтектики: Т = 1060 °C; 8 мае. % SiO2
(рис. 1). Для описания системы NiO-SiO2 были использованы данные по диаграмме состояния этой системы, обобщённые авторами справочника [4] (рис. 2).
Использованные в ходе работы справочные значения термодинамических параметров, характеризующих плавление компонентов исследуемых систем:
Си2О:
Т“ = 1242 °C; А„Я°0 = 64300 Дж/моль [6];
SiO2 - кристобалит:
Т” = 1728 °C; ДтЯ°о = 7698 Дж/моль [5];
SiO2 - тридимит:
Т” =1680 °C; ДтЯ°„ = 9002 Дж/моль [7];
NiO:
Т” = 1957 °C; АтЯ°0 = 50660 Дж/моль [7].
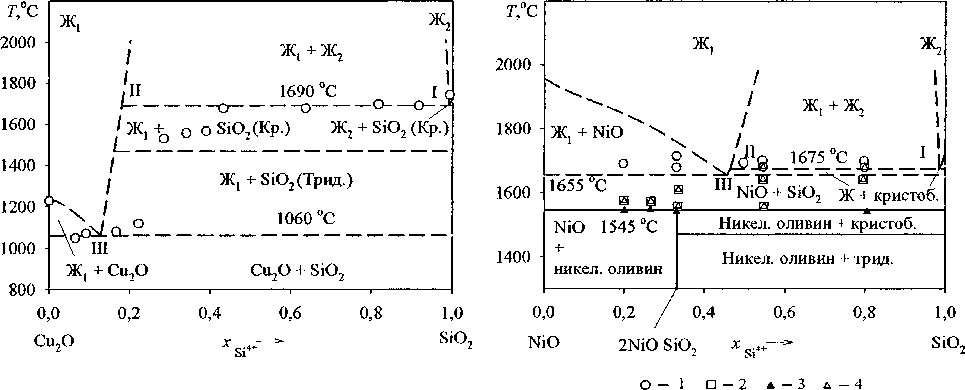
Рис. 2. Диаграмма состояния системы NiO-SiO2: сплошными линиями и точками указаны литературные данные [4]: 1 - жидкость, 2 - NiO, 3 -силикат никеля (никелевый оливин), 4 - SiO2. Штриховые линии - результаты расчета, римскими цифрами обозначены составы равновесных фаз, используемые при расчете
Рис. 1. Диаграмма состояния системы Cu2O-SiO2: точками указаны литературные данные [3]; штриховые линии - результаты расчета. Римскими цифрами обозначены составы равновесных фаз, используемые при расчете
Таблица 1 Константы равновесия реакций взаимодействия медного расплава и сопряжённых фаз (lg К = А / Т* В)
|
Уравнение реакции |
А |
В |
|
(Си2О) = 2 [Си]+ [О] |
-3141 |
2,251 |
|
(SiO2) = [Si] + 2 [О] |
-37 780 |
10,525 |
|
|Cu2O| = 2 [Си] + [О] |
-6500 |
4,468 |
|
[SiO2| = [Si] + 2 [О] |
-38 183 |
10,726 |
Таблица 2
Параметры взаимодействия первого порядка в медном расплаве е/
|
1 |
j |
|
|
О |
Si |
|
|
о |
-630/7 + 0,327 |
-4870/7 + 2,654 |
|
Si |
-8522,5/7 + 4,645 |
+ 159/7 |
Михайлов Г.Г., Самойлова О.В., Трофимов Е.А., Макровец Л. А.
Определённые и использованные в дальнейших расчётах значения модельных энергетических параметров для системы Cu2O-SiO2:
6п 12= -18309 Дж/моль;
61122 = 157963 Дж/моль;
61222= 70566 Дж/моль.
Для системы NiO-SiO2 значения аналогичных параметров:
61112= 31873 Дж/моль;
6н22= 23343 Дж/моль;
61222= 66149 Дж/моль.
Совокупность приведённых параметров позволила, используя уравнения (1) и (2), рассчитать координаты линий ликвидус исследованных систем для всех возможных составов и температур. Результаты расчетов приведены на рис. 1, 2.
Заметное отличие результатов расчёта диаграммы Cu2O-SiO2 от литературных эксперимен
Совершенствование параметрической базы, необходимой для термодинамического моделирования...
тальных данных [3], на наш взгляд, связано с тем, что авторы работы [3] проводили эксперименты в атмосфере воздуха и потому фактически полученные ими результаты относятся к тройной системе Cu2O-CuO~SiO2. Результаты расчёта диаграммы состояния системы NiO-SiO2 соответствуют литературным данным. Координаты точки Г. Т = 1675 °C; 98,52 мол. % SiO2, для точки II координаты: Т = 1675 °C; 46,36 мол. % SiO2 (рис. 2). Эвтектика (точка III) соответствует Т= 1655 °C и 45,57 мол. % SiO2.
Используя полученные в ходе работы результаты, главными из которых являются самосогласованные наборы модельных параметров, позволяющих описывать рассмотренные системы, можно моделировать более сложные, а значит приближенные к реальным шлакам оксидные системы.
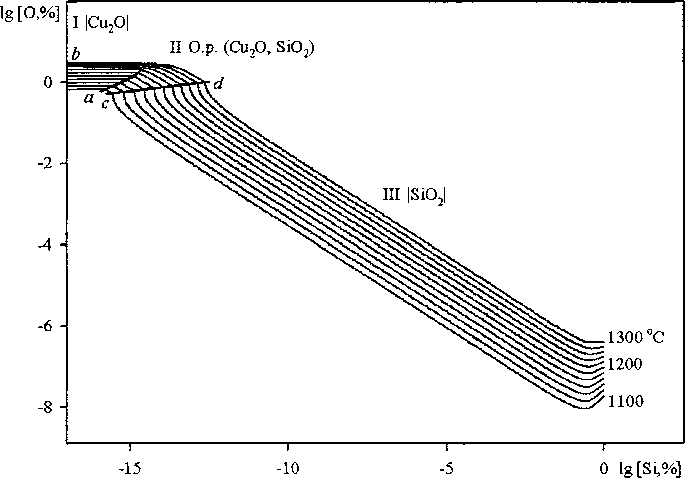
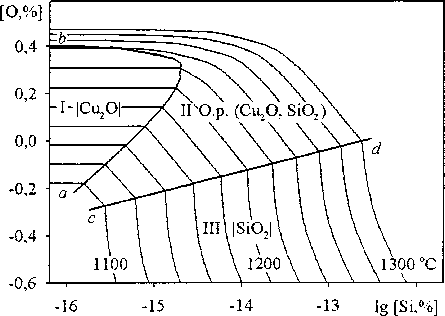
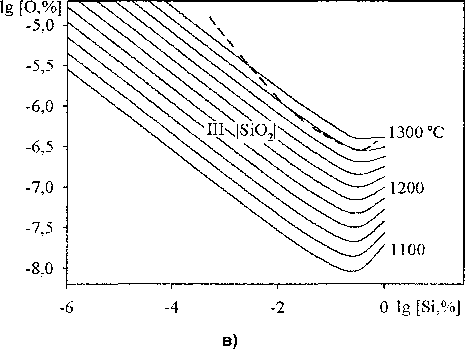
Рис. 3. ПРКМ системы Cu-Si-О для температурного интервала 1100-1300 °C: а - общий вид; б - увеличенный фрагмент верхней части ПРКМ; в - увеличенный фрагмент нижней части ПРКМ, штриховая линия - литературные данные [8] при 1250 °C
Помимо этого, опираясь на полученные данные, можно проанализировать равновесия, реализующиеся при высоких температурах в системах с участием медного расплава. Примером анализа такого рода систем является расчёт поверхности растворимости компонентов в металле (ПРКМ) [2] для системы Cu-Si-O.
Процесс взаимодействия оксидных и металлической фаз в системе Cu-Si-O может быть описан реакциями, константы взаимодействия для которых приведены в табл. 1. Параметры взаимодействия первого порядка по Вагнеру в медном расплаве приведены в табл. 2. Результаты расчета ПРКМ представлены на рис. 3.
Выводы
Используя приближение теории субрегулярных ионных растворов, рассчитаны линии ликвидус диаграмм состояния двойных оксидных систем Cu2O-SiO2 и NiO-SiO2. В ходе работы подобраны значения термодинамических параметров, характеризующих фазовые равновесия, реализующиеся в исследованных системах. Проведено сравнение расчетных диаграмм состояния с экспериментальными литературными данными. Полученные значения параметров использованы при построении ПРКМ системы Cu-Si-O для температурного интервала 1100-1300 °C.
Список литературы Совершенствование параметрической базы, необходимой для термодинамического моделирования огневого рафинирования меди
- Термодинамика процессов взаимодействия в системе Cu-Ni-O/Г.Г. Михайлов, О.В. Самойлова, Е.А. Трофимов и др.//Вестник ЮУрГУ. Серия «Металлургия». -2008, № 9 (109). -С. 31-33.
- Михайлов Г.Г. Термодинамика раскисления стали/Г.Г. Михайлов, Д.Я. Поволоцкий. -М.: Металлургия, 1993. -144 с.
- Бережной А.С. Системы Cu2O-SiO2 и CuO-SiO2/А. С. Бережной, Л.И. Карякин//Цветные металлы. -1955. -№ 2. -С. 26-33.
- Диаграммы состояния силикатных систем: справ. Вып. 1. Двойные системы/Н.А. Торопов, В.П. Барзаковский, В. В. Лапин, Н.Н. Курцева. -Л.: Наука, Ленинградское отделение, 1969. -822 с.
- Глушко В.П. Термические константы веществ. База данных/В.П. Глушко. -http://www.chem.msu.su/
- Химическая энциклопедия: в 5 т./под ред. И.Л. Кнунянца. -М: Сов. энцикл., -1990. -Т. 2. -671 с.
- Физико-химические свойства окислов: справ./под ред. Г.В. Самсонова. -2-е изд., пере-раб. и доп. -М.: Металлургия, 1978. -472 с.
- Линчевский Б.В. Термодинамика и кинетика взаимодействия газов с жидкими металлами/Б.В. Линчевский. -М.: Металлургия, 1986. -222 с.


