Совершенствование пластики пупочных грыж в условиях хирургии одного дня
Автор: Кривощеков Е.П., Хорошилов М.Ю., Молчанов М.А., Романов В.Е., Рахимов Б.М., Яковлев Р.Р.
Журнал: Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье @vestnik-reaviz
Рубрика: Клиническая медицина
Статья в выпуске: 2 т.13, 2023 года.
Бесплатный доступ
В статье рассмотрен усовершенствованный способ интраперитонеальной пластики пупочных грыж, приведена оценка результатов и эффективность его выполнения в условиях отделения стационара хирургии «одного дня». Классический способ ненатяжной герниопластики [1] дополнен хирургическими приёмами - «десквамацией» брюшины и «перитонеодезом» [2] грыжевого мешка. В ходе оперативного пособия применялось специальное запатентованное техническое устройство. Предложенный способ пластики пупочных грыж создаёт условия для снижения травматичности вмешательств, исключает возможность появления раневых осложнений, уменьшает время оперативного вмешательства и демонстрирует уникальные возможности использования в ходе операций естественных, физиологически обусловленных защитно-приспособительных систем организма для активизации восстановительных процессов [4, 5].
Интраперитонеальная ненатяжная пластика, пупочные грыжи, десквамация, перитонеодез
Короткий адрес: https://sciup.org/143180034
IDR: 143180034 | УДК: 617.555-007.43-089 | DOI: 10.20340/vmi-rvz.2023.2.CLIN.8
Improvement of umbilical hernia repair in one day surgery
The improved method of intraperitoneal plasty of umbilical hernia is considered in the article, the results and efficacy of its performance in the conditions of "one day" hospital department of surgery are estimated. The classical method of non-tension hernioplasty [1] is supplemented with surgical techniques - "peritoneal desquamation" and "peritoneodesis" [2] of the hernia sac. A special patented technical device was used in the course of surgical treatment. The suggested method of umbilical hernia plasty creates the conditions for traumatic interventions reduction, excludes the possibility of wound complications, reduces the operative intervention time and shows unique possibilities of using during the operations of natural, physiologically conditioned protective-adaptive systems of the body to activate restorative processes [4, 5].
Текст научной статьи Совершенствование пластики пупочных грыж в условиях хирургии одного дня
Эволюция методов оперативного лечения пациентов с пупочным грыжами в настоящее время достигла определённого постоянства– нет сомнений в использовании эндопротезов; разработаны чёткие последовательные алгоритмы выполнения различных видов оперативных вмешательств; произведено сравнение результатов лечения при различных способах операций [3, 6, 7]. Всё это позволило достигнуть определённого баланса между такими осложнениями, как клинически значимая серома, инфицирование раны, рецидив грыжи, внутрибрюшные осложнения и «классическим» выздоровлением пациента. Наиболее распространённым открытым вариантом лечения пупочных грыж является техника «sublay», подразумевающая под собой выделение, мобилизацию и иссечение грыжевого мешка из тканей передней брюшной стенки, мобилизацию задних листков влагалищ прямых мышц живота и размещение имплантата в ретромускулярном пространстве. Однако ряд авторов приводит данные, которые наглядно демонстрируют зависимость широкой мобилизации и скелетизации передней брюшной стенки с частотой развития раневых осложнений. Решение данной проблемы в настоящий момент существует в виде использования IPOM-пластики [8]. Однако, учитывая финансовую составляющую при сравнении эндопротезов для открытой гернио-пластики и эндопротезов для IPOM-пластики, стоимость последних на 2022 год значительно выше, что способствует поиску путей оптимизации применения полипропиленовых сетчатых эндопротезов.
Цель исследования: усовершенствовать способ оперативного лечения пупочных грыж путём интраперитонеальной пластики, десквамацией брюшины и перитонеоде-зом грыжевого мешка.
Материалы и методы исследования
В научное исследование включены результаты лечения 41 пациента с диагнозом «Пупочная грыжа», находившихся на стационарном лечении в хирургическом отделении ГБУЗ СО «Самарская городская больница № 7» в период 2020–2022 гг. Критерием включения в исследование являлось наличие у пациентов диагноза «приобретенная вправимая пупочная грыжа», критерием исключения было наличие осложнённых грыж.
Нами был разработан и использован усовершенствованный способ интраперитонеальной герниопластики пупочных грыж.
На разработанный способ получено положительное заключение экспертизы на изобретение в федеральном институте промышленной собственности (Заявка № 2022130311 от 23.11.2022).
Технический (лечебный) результат способа – снижение затрачиваемого времени и объёма оперативного вмешательства, обеспечение полной концепции ненатяжной гер-ниопластики, снижение риска рецидивов.
Отличительная особенность заявляемого способа от существующих заключается в том, что грыжевой мешок не иссекают, а обрабатывают путём десквамации внутренней поверхности. Грыжевой мешок вправляют в брюшную полость и равномерно его расправляют с сопоставлением внутренних поверхностей, интегрируют и фиксируют полипропиленовый имплант изнутри брюшной полости П-об-разными швами с точечной фиксацией на стороне полипропиленового импланта и формируют узел на стороне апоневроза прямых мышц. Укладывают и фиксируют прядь большого сальника между полипропиленовым имплантом и петлями кишечника.
На практике способ осуществляли следующим образом.
Выполняли полулунный разрез кожи кверху от пупка, образовавшийся кожный лоскут с пупком в центре отводили книзу. Выделяли верхний полюс грыжевого мешка, рассекали его стенку, вправляли содержимое в брюшную полость, освобождали грыжевые ворота от фиксированных петель кишки и прядей сальника (рис. 1).
Полость грыжевого мешка обрабатывали при помощи десквамации. Обработанный грыжевой мешок вправляли в брюшную полость и равномерно его расправляли с сопоставлением внутренних поверхностей.
В брюшную полость вводили полипропиленовый сетчатый имплантат и фиксировали изнутри брюшной полости по периметру грыжевых ворот сквозными П-образ-ными швами, проходящими через мышечно – апоневротический слой, брюшину, обработанный грыжевой мешок, с точечной фиксацией на стороне полипропиленового имплантата и фиксировали узел на стороне апоневроза прямых мышц (рис. 2).
Между поверхностью полипропиленового имплантата и петлями кишечника укладывали и фиксировали прядь большого сальника в качестве биологической защитной прокладки. По завершении пластического этапа над поверхностью фиксированного имплантата ушивали грыжевые ворота.
Для оценки эффективности разработанного способа нами были выделены две группы пациентов: первая группа (контрольная) – 20 пациентов, которым выполнялась классическая sublay-герниопластика; вторая группа (основная) – 21 пациент, которым выполнялось оперативное вмешательство в соответствие с разработанным нами способом.
Производили сравнение основных результатов лечения групп пациентов по следующим показателям: длительность госпитализации, показатель послеоперационной летальности, диагностика клинически значимой серомы, количество пункционно-дренирующих вмешательств под контролем УЗИ, количество повторных операций при нагноении раны, рецидив грыжи, внутрибрюшные осложнения, длительность операции.
Диагностику «клинически значимой» серомы выполняли при выявлении видимой выпуклости или флюктуации без признаков инфекции, требующих изменения тактики ведения послеоперационного периода [9].
Размеры грыжевого дефекта определяли путём выполнения предоперационного ультразвукового исследования и измерения расстояния между двумя наиболее удалёнными точками грыжевого дефекта.
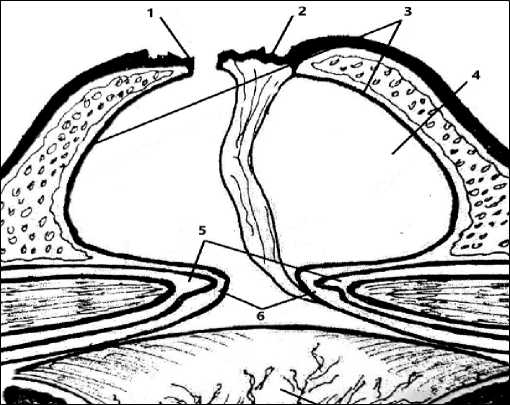
Рисунок 1. Взаимоотношение тканей передней брюшной стенки у пациентов с пупочной грыжей: 1 – кожный лоскут; 2 – пупок; 3 – стенки грыжевого мешка; 4 – полость грыжевого мешка; 5 – мышечно-апоневротический слой; 6 – грыжевые ворота
Figure 1. Relationship of the anterior abdominal wall tissues in patients with umbilical hernia: 1 – skin flap; 2 – navel; 3 – hernia sac walls; 4 – hernia sac cavity; 5 – muscular aponeurotic layer; 6 – hernia gate
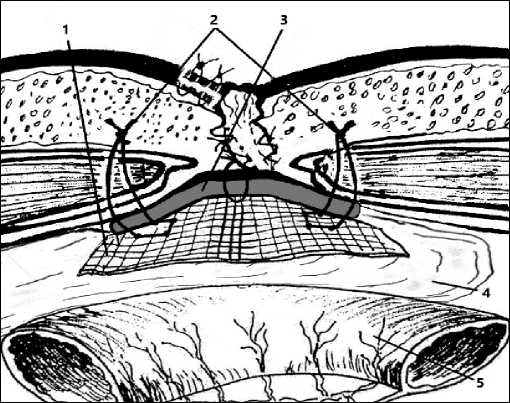
Рисунок 2. Результат применения разработанного способа: 1 – имплантат; 2 – П-образные швы с точечной фиксацией на стороне полипропиленового имплантата, проходящие через имплантат, грыжевой мешок и мышечно-апоневротический слой; 3 – обработанный грыжевой мешок; 4 – прядь большого сальника, 5 – петля кишки
Figure 2. the result of the designed method application: 1 – implant; 2 – U-shaped sutures with point fixation on the polypropylene implant side, passing through the implant, hernia sac and muscular-aponeurotic layer; 3 – treated hernia sac; 4 – strand of greater omentum; 5 – bowel loop
Всем пациентам выполняли стандартную антибиотико-профилактику раневых осложнений препаратами цефалоспоринов III поколения, профилактику тромбоэмболических осложнений (компрессионный трикотаж, применение профилактических доз антикоагулянтов).
В послеоперационном периоде применяли ношение пациентами абдоминального бандажа.
Тип исследования – одноцентровое параллельное проспективное нерандомизированное.
Нами было произведено сравнение групп пациентов по полу, возрасту, сопутствующим заболеваниям и среднему размеру грыжевого дефекта (табл. 1).
В контрольной группе было 13 мужчин (65 %) и 7 женщин (35 %), в основной группе – 12 мужчин (57,1 %) и 9 женщин (42,9 %) ( χ 2 = 0,266, p > 0,05).
Средний возраст в контрольной группе составил 34,18 ± 9,43 года, в основной группе – 35,23 ±11,17 года (t-критерий Стъюдента = 1,07, p > 0,05). Сопутствующие заболевания были выявлены у 5 (25 %) пациентов контрольной группы и у 7 (33,3 %) пациентов основной группы ( χ 2 = 0,344, p > 0,05).
Средний размер грыжевого дефекта в контрольной группе составил 4,1 ± 2,43 см, в основной группе – 3,7 ± 3,17 см (t-критерий Стъюдента = 1,11, p > 0,05).
Среди нозологий выявленных сопутствующих заболеваний в исследуемых группах статистически значимых различий не было (табл. 2).
Таким образом, статистически значимых различий между контрольной и основной группами по полу, возрасту, сопутствующим заболеваниям и среднему размеру грыжевого дефекта выявлено не было.
Это дало нам право в дальнейшем считать, что на результаты лечения мог повлиять только выбор способа оперативного вмешательства.
Результаты и их обсуждение
В результате проведённого нами исследования были получены следующие результаты (табл. 3).
В контрольной группе длительность госпитализации была статистически значимо дольше и составила 4,18 ± 3,43 суток, чем в основной группе – 2,18 ± 1,43 суток (t-критерий Стъюдента = 3,54, p < 0,05). Связано это было с тем, что отказ от выделения грыжевого мешка из тканей передней брюшной стенки предотвращал образование сецернирующей площади, что, в свою очередь, уменьшало риск возникновения раневых осложнений, способствовало лучшей переносимости болевого синдрома.
Средняя длительность операции в контрольной группе составила 77,45 ± 30,43 минуты, в основной группе – 50,33 ± 15,43 минуты. (t-критерий Стъюдента = 37,61, p < 0,05), что также было связано с отказом от длительного этапа выделения грыжевого мешка из тканей передней брюшной стенки.
В обеих группах летальных исходов зафиксировано не было.
Таблица 1. Сравнение групп пациентов по исходным данным Table 1. Comparison of patient groups according to initial data
|
Исследуемый признак |
Контрольная группа, n = 20 |
Основная группа, n = 21 |
Критерий |
|
Средний возраст |
34,18 ± 9,43 лет |
35,23 ± 11,17 |
t-Стъюдента = 1,07, p > 0,05 |
|
Мужской пол |
13 (65 %) |
12 (57,1 %) |
χ 2 = 0,266, p > 0,05 |
|
Женский пол |
7 (35 %) |
9 (42,9 %) |
|
|
Сопутствующие заболевания (ХСН, БА) |
5 (25 %) |
7 (33,3 %) |
χ 2 = 0,344, p > 0,05 |
|
Средний размер грыжевого дефекта |
4,1 ± 2,43 см |
3,7 ± 3,17 см |
t-Стъюдента = 1,11, p > 0,05 |
Таблица 2. Сопутствующие заболевания пациентов исследуемых групп
Table 2. Concomitant diseases of the patients of the study groups
|
Сопутствующие заболевание |
Пациенты контрольной группы с сопутствующими заболеваниями (n = 5) |
Пациенты основной группы с сопутствующими заболеваниями (n = 7) |
Критерий хи-квадрат |
|
Гипертоническая болезнь |
3 (60 %) |
2 (28,6 %) |
χ 2= 1,185, p > 0,05 |
|
Ожирение (II–III степени) |
1 (20 %) |
3 (42,8 %) |
χ 2 = 0,686, p > 0,05 |
|
Сахарный диабет 2 типа, инсулиннезависимый |
1 (20 %) |
2 (28,6 %) |
χ 2 = 0,144, p > 0,05 |
Таблица 3. Оценка основных показателей результатов лечения пациентов контрольной и основной групп.
Table 3. Evaluation of the main indices of the treatment results in the patients of the control and main groups
|
Результаты лечения пациентов |
Контрольная группа, n = 20 |
Основная группа, n = 21 |
Критерий |
|
Средняя длительность госпитализации |
4,18 ± 3,43 суток |
2,18 ± 1,43 суток |
t-Стъюдента = 3,54, p < 0,05 |
|
Средняя длительность операции |
77,45 ± 30,43 мин |
50,33 ± 15,43 мин |
t-Стъюдента = 37,61, p < 0,05 |
|
Осложнения послеоперационного периода (серома) |
5 (25 %) пациентов |
2 (9 %) пациента |
χ 2 = 1,733, p > 0,05 |
|
Пункционно-дренирующие вмешательства под контролем УЗИ |
3 (15 %) пациента |
1 (4,7 %) пациент |
χ 2 = 1,22, p > 0,05 |
В контрольной группе клинически значимая серома встречалась чаще – у 5 пациентов (25 %), чем в основной группе – у 2 пациентов (9,5 %), статистически значимых различий не было выявлено ( χ 2 = 1,733, p > 0,05). В связи с чем, можно предположить, что расположение полипропиленового имплантата между брюшиной, обработанным грыжевым мешком и прядью большого сальника имело клиническое значение: продуцируемая жидкость частично всасывалась брюшиной и её объём в ране снижал частоту клинических проявлений.
В обеих группах пациентам выполнялись пункционно-дренирующие вмешательства под контролем УЗИ: в контрольной группе – 3 (15 %) пациентам, в основной – 1 (4,7 %) пациенту ( χ 2 = 1,22, p > 0,05).
Повторных операций пациентам по поводу нагноения раны, внутрибрюшных осложнений, рецидива грыжи в обеих группах зарегистрировано не было.
Клинический пример
Пациент Г., 48 лет, поступил на плановое оперативное лечение по поводу приобретённой вправимой пупочной грыжи. При поступлении: в проекции пупка определяется опухолевидное образование размерами 7x7x4 см, мягкое, эластичное, вправимое, кожа в проекции образования не изменена. При пальпации - грыжевой дефект 2x2 см. Пациенту было выполнено грыжесечение, интраперитонеальная герниопластика полипропиленовым сетчатым имплантатом по разработанному нами способу. Длительность операции составила 52 минуты. В послеоперационном периоде оценивались: клиническая картина (болевой синдром, перистальтика кишечника, температура тела), результаты ультразвукового исследования области операционной раны на первые сутки после операции и перед выпиской, контроль раневого отделяемого.
В послеоперационном периоде: состояние пациент а оценивалось как удовлетворительное; болевой синдром был купирован к концу первых суток послеоперационного периода с помощью нестероидных противовоспалительных препаратов. Через 4 часа после выполнения оперативного вмешательства появилась активная перистальтика, отхождение газов, к концу первых суток после операции был однократный стул. Единожды, в первые сутки после операции, регистрирован эпизод субфебрилитета – температура тела составляла 37,1 °С. Эпизодов лихорадки не было. На первые сутки послеоперационного периода по данным УЗ-исследования области операционной раны была выявлена полоска жидкости шириной 2 мм в области грыжевого мешка, подвергнутого перитонеодезу, перед выпиской жидкостных образований в проекции операционной раны выявлено не было. Рана зажила первичным натяжением, отделяемого из раны за период госпитализации выявлено не было.
Длительность госпитализации составила трое суток (первые сутки госпитализации + двое суток послеоперационного периода). Был выписан с выздоровлением.
Заключение
Применение разработанного способа интраперитонеальной герниопластики неосложнённых пупочных грыж снижает длительность госпитализации (t-критерий Стъюдента = 3,54, p < 0,05), способствует снижению длительности оперативного вмешательства (t-критерий
Стъюдента = 37,61, p < 0,05). Перитонеодез и отказ от выделения грыжевого мешка из тканей передней брюшной стенки способствуют снижению риска возникновения раневых осложнений (клинически значимой серомы) с 25 % до 9 % и могут использоваться в качестве одного из вариантов стационарзамещающей операции у пациентов с неосложненными приобретёнными вправимыми пупочными грыжами.
Список литературы Совершенствование пластики пупочных грыж в условиях хирургии одного дня
- Белоконев В.И., Бабаев А.П., Ковалева З.В., Афанасенко В.П., Николаев А.В. Пути снижения осложнений при герниопластике комбинированным способом. XI конференция Актуальные вопросы герниологии. Москва, 2014:13-15.
- Григорьев С.Г., Григорьева Т.С., Дмитриева И.А. Десквамация и периотенодез грыжевого мешка при пластике послеоперационных грыжах. Вестник хирургии Казахстана: тез. III конгресса хирургов Казахстана с международным участием "Инновации в хирургии". 2012:248.
- Гуляев М.Г. Динамика результатов при лечении больных грыжами в зависимости от способа операции. Аспирантский вестник Поволжья. 2013;1-2:116-119.
- Кривощеков Е.П., Григорьева Т.С., Григорьев С.Г., Костин А.Ю. Защита кишечника от контактной травмы при внутрибрюшной пластике. Вестник хирургии Казахстана: тез. III конгресса хирургов Казахстана с международным участием "Инновации в хирургии". 2012:252.
- Кривощеков Е.П., Молчанов М.А., Вавилов А.В., Романов В.Е., Григорьева Т.С. Инновационный метод пластики пупочных грыж у пациентов с сахарным диабетом и морбидным ожирением. Здоровье и образование в 21 веке. 2019;21(2):33-37.
- Кривощеков Е.П., Молчанов М.А., Григорьева Т.С., Романов В.Е. Снижение рисков и осложнений при пластике пупочных и вентральных грыж. III Всероссийский съезд герниологов. Москва. 2018:72-74.
- Макаров И.В., Степанов П.Д., Степанов Д.Ю., Лопухов Е.С. Первый опыт применения подкожной эндоскопической пластики диастаза прямых мышц живота и пупочных грыж по методике SCOLA. Вестник медицинского института "РЕАВИЗ". Реабилитация, Врач и Здоровье. 2020;(3):119-124.
- Кривощеков Е.П., Григорьев С.Г., Молчанов М.А., Григорьева Т.С. Способ снижения интраоперационной травмы при внутрибрюшинной пластике пупочных и вентральных грыж. Фундаментальные исследования. 2015;5(1):980-983.
- Klink C.D. et al. Serum analyses for protein, albumin, and IL-1RA serve as reliable predictors for seroma formation after incisional Hernia repair. Hernia. 2011;15:69-73.


