Современная диагностика и хирургическая тактика при инсулиномах поджелудочной железы
Автор: Шевченко Ю.Л., Карпов О.Э., Стойко Ю.М., Левчук А.Л., Степанюк Илья Викторович, Седов А.Ю.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.11, 2016 года.
Бесплатный доступ
С 2004-2015 г. в НМХЦ им. Н.И. Пирогова проходили лечение 42 пациента с органическим гиперинсулинизмом, обусловленным опухолью поджелудочной железы. Дооперационное обследование состояло из синдромального этапа (клинические проявления) и топической диагностики (УЗИ, МСКТ, ЭндоУЗИ, ангиография, опухолевые маркеры). Солитарный характер инсулином выявлен у 36 (86%), мультифокальный и сочетанный с другими опухолями поджелудочной железы - у 6 (14%) пациентов. Все больные оперированы: у 29 пациентов выполнена - энуклеация инсулином, у 9 - дистальная резекция поджелудочной железы, у 1 - медиальная резекция поджелудочной железы, у 3 - панкреатодуоденальная резекция (ПДР). Объем оперативного вмешательства зависел от топической локализации, размеров опухоли, ее взаимоотношения с протоком ПЖ и сосудами, степенью злокачественности. У 14 пациентов (33%) развился послеоперационный панкреатит. Летальных исходов не было. Основными факторами прогноза результатов лечения больных с инсулиномами ПЖ являются: ранняя диагностика, щадящий миниинвазивный объем операции, прецизионная техника оперативного вмешательства, коррекция уровня глюкозы и профилактика послеоперационного панкреатита.
Инсулинома поджелудочной железы, диагностика, хирургическое лечение, профилактика осложнений
Короткий адрес: https://sciup.org/140188525
IDR: 140188525 | УДК: 616.37-006-089-073.756.8
Modern diagnostics and surgical tactics when the pancreas insulinoma
From 2004 - 2015, in NMHTS them. NI Pirogovwere treated 42 patients with organic hyperinsulinism caused by a tumor of the pancreas. Preoperative examination consisted of syndromic stage (clinical manifestations) and topical diagnosis (ultrasound, MSCT, EndoUZI, angiography, tumor markers). Solitary nature of insulin was detected in 36 (86%), multifocal, and combined with other pancreatic tumors in 6 (14%) patients. All patients were operated on: 29 - enucleation of insulin, 9 - distal resection of the pancreas, 1 - medial pancreatectomy, 3 - DA. The volume of surgery depend on the topical location, tumor size, its relationship with the duct of the pancreas and blood vessels, the degree of malignancy. In 14 patients (33%) developed postoperative pancreatitis. Deaths were not. The main predictors of treatment outcomes of patients with pancreatic insulinomas are: early diagnosis, sparing minimally invasive surgery volume, precision tactic surgery, correction of blood glucose and the prevention of postoperative pancreatitis.
Текст научной статьи Современная диагностика и хирургическая тактика при инсулиномах поджелудочной железы
Среди нейроэндокринных опухолей желудочно – кишечного тракта до 80% составляют новообразования поджелудочной железы [2, 5]. На долю инсулином приходится 75% гормонально – активных нейроэндокринных опухолей поджелудочной железы, которые являются причиной органического гиперинсулинзма и гипогликемической болезни [1, 6]. Инсулинома представляет собой опухоль В – клеток островков Лангерганса поджелудочной железы, секретирующая избыточное количество инсулина и проявляющаяся систематической гипогликемией. Несмотря на относительную редкость данной патологии осложнения после хирургического лечения инсулином поджелудочной железы составляют 15–40%, а летальность – 0,5–25% [1, 4].
Впервые опухоль из В – клеток поджелудочной железы островков Лангерганса была описана Niholls E. в 1902 году, но только в 1907 году Oberndorfer S. ввел термин «карциноид», описав инсулиному, как нейроэндокринное новообразование поджелудочной железы. Первая операция по удалению злокачественной инсулиномы была выполнена Mayo W.J. в 1927 году. Успешная операция (энуклеация) по удалению доброкачественной инсулиномы проведена Grahan E. в 1929 году. Гораздо позднее в 1944 году Уипплом A. были сформированы типичные клинико – лабораторные симптомы гиперин-сулинизма.
Материалы и методы
С 2004 по 2015 г. в НМХЦ им. Н.И. Пирогова проходили обследование и лечение 42 пациента с органическим гиперинсулинизмом, обусловленным опухолью поджелудочнолй железы. Из них мужчин было – 13 (31%), женщин – 29 (69%). Средний возраст больных составил 44 года.
Первичная диагностика осуществлялась в эндокринологическом отделении Центра на основании характерных клинических симптомов и триады Уиппла A.: возникновение приступов спонтанной гипогликемии натощак или через 2–3 часа после еды, падение уровня глюкозы крови до 0,3–2,3 ммоль\л во время приступа, быстрое купирование приступа гипогликемии внутривенным введением глюкозы. Средняя продолжительность заболевания с начала проявления первых симптомов до определения органического характера гиперинсулинизма составила 2 года. Постоянное чувство голода и необходимость частого приема пищи у 17 (40,5%) больных привели к развитию избыточной массы тела и ожирению II–III степени.
Всем пациентам синдромальный диагноз устанавливали на основании анализа клинических проявлений заболевания, исследования уровня глюкозы крови и результатов пробы с голоданием. Анализируя результаты первого (синдромального) этапа осуществляли второй этап топической диагностики опухоли. Для этой цели

Табл. 1. Алгоритм топической дооперационной диагностики инсулином поджелудочной железы
-
1. Неинвазивные методы исследования:
-
1.1 УЗИ (чувствительность 34,6%, специфичность 41,7%.)
-
1.2 МСКТ с болюсным усилением ( чувствительность 27,9%., специфичность 36,8%)
-
1.3 Сцинтиграфия с аналогами соматостатина (соматостатин, меченый индием – 111) (чувствительность-52%, специфичность-70%)
-
1.4 МРТ ( чувствительность-48,4%, специфичность -39,3%)
-
1.5 Эндоскопическое УЗИ ( чувствительность-85%, специфичность-39,3%)
-
-
2. Инвазивные методы исследования:
-
3. Комбинация неинвазивных и инвазивных методов диагностики (чувствительность – 97%, специфичность – 99%)
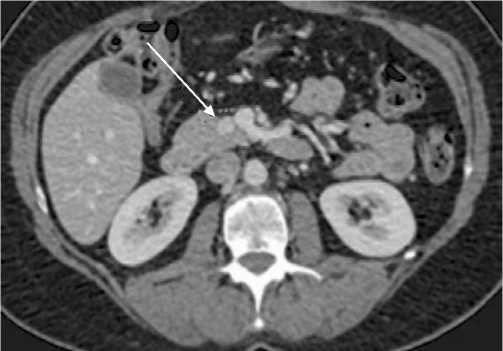
Рис. 1. Солитарный характер инсулиномы. Стрелкой указано расположение опухоли в области тела поджелудочной железы (размер опухоли 7 мм)
Ангиография с артериально-стимулированным забором крови для определения уровня гормонов (чувствительность -94%, специфичность – 69,3%)
использовали неинвазивные методы исследования: УЗИ, МСКТ органов брюшной полости с контрастированием, эндоскопическое УЗИ. Из инвазивных методик применяли у 13 пациентов ангиографию с артериально – стимулированным забором крови с последующим определением в ней уровня гормонов.
Наиболее чувствительными методами дооперацион-ной топической диагностики у наших больных оказалась комбинация ЭндоУЗИ и сочетанного ангиографического исследования, тогда как результаты МСКТ позволили поставить правильный диагноз лишь в 79% случаев (табл. 1). Наиболее часто инсулинома локализовалась в теле поджелудочной железы (головка – 12 (28,6%), тело – 21 (50,0%), хвост – 9 (21,4%)). Размер опухоли колебался от 0,5 до 2,3 см и в среднем составил 1,7 см. Инсулинома носила солитарный характер у 36 (86%) (рис. 1), мультифокальный – у 3 (7%) (с локализацией у 2 – в хвосте ПЖ, у 1 – в теле и хвосте ПЖ) (рис. 2) и сочетанный (с другими новообразованиями поджелудочной железы) – у 3 (7%) больных (у одного инсулинома и протоковая аденокарцинома локализовались в головке поджелудочной железы, у второго – муцинозная цистаденома тела сочетались с инсулиномой хвоста ПЖ (рис. 3), у третьего – инсулинома тела сопутствовала солидно – псевдопапиллярной опухоли хвоста ПЖ).
При сочетанном и мультифокальном характере патологии и характерной клинической картине гипе-ринсулинизма 6 больным (14,0%) проводили пункционную биопсию образований поджелудочной железы под контролем УЗИ с последующим гистологическим и иммуногистохимическим исследованиями. При неясности диагноза для исключения синдрома множественной эндокринной неоплазии (МЭН – 1) наряду с гормональными исследованиями у 8 пациентов (19%) использовали лучевые методы диагностики органов – «мишеней» (МРТ – гипофиза, УЗИ и сцинтиграфия паращитовидных желез, КТ – надпочечников).
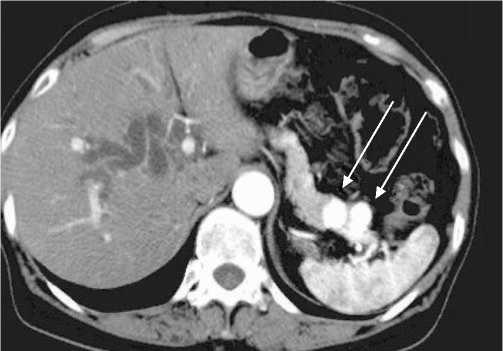
Рис. 2. Мультифокальный характер инсулином. Стрелками указано расположение опухолей в области хвоста поджелудочной железы
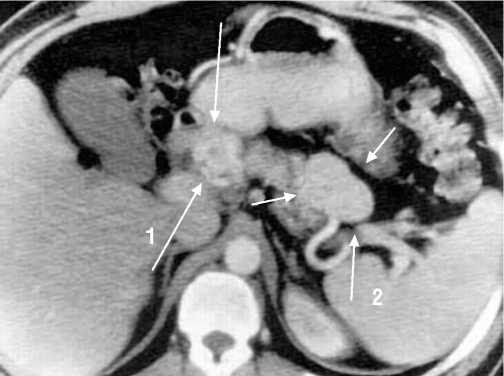
Рис. 3. Сочетанный характер локализации инсулиномы с другими новообразованиями поджелудочной железы. Стрелками указаны: муцинозная цистаденома тела (1) и инсулинома хвоста поджелудочной железы (2)
Все пациенты (n = 42) были оперированы, из них 20 больным (47,6%) в предоперационном периоде проводили биотерапию аналогами пролонгированного соматостатина («Октреотид – Депо»).
Характер выполненных оперативных вмешательств: энуклеация инсулиномы – 29 (69%) (из них лапароскопически – 6), дистальная резекция ПЖ – 9 (21,0%) (из них лапароскопически – 3), медиальная резекция поджелудочной ПЖ – 1 (2,9%), гастропанкреатодуоденальная резекция – 3 (7,1%) (из них лапароскопитчески – 1). В обязательном порядке интраоперационно проводилось УЗИ поджелудочной железы с уточнением локализации инсулиномы и ее взаимоотношения с сосудами и протоковой системы органа. При этом отмечена высокая диагностическая ценность данного исследования (чувствительность – 99,6%, специфичность – 100%), особенно при интрамуральном расположении опухоли. Срочное интраоперационное гистологическое исследование выполнено 39 пациентам только с целью подтверждения радикальности оперативного объема резекции или энуклеации. Результаты морфологического подтверждения инсулиномы у всех больных выполнялись иммуногистохимическим методом в плановом порядке. У 5 пациентов (11,9%) выявлено повышение специфического маркера – хромогранина «А», что подтверждало малигнизацию инсулиномы.
Результаты и обсуждение
У 14 больных (33%) развился послеоперационный панкреатит. Летальных исходов не было (табл. 3). В контрольной группе (n = 22) без проведения дооперационной биотерапии эти показатели были значительно хуже, чем в основной (n = 20) с применением в предоперационной подготовке «Октреотида – Депо» пролонгированного действия.
На основании литературных данных и собственного опыта нами выделены основные факторы, оказывающие наиболее значимое влияние на непосредственный исход хирургического лечения больных инсулинпродуцирую-щих опухолей ПЖ. Это позволило определить наиболее рациональный алгоритм дооперационного обследования больных, выбрать адекватный объем оперативного вмешательства в зависимости от размера опухоли, ее локализации, мультифокального и сочетанного характера, а так же разработать методику их ведения в ближайшем послеоперационном периоде, направленную на снижение частоты осложнений.
Операцией выбора при инсулиномах небольшого размера (от 0,5 до 2 см), расположенных на поверхности ПЖ у 29 пациентов (69%) явилась энуклеация опухоли. Эта операция характеризуется наименьшей травматичностью, что позволило у 6 пациентов (14,3%) выполнить ее лапароскопически. Дистальной резекции поджелудочной железы отдали предпочтение у 9 больных (21,4%) при расположении крупной инсулиномы (> 1,5 см) в глубине ткани тела и хвоста органа, а так же в непосредственной близости от панкреатического протока, селезеночных сосудов и при наличии множественных инсулином. При анатомической возможности троим больным этой группы корпоро – каудальная резекция ПЖ была выполнена лапароскопической методикой. Медиальная резекция ПЖ выполнена одному (2,9%) пациенту при крупной (2,5 см) инсулиноме перешейка ПЖ, с компрессией панкреатического протока и возможностью сохранения дистальных структур органа. При локализации новообразования в глубине ткани головки и крючковидном отростке ПЖ, подтверждении малигнизации инсулиномы – 3 больным (7,1%) выполнена гастропанкреатодуоденальная резекция (из них 1 (2,4%) лапароскопически).
Несмотря на примерно одинаковую частоту локализации инсулином во всех отделах ПЖ, осложненное течение послеоперационного периода наблюдали почти в 2 раза чаще при ее расположении в головке органа и крючковидном отростке (44,3%), чем в случаях с левосторонней локализацией опухоли (24,5%). Это объясняется большей травматизацией органа при его ревизии, независимо от размеров новообразования, а также необходимостью выполнения технически сложных органосохраняющих операций, даже в щадящем объеме – таких как энуклеация. Наиболее благоприятная картина отмечена у пациентов основной группы с левосторонним расположением опухоли. Выбор в пользу резекционных методик операций наиболее актуален при локализации образования в глубине ткани железы. При выполнении в такой ситуации органосберегающих оперативных вмешательств (энуклеация или эксцизия опухоли), частота осложнений значительно возрастала и составила 31%, против 10% при поверхностной локализации опухоли. При этом немаловажным фактором явилось расположение новообразования в непосредственной близости от желчного и панкреатического протоков, а так же магистральных сосудов, что было подтверждено при интра-опероационной ревизии ультразвукового исследования.
Интраоперационное УЗИ позволило не только наименее травматично выявить опухоль, но и определить ее топографоанатомические взаимоотношения с панкреатическим протоком и магистральными сосудами. Это способствовало тому, что в 31% наблюдений (n = 13) мы склонились в пользу резекционных методов лечения, а в 46% был определен наименее безопасный доступ для энуклеации опухоли.
В исследуемой группе пациентов (n = 20) в послеоперационном периоде удалось значительно уменьшить (почти в 3 раза) развитие послеоперационного панкреатита и количество гнойно – некротических осложнений, связанных с его развитием, путем тщательной коррекции уровня глюкозы крови инсулинотерапией, а так же использования «Октреотид – Депо» в дозе 0,01 г за 5–7 суток до операции. Однако экономические затраты на профилактику послеоперационного панкреатита после хирургического лечения инсулином не всегда оправдывают возлагаемые на нее надежды. Поэтому
вопрос клинико – экономической эффективности профилактики острого панкреатита до настоящего времени остается актуальным. В контрольной группе (n = 22) так же отмечены 3 случая (7%) гнойно – некротических осложнений (нагноение раны, деструкция ткани ПЖ), связанные с транзиторной гипергликемией, которая развилась на 2–5–е сутки послеоперационного периода. У этих пациентов нормализовать уровень глюкозы удалось дополнительным введением инсулина. Определенное влияние на возможность возникновения вышеперечисленных осложнений оказывают и технические аспекты резекционной прецизионной техники и возможность выполнения миниинвазивных оперативных вмешательств (эндо – и видеолапароскопические методики). Развитие миниинвазивной хирургии, щадящие органосохраняющие операции при удалении инсулином с использованием специального атравматического шовного материала (ПДС – 3,0), аргон – плазменной и биполярной коагуляции, гармоничного ультразвукового скальпеля, фибринового клея, эндоскопического стентирования панкреатического протока, – позволили так же в значительной мере уменьшить количество деструктивных панкреатитов, формирование свищей ПЖ, количество аррозивных кровотечений и постнекротических кист в послеоперационном периоде.
При патоморфологическом исследовании у всех 42 пациентов диагноз инсулиномы был подтвержден иммуногистохимически. У 15 % из них вывлены кистозные изменения, кальцификаты и внутриопухолевые кровоизлияния. Инсулиномы менее 2 см с низким пролиферативным индексом считались доброкачественными (n = 34), в то время как у 6 пациентов со степенью клеточной дифференцировки G2 и пролиферативным индексом Ki 67\MiB> 3 – 20% считали злокачественными, ровно как новообразования > 2 см с дифференцировкой G2, но индексом Ki 67\MiB 1> 20% характеризовались как нейроэндокринный рак. Таким образом, при инсулинпро-дуцирующих опухолях ПЖ операцией выбора является энуклеация. Это связано с тем, что инсулинома в большинстве наблюдений обладает наименьшим потенциалом злокачественности, а отдаленные функциональные результаты лучше при минимальной по объему операции.
Выводы
-
1. Операцией выбора в хирургическом лечении солитарных поверхностно расположенных инсулином (от 0,5 до 2 см) поджелудочной железы без вовлечения панкреатического протока и крупных сосудов является энуклеация новообразования. Резекционные методы (ПДР, дистальная и медиальная резекция ПЖ) используется при крупных солитарных ( > 2 см) и мультифокальных инсулиномах поджелудочной железы с вовлечением панкреатического протока и магистральных сосудов.
-
2. Расширенные и комбинированные оперативные вмешательства должны применяться только при малигнизации и сочетании инсулином с другими новообразованиями ПЖ, в том числе при наличии онкологического процесса.
-
3. Щадящий миниинвазивный объем оперативного вмешательства с применением в ряде случаев лапароскопических технологий с учетом тщательной коррекции уровня глюкозы крови, а также комплексная профилактика послеоперационного панкреатита с использованием пролонгированных форм антисекретор-ных препаратов (соматостатин, «Октреотид – Депо») определяют прогноз лечения больных органическим гиперинсулизмом и гипогликемической болезни.
Список литературы Современная диагностика и хирургическая тактика при инсулиномах поджелудочной железы
- Егоров А.В., Кузин Н.М. «Вопросы диагностики нейроэндокринных опухолей поджелудочной железы». Практическая онкология, 2005 -№4 -C. 206 -212.
- Калинин А.П. «Оперативное лечение инсулином поджелудочной железы».Ан. хирургической гепатологии, 2000 -№5 -C. 79 -84.
- Майстренко Н.А., Басос С.Ф., Юшкин А.С. и др. «Результаты хирургического лечения органического гиперинсулинизма.» Материалы конференции «Современные аспекты хирургической эндокринологии». Смоленск, 2002 -C. 239-240.
- Хижа В.В. «Особенности клинической картины, диагностики и лечения органического гиперинсулинизма»: Автореф.дис..канд. мед. наук. Санкт -Петербург, 2002 -16 с.
- Akerstrom G. «Surgical tretmentjf endocrine pancreatic tumor». Ann.Oncol. -2001. №1. -P. 62-66.
- Nayul M., David V. et al. «Pancreatic insulinoma: a surgical experience». World Journal of Surgery. 2009. -N 33 -P. 1966-1970.


