Современное состояние проблемы хирургической коррекции патологических извитостей внутренних сонных артерий
Автор: Батрашов В.А., Юдаев С.С., Землянов А.В.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Обзоры литературы
Статья в выпуске: 3 т.16, 2021 года.
Бесплатный доступ
Патологические извитости - удлинения сонных артерий с формированием перегибов (так называемых септальных стенозов), вплоть до полных петель на 360°. В развитии ишемических нарушений головного мозга патологические извитости сонных артерий занимают второе место после атеросклеротического поражения. В настоящее время остается много нерешенных задач в их лечении. До конца не изучены этиологические факторы, показания к операции, оценка эффективности и выбор тактики оперативных вмешательств. В настоящем обзоре представлены современные аспекты этиологии, классификация, показания и методы оперативных вмешательств. Продемонстрированы современные методы диагностики и оценки ишемии головного мозга, собраны данные о лабораторных маркерах ишемии, а также показаны методы интраоперационной защиты головного мозга при резекциях извитостей внутренних сонных артерий.
Патологическая извитость, кинкинг, койлинг, долихоартериопатия, интраоперационный нейромониторинг, маркеры ишемии головного мозга
Короткий адрес: https://sciup.org/140290437
IDR: 140290437 | DOI: 10.25881/20728255_2021_16_3_61
Surgical correction of pathological tortuosities of internal carotid arteries: current state of the problem
Pathological tortuosity-elongation of the carotid arteries with the formation of kinks (so-called septal stenoses), up to complete loops at 360°. In the development of ischemic brain disorders, pathological tortuosity of the carotid arteries takes the second place after atherosclerotic lesions. Currently, there are many unsolved problems in their treatment. The etiological factors, indications for surgery, evaluation of the effectiveness and choice of tactics of surgical interventions have not been fully studied. This review presents the current aspects of etiology, classification, indications and methods of surgical interventions. Modern methods of diagnosis and evaluation of cerebral ischemia are demonstrated, data on laboratory markers of ischemia are collected, and methods of intraoperative protection of the brain in resections of tortuosity of the internal carotid arteries are shown.
Текст обзорной статьи Современное состояние проблемы хирургической коррекции патологических извитостей внутренних сонных артерий
По экспертным оценкам ВОЗ в мире от цереброваскулярных заболеваний ежегодно умирает около 5 млн. человек [1]. По данным статистики на территории РФ ежегодно возникает около 400–450 тыс. инсультов, при этом лишь 8–10% инсультов являются малыми, которые заканчиваются восстановлением функций спустя 3 недели от развития симптомов [2]. Среди разнообразных причин ишемических нарушений мозгового кровообращения особое место занимают патологические извитости внечерепных отделов сонных артерий. Частота таких поражений среди населения неизвестна, однако по данным А.В. Покровского подобные аномалии (по данным ангиографического исследования) встречаются в 5% от общего числа обследуемых по причине острого нарушения мозгового кровообращения. В структуре причин развития сосудисто-мозговой недостаточности (СМН) патологическая извитость внутренней сонной артерии (ПИ ВСА) занимает второе место после атеросклеротического поражения. Часто такие пациенты имеют в анамнезе преходящий и/или стойкий неврологический дефицит, что подтверждает медико-социальную значимость этой патологии. [3]. Патологической извитостью сонных артерий называют состояния, характеризующиеся удлинениями общих и/или экстракраниальных порций внутренних сонных артерий с образованием изгибов, перегибов (так называемых септальных стенозов), вплоть до полных петель на 360°.
Этиология и симптоматика
Причины возникновения ПИ ВСА до сих пор неясны. Происхождение ПИ может иметь как врожденный, так и приобретенный характер. Признаками врожденного происхождения ПИ ВСА является: наличие извитостей сонных артерий в детском и молодом возрасте, часто двустороннее поражение, сочетанная извитость сонных артерий с формированием диссекции сонных артерий. Во многих исследованиях продемонстрирована связь извитостей сонных артерий с проявлениями системной дисплазии соединительной ткани — с синдромом Марфана, синдромом Элерса-Данло, коарктацией аорты, гипоплазиями сосудов, фибро-мускулярной дисплазией. Фибромышечная дисплазия (ФМД) может генетически опосредовать развитие извитости ВСА [4].
Причинами приобретенных ПИ считают: ослабление эластичного каркаса стенки артерии, атеросклероз ВСА, возрастные изменения шейного отдела позвоночника, сахарный диабет, ожирение и гипертоническую болезнь [24]. В исследовании P. Pancera et al. (2000) [5] было обследовано 590 пациентов с симптомами цереброваскулярной болезни, из которых 177 человек (30%) были гипертониками. В результате исследования выявлена статистическая значимость влияния артериальной гипертензии на развитие извитостей сонных артерий, а также дана патофизиологическая характеристика процесса. В процессе обследования было выявлено, что на сонную

артерию влияют дегенеративные изменения эластомеров и гладкомышечных клеток сосудов, возникающие вследствие дегенеративного атеросклероза и артериальной гипертензии, что способствует потере эластического каркаса сосуда [6].
Специфичных для ПИ ВСА симптомов почти не существует. С точки зрения диагностики среди клинических проявлений ПИ ВСА наиболее ценными являются симптомы сосудисто-мозговой недостаточности, к которым относятся общемозговые симптомы (головные боли, снижение памяти и интеллекта). В сосудистой хирургии с целью определения степени ишемического повреждения головного мозга принята классификация сосудисто-мозговой недостаточности по А.В. Покровскому [7]. В ней выделяют четыре степени:
I — асимптомное течение заболевания;
II — преходящие нарушения мозгового кровообращения (ТИА);
III — хроническое течение сосудисто-мозговой недостаточности (ДЭП);
IV —перенесенный инсульт в анамнезе (ОНМК).
Классификация
В настоящее время общепринятой во всем мире единой и обобщающей все формы классификации патологических извитостей сонных артерий не существует. Выявляемые деформации брахиоцефальных артерий отличаются большой вариабельностью и разнообразием. Данный факт диктует необходимость в их классификации.
Англо-американские исследователи используют термины: tоrtuоus (извилистая или извитая ВСА) обычно имеющие форму C- или S-образные, elоngatiоn (удлиненная ВСА), kinked, kinking (загиб, перегиб, изгиб ВСА), cоiling (петлеобразование, спиралевидная ВСА) (Рис. 1). Также существуют дополнительные термины, очень часто встречающиеся у итальянских и французских исследователей: lооps (петли ВСА), angulatiоn (углообразование ВСА); dоlichоarteriоpathes, dоlichоcarоtide (патологическое удлинение ВСА) [8]. По сути термин долихоартериопа-тия является общим термином и включает в себя три формы: tortuous (извитость), coiling (койлинг) и kinking (кинкинг) [9].
Аномалии геометрии ВСА обычно выявляются в ультразвуковых и ангиографических исследованиях, и их классификация как извитость, перегиб и петлеообразо-вание была впервые введена в 1965 г. Weibel и Fields [11]. Согласно этой классификации, извитость представляет собой S — или С-образное удлинение или волнообразное искривление по ходу ВСА. Койлинг был определен как удлинение или избыточность ВСА, приводящая к удлиненной петлеобразной кривой. Кинкинг, наиболее часто регистрируемый тип аномалий сонных артерий, был описан как острый угол ВСА и разделен на три степени (согласно классификации Metz), в зависимости от величины угла: первая — угол между двумя сегментами
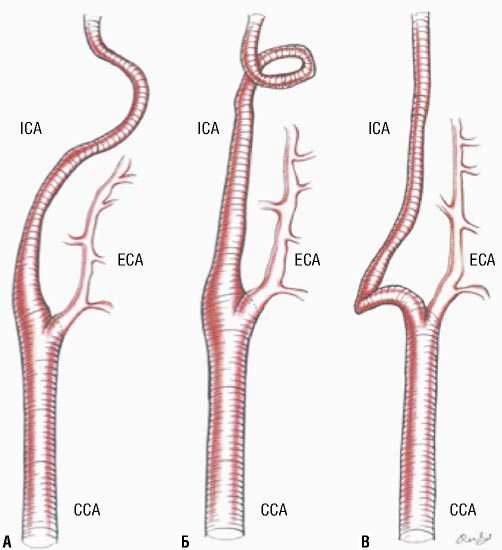
Рис. 1. Виды патологических извитостей. А — извитость; Б — койлинг (петля); В — кинкинг (перегиб) [10].
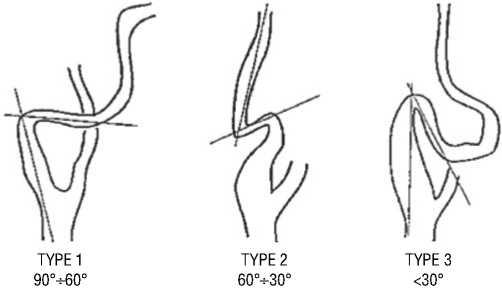
Рис. 2. Типы кинкинга ВСА по Metz [12].
равен 60–90°, вторая — 30–60°, третья — угол составляет менее 30. В своей классификации Метц также оценивает влияние патологической формы ВСА на нарушение мозгового кровообращения (Рис. 2) [12].
Методы диагностики
В настоящее время существует несколько методов визуализации, включая допплерографию, компьютерную томографию (КТА), магнитно-резонансную ангиографию (МРА) и цифровую субтракционную ангиографию (ЦСА), а также методы оценки церебральной перфузии с помощью однофотонной эмиссионной компьютерной томографии (ОФЭКТ) могут быть использованы в качестве диагностических инструментов для оценки долихоартериопатий [13].
Показания к оперативному вмешательству
Согласно Российским национальным рекомендациям по ведению пациентов с заболеваниями брахиоцефальных артерий от 2013 г., показаниями к оперативному лечению при ПИ ВСА являются: повышение ЛСК max в зоне деформации до 150 см/с и более и/или повышение ЛСК в зоне деформации более чем в 2 раза по сравнению с проксимальным (интактным) отделом ВСА. Также показания к хирургическому лечению пациентов с ПИ ВСА должны быть строго дифференцированы в зависимости от исходной степени сосудисто-мозговой недостаточности: — у пациентов со II и IV степенью показанием к операции является доказанное наличие ПИ; — у пациентов с III степенью — доказанное наличие и гемодинамическая значимость ПИ; — асимптомные больные могут быть прооперированы при доказанном наличии и гемодинамической значимости ПИ, только в качестве первого этапа хирургического лечения при необходимости выполнения иной операции (перед оперативными вмешательствами на других артериальных бассейнах или обширными операциями на других органах) [14].
Гавриленко А.В. с соавт. (2014) предлагают следующие показания: стеноз ВСА ≥60% с атеросклеротическими бляшками и любой степенью цереброваскулярной недостаточности; стеноз ВСА <60% с атеросклеротическими бляшками, умеренная или тяжелая степень цереброваскулярной недостаточности в сочетании с” S “- или “С” -образными долихоартериопатиями (ДАП), линейная скорость кровотока ≥110 см/с и турбулентный кровоток [15]. По данным других авторов, абсолютными показаниями к оперативному вмешательству у пациентов с ПИ ВСА являются койлинг и кинкинг с линейной скоростью кровотока более 180 см / с [16]. Таким образом, при оценке мировой литературы и данных Российских рекомендаций показания к оперативному лечению не являются однозначными и значительно варьируют по данным различных авторов.
Методы хирургического лечения ПИ ВСА
В различных исследованиях пациентов с ПИ ВСА авторы оценивали методы медикаментозного лечения извитостей, а также сравнивали их результаты с хирургической коррекцией. Гавриленко А.В. с соавт. (2012) провели сравнение хирургического и консервативного методов лечения патологического перегиба ВСА и установили, что хирургическое лечение патологического перегиба ВСА является эффективным методом профилактики прогрессирования цереброваскулярной недостаточности [17]. Enzo Ballotta et al. (2005) провели проспективное клиническое исследование, в котором случайным образом избирали симптомных пациентов с изолированным удлинением сонной артерии для проведения либо плановой операции, либо медикаментозного лечения. Было рандомизировано 92 пациента для хирургического вмешательства и 90 — для медикаментозного лечения. Всего было выполнено 129 каротидных хирургических коррекций у
92 пациентов. Частота поздних полушарных и ретинальных транзиторных ишемических атак была достоверно ниже в хирургической, чем в медикаментозной группе, соответственно 7,6% (7 из 92) в группе с хирургическим лечением против 21,1% (19 из 90) (р = 0,01) в группе медикаментозного лечения. Поздние инсульты, 2 (2,2%) из которых были фатальными, произошли только в группе с медикаментозным лечением (6 из 90, 6,6%; Р = 0,01). Поздние каротидные окклюзии развились только в медикаментозной группе (5 из 90, 5,5%; Р = 0,02). Авторы пришли к выводу, что хирургическая коррекция симптоматических изолированных удлинений сонных артерий с койлингом или кинкингом лучше подходит для профилактики инсульта, чем медикаментозное лечение [18].
Первой операцией, выполненной по поводу коррекции извитости ВСА, была операция описанная М. Riser et al. в 1951 году. Методика операции заключалась в подшивании избыточной части ВСА к грудино-ключичнососцевидной мышце [19].
В настоящее время существуют два основных метода оперативного вмешательства при извитостях ВСА. Когда стеноз извитого участка является продолжительным, в стенке извитой артерии отмечаются наличия аневризматических расширений, при этом выполнить редрессацию ВСА не представляется возможным, тогда хирургическая тактика направлена на ликвидацию этого извитого участка артерии. После пережатия, извитой участок ВСА иссекается, концы артерий сшиваются между собой «конец-в конец» полипропиленовой нитью 6/0 или 7/0.
При наличии стеноза устья ВСА с ее патологической извитостью устье артерии отсекают от ОСА вместе с участком извитости. При этом образуется довольно большое «окно» в ОСА. ВСА натягивают пинцетом, прикладывают к отдаленному участку «окна» в ОСА и определяют необходимую длину резекции ВСА. Последнюю пересекают поперечно и надсекают продольно по медиальной стенке на величину, равную длиннику «окна» в ОСА. Анастомоз накладывают непрерывным обвивным швом. Данную методику применяют при непродолжительном извитом участке и отсутствие аневризматических расширений [20].
Операцию каудальной реимплантации ВСА по типу «конец-в бок» в общую сонную артерию (ОСА) или в наружную сонную артерию (НСА) описал Е. Ballotta et al. в 2005 году. ВСА сначала рассекается в луковице с разрезом почти продольным до общей сонной артерии. Впоследствии, после выпрямления и расширения ВСА, в боковой стенке общей сонной артерии на уровне места реимплантации вырезают соответствующее по диаметру имплантируемой ВСА продольное окно, а затем ВСА ре-имплантируют в общую сонную артерию по типу конец-в бок (Рис. 3) [18].
G. Illuminati et al. в своей статье описали ситуации, когда НСА является хорошим выбором, особенно когда перегиб охватывает значительный сегмент ВСА. Пораженный артериальный сегмент резецируют, а дистальную
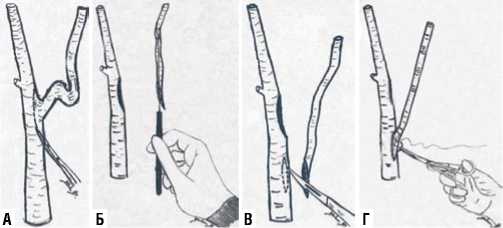
Рис. 3. Каудальная реимплантация ВСА в ОСА по типу «конец-в бок».
ВСА реконструируют путем транспозиции с боковым анастомозом на наружную сонную артерию [21].
На сегодняшний день выполняются следующие виды операций при патологической извитости ВСА: резекция ВСА с редрессацией и имплантацией в старое русло (Рис. 4–5), аутовенозное протезирование ВСА, резекция патологической деформации ВСА с анастомозом «конец в конец» [22].
Оперативные вмешательства по поводу извитостей ВСА имеют многочисленные риски и осложнения, включая сужение просвета, несостоятельность шва и послеоперационную окклюзию, вызванную диссекцией интимы и интрамуральной гематомой [23]. Нейропатии черепно-мозговых нервов (ЧМН) наблюдаются у 1,2 — 9% больных. Ишемический инсульт и смерть возникают не более чем у 2% оперированных пациентов, что соответствует мировым рекомендациям по хирургическому лечению больных с асимптомными стенозами [46]. Например, Гавриленко А.В. с соавт. (2014) сообщили об одном пациенте, у которого развился тромбоз зоны реконструкции с развитием острого нарушения мозгового кровообращения ишемического типа [17]. В послеоперационном периоде может возникнуть рестеноз. Так, в исследовании, проведенном G. Illuminati et al. в 2008 году у шести пациентов (3%) развился рестеноз ВСА после укорочения удлиненного участка ВСА и транспозиции ВСА в НСА [21].
Современные методы диагностики и оценки ишемии головного мозга при операциях по поводу ПИ ВСА
Выполнение операций на сонных артериях в условиях общей анестезии требует непрямых методов неврологического мониторинга: электроэнцефалография (ЭЭГ), транскраниальная допплерография (ТКДГ), соматосенсорные вызванные потенциалы (ССВП), а также измерение ретроградного давления (РД) в сонной артерии дистальнее места стеноза или извитости, исследование кислородного обеспечения головного мозга (ГМ) путем измерения насыщения гемоглобина кислородом и парциального насыщения в крови яремной вены на стороне оперативного вмешательства [24]. В настоящее время с целью контроля над адекватным кровоснабжением ГМ используют комбинацию методик — мультимодальный нейромониторинг [25]. Итак, одним из неинвазивных методов мониторинга внутримозгового кровообращения является ТКДГ, которая дает постоянную информацию о скорости кровотока в горизонтальном сегменте средней мозговой артерии (СМА) и других базальных артериях. Одним из ограничений данного метода является отсутствие акустических окон, когда невозможно проведение допплеровского мониторирования [26]. По данным литературы в среднем у 9–25% больных регистрируется отсутствие ультразвукового височного окна (R. Giali et. al., 1997). Учитывая этот фактор, Кунцевич Г.И. с соавт.
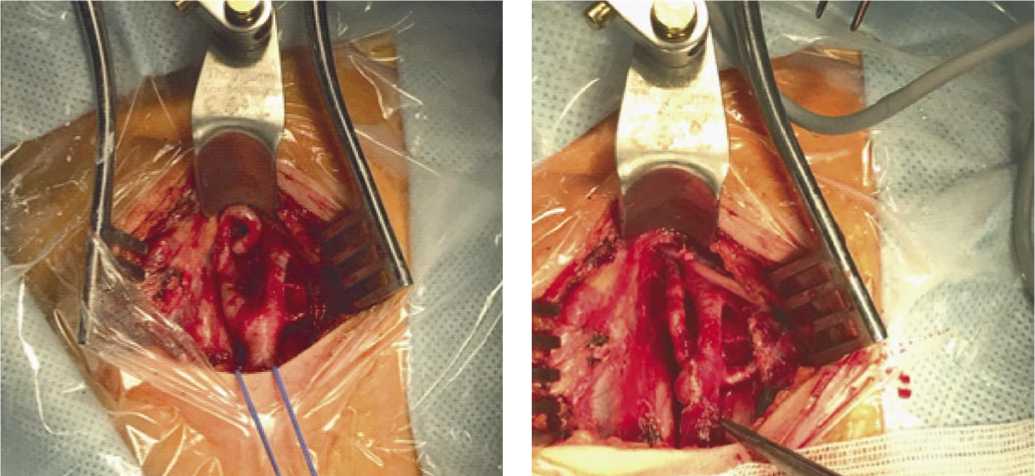
Рис. 4. Извитость ВСА по типу койлинга (петлеобразная извитость) до резекции.
Рис. 5. Вид ВСА после резекции извитости, редрессации и реимплантации ВСА в ОСА по типу «конец-в-бок».
[27] предложили использовать глазничную артерию для оценки мозгового кровотока в бассейне реконструируемой внутренней сонной артерии (ВСА). Другим недостатком метода ТКДГ является ослабление сигнала, характеризующееся резким снижением кровотока, вызванное смещением ультразвукового детектора [28]. Мониторинг соматосенсорных вызванных потенциалов (ССВП) непосредственно связан с кровотоком по СМА, образуясь от 100 250 повторных стимуляций. Увеличение латентности ответа отражает появление эпизода фокальной церебральной ишемии. Простота метода осложняется тем, что фармакологическая протекция во время операции затрудняет интерпретацию данных, вследствие оказываемого влияния на электрофизиологический мониторинг [29]. Наиболее распространенным методом оценки ишемии ГМ при операциях на сонных артериях является измерение РД в сонной артерии дистальнее места стеноза или извитости. Однако вопрос об оптимальном уровне РД и способах его увеличения не решен окончательно [30]. Большинство авторов при установлении показаний к установке ВШ на этапе пробного пережатия сонной артерии порогом значения РД используют его снижение ниже 40 мм рт. ст. [31]. Тем временем снижение РД во ВСА не считается достаточно информативным в связи с высокой частотой ложно-негативных и ложнопозитивных результатов. Более информативным представляется индекс ретроградного давления (ИРД), то есть отношение РД к системному артериальному давлению, выраженное в процентах [24] (Рис. 6).
ретроградное давление в ВСА
ИДР (%) = х 100% антеградное давление в ВСА
Рис. 6. Формула индекса ретроградного давления.
Таким образом, несмотря на большое количество научных исследований направленных на определение показаний к применению противоишемической защиты ГМ, проблема адекватной своевременной диагностики интраоперационной церебральной ишемии и её коррекции не решена окончательно, что требует проведения исследований в данном направлении.
Маркеры повреждения головного мозга в диагностике ишемии головного мозга
В качестве маркеров тканевого повреждения мозга в последние годы предлагается использовать ряд ней-роспецифических белков, входящих в состав нервной и глиальной ткани и появляющихся в крови в повышенных концентрациях при различных повреждениях мозга, такими белками являются протеин-S100 и нейронспецифи-ческая енолаза (NSE) [32]. Данные протеины, выделенные из мозга, были предложены в качестве биохимических маркеров неблагоприятного неврологического исхода у больных при черепно-мозговой травме, субарахноидальных кровоизлияниях, инсультах и иных неврологических расстройствах [33]. Протеин S100 является специфи- ческим белком астроцитарной глии, клетки которой являются наиболее многочисленными в мозговой ткани. Они образуют трехмерную сеть, которая является опорным каркасом для нейронов. Увеличение концентрации протеин-S100 в спинно-мозговой жидкости и плазме является маркером повреждения ГМ, что обусловлено активацией микроглии [34]. Было показано, что микро-глиальные клетки в периинфарктной зоне экспрессируют S100 и активно пролиферируют в течение не более трех дней после церебрального инфаркта. Концентрация S100 может иметь как диагностическое, так и прогностическое значение, являясь ранним маркером повреждения ГМ при различных патологических состояниях, а его концентрация дает возможность оценивать эффективность лечения [35].
Основным маркером повреждения нервной ткани является NSE, который является внутриклеточным ферментом нейронов ГМ и периферической нервной ткани. NSE является общим нейронспецифическим маркером всех дифференцированных нейронов [36]. Качественные и количественные определения этого белка в спинномозговой жидкости или сыворотке крови дают ценную информацию о степени выраженности повреждений нейронов и нарушениях общей целостности гематоэнцефалического барьера. Фермент NSE был идентифицирован и изучен в 70–80-х гг. прошлого века [37]. В 1992–1994 гг. A.J. Rabinowicz et al. доказали возможность использования NSE как лабораторного критерия в оценке степени поражения нейронов при ишемических и геморрагических инсультах. Авторами обнаружен эффект повышения концентрации NSE в сыворотке крови больных c инсультами и продемонстрирована корреляционная зависимость уровня этого антигена от тяжести патологического процесса [38]. Также выявлена взаимосвязь показателей NSE с прогнозированием течения и последствия перенесенного инсульта в отдаленном периоде [39]. Таким образом, изучение динамики маркеров повреждения ГМ при выполнении операций на сонных артериях открывает дополнительные возможности для исследования гипоксических процессов в ткани мозга в интраоперационном и в раннем послеоперационном периодах.
Методы интраоперационной защиты головного мозга от ишемии при выполнении резекции ПИ ВСА
По данным разных авторов при выполнении оперативных вмешательств на артериях каротидного бассейна риск ишемического поражения ГМ в результате церебральной гипоперфузии отмечен в пределах от 1,5 до 13% от числа оперированных больных [40]. В связи с этим, интраоперационная защита ГМ в период временной окклюзии ВСА остается на сегодняшний день важной задачей при хирургическом лечении патологии сонных артерий, от решения которой во многом зависит успех операции. Наиболее распространенным способом защиты ГМ в хирургии сонных артерий является временное шунтирование, заключающееся в сохранении крово-
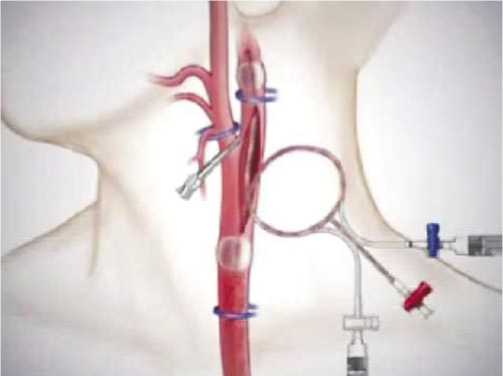
Рис. 7. Применение временного внутрипросветного шунта при операциях на сонных артериях.
тока и перфузионного давления в бассейне оперируемой артерии. Сущность метода заключается в том, что после пережатия сонных артерий и выполнения артериотомии в просвет ВСА и ОСА вводят временный шунт (ВШ), через который кровь поступает в сосуды ГМ. После резекции извитости, перед пуском кровотока по ВСА ВШ удаляется. Использовать ВШ необходимо у больных не толерантных к пережатию ВСА, а рутинное использование его несет риск развития осложнений и ограничивает экспозицию внутренней поверхности артерии [41]. В ряде исследований отмечено, что в применении ВШ нуждаются лишь 4,2% больных, если контралатеральная ВСА проходима и 20% больных, у которых она окклюзирована. Поэтому, если рутинно применять шунт, то более чем 80% операций окажется необоснованным и увеличит число осложнений [42].
Еще одним способом интраоперационной защиты ГМ является регулярное использование искусственной артериальной гипертензии, в котором используются стандартные сердечно-сосудистые препараты для поддержания уровня мозговой перфузии и уменьшения потребности в каротидном шунтировании для предотвращения инсульта [43].
Таким образом, в хирургическом лечении ПИ ВСА до сих пор остается много нерешенных вопросов и задач. Не определены точные показания к операции у пациентов с I ст СМН, нет общего мнения среди различных авторов по поводу гемодинамически значимой ЛСК, не существует единой классификации, которая бы включала в себя все варианты ПИ ВСА. До сих пор не разработаны методы комбинированной оценки эффективности и безопасности при операции резекции ПИ ВСА. Также, учитывая высокую частоту периоперационных инсультов, проблема адекватного обеспечения защиты ГМ от интраоперационной ишемии остается весьма актуальной и требует поиска альтернативных способов нейромониторинга во время операции. Показания к применению тех или иных методов защиты ГМ на сегодняшний день требуют уточнения. Все эти обстоятельства являются предметом дальнейших исследований.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Современное состояние проблемы хирургической коррекции патологических извитостей внутренних сонных артерий
- Суслина З.А., Варакин Ю.Я., Верещагин Н.В. Сосудистые заболевания головного мозга. — М.: МЕДпресс-информ, 2009. [Suslina ZA, Varakin JuJa, Vereshhagin NV. Sosudistye zabolevanija golovnogo mozga. Moscow: MEDpress-inform; 2009. (In Russ).]
- Суслина З.А., Пирадов М.А. Инсульт: диагностика, лечение, профилактика. — М.: МЕДпресс-информ, 2009. [Suslina ZA, Piradov MA. In-sul't: diagnostika, lechenie, profilaktika Moscow: MEDpress-inform; 2009. (In Russ).]
- Дадашов Сабухи Асаф оглы, Тактика хирургического лечения патологической извитости внутренней сонной артерии. Дис. ... канд. мед. наук. — Москва; 2012. [Dadashov Sabuhi Asaf ogly, Taktika hirurgichesk-ogo lechenija patologicheskoj izvitosti vnutrennej sonnoj arterii. [dissertation]; Moskva; 2012. (In Russ).]
- Пальцева Е.М., Осколкова С.А., Полякова В.О., Крылова Ю.А., Иванова А.Г., Абрамян А.В. Строение стенки внутренней сонной артерии при патологической извитости // Архив патологии. — 2015. — Т.77. — №3. — С. 3-8. [Pal'ceva EM, Oskolkova SA, Poljakova VO, Krylova JuA, Ivanova AG, Abramjan AV. Stroenie stenki vnutrennej sonnoj arterii pri patologicheskoj izvitosti. Arhiv patologii. 2015; 77(3): 3-8 (In Russ).]
- P. Pancera M. Ribul B. Presciuttini A. Lechi. Prevalence of carotid artery kinking in 590 consecutive subjects evaluated by Echocolordoppler. Is there a correlation with arterial hypertension? Journal of internal Medicine. 2000; 25(1): 7-12.
- Ghilardi G, Longhi F, De Monti F, Bortolani E. Kinking carotideo ed iperten-sione arteriosa. Risultati preliminari del programma OPI. Minerva Cardioa-ngiologica. 1993; 41: 287-291.
- Покровский А.В. Клиническая ангиология. Руководство для врачей.— М: Медицина, 2004. [Pokrovskij A.V. Klinicheskaja angiologija. Rukov-odstvo dlja vrachej. Moscow: Medicina; 2004. (In Russ).]
- Pancera P. Prevalence of carotid artery kinking in 590 consecutive subjects evaluated by Echocolordoppler. Is there a correlation with arterial hypertension? Journal of Internal Medicine. 2010; 248: 7-12.
- Amidzic А, Naida T. Kinking of Bilateral Internal Carotid Arteries as Cause of Cognitive Dysfunction. Medical Archives. 2020; 74(1): 58-60
- Jinlu Yu, Lai Qu, Baofeng Xu, Shouchun W, Chao Li, Xan Xu, Yi Yang. Current Understanding of Dolichoarteriopathies of the Internal Carotid Artery: A Review. International Journal Medical Sciences. 2017; 14(8): 772-784.
- Weibel J., Fields WS. Tortuosity, coiling, and kinking of the ICA. Etiology and radiographic anatomy. Neurology. 1965; 15: 7-11.
- Metz H, Murray-Leslie RM, Bannister RG, Bull JWD, Marshall J. Kinking of the ICA in relation to cerebrovascular disease. The lancet. 1961; 25: 424-26.
- Amidzic А, Naida T. Kinking of Bilateral Internal Carotid Arteries as Cause of Cognitive Dysfunction. Medical Archives. 2020; 74(1): 58-60.
- Национальные рекомендации по ведению пациентов с заболеваниями брахиоцефальных артерий // Российский согласительный документ. Москва, 2013. [Nacional'nye rekomendacii po vedeniju pacientov s zabol-evanijami brahiocefal'nyh arterij. Rossijskij soglasitel'nyj dokument. Moskva; 2013. (In Russ).]
- Гавриленко А.В., Куклин А.В., Хрипков А.С., Абрамян А.В. Оценка эффективности реконструктивных операций на сонных артериях в сочетании стеноза и патологической извитости // Ангиология и сосудистая хирургия. — 2014. — Т.20. — №3. — С. 116-122. [Gavrilenko AV, Kuklin AV, Khripkov AS, Abramian AV. Assessment of efficacy of reconstructive operations on carotid arteries in combination of stenosis and pathological tortuosity. Angiologia and sosudistaya hirurgiya. 2014; 20(3): 116-22. (In Russ).]
- Казаков Ю.И., Иванова О.В., Поспелова А.М., Вардак А. Особенности диагностики, хирургическая тактика, оценка эффективности реконструктивных операций при патологической извитости внутренних сонных артерий // Ангиология и сосудистая хирургия. —2015. — Т.21. — №4. — С.153-157. [Kazakov У, Ivanova OV, Pospelova AM, Vardak A. Diagnostic peculiarities, surgical policy, and efficacy of reconstructive operations in pathological tortuosity of internal carotid arteries. Angiologiya and sosudistaya hirurgiya. 2015; 21(4): 153-7. (In Russ).]
- Гавриленко А.В., Абрамян А.В., Куклин А.В. Сравнительный анализ результатов хирургического и консервативного лечения больных с патологической извитостью сонных артерий //Ангиология и сосудистая хирургия. — 2012. — Т.18. — №4. — С.93-99. [Gavrilenko AV, Abramian AV, Kuklin AV. Comparative analysis of the outcomes of surgical and conservative treatment of patients with pathological kinking of carotid arteries. Angiologia and sosudistaya hirurgiya. 2012; 18(4): 93-9. (In Russ).]
- Ballotta E, Thiene G, Baracchini C, Ermani M, Militello C, Da Giau G, Barbon B, Angelini A. Surgical vs medical treatment for isolated internal carotid artery elongation with coiling or kinking in symptomatic patients: A prospective randomized clinical study. Journal of Vascular Surgery. 2005; 42(5): 838-846.
- Riser M, Gerard J, Ribaut L. Dolichocarotide interne avec syndrome vertigineux. Revue Neurologique. 1951; 85: 145-151.
- Белов Ю.В. Руководство по сосудистой хирургии с атласом оперативной техники. — М.: Медицинское информационное агентство, 2011. — 464 с.: ил. [Belov JuV. Rukovodstvo po sosudistoj hirurgii s atlasom operativnoj tehniki. 2011: 464 р. (In Russ).]
- Illuminati G, Ricco JB, Calio FG, D'Urso A, Ceccanei G, Vietri F. The results in a consecutive series of 83 surgical corrections of symptomatic stenotic kinking of the internal carotid artery. Surgery. 2008; 143: 134-139.
- Выбор метода хирургического лечения патологической извитости внутренней сонной артерии в сочетании со стенозом // 109 Бюллетень НЦССХ им. А.Н.Бакулева РАМН «Сердечно-сосудистые заболевания». — Москва. — 2014. — Т.15. — №6. — С. 138. [Vybor metoda hirurg-icheskogo lechenija patologicheskoj izvitosti vnutrennej sonnoj arterii v sochetanii so stenozom. 109 Bjulleten' NCSSH im. A.N.Bakuleva RAMN «Serdechno-sosudistye zabolevanija». 2014; 15(6): 138. (In Russ).]
- Dirrenberger RA, Sundt TM.Temporal profile of the healing process and effects of anticoagulation therapy. Journal of Neurosurgery. 1978; 48: 201-219.
- Покровский А.В. «Классическая» каротидная эндартерэктомия // Ангиология и сосудистая хирургия. — 2001. — №2. С. 101-104. [Pokrovskij AV. «Klassicheskaja» karotidnaja jendarterjektomija. Angiologija i sosudist-aja hirurgija. 2001; 2: 101-104. (In Russ).]
- Арутюнян О.М., Яворовский А.Г., Гулешов В.А., Дутикова Е.Ф., Федуло-ва С.В., Бунятян А.А. Применение нейромониторинга на основе энтропии для определения гипоперфузии головного мозга при операциях на сонных артериях // Патология кровообращения и кардиохирургия. — 2011. — №3. С. 51-56. [Arutjunjan OM, Javorovskij AG, Guleshov VA, Dutikova EF, Fedulova SV, Bunjatjan AA. Primenenie nejromonitoringa na osnove jentropii dlja opredelenija gipoperfuzii golovnogo mozga pri oper-acijah na sonnyh arterijah. Patologija krovoobrashhenija i kardiohirurgija. 2011; 3: 51-56. (In Russ).]
- Pennekamp CW, Bots ML, Kappelle LJ, et al. The value of near-infared spectroscopy measured cerebral oximetry during carotid endarterectomy in perioperative stroke prevention. A review // Eur J Vasc Endovasc Surg. 2009; 38(5): 539-545.
- Кунцевич Г.И., Танашян М.М., Скрылев С.И., Кротенкова М.В и др. Ин-траоперационное мониторирование мозгового кровотока и состояние вещества головного мозга при открытых и эндоваскулярных вмешательствах в каротидной системе // Ангиология и сосудистая хирургия. — 2011. — Т.17. — №3. — С. 43-48.[ Kuncevich GI, Tanashjan MM, Skrylev SI, Krotenkova MV. Intraoperacionnoe monitorirovanie mozgovogo krovotoka i sostojanie veshhestva golovnogo mozga pri otkrytyh i jendov-askuljarnyh vmeshatel'stvah v karotidnoj sisteme. Angiologija i sosudistaja hirurgija. 2011; 17(3): 43-48. (In Russ).]
- Dalman JE, Beenakkers IC, Moll FL, Leusink JA. Transcranial Doppler monitoring during carotid endarterectomy helps to identify patients at risk of postoperative hyperperfusion. J. Vasc Endovasc Surg. 1999; 18: 222-227.
- Караваев Б.И., Гавриленко А.В., Золичева Н.Ю. Периоперационная диагностика церебральной ишемии при реконструктивных операциях на сонных артериях // Анестезиология и реаниматология. — 1999. — №5. — С. 71-74. [Karavaev BI, Gavrilenko AV, Zolicheva NJu. Perioperacionna-ja diagnostika cerebral'noj ishemii pri rekonstruktivnyh operacijah na sonn-yh arterijah. Anesteziologija i reanimatologija. 1999; 5: 71-74.(In Russ).]
- Покровский А.В. Можно ли избежать ишемического инсульта с помощью сосудистой операции? // Хирургия. Журнал им. Н.И.Пирогова. — 2003. — №3. — С.1-10. [Pokrovskij AV. Mozhno li izbezhat' ishemic-heskogo insul'ta s pomoshh'ju sosudistoj operacii? Hirurgija. Zhurnal im. N.I.Pirogova. 2003; 3: 1-10. (In Russ).]
- Calligaro K.D., Dougherty M.J. Сorrelation of carotid artery stump pressure and neurologic changes during 474 carotid endarterectomies performed in awake patients // J Vasc Surg. 2005; 42(4): 684-689.
- Молочный В.П., Макарова Т.Е., Головкова Н.Ф., Обухова Г.Г. Нейро-специфическая енолаза и глиофибрилярный кислый протеин крови и цереброспинальной жидкости как маркер повреждения ткани мозга при бактериальных гнойных менингитах у детей // Дальневосточный медицинский журнал. — 2012. — №2. — С. 48-51. [Molochnyj VP, Makarova TE, Golovkova NF, Obuhova GG. Nejrospecificheskaja enolaza i gliofibriljarnyj kislyj protein krovi i cerebrospinal'noj zhidkosti kak marker povrezhdenija tkani mozga pri bakterial'nyh gnojnyh meningitah u detej. Dal'nevostochnyj medicinskij zhurnal. 2012; 2: 48-51. (In Russ).]
- Flierl MA, Stahel PF, Touban BM, et al. Bench-to-bedside review: Burnind-uced cerebral inflammation — a neglected entity. Critical Care. 2009; 13: 215-223.
- Shaaban MА. Serum protein S100 as a marker of cerebral damage during cardiac surgery. Brit. J. of Anaesthesia. 2000; 85(2): 287-298.
- Rigamonti A, Scandroglio M, Minicucci F, Magrin S, et al. A clinical evaluation of near-infrared cerebral oximetry in the awake patient to monitor cerebral perfusion during carotid endarterectomy. J Clin Anesth. 2005; 17(6): 426-430.
- Крылова О.В., Воробьева В.А., Овсянникова О.Б., Соловьева Е.Н. и др. Нейроспецифическая енолаза в диагностике перинатальных поражений центральной нервной системы у недоношенных детей // Педиатрическая фармакология. — 2010. — №3. — С. 66-70. [Krylova OV, Vorob'eva VA, Ovsjannikova OB, Solov'eva EN. Nejrospecificheskaja enolaza v diagnostike perinatal'nyh porazhenij central'noj nervnoj sistemy u nedonoshennyh detej. Pediatricheskaja farmakologija. 2010; 3: 66-70. (In Russ).]
- Бурбаева Г.Ш. Физиологически активные белки мозга как возможные маркеры психических заболеваний // Вестник РАМН. — 1992. — №7. — С. 51-54. [Burbaeva GSh. Fiziologicheski aktivnye belki mozga kak voz-mozhnye markery psihicheskih zabolevanij. Vestnik RAMN. 1992; 7: 51-54. (In Russ).]
- Rabinowicz A.J., Correale J., Boutros R.B. et al. Neuronspecific enolase is increased after single seizures during inpatient video/EEG monitoring. Epilepsia. 1996; 37: 122-125.
- Карякина Г.М., Надеждина М.В., Хинко М.А. Нейроспецифическая енолаза как индикатор поражения мозговой ткани при ишемических инсультах // Неврологический вестник. — 2007. — Т.39. — №1. — С. 41-44. [Karjakina GM, Nadezhdina MV, Hinko MA. Nejrospecificheskaja enolaza kak indikator porazhenija mozgovoj tkani pri ishemicheskih insul'tah. Nevrologicheskij vestnik. 2007; 39(1): 41-44. (In Russ).]
- Cunningham, EJ, Bond, Mehta RZ. The European Carotid Surgery Trialists' Collaborative Group. Long-term durability of carotid endarterectomy for symptomatic stenosis and risk factors for late postoperative stroke. Stroke. 2002; 33: 2658-2663.
- Чернявский А.М., Ломиворотов В.Н., Столяров М.С., Дерягин М.Н., Струнин О.В. Кислородное обеспечение головного мозга в условиях на этапах операции каротидной эндартерэктомии // Патология кровообращения и кардиохирургия. — 2003. — №2. — С. 38-41. [Chernjavskij AM, Lomivorotov VN, Stoljarov MS, Derjagin MN, Strunin OV. Kislorodnoe obespechenie golovnogo mozga v uslovijah na jetapah operacii karotidnoj jendarterjektomii. Patologija krovoobrashhenija i kardiohirurgija. 2003; 2: 38-41. (In Russ).]
- Гавриленко А.В., Куклин А.В., Скрылев С.И., Агафонов И.Н. Показания для использования внутрипросветного временного шунта при операциях на сонных артериях // Ангиология и сосудистая хирургия. — 2007. — Т.13. — №4. — С.105-112. [Gavrilenko AV, Kuklin AV, Skrylev SI, Agafonov IN. Pokazanija dlja ispol'zovanija vnutriprosvetnogo vreme-nnogo shunta pri operacijah na sonnyh arterijah. Angiologija i sosudistaja hirurgija. 2007; 13(4): 105-112. (In Russ).]
- Antunes M, Biala G. The novel object recognition memory: neurobiolo-gy, test procedure, and its modifications. Cogn. Process. 2012; 13(2): 93-110.


