Современные лапароскопические и роботические технологии в лечении эхинококкоза печени
Автор: Шабунин А.В., Бедин В.В., Тавобилов М.М., Лебедев С.С., Карпов А.А., Ланцынова А.В.
Журнал: Московский хирургический журнал @mossj
Рубрика: Абдоминальная хирургия
Статья в выпуске: 1 (75), 2021 года.
Бесплатный доступ
Введение. Неуклонное развитие мини-инвазивных технологий, повышение хирургических навыков позволяет использовать современные лапароскопические и роботические способы лечения у больных кистозным эхинококкозом печени.Материалы и методы. В статье проведен анализ результатов лечения больных эхинококкозом печени, находившихся на лечении в хирургической клинике Боткинской больницы с 2015 по 2020 годы. Основой для проведения исследования послужило начало применения современных видеоэндоскопических и роботических технологий в лечении пациентов с паразитарным поражением печени. Первая группа больных включила 47 пациентов, перенесших перицистэктомию лапаротомным способом. Во вторую группу вошли 8 больных, которым выполнены лапароскопические и роботические перицистэктомии. Оценены непосредственные и отдаленные результаты хирургических вмешательств.Результаты. При сравнении непосредственных и отдаленных результатов не выявлено различий по длительности операции, частоте переливания компонентов крови, частоте тяжелых послеоперационных осложнений (III и более класса по Clavien-Dindo), наличию специфических осложнений по классификации ISGLS. Минимально инвазивные операции сопровождались статистически значимо меньшей кровопотерей по сравнению с открытыми: 54 (0-270) мл и 157 (70-560) мл (р function show_abstract() { $('#abstract1').hide(); $('#abstract2').show(); $('#abstract_expand').hide(); }
Эхинококкоз печени, лапароскопическая перицистэктомия, роботическая перицистэктомия
Короткий адрес: https://sciup.org/142230013
IDR: 142230013 | УДК: 621.386.85: | DOI: 10.17238/issn2072-3180.2021.1.34-38
Laparoscopic and robotic surgery: pathways to improving liver echinococcosis perioperative results (original article)
Background. The steady development of modern minimally invasive technologies makes it possible to use laparoscopic and robotic methods of treatment for liver echinococcosis.Material and methods: Since 2018, in the surgical clinic of the Botkin Hospital, laparoscopic and robotic interventions in the volume of pericystectomy and liver resection have been used for liver echinococcosis. During the period from February 2018 to November 2020, 8 minimally invasive interventions were performed: 5 laparoscopic and 3 robotic. The study assessed postoperative complications according to the Clavien-Dindo classification, specific complications according to ISGLS, and relapses during the first year after surgery.Results. Comparing immediate and long-term results, no differences were found in the duration of the operation, the frequency of transfusion of blood components, the incidence of severe postoperative complications (class III and more according to Clavien-Dindo), the presence of specific complications according to the ISGLS classification. Minimally invasive operations were accompanied by statistically significantly less blood loss compared to open ones: 54 (0-270) ml and 157 (70-560) ml (p function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Современные лапароскопические и роботические технологии в лечении эхинококкоза печени
На протяжении всей истории хирургических вмешательств на печени при её эхинококковом поражении «золотым» стандартом операции служила лапаротомия в различных модификациях. Однако в последние годы развитие малоинвазивных технологий обусловило рост количества видеоэндоскопиче-ских операций, и начало этому процессу было положено в 1991 году, когда во Франции Katkhouda была выполнена первая лапароскопическая перицистэктомия у больного с кистозным эхинококкозом печени [1]. В 2014 году был опубликован обзор, являющийся на сегодняшний день наиболее полным и самым большим по количеству случаев (более 900 пациентов), продемонстрировавший позитивные результаты — в виде уменьшения раневых осложнений, болевого синдрома после операции и сопоставимые с открытыми вмешательствами отдаленные результаты [2].
Начиная с первых публикаций об использовании робототехники при резекционных вмешательствах на печени у авторов возникали попытки применения этой малоинвазивной современной технологии для лечения пациентов с эхинококкозом печени. Первая публикация Giulianotti et al, опубликованная в 2011 году, сообщала о двух пациентах, которым были выполнены роботические вмешательства [3]. С тех пор опубликованы ряд статей, описывающих применение робототехники у больных эхинококкозом печени, однако большинство из них представляют собой лишь клинические случаи и не доказывают явного преимущества роботической хирургии над традиционными и лапароскопическими хирургическими вмешательствами [4, 5, 6]. Так, в 2011 году Casciola опубликовал случай роботической атипичной резекции I–VIII сегментов, включая перицистэктомию из IV a и VII сегментов (по одному случаю). Данное исследование продемонстрировало преимущества роботичесокй хирургии при операциях на задних сегментах печени, особенно при близком контакте с печеночными венами [7].
В 2013 году Troisi сравнил лапароскопические и роботические резекции печени у больных эхинококкозом печени и пришел к выводу, что роботическая технология дает преимущество в лучшей визуализации, сохранении объема паренхимы печени, в особенности при резекциях задних сегментов печени [8].
В 2016 году Di Benedetto et al. опубликовали клинический случай роботической резекции S1 печени с хорошими интра- и послеоперационными показателями [9].
Одной из последних работ явился обзор итальянских авторов под руководством Magidtri, объединивший опыт 15 роботических вмешательств при эхинококкозе печени. Выводом работы так же стала демонстрация возможностей роботического комплекса при резекциях печени сложных сегментов [10]. Однако на сегодняшний день нет исследований, с достаточной степенью достоверности позволяющих сделать вывод о бесспорном преимуществе мини-инвазивных техник при хирургическом лечении кистозного эхинококкоза печени, что и привело нас к необходимости проведения анализа полученных данных после первого опыта применения лапароскопических и роботических вмешательств при эхинококкозе печени.
Материалы и методы
В статье проведен анализ результатов лечения больных эхинококкозом печени, находившихся на лечении в хирургической клинике Боткинской больницы с 2015 по 2020 годы. Основой для проведения исследования послужило начало применения современных видеоэндоскопических и роботических технологий в лечении пациентов с паразитарным поражением печени.
За указанный период в клинике пролечено 79 больных с эхинококкозом печени. В исследование были включены только те пациенты, которые перенесли открытую (группа 1) и мини-инвазивную (группа 2) перицистэктомии. В группу 1 вошло 47 пациентов, в группу 2 — 8 больных.
В исследовании были оценены возраст больных, пол, уровень операционно-анестезиологического риска по шкале ASA, локализация паразитарной кисты, факторы, определяющие сложность резекции: индекс сложности лапароскопической резекции печени, резекций сложных сегментов, контакт с сосудами. Оценены непосредственные и отдаленные результаты хирургических вмешательств: время операции, объем кровопотери, длительность госпитализации, послеоперационные осложнения по классификации Clavien–Dindo, специфические осложнения по ISGLS, рецидивы в течение первого года после хирургического вмешательства [11, 12].
Результаты
Первая группа больных включила 47 пациентов, перенесших перицистэктомию лапаротомным способом. Во вторую группу вошли 8 больных, которым выполнены лапароскопические и роботические перицистэктомии.
Возраст больных первой группы составил 63,3±7,1 лет (от 20 до 78 лет). Соотношение мужчин и женщин: 24:23. Во второй группе возраст составил 59,5±6,3 лет (от 19 до 59 лет). Соотношение мужчин и женщин: 2:6.
Распределение больных по классификации ASA было следующим (рис. 1).
Распределение больных первой группы по ультрасонографической классификации ВОЗ представлено на рисунке 2.
Хотелось бы отметить, что во второй группе пациенты были предствлены только категориями СЕ2 и СЕ3, что было обусловлено изменением концепции необходимости хирургического лечения как кист СЕ 1, так и «мертвых» паразитарных кист СЕ4 и СЕ5. Как видно из графика, большая часть пациентов (62,5%) имела стадию эхинококкового процесса СЕ2 и СЕ3.
Также было оценено распределение кист по сегментам печени (рис. 3)
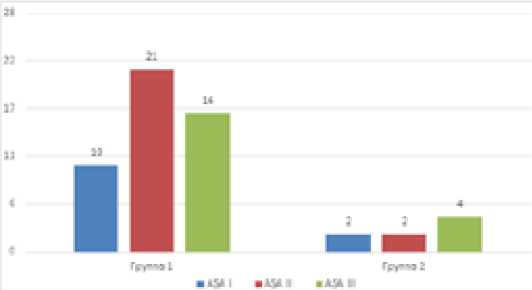
Рис. 1. Распределение больных по степени операционноанестезиологического риска по классификации ASA
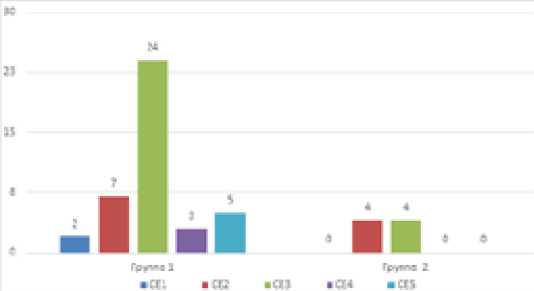
Рис. 2. Распределение больных по классификации ВОЗ
результатов лечения пациентов с эхинококкозом печени, перенесших перицистэктомии в традиционном и мини-инвазивном вариантах, комплексная оценка послеоперационных осложнений. Проанализированы как общие (по классификации Clavien–Dindo), так и специфические хирургические осложнения — это пострезекционная печеночная недостаточность, геморрагические и билиарные осложнения по классификации ISGLS [7, 8]. Также оценено наличие рецидивов в течение первого года после хирургического вмешательства.
Длительность хирургических вмешательств составила в первой группе 126,4 (92–311) минут, во второй группе — 135,3 (100–334) минуты. Минимально инвазивные операции сопровождались статистически значимо меньшей кровопотерей по сравнению с открытыми операциями: 54 (0–270) мл и 157(70–560) мл (р < 0,001) соответственно. Необходимость в интраоперационной гемотрансфузии в группе 1 выявлена у 7 оперированных пациентов, в группе 2 — у одного больного с исходно сниженным уровнем гемоглобина на фоне хронического лимфопролиферативного заболевания. В группе 1 средняя длительность послеоперационного койко-дня составила 12 (7–35) дней (р < 0,001), в группе 2 — 4 (1–6) (р < 0,001). В работе оценены как общие, так и специфические послеоперационные осложнения.
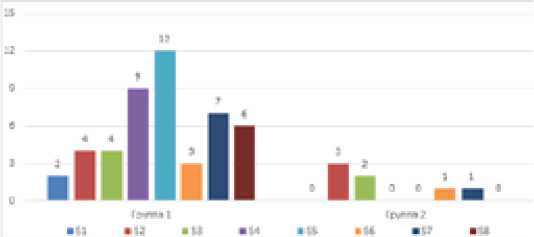
Рис. 3. Распределение больных по пораженным сегментам печени
Необходимо отметить, что на первых этапах применения мини-инвазивных технологий, пациенты с паразитарными кистами сложных локализаций (задние сегменты) были оперированы традиционным способом. В связи с чем в работе были оценены только результаты лечения больных, которым были выполнены вмешательства на передних сегментах печени (средний показатель индекса сложности хирургического вмешательства — 5,2 единицы).
В нашем исследовании проведена оценка как непосредственных (объем кровопотери, необходимость гемотрансфузии, послеоперационный койко-день), так и отдаленных
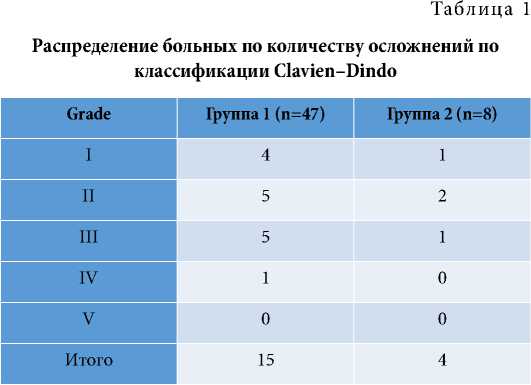
Как можно увидеть из таблицы, только у одного больного после лапароскопической перицистэктомии потребовалось проведение пункционно-дренирующего способа лечения острого жидкостного скопления в области операции.
В группе 2 выявлен один случай ОППН у пациента, перенесшего лапароскопическую перицистэктомию (класс «А»). Осложнений класса В и С не было.
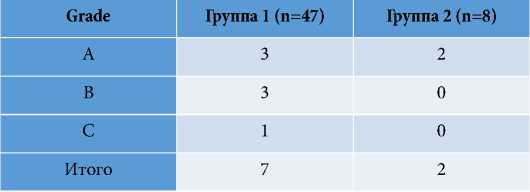
Выявлены два случая послеоперационных геморрагических осложнений, относящихся к классу А, не потребовавших проведения дополнительных вмешательств.
Таблица 2
Распределение больных по количеству случаев печеночной недостаточности по классификации ISGLS
|
Grade |
Группа 1 (n=47) |
Группа 2 (n=8) |
|
А |
5 |
1 |
|
В |
4 |
0 |
|
С |
1 |
0 |
|
Итого |
10 |
1 |
Таблица 3
Распределение больных по количеству случаев послеоперационных геморрагических осложнений по классификации ISGLS
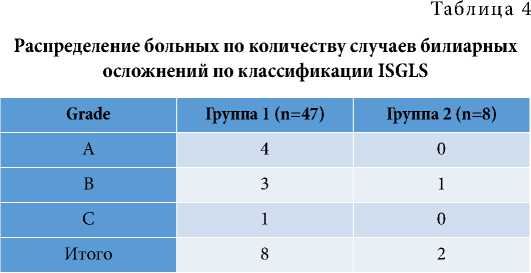
В группе 2 выявлен один случай желчного свища у пациента, перенесшего лапароскопическую перицистэктомию (класс «В»). В послеоперационном периоде у больного сформировалась билома, потребовавшая чрескожного дренирования жидкостного скопления. В течение 14 суток явления желчного свища купировались. Осложнений класса С не было.
Таким образом, хотелось бы отметить, что количество послеоперационных осложнений III класса и выше было представлено одним событием (12,5%), что, даже несмотря на малое общее количество пациентов, коррелирует с данными хирургической клиники Боткинской больницы (процент осложнений после перицистэктомии лапаротомным способом составляет около 12,8%).
Обсуждение
Хирургическая клиника Боткинской больницы, обладая опытом более чем 2500 роботических операций, начиная с 2018 года стала активно внедрять в хирургическую практику роботические, а затем и лапароскопические вмешательства при эхинококкозе печени.
Как видно из полученных нами результатов, при сравнении лапаротомных и мини-инвазивных вмешательств не выявлено различий в длительности операции, частоте переливания компонентов крови, частоте тяжелых послеоперационных осложнений (III и более класса по Clavien–Dindo), наличию специфических осложнений по классификации ISGLS, длительности нахождения в клинике, рецидива в течение года. Минимально инвазивные операции сопровождались статистически значимой меньшей кровопотерей по сравнению с открытыми: 54 (0–270) мл и 157 (70–560) мл (р < 0,001) соответственно, а также более коротким стационарным лечением: 4 (1–6) и 12 (7–35) дней (р < 0,001).
Данные результаты, не обладают значимой статистической достоверностью в связи с различным составом групп по классификации ВОЗ и малой выборкой во второй группе, однако они позволили оценить тенденцию к улучшению ряда вышеуказанных показателей.
Таким образом, полученный нами первый опыт применения лапароскопических и роботических технологий в лечении эхинококкоза печени, позволяет надеяться на перспективность методики, расширение показаний с накоплением опыта. Вопрос о хирургическом лечении рецидивного эхинококкоза, а также эхинококкоза задних сегментов печени, где, как правило, требуется применение комбинированных способов лечения (включая криоаблацию), может быть решен после проведения рандомизированных многоцентровых исследований.
Выводы
Таким образом, лапароскопические и роботические технологии могут быть использованы в лечении эхинококкового поражения печени. Данные модификации традиционных хирургических вмешательств позволяют уменьшить количество и тяжесть послеоперационных осложнений и улучшить результаты лечения.
Список литературы Современные лапароскопические и роботические технологии в лечении эхинококкоза печени
- Katkhouda N., Fabiani P., Benizri E., Mouiel J. Laser resection of a liver hydatid cyst under videolaparoscopy. British journal of surgery, 1992, V. 79, No. 6, рр. 560–561. https://doi.org/110.1002/bjs.1800790628
- Tuxun T., Zhang J.H., Zhao J.M., Tai Q.W., Abudurexti M., Ma H.Z., Wen H. World review of laparoscopic treatment of liver cystic echinococcosis — 914 patients. International Journal of Infectious Diseases, 2014, No. 24, рр. 43–50. https://doi.org/10.1016/j.ijid.2014.01.012
- Giulianotti P.C., Coratti A., Sbrana F., Addeo P., Bianco F.M., Buchs N.C., Benedetti E. Robotic liver surgery: results for 70 resections. Surgery, 2011, V. 149, No. 1, рр. 29–39. https://doi.org/10.1016/j.surg.2010.04.002
- Zhao Z.M., Yin Z.Z., Meng Y., Jiang N., Ma Z.G., Pan L.C., Liu R. Successful robotic radical resection of hepatic echinococcosis located in posterosuperior liver segments. World journal of gastroenterology. 2020, V. 26, No. 21, p. 2831. https://doi.org/10.3748/wjg.v26.i21.2831.
- Ibrahim I., Tuerdi M., Zou X., Wu Y., Yasen A., Abihan Y., Tuxun T. Laparoscopic versus open surgery for hepatic cystic echinococcosis: a systematic review and meta-analysis. International J. of Clinical and Experimental Medicine. 2017. V. 10, No. 12, pp. 16788–16797.
- Busic Z., Cupurdija K., Servis D., Kolovrat M., Cavka V., Boras Z., Busic N. Surgical treatment of liver echinococcosis open or laparoscopic surgery? Collegium antropologicum, 2012. V. 36, No. 4, pp. 1363–1366. PMID: 23390834
- Casciola L., Patriti A., Ceccarelli G., Bartoli A., Ceribelli C., Spaziani A. Robot-assisted parenchymal-sparing liver surgery including lesions located in the posterosuperior segments. Surgical endoscopy, 2011, V. 25, No. 12, pp. 3815–3824. https://doi.org/10.1007/s00464-011-1796-9
- Di Benedetto F., Ballarin R., Tarantino G. Totally robotic isolated caudate‐lobe liver resection for hydatid disease: report of a case. The International Journal of Medical Robotics and Computer Assisted Surgery, 2016, V. 12, No. 2, pp. 254–261. https://doi.org/10.1002/rcs.1685
- Troisi R.I., Patriti A., Montalti R., Casciola L. Robot assistance in liver surgery: a real advantage over a fully laparoscopic approach? Results of a comparative bi‐institutional analysis. The International Journal of Medical Robotics and Computer Assisted Surgery. 2013. V. 9, No. 2, pp. 160–166. https://doi.org/10.1002/rcs.1495. Epub. 2013 Mar. 21.
- Magistri P., Pecchi A., Franceschini E., Pesi B., Guadagni S., Catellani B., Ballarin R. Not just minor resections: robotic approach for cystic echinococcosis of the liver. Infection. 2019, V. 47, No. 6, pp. 973–979. https://doi.org/10.1007/s15010-019-01333-2
- Clavien P.A., Barkun J., De Oliveira M.L., Vauthey J.N., Dindo D., Schulick R.D., Graf R. The Clavien–Dindo classification of surgical complications: five-year experience. Annals of surgery. 2009, V. 250, No. 2, pp. 187–196. https://doi.org/10.1097/SLA.0b013e3181b13ca2.
- Rahbari N.N., Garden O.J., Padbury R., Brooke-Smith M., Crawford M., Adam R., Koch M., Makuuchi M., Dematteo R.P., Christophi C., Banting S., Usatoff V., Nagino M., Maddern G., Hugh T.J., Vauthey J.N., Greig P., Rees M., Yokoyama Y.Y., Fan S.T., Nimura Y., Figueras J., Capussotti L., Büchler M.W., Weitz J. Posthepatectomy liver failure: a definition and grading by the International Study Group of Liver Surgery (ISGLS). Surgery. 2011, May.; 149 (5):713–24. https://doi.org/10.1016/j.surg.2010.10.001. Epub. 2011 Jan. 14. PMID: 21236455.


