Современные методы лечения гнойных и ожоговых ран
Автор: Емельянова Альбина Миннегаязовна, Стяжкина Светлана Николаевна, Федоров Владимир Григорьевич, Субботин Андрей Владимирович
Журнал: Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье @vestnik-reaviz
Рубрика: Клиническая медицина
Статья в выпуске: 1 (43), 2020 года.
Бесплатный доступ
В представленной статье проведен анализ лечения пациентов с ожоговой травмой с позиции влияния коморбидной патологии в виде дисплазии соединительной ткани. Гистологические исследования биоптатов аутокожи показывают взаимосвязь степени дисплазии и её влияние на процессы регенерации ран. Приведены клинические примеры больных с глубокими ожогами функционально значимых областей с применением в комплексе лечения цитокинов.
Ожоговая травма, гнойные раны, дисплазия соединительной ткани, цитокинотерапия
Короткий адрес: https://sciup.org/143172308
IDR: 143172308 | УДК: 616-035.1
Current treatment methods for purulent and burn wounds
This article analyzes treatment of patients with burns complicated by connective tissue dysplasia. Histological examination of skin biopsy samples demonstrated an association between the grade of dysplasia and the processes of wound regeneration. We provided case reports describing patients with deep burns in functionally significant areas and their comprehensive treatment with cytokines.
Текст научной статьи Современные методы лечения гнойных и ожоговых ран
В структуре больных общехирургических стационаров пациенты с гнойными заболеваниями кожи и мягких тканей составляют 30–35 % [1]. Увеличение числа гнойных заболеваний и послеоперационных осложнений, учащение случаев генерализации инфекции и различного рода токсико-аллергических реакций свидетельствует о нерешенности проблемы гнойной инфекции в хирургии [1, 6]. В связи с этим дальнейшее совершенствование методов лечения острых гнойных заболеваний мягких тканей и их осложнений остается одним из актуальных направлений современной практической хирургии.
Понятно, что проблема раневой инфекции не может быть решена за счет новых лекарственных средств, так как основное значение в борьбе с хирургической инфекцией принадлежит защитным способностям самого организма, его реактивности и созданию ранних оптимальных условий для жизнедеятельности клеток и тканей.
Основа современных методов лечения ран включает:
-
- профилактику и борьбу с раневой инфекцией и интоксикацией;
-
- учет местной и общей реакции организма на травму и инфекцию раны;
-
- динамические данные (период или фаза раневого процесса);
-
- индивидуальные особенности больного.
Из многочисленных микробов, попавших в рану, лишь те виды их могут быть ис- точником развития раневых осложнений, которые обладают патогенной активностью (молниеносный сепсис), или развитию которых благоприятствуют условия раневой среды (сгустки крови, мертвые ткани, инородные тела и др.). Одним из условий, повышающих патологическую активность микробов, является синергическое действие отдельных их групп.
Местная реакция тканей является проявлением общей реакции организма. При инфицированной ране местная реакция тканей выражается в нервно-сосудистых расстройствах, отеке, в мобилизации клеточных элементов и укреплении раневого барьера. При свежей инфицированной ране большое значение имеет профилактика развития инфекции (специфическая и неспецифическая). При наличии инфекции в ране создаются условия оттока гноя из нее, повышается иммуннобиологическое состояние организма.
Одним из видов гнойных ран являются ожоговые раны. По данным ВОЗ, на термические поражения приходится 6 % от всех травм. Ежегодно в России регистрируется более 800 тыс. случаев ожогов различной тяжести, а частота их составляет 300-350 случаев на 10 тыс. населения [4]. Лечение обожженных является сложным и высоко затратным процессом [5, 3]. Общая летальность от ожогов в целом по России колеблется от 2,3 до 3,6 %. Из 180-200 тысяч пострадавших, госпитализируемых во все лечебные учреждения России, ежегодно погибают 8-10 тыс. человек. При этом 85-90 % -лица трудоспособного возраста и дети. Из числа выживших 12–15 тыс. человек нуждаются в длительной медицинской, социально-трудовой и психологической реабилитации [4]. Лечение ран и ожогов проводят дифференцированно в зависимости от стадии и фазы течения раневого процесса, при этом последовательно используются разнообразные лекарственные формы препаратов с различным механизмом действия.
В последние годы лечение гнойных ожоговых ран рассматривается как комплексный многоуровневый процесс, вклю- чающий в себя не только активное местное лечение ран, но и общее лечение организма с учетом нарушения таких процессов, как метаболических, эндокринных, иммунных и других.
Сложность лечения пациентов с гнойными ранами заключается также и в том, что зачастую у пациентов имеется комор-бидная патология. В нашей работе мы акцентировали внимание на такую патологию, которая в последние десятилетия привлекает внимание многих исследователей -дисплазия соединительной ткани [2]. Дисплазия - патологическое развитие клеток, тканей, органов человека. Диспластические изменения лежат в основе многих заболеваний. Важным является выявление признаков дисплазии у пациентов с ожоговой травмой, так как это помогает прогнозировать течение раневого процесса и в последующем развитии рубцов.
Материалы и методы исследования
Исследовательская работа проведена на базе ожогового отделения БУЗ УР «Первая республиканская больница МЗ УР» г. Ижевска за период с 2017 по 2019 годы. Проведены обследования, оперативное лечение и анализ результатов лечения пациентов с глубокими ожогами различной локализации.
Всего пациентов было 81, гендерный состав: мужчин 54 (66,67 %), женщин 27 (33,33 %). Возраст варьировал в пределах от 18 до 82 лет. Средний возраст составил 53,57 ± 3,52 года. Пациентам проводились лабораторные, цитологические, морфологические исследования, изучались внешние проявления диспластического процесса, проведен их подсчет и верификация по шкале Л.Н. Аббакумовой.
Результаты исследования и их обсуждение
Среди обследованных согласно классификации ВОЗ пациентов молодого возраста (до 44 лет) было 25 (30,86 %), среднего (45-59 лет) - 27 (33,33 %), пожилого
(60–74 года) – 21 (25,92 %), старческого – 8 (9,87 %).
По поражающему фактору на первом месте были ожоги пламенем – 40,74 % случаев, на втором месте – контактные ожоги, они зафиксированы в 37,03 % случаев, на третьем месте – ожоги от воздействия кипятка 22,22 %.
Среднее количество койко-дней составило 42,95 ± 4,77. Надо отметить, что у пациентов с дисплазией выраженной степени тяжести длительность госпитализации была 48,44 ± 2,23 койко-дня, у пациентов с дисплазией средней и легкой степени тяжести длительность лечения в стационаре была 39,0 ± 1,53 и 35,5 ± 1,77 койко-дня соответственно.
От момента поступление в ожоговое отделение до проведения аутодермопластики длительность лечения составила 17,27 ± 3,74 койко-дня. Пациенты, поступившие из районных больниц (49,38 %), оперировались через 25,75 ± 3,78 дней.
Пациентам с дисплазией соединительной ткани была необходима повторная аутодермопластика в связи с плохой приживаемостью аутотрансплантата в19,75 % случаев.
Микробиологические посевы с ран выполнены 51 пациенту, из них 12 (23,53 %) потребовалось повторно выполнять посевы для коррекции антибиотикотерапии. Из ран высевалась следующая патогенная микрофлора: St. aureus в 45,6 % случаев, из них больше половины 51 % штаммы MRSA; Ps. Aeruginosa в 32,4 % случаев; Klebsiella pneumoniae в 20,6 %, из них БЛН – 21,4 %; Acinetobacter Baumanii в 16,2 %; Enterococcus faecium в 7,4 %; C. albicans, parapsilosis прорастали в 2,9 %.
Другие микроорганизмы, такие как Corinebacterium, Klebsiella oxytoca, E. coli, Stenotrophamonas maltophilia, Raoltellaorny-tinolitica высевались в 1,48 % посевов. В 3 случаях роста микрофлоры не выявлено.
Степень обсеменённости ран выглядела следующим образом: единичный рост – 1,02 %; 1 степень – 7,1 %; 2 степень – 13,3 %;
3 степень – 17,3 %; 4 степень – 54,1 %; сплошной рост – 7,1 %.
Полученные результаты показывают выраженную обсемененность ожоговых ран, что указывает на решающее значение в проведении антибактериальной терапии.
С учетом чувствительности проводилась терапия следующими группами антибактериальных препаратов (табл. 1). Для стартовой терапии использовались антибиотики из группы цефалоспоринов 1 и 2 поколений и аминогликозиды. Монотерапию проводили 29 пациентам (31,9 %).
В ожоговом отделении БУЗ УР «Первая республиканская клиническая больница» МЗ УР обследован 81 человек с диагнозом глубокие ожоги различной локализации. В исследовании было выделено 3 группы пациентов. В первую группу вошли те, у кого отсутствуют фенотипические проявления дисплазии – 33 человека (40,74 %). Во вторую группу вошли пациенты с дисплазией соединительной ткани различной степени тяжести 30 человек (37,04 %). Третью группу составили пациенты с дисплазией, в комплексное лечение которых была включена цитокинотерапия 18 человек (22,22 %).
Вторая и третья группы пациентов были подвергнуты тщательному осмотру, были обнаружены признаки синдрома дисплазии соединительной ткани. Данные признаки проявлялись врожденными пороками развития, а также малыми аномалиями.
Наиболее часто встречающимся признаком, по которому происходит диагностика диспластического синдрома, является патология скелета, а именно: гипермобильность суставов, диагностированная у 27 исследованных (56,25 %), плоскостопие – у 30 (62,5 %) пациентов, деформации позвоночника и грудной клетки – в 37,5 % случаях. Косметические дефекты, являющиеся проявлением дисплазии соединительной ткани, в виде увеличения растяжимости и дряблости кожи были выявлены у 31 пациента (64,58 %).
Таблица 1
Антибактериальные препараты, использованные в лечении
|
Название препарата |
Число пациентов, получавших антибактериальную терапию |
||
|
Абсолютное число |
Процент от общего числа назначений |
||
|
Цефалоспорины |
Цефазолин |
9 |
9,9 |
|
Цефтриаксон |
56 |
61,5 |
|
|
Цефотаксим |
9 |
9,9 |
|
|
Цефепим |
20 |
21,9 |
|
|
Цефоперазон сульбактам |
22 |
24,2 |
|
|
Зинфоро |
1 |
1,1 |
|
|
Аминогликозиды |
Амикацин |
46 |
50,5 |
|
Гентамицин |
1 |
1,1 |
|
|
Гликопептиды |
Ванкомицин |
24 |
26,4 |
|
Карбапенемы |
Меропенем |
6 |
6,6 |
|
Тиенам |
2 |
2,2 |
|
|
Защищенный пенициллин |
Тациллин |
4 |
4,4 |
|
Пиперациллин тазобактам |
1 |
1,1 |
|
|
Тетрациклины |
Тигециклин |
3 |
3,3 |
|
Фторхинолоны |
Ципрофлоксацин |
1 |
1,1 |
|
Лефлобакт |
1 |
1,1 |
|
|
Противогрибковые |
Флюконазол |
1 |
1,1 |
|
Противопротозойный препарат с антимикробной активностью |
Метрогил |
4 |
4,4 |
|
Без антибактериальной терапии |
– |
7 |
7,7 |
Оценивая степень тяжести синдрома дисплазии соединительной ткани по шкале Л.Н. Аббакумовой, мы выявили следующее: у 25 пациентов наблюдался синдром дисплазии соединительной ткани крайней степени, что соответствовало тяжелой дисплазии (пациенты данной группы набрали более 24 баллов), синдром дисплазии соединительной ткани проявлялся умеренно у 17 пациентов (по шкале Л.Н. Аббакумовой пациенты данной группы набрали 12–23 балла), легкой степени тяжести синдром дисплазии соединительной ткани встречался у 6 пациентов (в данной группе пациенты набрали меньше 12 баллов по шкале Л.Н. Аббакумовой).
При патогистологическом исследовании расщепленного кожного лоскута, взятого во время операции при аутодермопластике, обнаружено, что у больных с дисплазией соединительной ткани выраженной степени тяжести слабо развита аргирофильная сеть, отсутствуют придатки кожи, атрофия эпидермиса, фиброз дермы (52,08 %); у больных с дисплазией соединительной ткани средней степени тяжести, отмечается превалирование молодой грануляционной ткани, разная ориентированность коллагеновых волокон дермы, преобладает сглаженность сосочкового слоя дермы, а также слабая развитость аргирофильной сети (35,42 %); у пациентов с легкой степенью тяжести дисплазии соединительной ткани при микроскопическом исследовании в биоптате выявлено преобладание грануляционной ткани, многослойный плоский ороговевающий эпителий (12,5 %).
Нами в ходе предоперационного лечения ожоговой травмы у пациентов с наличием признаков дисплазии, учитывая патогенез формирования грубых келоидных рубцов, включались препараты магния и иммуномодуляторы.
Далее приводим примеры лечения пациентов с дисплазией и результаты их лечения.
Пример 1
На лечении в ожоговом отделении БУЗ УР «1 РКБ МЗ УР» находился пациент Б., 54 года, работает в колхозе. Поступил в ожоговое отделение БУЗ УР «1РКБ МЗ УР» 19.03.2018 г. с диагнозом: ожог пламенем 3АБ степени туловища, правой верхней конечности 12 % (3Б 8 %).
Обстоятельства травмы: 27.02.2018 г. в алкогольном опьянении курил в постели и загорелась одежда. Был госпитализирован в хирургическое отделение центральной районной больницы, где выполнялись этапные некрэктомии, переведен в ожоговое отделение для дальнейшего лечения в связи с необходимостью более качественной подготовки ран и проведения аутодермопластики.
При поступлении в ожоговое отделение состояние пациента было удовлетворительным. Локальный статус: на туловище справа с переходом спереди на грудную клетку, сзади – на спину, правом плече и предплечье были ожоговые раны, часть ран гранулировали, были покрыты налетом фибрина, на других ранах имелся темнокоричневый струп. Отведение в правом плечевом суставе было ограничено до 40 градусов.
У пациента были выявлены клинические признаки дисплазии соединительной ткани: умение сворачивать язык в трубочку, нарушения зубной эмали, приросшие мочки ушей, асимметрия носовой перегородки, легкое вдавление на грудине, плоскостопие, натоптыши, халюксвальгус, варикозное расширение вен нижних конечностей. Согласно схеме диагностических критериев дисплазии соединительной ткани Т. Милковска-Дмитровой и А. Каракашева, пациент Б. имел главные диагностические критерии – плоскостопие, расширение вен, деформация грудной клетки, второстепенные диагностические критерии – аномалии ушных раковин, аномалии зубов. Согласно классификации тяжести дисплазии соединительной ткани пациенту выставлена 2-я степень тяжести.
За время нахождения в ожоговом отделении выполнены аутодермопластики – 3.04.2018 г. и 19.04.2018 г. (35 и 51 дни с момента получения травмы). После первой операции частичный лизис аутотрансплантатов на площади 350 см2, после второй – лизис незначительный (рис. 1). Во время первой операции была взята кожа на гистологическое исследование и получено заключение – дистрофия эпидермиса, деструкция и дезорганизация коллагеновых и эластических волокон, изменение биосинтетической активности фибробластов и патология сосудов микроциркуляторного русла.
Необходимо отметить, что помимо хирургического лечения ран пациент получал стандартную терапию ожоговой болезни, которая включала:
-
1. Медикаментозную терапию – антибактериальная терапия с учетом чувствительности (амикацин, цефепим), инфузионная, обезболивающая терапия.
-
2. Пациенту проводилась лечебная физкультура под контролем инструктора с момента госпитализации в ожоговое отделение, выполнялось позиционирование правой верхней конечности.
-
3. Местное лечение ран – при подготовке ран к аутодермопластике использовались следующие повязки – пермофом, фиб-росорб, левосин, воскопран, раствор хлор-филлипта.
Выписан 28.04.2018 г., 40 койко-дней, всего 61 день с момента травмы и начала лечения. На момент выписки аутотрансплантаты кожи прижились, остаточные раны эпителизировались, сформировалась приводящая послеожоговая рубцовая контрактура правого плечевого сустава 2 степени (рис. 2).
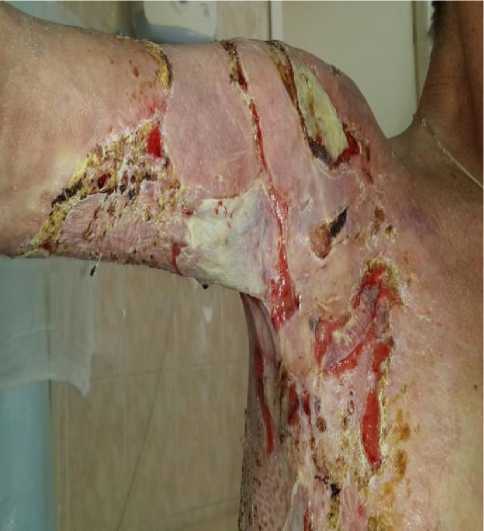
Рис. 1. Перевязка через 3 дня после второй аутодермопластики
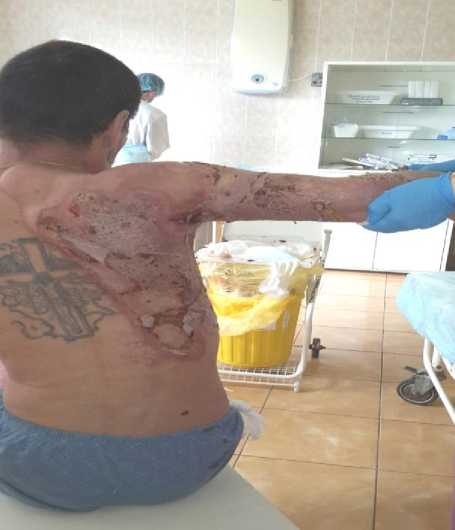
Рис. 2. Максимальное отведение в правом плечевом суставе до 90 градусов
При выписке пациенту была рекомендована противорубцовая терапия, включающая: лечебную физкультуру, курсы электрофореза с лидазой и фонофореза с фер-менколом, противорубцовые гели, силиконовые пластины, санаторно-курортное лечение, диспансерное наблюдение у комбу-стиолога.
Пример 2
Пациент С., 38 лет, работает мастером на заводе, находился на лечении в ожоговом отделении БУЗ УР «1 РКБ МЗ УР» с 5.09.2019 г. с диагнозом: контактный ожог 3АБ степени туловища, левой верхней конечности 6 % (3Б 5 %).
Обстоятельства травмы: 4.09.2019 г. упал в бане на печь, на следующий день обратился в приемное отделение ожогового отделения и был госпитализирован.
При поступлении состояние пациента было удовлетворительным. Локальный статус: на туловище слева на спине, левом плече и предплечье ожоговые раны, покрытые плотным коричневым струпом, умеренная перифокальная воспалительная реакция.
У пациента были выявлены клинические признаки дисплазии соединительной ткани: умение сворачивать язык в трубочку, нарушения роста зубов, приросшие мочки ушей, асимметрия носовой перегородки, стрии на коже, сколиоз, гипермобильность суставов. Согласно схеме диагностических критериев дисплазии соединительной ткани Т. Милковска-Дмитровой и А. Каракаше-ва, пациент С. имел главные диагностические критерии – деформация позвоночника, гипермобильность суставов, нарушение растяжимости кожи, второстепенные диагностические критерии – аномалии ушных раковин, аномалии зубов. Согласно классификации тяжести дисплазии соединительной ткани пациенту выставлена 2-я степень тяжести.
За время нахождения в ожоговом отделении выполнены аутодермопластики – 19.09.2019 г. и 03.10.2018 г. (15 и 29 дни с момента получения травмы). Вторая операция была проведена из-за того, что в области плечевого сустава раны были более глубокими (площадь 124 см2) и не были готовы к пластическому закрытию на первой операции. Во время первой операции была взята кожа на гистологическое исследование и получено заключение – эпидермис истончен с признаками ороговения, развиты аргирофильная сеть и сосочковый слой дермы, развита капиллярная сеть дермы.
Необходимо отметить, что помимо хирургического лечения ран пациент получал стандартную терапию ожоговой болезни, которая включала:
-
1. Медикаментозную терапию – антибактериальная терапия цефтриаксоном, инфузионная, обезболивающая терапия.
-
2. Пациенту проводилась лечебная физкультура под контролем инструктора с момента госпитализации в ожоговое отделение, выполнялось позиционирование левой верхней конечности.
-
3. Местное лечение ран – при подготовке ран к аутодермопластике использовались следующие повязки – пермофом, фиб-росорб, левосин, воскопран, раствор хлор-филлипта.
-
4. Помимо вышеперечисленного пациенту был проведен курс лечения цитокинами и препаратами, содержащими магний.
Выписан 28.04.2018 г., 39 койко-дней, всего 40 дней с момента травмы и начала лечения. На момент выписки аутотрансплантаты кожи прижились (рис. 3), сформировалась приводящая послеожоговая рубцовая контрактура левого плечевого сустава 1 степени (рис. 4).
При выписке пациенту была рекомендована стандартная противорубцовая терапия.
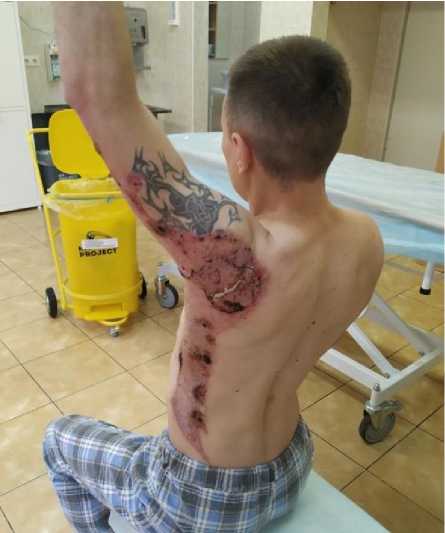
Рис. 3. После второй аутодермопластики
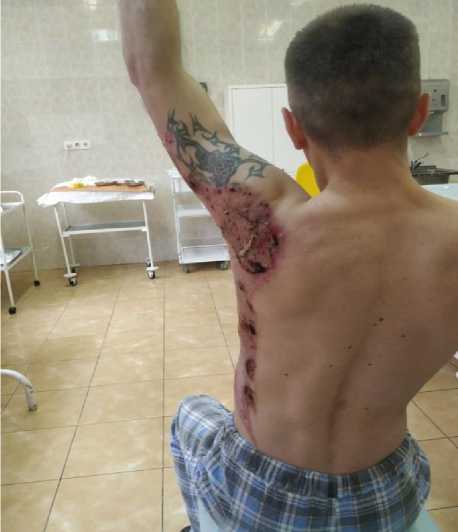
Рис. 4. Максимальное отведение в левом плечевом суставе до 140 градусов
Заключение
-
1. Лечение гнойных и в частности ожоговых ран – это трудоемкий длительный процесс, требующий от лечащего врача применение полного комплекса диагностических и лечебных манипуляций.
-
2. Существует зависимость между количеством и тяжестью внешних фенотипических проявлений дисплазии соедини-
- тельной ткани и результатов лечения глубоких ожогов, особенно функционально значимых областей, что отображено в приведенных клинических случаях.
-
3. Наличие диспластического синдрома у пациентов с ожоговой травмой становится причиной трудности в лечении данной группы больных, в частности удлинение периода подготовки ран к аутодермопла-
- стике, лизис кожных трансплантатов после операции и формирование более грубых рубцов.
-
4. Эта проблема еще раз указывает на высокую значимость данной патологии в
клинической практике врача ожогового отделения, требующая нового подхода в лечении данной категории пациентов.
Список литературы Современные методы лечения гнойных и ожоговых ран
- Vinnik Yu.S., Markelova N.M., Tyuryumin V.S. Sovremennye metody lecheniya gnojnyh ran // Sibirskoe medicinskoe obozrenie. - 2013. - № 1. - S. 19-24.
- Emel'yanova A.M., Styazhkina S.N., Fedorov V.G. i dr. Vzaimosvyaz' gistologicheskoj kartiny i stepeni klinicheskih proyavlenij displazii u pacientov s glubokimi ozhogami // Sovremennye problemy nauki i obrazovaniya. - 2019. - № 2.
- Fayazov A.D., Kamilov U.R., Shukurov S.I. i dr. Puti uluchsheniya kombustiologicheskoj pomoshchi v sisteme ekstrennoj medicinskoj pomoshchi // Sbornik nauchnyh trudov 3-go S"ezda kombustiologov Rossii. - M., 2010. - S. 39-40.
- Fayazov A.D., Ruzimuratov D.A. Sovremennye metody mestnogo lecheniya ozhogovyh ran // Vestnik ekstrennoj mediciny. - 2012. - № 3. - S. 97-103.
- Herdon D.N. Nutritional and pharmacological support of the metabolic response to injury. Minerva Anestesiol 2003; 69(4):264-74.
- Wheeland R.G. Wound healing and the newer surgical dressings // Dermatology. Philadelphia: WBSaunders. - 1992. - P. 2305-2311.


