Современные подходы к лечению и реабилитации больных опухолями придаточных пазух носа с применением никелида титана и компьютерных технологий
Автор: Новиков В.А., Штин В.И., Фролова И.Г., Трухачва Н.Г., Шилова О.Г., Никитчук А.В., Кучерова Т.Я., Молчанов Н.А.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Опыт работы онкологических учреждений
Статья в выпуске: 2 (22), 2007 года.
Бесплатный доступ
В статье представлены результаты комбинированного лечения больных злокачественными новообразованиями придаточных пазух с использованием современных хирургических технологий, основанных на индивидуальном эндопротезировании послеоперационных костных дефектов. В раннем послеоперационном периоде проводилась стимуляция репаративных процессов в ране с использованием лазерного инфракрасного излучения низкой интенсивности и постоянного магнитного поля. Использование данных методик позволило сократить сроки реабилитации, повысить уровень социальной адаптации больных, улучшить косметический и функциональный эффект от лечения.
Злокачественные опухоли придаточных пазух носа, индивидуальное протезирование, комбинированное лечение, качество жизни
Короткий адрес: https://sciup.org/14054564
IDR: 14054564 | УДК: 616.216-006-089.844
Novel approaches to treatment and rehabilitation of patients with cancer of nasal accessory sinuses using titanium nickelid and computer-bases technologies
Results of the combined modality treatment for patients with cancer of accessory sinuses using the modern surgical technologies based on individual endoprosthesis of postoperative bone defects have been presented. Stimulation of reparative processes in the wound with the use of low intensity laser infra-red radiation and permanent magnetic field was performed in early postoperative period. The application of the above methods allowed the reduction in rehabilitation period, increase in the level of social adaptation of the patients and improvement of cosmetic and functional effects of the treatment.
Текст научной статьи Современные подходы к лечению и реабилитации больных опухолями придаточных пазух носа с применением никелида титана и компьютерных технологий
Злокачественные новообразования полости носа и придаточных пазух составляют 1–2 % всех злокачественных опухолей человека. Последние статистические данные свидетельствуют о возрастании удельного веса опухолей этой локализации. Самая высокая в мире заболеваемость за- регистрирована у мужского населения Японии, а также у жителей Китая и стран Юго-Восточной Азии (2,5–2,6 на 100 000 населения) [4]. Самая низкая заболеваемость опухолями полости носа и придаточных пазух отмечена у населения Западной Европы (0,1–1,0 на 100 000 населения).
В Российской Федерации наиболее часто эта патология встречается у коренного населения Якутии, у которых новообразования данной локализации составляют 63,3 % в структуре злокачественных опухолей верхних дыхательных путей. В целом по России этот показатель колеблется в пределах 13–23 % [3, 5, 6].
Лечение опухолей полости носа и придаточных пазух является одной из самых сложных задач современной онкологии. Несмотря на успехи ранней диагностики, 60–90 % больных госпитализируются в специализированные учреждения с местно-распространенными процессами III–IV стадии. Развитие опухолей околоносовых пазух с поражением смежных областей ухудшает прогноз, снижает эффективность лечебных и реабилитационных мероприятий. Комбинированный метод лечения, включающий хирургическое вмешательство и лучевую терапию, остается основным и наиболее эффективным. Использование данной комбинации, по мнению многих авторов, позволяет добиться достаточно высоких результатов лечения больных местно-распространенными опухолями полости носа и придаточных пазух (49–56 %) [1, 2].
Объем хирургического вмешательства зависит от исходной локализации и распространенности опухоли. Большинство хирургов при местно-распространенных опухолях полости носа и околоносовых пазух производят комбинированные операции, включающие резекцию верхней челюсти, решетчатого лабиринта с ревизией глазницы, основной и лобной пазух, носоглотки. В отношении показаний к экзентерации орбиты существуют различные мнения, но большинство исследователей [3, 7] считают, что при злокачественных опухолях верхней челюсти и полости рта, вызывающих ограниченную деструкцию костных стенок орбиты без инфильтрации интраорбитальной клетчатки, оправдано выполнение электрохирургической резекции верхней челюсти с удалением пораженной стенки глазницы и прилежащей интраорбитальной клетчатки с сохранением глазного яблока и мышц.
Анатомические особенности челюстно-лицевой области являются причиной того, что даже небольшие по объему новообразования вынуждают хирургов к проведению тяжелых деструктивных вмешательств. Косметические и функциональные нарушения после подобных операций вызывают тяжелые страдания у больных. Нарушения функций глотания, жевания, речи, дыхания затрудняют процессы социальной адаптации пациентов, лишают возможности трудиться [1]. В современных условиях, когда качество жизни становится одним из основных показателей эффективности лечения, важнейшее значение приобретает реабилитация больных, нуждающихся в выполнении реконструктивных вмешательств и адекватного протезирования. Исследователи, изучающие проблему первичной пластики и эндопротезирования, указывают на ряд особенностей реконструктивной хирургии челюстно-лицевой области [2]. Одна из них – частый контакт операционной раны со слюной и высоковирулентной флорой. Кроме этого, полость рта – зона повышенной функциональной активности, этим объясняются высокие требования, предъявляемые к материалу для изготовления эндопротезов. Материал, используемый для изготовления имплантатов, должен быть устойчив к агрессивным средам организма, иметь высокую биохимическую и биомеханическую совместимость. Этим требованиям соответствует имплантационный материал на основе никелида титана. Такие особенности поведения никелида титана в тканях организма, как биоадгезивность, характеризующая способность материала имплантата связываться с белками, не изменяя существенно их структуры, не вызывая иммунных реакций и воспалительных процессов; способность изменять свою форму без участия пластической составляющей деформации в условиях знакопеременной деформации тканей, позволяют считать последний наиболее приемлемым для использования в качестве имплантируемых материалов.
В НИИ онкологии ТНЦ СО РАМН разработана и с 1993 г. применяется в клинической практике методика комбинированного лечения злокачественных опухолей полости носа и околоносовых пазух, включающая предоперационный курс гамма-терапии, оперативное вмешательство и интраоперационное облучение ложа опухоли пучком быстрых электронов с энергией 6 МэВ, с одномоментным замещением послео- перационного дефекта типовыми эндопротезами из пористого никелида титана. Проведено лечение 84 больных. Все пациенты перенесли лечение вполне удовлетворительно. Показатель 5-летней общей выживаемости составляют 61,0 ± 8,1 %, 5-летней безрецидивной выживаемости – 66,2 ± 8,8 %. Для восстановления костных структур средней зоны лица использовались эндопротезы из пористого никелида титана, изготавливаемые на основе типового шаблона с учетом антропометрических данных пациента. Методика позволила решить проблему восстановления опоронесущих структур орбиты и средней зоны лица после комбинированных резекций верхней челюсти [3]. Это дало возможность значительно повысить качество жизни большинства больных. Вместе с тем в результате многолетних наблюдений были выявлены существенные недостатки типового изготовления имплантатов по усредненным шаблонам. Отсутствие полной конгруэнтности имплантата с окружающими тканями приводило к локальному отторжению эндопротеза в зонах с недостаточностью интеграции. По данным В.А. Новикова с соавт. [3], осложнения эндопротезирования средней зоны лица и глазницы имплантатами из никелида титана зарегистрированы у 18 % больных. В период с 2002 по 2004 г. включительно в НИИ онкологии эндопротезирование стенок орбиты выполнено 19 пациентам. В ходе наблюдения за пациентами в послеоперационном периоде установлено, что в 5 (26 %) случаях имелось локальное отторжение эндопротезов через 1–1,5 мес и более. Изучая процесс заживления послеоперационных ран у больных, эндопротезирование которым выполнялось данным способом, представилось возможным определить следующие этапы его развития: на 10-е сут после оперативного вмешательства начиналось отторжение струпа и очищение раны от некротизированных тканей. Данная фаза заживления длилась 7–10 сут. Одновременно с процессом очищения стенок полости от некротизированных тканей отмечается рост грануляционной ткани, которая через 3–4 нед после операции полностью закрывала раневую поверхность. Эпителизация стенок полости обычно заканчивалась через 3–4 мес. Особенности течения раневого процесса у боль- ных, оперированных по поводу опухолей челюстно-лицевой области, а именно: первичная инфицированность, снижение местного и общего иммунитета, нарушение микроциркуляции и реологических свойств крови как реакция на операционную травму, способствуют увеличению длительности процессов репарации и эпи-телизации стенок послеоперационной полости, развитию воспаления в области эндопротеза и, как следствие, отторжению последнего в зонах с недостаточностью процессов интеграции имплантатов с окружающими тканями.
В настоящее время в НИИ онкологии ТНЦ СО РАМН совместно с сотрудниками НИИ медицинских материалов разрабатывается комплекс реабилитационных мероприятий, включающий индивидуальное эндопротезирование и стимуляцию репаративных процессов в послеоперационной ране, с использованием лазерного инфракрасного излучения низкой интенсивности и постоянного магнитного поля. Шаблоном для изготовления и моделирования индивидуальных имплантатов из никелида титана служит пластмассовая модель черепа пациента, получаемая на основании данных спиральной компьютерной томографии, которая выполняется на мультиспиральном томографе «Somatom sensation-4» в аксиальной, коронарной и фронтальной проекциях по программе спирального сканирования (срезы 1/1 мм, pitch равный 1–1,5), с последующими мультипланар-ными реформациями и построением объемного (3D) изображения. Анализ изображений осуществляется в режимах мягкотканого и костного окон. С помощью КТ удается точно локализовать первичную опухоль, определить ее размеры, структуру, распространенность патологического процесса на пограничные анатомические области (орбиту, полость черепа, твердое небо, основание черепа и др.) Результаты обследования пересылаются через Интернет в Институт проблем лазерных и информационных технологий (ИПЛИТ) РАН г. Шатура Московской области, где используются для выращивания пластмассовой модели черепа пациента методом лазерной стереолитографии на установке ЛС-250/3. Методика позволяет изготавливать эндопротезы с учетом анатомических особенностей пациента и распространенности опухолевого процесса.
Это способствует увеличению точности выполнения операции, повышает функциональность и улучшает процесс адаптации протеза с окружающими тканями. Структура имплантата позволяет решить проблему фиксации с удовлетворением требований совместимости. При этом создаются два способа связей между имплантатом и живой тканью: механическое сцепление в результате прорастания ткани в порах имплантата и химическое соединение за счет взаимодействия ткани с компонентами элементного состава имплантата.
С целью стимуляции репаративных процессов в послеоперационной ране и сокращения сроков реабилитации данной группе больных в послеоперационном периоде проводится магнитно-лазерная терапия с использованием инфракрасного лазерного излучения и постоянного магнитного поля аппаратов «Милта-Ф» и «Мустанг-2000». Терапия проводится ежедневно, начиная с 10-х сут после операции и до момента выписки пациента, с величиной магнитной индукции от 10 мТл до 30 мТл и частотой в пределах 80 Гц.
Для оценки эффективности реабилитационных мероприятий нами разработан следующий комплекс критериев:
-
- комплексная оценка состояния органа зрения и стенок глазницы (компьютерная томография и ультразвуковое обследование по специальной программе; определение характера зрения с помощью 4-точечного светотеста, определение девиации глаза с помощью синоптофо-ра, определение подвижности глаза, визометрия, экзофтальмометрия, гипофтальмометрия),
-
- эндоскопический контроль состояния послеоперационной полости. Эндофотографирование и эндовидеосъёмка стенок послеоперационной полости и поверхности эндопротеза,
-
- фотографирование пациента в шести стандартных проекциях,
-
- изучение динамики течения раневого процесса и изменений местного иммунитета в послеоперационной полости (спектр цитокинов, уровень противовоспалительных иммуноглобулинов, процентное соотношение нейтрофильных лейкоцитов, определение количества макрофагов, фибробластов, фиброцитов),
-
- исследование качества жизни пациентов по
С использованием разработанного комплекса реабилитационных мероприятий пролечено 5 пациентов. Во всех случаях удалось сохранить нормальное положение глазного яблока, сократить сроки заживления послеоперационной полости.
Клинический пример:
Пациент Л. 29 лет. Диагноз: периферическая примитивная нейроэктодермальная опухоль полости носа слева, состояние после нерадикального удаления опухоли, лучевой терапии.
Пациент считает себя больным с февраля 2004 г., когда появились головные боли, носовые кровотечения. Проходил обследование у ЛОР – врача по месту жительства. С подозрением на опухолевое поражение верхнечелюстной пазухи был отправлен в онкологический диспансер г. Красноярска. Произведена диагностическая гайморотомия и биопсия опухоли, по результатам которой получено гистологическое заключение: эстезионейробластома. По месту жительства проводилась лучевая терапия в СОД 46 Гр. В дальнейшем больной специального лечения не получал. Самостоятельно обратился в НИИ онкологии.
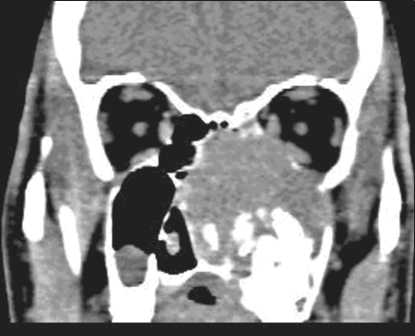
При поступлении регионарные лимфоузлы пальпаторно не определялись. По данным компьютерной томографии в проекции левой верхне-челюстной пазухи опухоль неоднородной
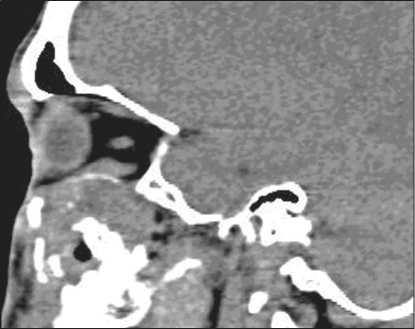
Рис. 2. Компьютерная томограмма лицевого скелета больного Л. в сагиттальной проекции
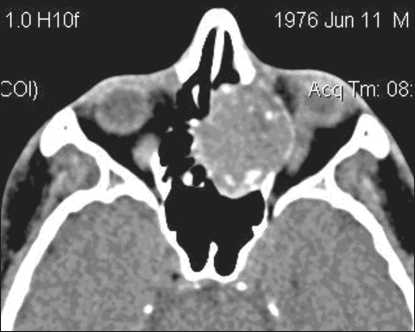
Рис. 3. Компьютерная томограмма лицевого скелета больного Л. в аксиальной проекции
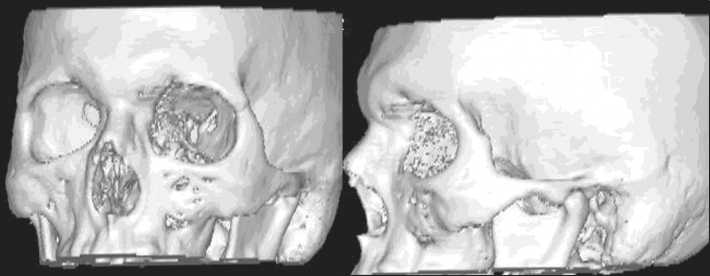
Рис. 4. Модель объемного изображения черепа для последующего изготовления стереолитографической модели черепа пациента
структуры (вероятнее всего, за счет участков распада). Опухоль разрушает почти все стенки верхнечелюстной пазухи, альвеолярный отросток, распространяется на клетки решетчатого лабиринта, в полость носа, обтурирует хоаны, инфильтрирует носоглотку слева на небольшом протяжении. Разрушены медиальная и нижняя стенки глазницы слева, глазное яблоко оттеснено латерально. Разрушена передненижняя стенка основной пазухи (рис. 1–3).
Пациенту был проведен курс предоперационной дистанционной гамма-терапии в СОД 40 Гр. Параллельно было выполнено компьютерное моделирование и изготовление стереолитографической модели черепа пациента (рис. 4), которая в дальнейшем использована для изготовления индивидуального эндопротеза нового типа на основе сетки из никелидтитановой нити. На втором этапе комбинированного лечения выполнена комбинированная электрорезекция верхней челюсти слева с индивидуальным эндопротезированием имплантатом из никелида титана. При иммуногистохимическом исследовании послеоперационного материала установлен следующий диагноз: периферическая примитивная нейроэктодермальная опухоль PNET (peripheral primitive neuroectodermal tumor).
С целью улучшения репаративных процессов в послеоперационной полости, начиная с 10-х суток после операции и до момента выписки, пациенту проводилась магнито-лазерная терапия с использованием аппаратов «Милта-Ф» и «Мустанг-2000».
Качество реабилитационных мероприятий оценивалось на основании разработанного комплекса критериев. Данные оценки состояния органа зрения представлены в таблице. В
Таблица
Офтальмологическая функциональная оценка


