Создание аналитической установки для биологических исследований на основе оптического микроскопа Axio Observer D1 и микрочиповых технологий. Ч. 1
Автор: Кухтевич Игорь Владимирович, Букатин А.С., Евстрапов А.А., Мухин И.С.
Журнал: Научное приборостроение @nauchnoe-priborostroenie
Рубрика: Приборные исследования и методики
Статья в выпуске: 3 т.20, 2010 года.
Бесплатный доступ
Проведены расчет и моделирование топологии микрофлюидного чипа для диэлектрофореза микрочастиц. Изготовлены экспериментальные образцы микрочипов с квадрупольными планарными электродами. На основе инвертированного оптического микроскопа и микрофлюидных чипов создана экспериментальная установка для исследований диэлектрофореза частиц. Продемонстрирована возможность управления движением и фиксация частиц в рабочей области микрочипа.
Микрофлюидные чипы, диэлектрофорез, аналитические системы, оптическая микроскопия, микрочастицы, клетки
Короткий адрес: https://sciup.org/14264664
IDR: 14264664 | УДК: 621.317.329
Development of analytical instrumentation based on optical microscope Axio Observer D1 and microchip technologies for biological research. Part 1
The calculation and simulation of microfluidic chip topology for dielectrophoresis of microparticles was done. Experimental chip samples with planar quadrupole electrodes were manufactured. On the basis on the inverted optical microscope and microfluidic chips the experimental instrumentation for microparticles dielectrophoresis investigation was developed. The possibility of microparticles control and fixation in the working area of the chip was demonstrated.
Текст научной статьи Создание аналитической установки для биологических исследований на основе оптического микроскопа Axio Observer D1 и микрочиповых технологий. Ч. 1
ВВЕДЕНИЕ лены относительно простые микрофлюидные чи-
Среди методов управления движением микрочастиц, основанных на воздействии внешних полей, наиболее известными и широко распространенными считаются ультразвуковые методы [1], электрофорез [2], диэлектрофорез [3, 4]. Эти методы в той или иной степени используются в микроаналитических системах (lab-on-a-chip и µ-TAS) [5, 6]. Области применения этих систем различны: аналитическая химия, фармацевтические исследования, биотехнология, судебная медицина и криминалистика, экологический мониторинг и т. д. Наибольший интерес вызывает использование микроаналитической техники для изучения и анализа биологических объектов (молекул, бактерий, клеток, ДНК) [7]. Анализ содержания и поведения отдельных клеток важен для фундаментального понимания их функций в окружающей среде: процессов взаимодействия клеток, реакции на внешние воздействия и т. д. Но живые клетки являются сложными объектами для исследований. Традиционно для изучения клетки используются электро-кинетические методы. Наличие у клетки таких свойств, как двойной электрический слой, окружающий клетку, приводит к тому, что электроки-нетическое движение клеток происходит по несколько иным принципам, чем в случае высокомолекулярных микрочастиц (ДНК, белки). Электрофорез не позволяет воспроизводимо разделять клетки по каким-либо характеристикам, поэтому применяют разные варианты диэлектрофореза (ДЭ) [8]. Для реализации ДЭ могут быть изготов- пы (МФЧ) с системой внутренних электродов. Подобные устройства применяются для исследований бактерий, раковых клеток, стволовых клеток и т. д. [9, 10].
В рамках работы представлены результаты исследований по созданию экспериментальной установки на основе оптического микроскопа и мик-рофлюидных чипов для исследований диэлектро-форетических методов управления движением микрочастиц.
МОДЕЛИРОВАНИЕ РАСПРЕДЕЛЕНИЯ ЭЛЕКТРИЧЕСКИХ ПОЛЕЙ В МФЧ ДЛЯ ДЭ
Наиболее простой и доступной для реализации в лабораторных условиях является квадрупольная конфигурация внутренних электродов, выполненная на диэлектрической подложке [3]. Такая конструкция может быть получена методами магнетронного напыления токопроводящего покрытия на стеклянную подложку, последующего нанесения фоторезиста, фотолитографии и травления. На сформированные электроды подаются потенциалы, сдвинутые по фазе друг относительно друга, что позволяет создавать неоднородное электрическое поле, необходимое для реализации ДЭ.
Сила, действующая на незаряженную частицу в неоднородном электрическом поле, зависит от градиента электрического поля, создаваемого электродами. Для вычисления величины диэлек-трофоретической силы, определения размеров и формы электродов, а также характеристик по- тенциалов, подаваемых на электроды, проведено численное моделирование распределения электрического поля в МФЧ. Потенциальная энергия частицы в электрическом поле имеет следующий вид [2]:
W = - 4 ne 1 K
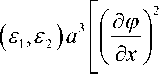
+
Ф l= y )
где ε 1, ε 2 — диэлектрические проницаемости среды и частицы; a — ее радиус; K ( ε 1, ε 2) — фактор
Клаузиуса—Мосотти; φ — потенциал электрического поля, подчиняющийся уравнению Лапласа Аф = 0 с соответствующими граничными усло виями:
д 2 Ф . d ф = 0 d x 2 d y 2 , ф | sn = u ( t ),
u ( t ) — потенциал электродов в зависимости от времени.
×10
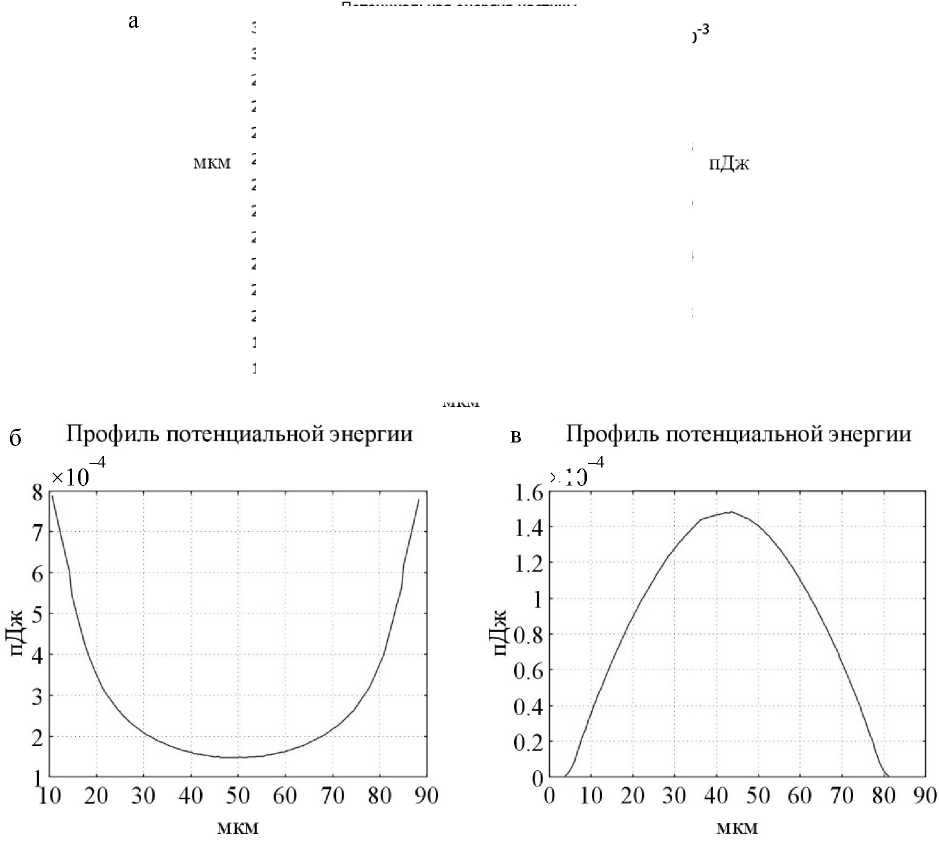
Рис. 1. Распределение потенциальной энергии частицы в постоянном электрическом поле (а) и в двух взаимно перпендикулярных направлениях, показанных штриховой линией: в направлении 1 (б) и направлении 2 (в)
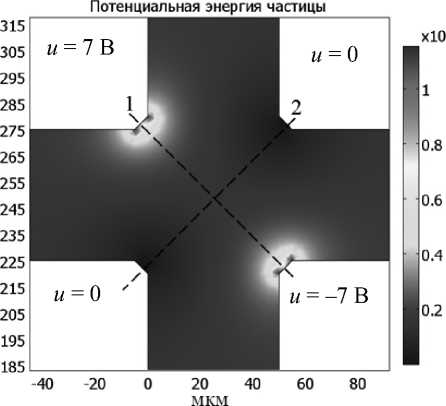
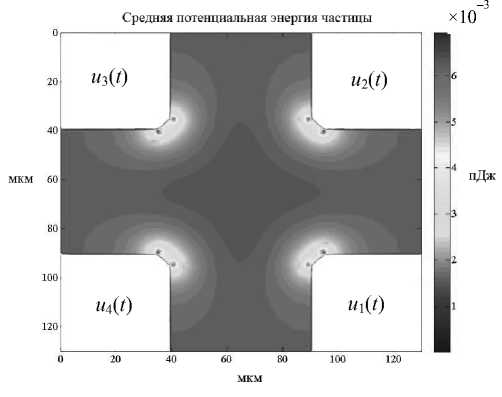
Рис. 2. Средняя потенциальная энергия частицы в диэлектрофоретической ловушке.
u 1( t ) = A cos( wt ), u 2( t ) = A cos( wt + π /2), u 3( t ) = = A cos( wt + π ), u 4 ( t ) = A cos( wt + 3 π /2); ε 1 = 78 ε 0 , ε 2 = = 2.75 ε 0 , a = 1 мкм, А =7 В, w = 105 с–1
гии во взаимно перпендикулярных направлениях МФЧ с квадрупольной конфигурацией показаны на рис. 1, б, в. Расчет выполнен для параметров системы: ε 1 = 78 ε 0 , ε 2 = 2.75 ε 0 , a = 1 мкм, граничные условия указаны на рис. 1. Из представленных распределений следует, что потенциальная энергия частицы в постоянном электрическом поле не имеет локального минимума в центре МФЧ, поэтому фиксация частицы в данной области невозможна. Для того чтобы между электродами МФЧ был минимум потенциальной энергии, необходимо использовать переменные электрические поля, для создания которых на электроды нужно подать одинаковые по амплитуде и сдвинутые по фазе сигналы. Усредненное по периоду распределение потенциальной энергии частицы приведено на рис. 2, из которого следует, что при использовании переменных электрических полей наблюдается минимум потенциальной энергии, что позволяет фиксировать частицу в данной области.
МАТЕРИАЛЫ И ОБОРУДОВАНИЕ
Моделирование электрических полей и распределения потенциальной энергии осуществлялось с использованием программы COMSOL Multi physics (Femlab). Распределение потенциальной энергии при приложении постоянных напряжений на электроды в квадрупольной конфигурации показано на рис. 1, а. Профили потенциальной энер-
Для исследований ДЭ на микрофлюидном чипе была создана экспериментальная установка на основе оптического микроскопа Axio Observer D1 (Carl Zeiss, Германия). В состав установки входят МФЧ для ДЭ, специально разработанное устройство управления и генератор сигналов GFG-8250A (GW-insTEK, Тайвань). Общий вид установки
а
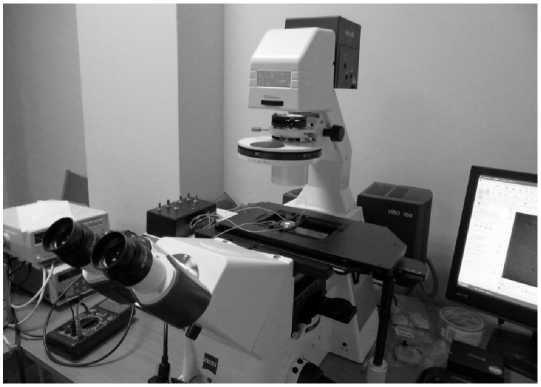
Рис. 3. Экспериментальная установка на базе оптического микроскопа Axio Observer D1 и микрочиповых технологий (а); МФЧ для ДЭ (б)
б

представлен на рис. 3, а. МФЧ для ДЭ был изготовлен из стекла марки К8, квадрупольная конфигурация электродов формировалась методами магнетронного нанесения металла (Cr), фотолитографии и травления. Затем на чип помещалась полидиметилсилоксановая (ПДМС) пленка (толщиной ~ 1 мм), в которой было сформировано отверстие для нанесения пробы (рис. 3, б). После загрузки пробы на ПДМС-пленку накладывалось покровное стекло, предотвращающее испарение пробы и защищающее от попадания пыли в ходе эксперимента. Для управления электрическими полями необходимо подавать на электроды ДЭ МФЧ сигналы, имеющие разные амплитуды и фазы. При этом условия захвата микрочастицы (биологического объекта) требуют подачи потенциалов, с равными амплитудами и сдвинутыми по фазе на π/2 друг относительно друга в диапазоне частот 0.1–1 МГц. Поэтому в качестве источника сигнала использовался генератор GFG-8250A, способный выдавать гармонический сигнал в диапазоне 0–10 В, 0–10 МГц, и электронная схема, построенная на операционных усилителях, обеспечивающая формирование четырех независимых сигналов со сдвигом фазы π/2 от генератора.
ЭКСПЕРИМЕНТАЛЬНЫЕ ИССЛЕДОВАНИЯ
Экспериментальные исследования проводились с 0.5 %-ным раствором KОН, в котором находились латексные полистирольные сферы диаметром 6 мкм в концентрации ~500 шт./мкл. Некоторые результаты исследований, полученные на экспериментальной установке, представлены на рис. 4. При отсутствии электрических полей наблюдалась
а
б
в

г


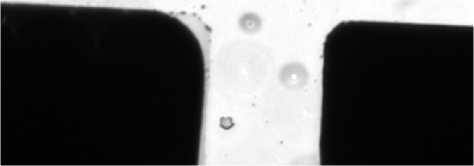
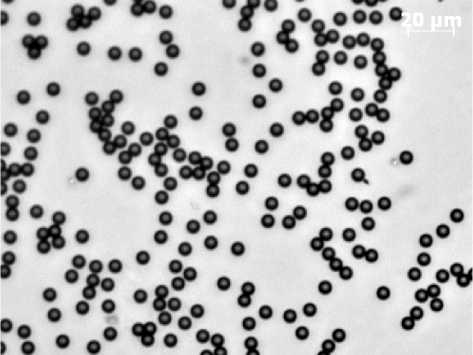
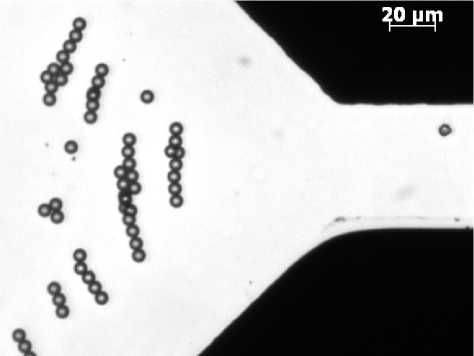
Рис. 4. Изображения полистирольных частиц в реакционной камере МФЧ для ДЭ.
Расположение частиц вне реакционной зоны при отсутствии (а) и наличии электрических полей (б); фиксация отдельной частицы (в) и группы частиц (г) в рабочей области микрочипа при ДЭ
хаотичность в расположении латексов в буферном растворе как в рабочей области МФЧ для ДЭ, так и вне нее (рис. 4, а). В случае наличия электрических полей вне рабочей зоны МФЧ латексы выстраиваются в ряды в соответствии с минимумами потенциальной энергии (рис. 4, б). В то же время в рабочей области ДЭ МФЧ наблюдается захват отдельных частиц (рис. 4, в) или группы, состоящей из нескольких частиц (рис. 4, г), вследствие наличия минимума потенциальной энергии в центре (на оси симметрии) электродов. Проведенные эксперименты показывают возможность управления движением микрочастиц методом ДЭ на МФЧ.
ЗАКЛЮЧЕНИЕ
Выполнен расчет и моделирование топологии микрофлюидного чипа для ДЭ. На основе оптического микроскопа Axio Observer D1 создана экспериментальная установка для исследований ДЭ микрочастиц на МФЧ. Разработана, изготовлена и апробирована управляющая электроника для микрочипа с системой квадрупольных электродов. Изготовлены экспериментальные образцы МФЧ для ДЭ. Проведены эксперименты по управлению движением полистирольных латексов (диаметром 6 мкм) методом ДЭ на МФЧ, продемонстрировавшие возможность фиксации микрочастицы или группы частиц в рабочей области чипа на длительное время, что может быть использовано для изучения биологических объектов в естественном состоянии методами микроскопии.
Исследования проведены в рамках аналитической ведомственной целевой программы "Развитие научного потенциала высшей школы", проект "Исследования и диагностика клеточных структур: новые методические подходы и инструментальные решения на основе сканирующей зондовой микроскопии и микрочиповых технологий" (N 4247) и в рамках Программы Carl Zeiss поддержки научноисследовательской работы молодых ученых вузов России (договор СПБГУ ИТМО 1/11 КЦ).


