Создание базы данных клинически значимых радиобиологических показателей опухолей и нормальных тканей для фотонной и нейтронной терапии
Автор: Селихова Е.А., Сагов И.Р., Сухих Е.С., Стахова О.М., Грибова О.В., Великая В.В., Старцева Ж.А., Бразовский К.С., Конев А.В., Сутыгина Я.Н.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Опыт работы онкологических учреждений
Статья в выпуске: 1 т.25, 2026 года.
Бесплатный доступ
Актуальность. Лучевая терапия является одним из основных методов лечения злокачественных новообразований, эффективность которого зависит от соотношения доз излучения, поглощенных опухолевыми и здоровыми клетками. Качество дозиметрического плана традиционно оценивается на основе физико-дозиметрических критериев, однако для достижения максимального прогнозируемого терапевтического эффекта необходимо учитывать радиобиологические аспекты. Существующее разнообразие радиобиологических моделей и отсутствие единого подхода к систематизации их численных параметров затрудняют их практическое применение, что делает актуальной задачу создания специализированной базы данных. Цель исследования – разработка базы данных клинически значимых радиобиологических показателей опухолей и нормальных тканей для фотонной и нейтронной терапии как единого специализированного инструмента для повышения точности дозиметрического планирования и прогнозирования клинических результатов лечения злокачественных новообразований. Материал и методы. Проведен анализ более 100 научных работ из открытых источников, посвященных расчетам клинически значимых радиобиологических показателей широко используемых радиобиологических моделей. В ходе исследования данные систематизированы с учетом различных режимов фракционирования, энергии и вида излучения, методик лучевой терапии, локализации и объема области облучения, а также индивидуальных особенностей пациентов. Результаты. Создана база данных клинически значимых радиобиологических показателей для фотонной и нейтронной терапии. На основе структурированных данных разработано веб-приложение с использованием языков программирования Python и JavaScript. Веб-приложение интегрировано в программное обеспечение «Калькулятор TCP/NTCP» и обеспечивает возможность хранения, быстрого поиска и анализа радиобиологических показателей. Заключение. Созданная база данных систематизирует клинически значимые радиобиологические показатели и предоставляет специалистам единый инструмент для прогнозирования вероятного результата лечения и оценки риска нежелательных последствий для критических органов и тканей. Данный инструмент может применяться в клинической практике, образовательных программах для подготовки специалистов в области медицинской физики и лучевой терапии, а также для углубленного изучения радиобиологических эффектов и разработки новых методов лечения.
База данных, фотонная терапия, нейтронная терапия, радиобиологические параметры, радиобиологические модели, радиобиологические показатели
Короткий адрес: https://sciup.org/140314351
IDR: 140314351 | УДК: 616-006-08:615.849.12 | DOI: 10.21294/1814-4861-2026-25-1-95-106
Creation of a database of radiobiological parameters of tumors and normal tissues based on clinical data of photon and neutron radiation therapy
Background. Radiotherapy is one of the primary methods for treating malignant neoplasms, and its effectiveness depends on the ratio of radiation doses absorbed by tumor and healthy cells. The quality of a dosimetric plan is traditionally assessed based on physical and dosimetric criteria; however, radiobiological aspects should be taken into account to achieve the maximum predicted therapeutic effect. The existing variety of radiobiological models and the lack of a unifed approach to systematizing their numerical parameters hinder their practical application, making the creation of a specialized database a relevant task. Objective: to develop a database of clinically signifcant radiobiological parameters for tumors and normal tissues for photon and neutron therapy as a unifed specialized tool to improve the accuracy of dosimetric planning and predict clinical treatment outcomes for malignant neoplasms. Material and Methods. An analysis of more than 100 scientifc publications from open sources dedicated to the calculation of clinically signifcant radiobiological parameters of widely used radiobiological models was conducted. During the study, data were systematized considering various fractionation regimens, radiation energy and type, radiotherapy techniques, localization and volume of the irradiated area, as well as individual patient characteristics. Results. A database of clinically signifcant radiobiological parameters for photon and neutron therapy was created. Based on the structured data, a web application was developed using the Python and JavaScript programming languages. The web application is integrated into the “TCP/NTCP Calculator” software and provides capabilities for storage, rapid search, and analysis of radiobiological parameters. Conclusion. The created database systematizes clinically signifcant radiobiological parameters and provides specialists with a unifed tool for predicting probable treatment outcomes and assessing the risk of adverse effects on critical organs and tissues. This tool can be used in clinical practice, educational programs for training specialists in medical physics and radiotherapy, as well as for the in-depth study of radiobiological effects and the development of new treatment methods.
Текст научной статьи Создание базы данных клинически значимых радиобиологических показателей опухолей и нормальных тканей для фотонной и нейтронной терапии
Лучевая терапия (ЛТ) является одним из наиболее распространенных и эффективных методов лечения злокачественных новообразований. Клиническая результативность этого метода во многом зависит от соотношения доз излучения, поглощенных опухолевыми и здоровыми клетками.
Процесс дозиметрического планирования направлен на поиск оптимального распределения поглощенной дозы в теле пациента. Качество дозиметрического плана традиционно оценивается на основе физико-дозиметрических критериев, таких как анализ распределения изодозовых линий, гистограммы «доза-объем» (ГДО) и расчет индексов конформности и однородности. Однако для достижения максимального прогнозируемого терапевтического эффекта при минимальном прогнозируемом повреждении нормальных тканей необходимо учитывать радиобиологические аспекты.
Прогнозируемый радиобиологический ответ зависит как от физико-дозиметрических параметров (вид и энергия излучения, методика ЛТ, суммарная доза, режим фракционирования, локализация и объем области облучения, распределение поглощенной дозы в облучаемом объеме), так и от индивидуальных особенностей пациента (радиочувствительность, физиологический статус, сопутствующие заболевания) [1]. Для комплексного учета этих факторов и количественного прогнозирования исхода лечения применяются радиобиологические модели.
Благодаря достижениям в диагностике злокачественных новообразований и совершенствованию методик облучения возрастает роль радиобиологической оптимизации (РО) дозиметрических планов. Это, в свою очередь, обусловливает необходимость анализа и учета клинически значимых показателей, лежащих в основе радиобиологических моделей.
Радиобиологические модели позволяют количественно прогнозировать влияние облучения на опухоль и нормальные ткани, рассчитывать поглощенную дозу, количество фракций в курсе лечения, а также оценивать биологический эффект облучения при разных режимах фракционирования. Следовательно, понимание биологического смысла и естественной вариабельности клинически значимых радиобиологических показателей, входящих в различные модели, становится критически важной составляющей прогнозирования радиобиологического ответа.
Однако существующее разнообразие радиобиологических моделей и отсутствие единого подхода к систематизации их численных параметров затрудняют их практическое применение [2]. Как следствие, актуальной задачей в современной радиобиологии и лучевой терапии является создание специализированной базы данных, охватывающей ключевые клинически значимые показатели радиобиологических моделей для фотонной и нейтронной терапии. Создание такой базы данных позволит повысить качество прогнозирования результатов лечения, оптимизировать индивидуальные дозиметрические планы ЛТ, систематизировать существующие численные значения, а также упростит доступ к информации для научных исследований и образовательных целей.
Материал и методы
Радиобиологические модели в ЛТ представляют собой теории, которые предсказывают эффекты ионизирующего излучения на опухолевые и нормальные ткани организма [3]. Эти модели, опирающиеся на математические расчеты, позволяют рассчитывать величину разовой поглощенной дозы, количество фракций в курсе лечения и оценить реакцию отдельных клеток на облучение. В клинической практике расчет дозы излучения и числа фракций в курсе лечения обеспечивает подведение к опухоли дозы, достаточной для ее уничтожения, при сохранении жизнеспособности и физиологиче- ской функции нормальных тканей и органов. Кроме того, радиобиологические модели позволяют сравнивать биологический эффект облучения при различных режимах фракционирования.
В фотонной терапии (ФТ) широко используются модели для преобразования физических величин, таких как поглощенная доза, в клинически значимые показатели, например: биологически эффективная доза (BED – Biologically Effective Dose), вероятность локального контроля над опухолью (TCP – Tumor Control Probability) и вероятность возникновения осложнений в нормальных тканях (NTCP – Normal Tissue Complication Probability). Эти показатели являются ключевыми в оптимизации планов облучения и индивидуализации лечения пациентов.
Выживаемость опухолевых клеток описывается кривой доза-эффект или кривой выживаемости. Самой простой и понятной моделью для описания кривой доза-эффект является линейно-квадратичная модель [4]. Данная модель зависит от экспоненциальной функции с линейноквадратичным показателем и выражается как
SFdD) = exp (-aD - {ID2) , (1) где SF(D) – доля выживших клеток после облучения поглощенной дозой D ; α и β – коэффициенты, специфичные для разных органов.
В современной ЛТ все больше применяются нестандартные подходы к фракционированию лечебной дозы излучения. Линейно-квадратичная модель (ЛКМ) позволяет легко перевести поглощенную дозу в нестандартном фракционировании в стандартное фракционирование в 2 Гр за фракцию. Данный параметр – это эквивалентная доза по 2 Гр за фракцию ( EQD2 – EQuivalent Dose in 2 Gy) и выводится из отношения BED [5] референсного режима фракционирования (режима фракционирования, который требуется преобразовать в классический) и классического (по 2 Гр за фракцию):
BED = 0(1 + ^-\ (2)
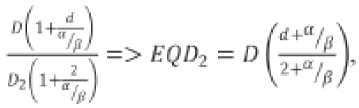
где D – полная поглощенная доза, Гр; d – доза
за фракцию, Гр.
Именно ЛКМ, в большинстве случаев, используется для описания эффектов от нестандартных подходов к фракционированию поглощенной дозы. И отношение α /β является ключевым параметром в данной модели для описания этих эффектов. Данный параметр выражает поглощенную дозу, при которой число клеток с ранним летальным исходом равно числу клеток с поздним летальным исходом. В большинстве случаев, в среднем, для опухолей и рано реагирующих нормальных тканей α/β составляет 10 Гр, для поздно реагирующих нормальных тканей – 3 Гр. Тем не менее данный параметр может варьироваться как для опухолей, так и для нормальных тканей, как среди населения, так и для индивидуального пациента в течение курса ЛТ.
Многие исследователи сделали огромный вклад в радиобиологическую оценку ЛТ. В открытых источниках можно найти различные подходы для расчета вероятности контроля опухоли и осложнения в нормальных тканях [6–14].
Модели вероятности контроля опухоли для ФЛТ
Большинство математических моделей TCP основаны на том, что число выживших клоногенных клеток (клеток, способных воспроизвести колонию), подчиняются распределению Пуассона. Одной из главных гипотез в вычислении вероятности контроля опухоли является то, что для продолжения роста опухоли достаточно одного жизнеспособного клоногена. Поэтому TCP можно выразить как [6]
(4) где N – общее количество клоногенных клеток; S – выжившая фракция клеток после облучения; тогда SN – это среднее число выживших клоногенов.
А для практического применения на основе математического распределения поглощенной дозы TCP можно выразить как [7]
где M – число вокселей (элементарный объем изображения); – относительный объем вокселя.
Для практических расчетов используются интервалы дифференциальной ГДО .
Некоторые TCP модели описываются логистической функцией, например, P. Okunieff et al. [8] использовали следующее выражение:
pt T) \ — —^^Pj^f^^SO^A^.
(6) где k связано с нормированным градиентом доза-ответ; k=TCD50/4γ50 ; TCD50 – доза ЛТ, необходимая для контроля 50 % объема равномерно облучаемой опухоли, Гр; γ50 – параметр ЛКМ, специфичный для опухоли и определяющий наклон кривой доза-ответ как тангенс угла этого наклона. Наглядное объяснение этих параметров приведено на рис. 1.
Эмпирическую логистическую функцию в своих моделях также используют H.A. Gay, A. Niemierko [9], и выглядит она следующим образом:
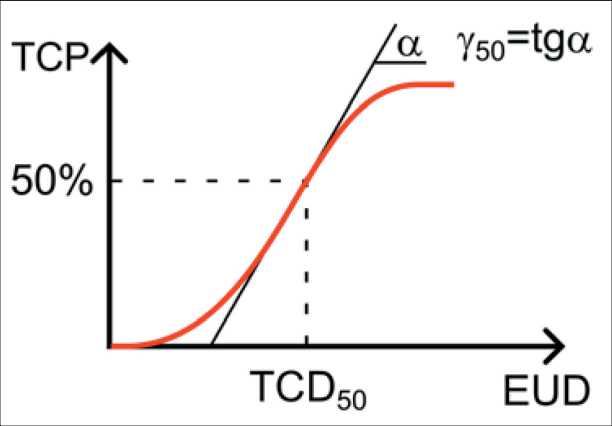
Рис. 1. Определение параметров TCD 50 и y 50 . Примечание: рисунок выполнен авторами
Fig. 1. Definition of parameters TCD 50 and y50. Note: created by the authors где EUD [10] – однородная эквивалентная доза, Гр.
Как можно заметить, модель TCP Немирко основана на эквивалентной однородной дозе ( EUD ). Даная концепция делает эту модель простой в практическом применении, так как она не требует больших математических вычислений. Функция EUD вычисляется следующим выражением:
(8) где – относительный объем, представляющий собой частичный i -й объем, который получает поглощенную дозу в абсолютном выражении (Гр). Поскольку относительный объем всей интересующей структуры соответствует 1, сумма всех частичных объемов будет равна 1. Параметр – это безразмерный параметр модели, который специфичен для определенного органа или мишени.
Модели вероятности осложнения в нормальных тканях при ФЛТ
Одна из самых простых моделей вероятности осложнения в нормальных тканях была предложена тем же Немирко [9]. Модель NTCP на базе EUD выглядит следующим образом:
где TD50 – поглощенная доза, которая при равномерном распределении по всему объему органа с вероятностью 50 %, вызовет осложнения в нормальных тканях (Гр).
Данная модель также основывается на концепте EUD . Параметр является специфичным для каждого органа. Здесь стоит отметить, что данный параметр для органов риска имеет отрицательные значения.
Еще одним подходом к расчету вероятности осложнений в нормальных тканях является модель Лаймана–Катчера–Бермана (LKB модель) [11], которая основана на работе Лаймана [12]. Ключевым ограничением модели Лаймана являлось предположение о равномерности облучения, тогда как в клинической практике нормальные ткани и органы обычно подвергаются неоднородному воздействию. В связи с этим были разработаны алгоритмы, преобразующие неоднородное распределение поглощенной дозы в однородное. Наибольшее признание получил алгоритм Лаймана–Катчера– Бермана, представленный в более доступной интерпретации, предложенной Моханом в 1992 г. [13]. Согласно данной формулировке, выражение NTCP в модели LKB выглядит следующим образом:
хг
NTCP ^— ff^в dxs(10)
гпТРлп(11)
Dc„ = OX")2.(12)
где Deff – поглощенная доза, которая при равномерном распределении по всему объему приведет к такому же значению NTCP , как и фактическое неравномерное распределение поглощенной дозы, Гр; m – параметр наклона сигмоидной кривой выживаемости клеток; z – безразмерный параметр, специфичный для каждого органа. Стоить отметить, что Deff концептуально идентична EUD с параметром α = 1 / z . Для учета различий в поглощенной дозе за фракцию принято заменять Di эквивалентной дозой, доставляемой фракциями по 2 Гр, EQD2 .
Вероятность осложнения в нормальных тканях как для последовательной, так и для параллельной архитектуры строения органа описывает модель Келлмана [14]. Относительный вклад каждого типа архитектуры органа описывается параметром s , который равен единице для полностью последовательной архитектуры органа и нулю для полностью параллельной архитектуры. NTCP задается следующим уравнением:
ntcp = П - IL D - /WT-)1/^ (13)
где P(Di) – вероятность осложнения. Несмотря на то, что s -модель была разработана с использованием принципов механистической архитектуры тканей, на практике значения параметра s , найденные для обеспечения наилучшего соответствия клиническим данным, часто превышают теоретический максимум, равный единице, что побудило считать модель феноменологической [7].
Радиобиологические аспекты нейтронной терапии
Клинический опыт проведения терапии быстрыми нейтронами значительно меньше относительно опыта в ФТ [15], поэтому РО имеет особое значение. Терапия быстрыми нейтронами является способом повышения эффективности лечения опухолей, резистентных к редко ионизирующему излучению, и ее часто сочетают с ФТ [16, 17].
Для предупреждения осложнений в нейтронной и нейтронно-фотонной терапии (НФТ) применяются модели «время – доза – фракционирование» (ВДФ) и ЛКМ, рассмотренные в работах [18] и [19] на циклотроне У-120 со средней энергией ~6,3 МэВ.
Модель (модификация концепции Ellis [20]) ВДФ в терапии пучком быстрых нейтронов циклотрона У-120 со средней энергией 6,3 МэВ в случае равномерного режима фракционирования дозы имеет вид [21]:
ПДФ = 6,9Ated/1V U3, (14) где dH – однократная доза в терапии пучком быстрых нейтронов, Гр; N – число сеансов; x – средний временной интервал между сеансами, сут.
В планировании терапии быстрыми нейтронами, наряду с ЛКМ (формула 1), для предсказания реакции облучаемой ткани также применяется многомишенная модель (ММ) клеточной выживаемости [22]:
SF(D) = [1- (1 - e-1^)"1].
где SF(D) – доля выживших клеток после облучения поглощений дозой D ; D0 и n – радиобиологические параметры, характеризующие степень радиочувствительности клеток.
В качестве аналога фактора ВДФ в ЛКМ выступает «суммарный биологический эффект» [23]:
I “ (16)
Поэтому выражение для однократных доз, соответствующих полным курсам нейтронной терапии при ежедневном облучении, на основе ЛКМ и с учетом α H / β H = 45 [25], СЭ (предел толерантности нормальных тканей) = 720 [24] имеет следующий вид [19]:
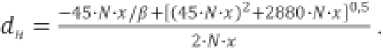
Параметры линейно-квадратичной модели для терапевтического пучка быстрых нейтронов циклотрона У-120 со средней энергией 6,3 МэВ: α H = 1,03 Гр-1; β H = 0,023 Гр-2 [21], которые необходимы для расчета зависимости относительной биологической эффективности (ОБЭ) для быстрых нейтронов от поглощенной дозы, а правильное определение ОБЭ, в свою очередь, влияет на выбор эффективных и безопасных режимов облучения [25]. Формула для ОБЭ выглядит следующим образом [26]:
ОБЭ= - ^ln
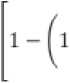
И
где D 0γ , D0H и n – радиобиологические параметры, определяющие радиочувствительность облучаемой ткани для нейтронов и гамма-излучения; DH – некоторая произвольная доза нейтронов; D γ – поглощенная доза фотонного излучения.
ОБЭ зависит от энергии быстрых нейтронов (различные источники нейтронов) и лежит в пределах от 2 до 6 [15].
Результаты
Перечень клинически значимых радиобиологических показателей, вошедших в разработанную базу данных, был составлен по результатам исследования более 100 работ из открытых источников. Работы, вошедшие в базу данных [27–59], идентифицированы из открытых источников с использованием электронных научных библиотек и поисковых систем Google Scholar, PubMed, Science Direct, ResearchGate с комбинациями поисковых терминов «neutron radiation therapy», «photon radiation therapy», «radiobiologic models», «tumor control probability», «normal tissue complication probability», «TCP, NTCP calculation» и др. Поиск включал статьи на русском и английском языках.
По клиническим факторам в исследование включались пациенты с любым типом опухоли, независимо от ее локализации, стадии и гистологии. Распределение по видам лучевой терапии: фотонная и нейтронная. Методика облучения: кон- венциональная, 3D-конформная, лучевая терапия с модуляцией интенсивности фотонного излучения, объемно-модулированная лучевая терапия. Исследования должны были содержать расчетные значения α, β или α/β, EQD2, BED, γ50, EUD, TD50, ВДФ, ОБЭ, TCP, NTCP. Клиническая конечная точка (например, местный/локальный контроль, выживаемость, биохимический контроль), на которой основывались эти оценки, не ограничивалась. В случае терапии быстрыми нейтронами: исследования сочетанной ЛТ (НФТ), комбинированной (терапия быстрыми нейтронами после хирургического вмешательства), а также нейтрон-захватной включались как отдельные результаты.
Результатом данной работы стало веб-приложение «База данных радиобиологических параметров для фотонной и нейтронной лучевой терапии» [60] (языки программирования: Python, JavaScript) для сбора и структурирования большого объема данных радиобиологических показателей опухолей и нормальных тканей на основе клинических данных, которые могут быть использованы для прогнозирования результатов фотонной и нейтронной терапии. Схема БД представлена на рис. 2.
На данный момент БД включает клинически значимые радиобиологические показатели фотонной и нейтронной ЛТ. Фотонная ЛТ является наиболее распространенным видом ЛТ и поэтому привлекает внимание многих исследователей. Наиболее исследованными радиобиологическими
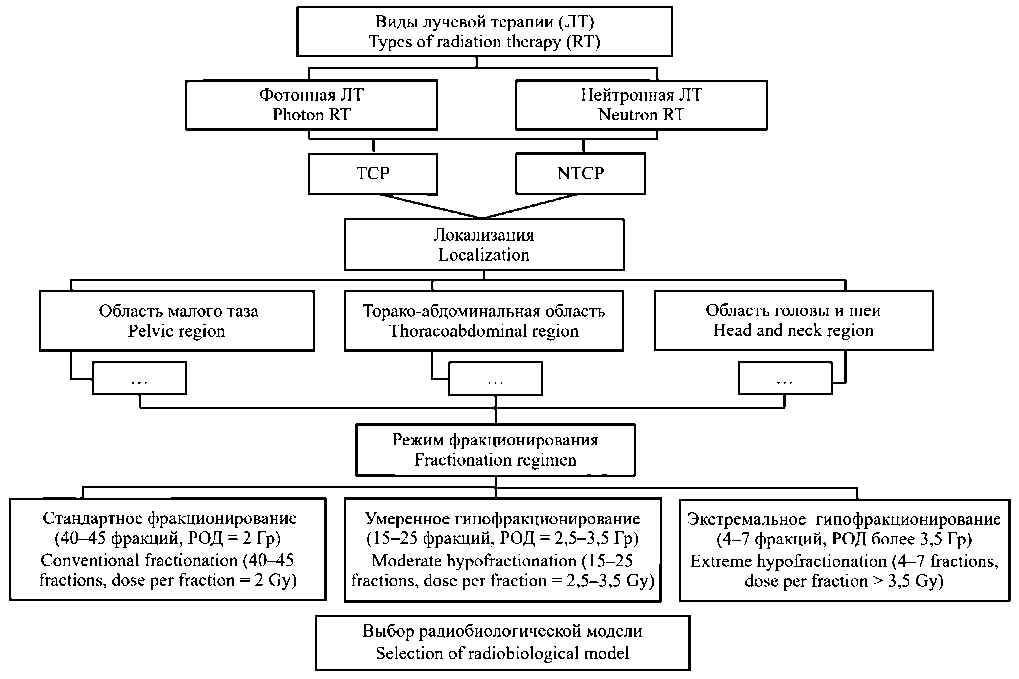
Рис. 2. Структура веб-приложения «База данных радиобиологических параметров опухолей и нормальных тканей для фотонной и нейтронной лучевой терапии». Примечание: рисунок выполнен авторами
Fig. 2. Structure of the web application “Database of radiobiological parameters of tumors and normal tissues for photon and neutron radiation therapy”. Note: created by the authors
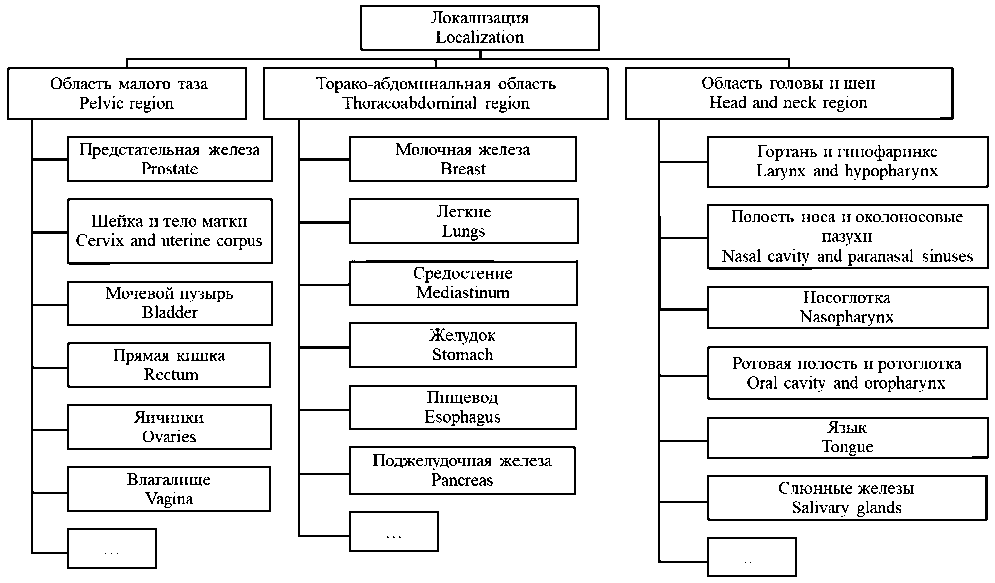
Рис. 3. Локализации с выпадающим списком опухолей и нормальных тканей в веб-приложении «База данных радиобиологических параметров опухолей и нормальных тканей для фотонной и нейтронной лучевой терапии».
Примечание: рисунок выполнен авторами
Fig. 3. Localizations with a drop-down list of tumors and normal tissues in the web application “Database of radiobiological parameters of tumors and normal tissues for photon and neutron radiation therapy”. Note: created by the authors
показателями для фотонной ЛТ являются показатели моделей Пуассона [8] и Немирко [9] – для вероятности контроля опухоли; модели Лаймана– Катчера–Бермана [11] и Немирко [9] – для вероятности осложнения в нормальных тканях, поэтому радиобиологические показатели данных моделей включены в БД.
Для удобства пользования данной базой и быстроты поиска нужного радиобиологического показателя клинические данные разделены по трем локализациям с выпадающим списком типов опухолей и нормальных тканей (рис. 3). Также некоторые клинически значимые радиобиологические показатели разделены по режимам фракционирования, в которых они были получены: стандартный режим (разовая доза (РД) 2 Гр), умеренное гипофракционирование (РД 2,5–3,5 Гр) и экстремальное гипофракционирование (РД более 3,5 Гр).
Нейтронная ЛТ в данной работе представлена как дистанционная терапия на пучках быстрых нейтронов, где в качестве критериев для оценки эффективности описаны: локальный контроль над ростом опухоли (TCP), относительная биологическая эффективность (ОБЭ), фактор «время – – доза – фракционирование» (ВДФ), вероятность возникновения осложнений в нормальных тканях (NTCP), показатель выживаемости.
Все данные, приведенные в данной работе, ссылаются на открытые источники [27–59], эти источники также приведены в базе данных для более подробного ознакомления с интересующими параметрами.
Веб-приложение для работы с базой данных клинически значимых радиобиологических показателей опухолей и нормальных тканей для фотонной и нейтронной ЛТ интегрировано в программное обеспечение по расчету локального контроля над ростом опухоли и вероятности пострадиационных осложнений в нормальных тканях «Калькулятор TCP/NTCP» [61], разработанное Томским политехническим университетом.
Права доступа пользователей разграничиваются следующим образом:
-
1. Роли пользователей (различные группы с определенными правами):
– администратор: доступ ко всем функциям приложения, включая управление пользователями и редактирование базы данных, но без права настройки приложения и изменения/удаления радиобиологических данных;
– исследователь/пользователь: доступ только к просмотру и анализу данных, без возможности их редактирования.
-
2. Авторизация (первичная регистрация, использование пароля) + интеграция с внешними системами (через ПО «Калькулятор TCP/NTCP», свидетельство о государственной регистрации программы для ЭВМ № 2023664910 от 10.07.2023) – возможность использования внешней системы аутентификации.
-
3. Учет и анализ действий пользователей. Все действия пользователей, такие как «запрос на добавление, изменение или удаление данных», фиксируются.
Заключение
Учет объемных характеристик опухоли и нормальных тканей при дозиметрическом планировании лучевой терапии повышает эффективность лечения и снижает риск развития побочных эффектов (радиационных осложнений). Основная цель создания базы данных клинически значимых радиобиологических показателей опухолей и нормальных тканей, а также ее интеграции в вебприложение – предоставить специалистам единый инструмент для систематизированного хранения и использования радиобиологических данных, что позволит более точно прогнозировать исход лечения и оценивать риск нежелательных последствий для критически важных органов и тканей с учетом индивидуальных особенностей пациента. Разработанная база данных основана на анализе широкого спектра клинических исследований и включает


