Создание исходного материала для гибридной селекции лука батуна с устойчивостью к пероноспорозу
Автор: Монахос М.Г., Эйдлин Я.Т., Монахос С.Г.
Журнал: Овощи России @vegetables
Рубрика: Селекция, семеноводство и биотехнология растений
Статья в выпуске: 1 (87), 2026 года.
Бесплатный доступ
Актуальность. Целью работы было – создание исходного материала для селекции F1 гибридов лука батуна с устойчивостью к пероноспорозу. Материал и методика. Проведена межвидовая гибридизация с использованием A. Roylei (донор доминантного гена устойчивости Pd1) и A. galanthum (донор Gal-типа цитоплазмы, индуцирующей ЦМС) с последующими насыщающими скрещиваниями с A. Fistulosum (сорт «Ishikura» и линией из гибрида «Katana F1»). Оценку фертильности пыльцы проводили методом ацетокарминового окрашивания с подсчетом доли окрашенных зерен в трех полях зрения. Оценку устойчивости/восприимчивости полученных популяций проводили на искусственном инфекционном фоне (инокулюм патогена Peronospora destructor в концентрации 3*106 спор/мл), а также с использованием молекулярного SCAR-маркера DMR1. Результаты. Установлено, что гибриды первого поколения (A. roylei × A. fistulosum) и (A. galanthum × A. fistulosum) характеризуются крайне низкой фертильностью пыльцы (17,9% и 14,9% соответственно), обусловленной нарушениями мейоза при отдаленной гибридизации. Однако однократное беккроссирование гибрида (A. roylei × A. fistulosum) с A. fistulosum привело к полному восстановлению мужской фертильности, и она составила 95,4%. Фенотипический анализ на инфекционном фоне выявил отсутствие симптомов поражения пероноспорозом у всех растений популяций BC1 и потомства беккросных растений, что не соответствует ожидаемому моногенному доминантному расщеплению. При этом ПЦР-анализ с маркером DMR1 продемонстрировал амплификацию неспецифичных фрагментов (350, 490 и 580 п.н.) у растений BC1. В результате исследования показана возможность передачи в геном лука батуна ЦМС-индуцирующего фактора от A.galanthum и гена устойчивости Pd1 от A. roylei. Отсутствие расщепления по устойчивости к пероноспорозу при беккроссировании восприимчивыми образцами Allium fistulosum, а также в самоопыленном потомстве беккроссных растений позволяет выдвинуть гипотезу, о наследственном факторе в цитоплазме Allium roylei препятствующем образованию зигот, с рецессивным гомозиготным генотипом pd1pd1. Эту гипотезу подтверждает факт обнаружения восприимчивых растений в потомствах, где устойчивые растения гибрида A. roylei × A. fistulosum использовали в качестве опылителей на растения с цитоплазмой A.galanthum и A. fistulosum. Полученные беккроссные популяции представляют ценный материал для селекции гетерозисных гибридов лука батуна.
Лук батун, Allium roylei, Allium galanthum, мужская стерильность, ПЦР, межвидовая гибридизация
Короткий адрес: https://sciup.org/140314218
IDR: 140314218 | УДК: 635.264:631.526:631.524.86 | DOI: 10.18619/2072-9146-2026-1-66-74
Development of Initial Material for Hybrid Breeding of Welsh Onion with Resistance to Downy Mildew
Relevance. The aim of our work was to create initial material for the breeding of F1 hybrids of Welsh onion (Allium fistulosum) with resistance to downy mildew. Materials and Methods. To achieve this goal, interspecific hybridization was carried out using A. roylei (donor of the dominant resistance gene Pd1) and A. galanthum (donor of the Ga-type cytoplasm inducing CMS), followed by backcrossing with A. fistulosum (cultivar 'Ishikura' and self-pollinated lines from the 'Katana F1' hybrid). Pollen fertility was assessed using the acetocarmine staining method, calculating the proportion of stained grains in three fields of view. Evaluation of resistance/susceptibility of the obtained populations was conducted under an artificial infection background (inoculum of the pathogen Peronospora destructor at a concentration of 106 spores/ml), as well as using the molecular SCAR marker DMR1. Results. It was found that first-generation hybrids (A. roylei × A. fistulosum) and (A. galanthum × A. fistulosum) are characterized by extremely low pollen fertility (17.9% and 14.9%, respectively), caused by meiotic disturbances during distant hybridization. However, a single backcross of the hybrid (A. roylei × A. fistulosum) with A. fistulosum led to a complete restoration of male fertility in the BC1 population, where the average fertility was 95.4%. Phenotypic analysis under the artificial infection background revealed an absence of downy mildew symptoms in all plants of the BC1 and its populations containing genetic material from A. roylei, which does not correspond to the expected monogenic dominant segregation. At the same time, PCR analysis with the DMR1 marker demonstrated the amplification of non-specific fragments (350, 490, and 580 bp) in BC1 plants, indicating structural rearrangements in the introgression region of the Pd1 gene. The study demonstrated the possibility of transferring the CMS-inducing factor from A. galanthum and the Pd1 resistance gene from Allium roylei into the genome of Welsh onion. The obtained BC populations represent valuable material for the breeding of heterotic Welsh onion hybrids resistant to downy mildew.
Текст научной статьи Создание исходного материала для гибридной селекции лука батуна с устойчивостью к пероноспорозу
Оригинальная статья / Original article УДК:635.264:631.526:631.524.86
Лук батун (Allium fistulosum L., 1753) – многолетнее травянистое растение, возделывается ради сочной зелёной части ложного стебля (пера) для пищевых и пряных целей. Растение родом из восточной части Центральной Азии, а именно Алтайских гор и озера Байкал. В сельском хозяйстве Китай занимает первое место по посевным площадям лука батуна (свыше 500 тыс. га). Япония и Южная Корея также имеют первенство по площадям выращивания, с площадями по 25 тыс. га [1]. В Европе и Северной Америке лук-батун встречается реже, однако в последние годы как салатный лук он привлекает внимание селекционеров и фермеров своей высокой урожайностью зелёной массы и холодостойкостью. Культура характеризуется ранним началом вегетации весной, высоким выходом зелёной массы, до 90% урожая приходится на перо, что значительно выше, чем у репчатого лука, а также богатым витаминным составом листьев
Пероноспороз луковых или ложная мучнистая роса – грибное облигатно-биотрофное заболевание, возбудителем которого является оомицет Peronospora destructor (Berk.) Casp. При благоприятных условиях (высокая влажность и низкие температуры) патоген быстро распространяется по листу, образуя характерный серо-пурпурный пушистый налёт. Инфицирование листьев приводит к их пожелтению, некрозам и гибели, что существенно снижает фотосинтез и урожайность растения. По оценкам фитоэпидемиологов, пероноспороз может наносить чрезвычайно серьёзный ущерб. При полном развитии эпифитотии потери урожая репчатого лука достигают 50-75%. Для контроля болезни обычно требуются множественные обработки фунгицидами (до 10-12 раз за сезон), что обременительно и нежелательно с экологической точки зрения. Таким образом, пероноспороз остаётся одной из наиболее опасных болезней для луковых культур, включая лук батун, и требует поиска длительных решений [2, 3].
Устойчивость к пероноспорозу у Allium roylei впервые была обнаружена и описана Van Der Meer и De Vries оценкой на инфекционном фоне. Результаты их опыта показали, что симптомы поражения в условиях инфекционного фона полностью отсутствуют как у самого Allium roylei , так и у его гибридного потомства от лука репчатого [4]. Позднее A. Kofoet , в результате скрещивания устойчивого Allium roylei и сорта репчатого лука «Jumbo» и дальнейшим беккроссом с репчатым луком в качестве повторного родителя, установил что устойчивость контролируется доминантным геном Pd [5]. Более подробно ген Pd был изучен Хрусталёвой и соавторами. Проведя GISH анализ, ею было определено, что ген локализован на 3 хромосоме в дистальной части её длинного плеча [3]. Подобный подход межвидовой гибридизации, может быть применён и к луку батуну, для получения устойчивых к пероноспорозу гибридов.
Гибридная селекция и семеноводство лука батуна подразумевает использование ЦМС систем, для получения 100% гибридных семян, упрощения семеноводства и дополнительной биологической защиты авторских прав. Учитывая то, что внутри вида нет изученных и используемых ЦМС систем, необходима передача этого признака из близкородственных видов.
Наиболее перспективным является поиск и передача ЦМС системы контролируемой исключительно цитоплазматическим фактором, что исключает необходимость в создании генотипов закрепителей стерильности. Это отражается в отсутствии необходимости анализирующих скрещиваний или маркер-опосредованного отбора генов восстановле-ния/закрепления стерильности. Потомства, полученные от таких скрещиваний, будут полностью стерильными, вне зависимости от выбора отцовского компонента в качестве опылителя.
Наиболее перспективным источником ЦМС системы может служить близкродственный лук молочноцветковый (Allium galanthum). Цитоплазма лука молочноцветкового может стать хорошим инструментом для селекции гибридного лука батуна. Впервые она была передана в результате межвидовой гибридизации в репчатый лук. Фенотипически цветки растения молочноцветкового лука отличаются скручиванием сегментов околоцветника вверх и тычиночными нитями без пыльников. Это уникальные морфологические признаки, отличающие ЦМС лука молочноцветкового от стерильности S-, R- и Т-типа лука репчатого.
Исследования M.J. Havey показали, что аллели, восстанавливающие мужскую фертильность у лука, обладающего S-цитоплазмой, не восстанавливали мужскую фертильность у лука с ЦМС из цитоплазмы лука молочноцветкового. Это подтверждает, что ЦМС, индуцированная цитоплазмой лука молочноцветкового, имеет другой генетический фон, отличный от S-типа ЦМС лука и имеет цитоплазматическое наследование [6]. Вместе с тем, командой Yamashita был найден внутривидовой ген, обозначенный как Rf, который в доминантном аллельном состоянии восстанавливает фертильность у растений лука батуна. GISH анализ показал, что ген локализован на 5 хромосоме лука молочноцветкового [7].
Целью настоящего исследования является передача гена устойчивости к ложной мучнистой росе (Pd1) из Allium roylei в лук батун. А также испытание лука молочноцветкового ( Allium galanthum ) в качестве донора специфичной ЦМС в лук батун.
В рамках исследования будет проведена меживдовая гибридизация лука батуна с Allium roylei и Allium galanthum ; Оценка фертильности полученных популяций межвидовых гибридов; Оценка устойчивости к пероноспорозу популяций, с геномом Allium roylei ; Изучение факторов наследования целевых признаков ЦМС и устойчивости к ложной мучнистой росе.
Материалы и методыРастительный материал
Представители видов лука, используемые как доноры признаков были взяты в качестве исходного материала из коллекции ООО «Селекционная станция имени Н.Н. Тимофеева». Allium galanthum – донор цитоплазматической мужской стерильности (ЦМС) и Allium roylei – донор гена устойчивости к пероноспорозу (Pd1).
Сорт Allium fistulosum «Ishikura/Long white» был выбран на ранних стадиях селекционного процесса в 2019 году, так как является одним из лучших коммерческих сортов лука батуна ( Allium fistulosum ). Скороспелый сорт, урожайность 1,4 кг/м2, устойчив к фузариозной гнили, розовой гнили и пожелтению листьев.
Гибрид лука батуна «Katana F1» (Sakata) – один из лучших коммерческих F1 гибридов лука батуна использовали для возвратного скрещивания. Обладает прекрасными хозяйственно ценными признаками среди гибридов лука батуна на момент 2023 года. Скороспелый сорт, урожайность до 7 кг/м2, устойчив к стрелкованию и полеганию. Для селекционного процесса использовали фертильное растение из потомства F2. Также на основе «Katana F1» создана чистая линия лука батуна путём самоопыления и отбора наилучших форм.
Имеющиеся и полученные семена растений лука высевали в кассеты с ячейками размером 3,2×3,2×4,0(Д×Ш×В см).Через 10 дней после прорастания растения переваливали в горшки 11×8 (ДМ×В см).Далее растения в возрасте 20-30дней с момента прорастания пересаживали в открытый грунт на опытный участок со схемой посадки 70×20 см.Растения популяции (( A. roylei × A. fistulosum ) × A. fistulosum ) переваливали из кассет в горшки 26×20(ДМ×В см) и расставляли в открытом грунте без высадки.В качестве субстрата использовался грунт торфяной универсальный «Агробалт».
Определение фертильности межвидовых гибридов
Жизнеспособность пыльцы оценивали у 4 растений популяции ( A. roylei × A. fistulosum ), 10 растений популяции ( A. galanthum × A. fistulosum ) и 20 растений популяции [( A. roylei × A. fistulosum ) × A. fistulosum ] методом ацетокармино-вого окрашивания. Цветки собирали из зонтиков, у которых распустилось по меньшей мере 2/3 всех цветков. С одного зонтика каждого растения было отобрано по 3 цветка. Жизнеспособность пыльцы проверялась в течение одного часа после сбора цветков, чтобы не допустить обезвоживания пыльцы. С каждого из трёх цветков одного растения было отобрано по одному пыльнику, эти 3 пыльника помещались на предметное стекло в 30 мкл окрашивающего раствора (ацетокармин 0,5%). Пыльники в окрашивающем растворе накрывали покровным стеклом, после чего на покровное стекло оказывали небольшое давление, для разрушения оболочки пыльника и выхода в окрашивающий раствор пыльцевых зёрен. Полученные препараты были просмотрены на электрическом световом микроскопе. В препаратах жизнеспособная пыльца окрашивалась в красный цвет тогда как нежизнеспособная пыльца оставалась неокрашенной или окрашивалась слабо. В каждом препарате было посчитано общее число пылевых зёрен и окрашенных, то есть фертильных, подсчёт вёлся в трёх разных полях зрения в каждом препарате.
Анализ устойчивых к пероноспорозу форм
Маркер-опосредованный отбор применяли для выделения устойчивых к пероноспорозу растений, обладающих геном Pd1, а также определения его аллельного состояния. Выделение ДНК проводилось CTAB-методом [8]. Для выделения использовали 150-200 мг свежей ткани молодых листьев. Амплификация проводилась в ПЦР-амплификато-ре Thermal Cycler C1000 Touch (Bio-Rad). Молекулярно-генетический анализ и дифференциация генотипов в расщепляющихся популяциях была проведена с использованием маркера DMR1 – SCAR-маркера ядерного гена устойчивости к пероноспорозу Pd1 [9]. Молекулярный маркер DMR1 гена устойчивости к пероноспорозу Pd1 был амплифицирован с парой праймеров, прямым DMR1-F 5'-TGAGGCTCAAGTTGACATG-3' и обратным DMR1-R 5'-TTCGTAGCAGCATCAAGGTG-3' при температуре отжига 65 °С. Амплифицируемый ДНК-фрагмент длиной 505 bp. сцеплен с доминантным Pd1-аллелем, ДНК-фрагмент длиной 438 bp. с рецессивным аллелем pd1. Разделение ДНК-продуктов амплификации проводили электрофорезом под напряжением 100 V в течение 1 часа 15 минут в 1,5% агарозном геле. ДНК-фрагменты окрашивали флуоресцентным красителем GelRed (Biotium, USA). Визуализация и фотодокументация разделенных электрофорезом фрагментов ДНК, продуктов амплификации, осуществлялась с помощью гель-документирующей системы
В соответствии с методикой V.Buloviene и E.Surviliene,про-водились испытания на искусственном инфекционном фоне, для идентификации устойчивых растений полученных от скрещивания популяций, имеющих ген Pd1 [10].C листьев,пора-жённых пероноспорозом, растений лука репчатого,произрас-тавшего на одном из опытных участков,методом смыва был создан инокулюм Peronospora destructor с концентрацией 3*106спор/мл.Популяции растений,среди которых проводился отбор,опрыскивали инокулюмом Peronospora destructor в начале и конце дня в течение семи дней.Помимо межвидовых гибридов,среди которых проводили отбор, также на опытном участке были высажены и обработаны восприимчивые к пероноспорозу растения лука батуна сорта «Ishikura» и лука репчатого сорта «Exhibition» в качестве индикаторов заражения патогеном на опытном участке.
Результаты
Устойчивость к пероноспорозу у межвидовых гибридов с Allium roylei
В 2020 году была проведена межвидовая гибридизация растений Allium roylei с луком батуном сорта «Ishikura»,мате-ринским компонентом скрещивания использовали Allium roylei , так как у него цветки с открытым типом и легко проводить кастрацию и гибридизацию.От скрещивания получили 4 гибридных растения.У гибридов наблюдался сильный гетерозисный эффект в сравнении с обоими родителями,они формировали крупные длинные листья,а растения были более ветвистыми со сложными луковицами (рис.1).Однако они отличались более поздним переходом к стрелкованию в сравнении с

Рис. 1. Растения луков, где A – материнское растение Allium roylei; B – межвидовой гибрид (A. roylei × A. fistulosum); С – отцовское растение A. fistulosum Fig. 1. Allium plants, where A – maternal plant Allium roylei; B – interspecific hybrid (A. roylei × A. fistulosum); C – paternal plant A. fistulosum
2020 год
2021 год
A. roylei (PdPd)
(Pdpd)
[(A roylei * A. fistulosum) х A. fistulosum]
^(Pdpd)/ ^(pdpd)
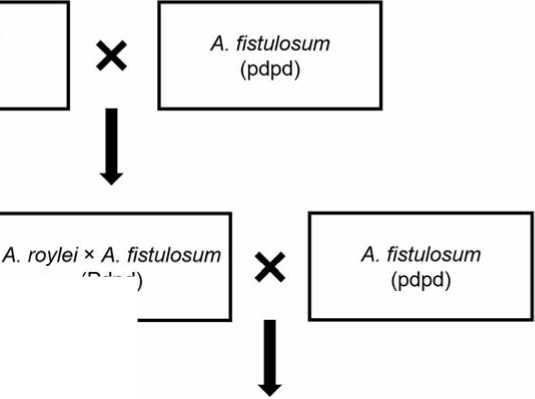
Рис. 2. Схема гибридизации 2020 и 2021 года, где в скобках под генотипом растений обозначено предполагаемое аллельное состояние гена устойчивости к пероносопорозу Pd1, в соответствии с наследованием по законам Менделя
Fig. 2. Hybridization scheme for 2020 and 2021. In parentheses below the plant genotype, the putative allelic state of the downy mildew resistance gene Pd1 is indicated, according to Mendel inheritance patterns луком батуном и занимали промежуточное положение,так как растения Allium roylei стрелковались еще позже. Самоопыление растений F1 гибридов с помощью шмелей в изодомике оказалось безуспешным,все растения были стерильными и семян F2 потомства получить не удалось.
В 2021 году провели беккроссное скрещивание гибрида ( A. roylei × A. fistulosum ), в качестве отцовского родителя был взят представитель потомства F 2 , полученного от самоопыления лука батуна гибрида «Katana F 1 ». В дальнейших скрещиваниях в качестве лука батуна как компонента скрещивания будет представлено растение F 2 из гибрида «Katana F 1 ». От беккросса получили 23 семени. Растения популяции [( A. roylei × A. fistulosum ) × A. fistulosum ] в дальнейшем были изолированы и каждом растении было проведено самоопыление с использованием ватного диска.
Схема гибридизации представлена на рисунке 2.
В 2022 году было проведено свободное опыление 20 растений [( A. roylei × A. fistulosum ) × A. fistulosum ] и было получено 260 семян. Учитывая, что ген Pd1 находится в гетерозиготном состоянии у каждого представителя скрещиваемой популяции, в потомстве по этому гену теоретически должно происходить расщепление 1:2:1 (1Pd1Pd1:2Pd1pd1:1pd1pd1) (рис.3.).
Так же для анализа влияния цитоплазмы на работу гена устойчивости к пероноспорозу ( Pd1 ), был проведён беккросс растения генотипа [( A. roylei × A. fistulosum ) x A. fistulosum ] с A. fistulosum , при этом лук батун ( Allium fistulosum ) использовался уже как стерильный материнский компонент скрещивания. В результате скрещивания было получено 27 семян, схема скрещивания представлена на рисунке 4.
|
2022 год |
[(A. royleix A. fistulosum) x A. fistulosum] 72(Pdpd) / ^(pdpd) |
X |
[(A roylei x A. fistulosum) x A. fistulosum] 72(Pdpd) / 72(pdpd) |
I
[((A roylei x A. fistulosum) x A. fistulosum) x ((A. royleix A. fistulosum) * A. fistulosum)]
1/2(Pdpd) / %(pdpd) / %(PdPd)
Рис. 3. Схема свободного опыления между 20 растениями межвидового гибрида [(A. roylei × A. fistulosum) × A. fistulosum] Fig. 3. Scheme of open pollination among 20 plants of the interspecific hybrid [(A. roylei × A. fistulosum) × A. fistulosum]
Наследование мужской стерильности при гибридизации Allium galanthum и Allium fistulosum
В 2020 году было проведено первое скрещивание Allium galanthum и Allium fistulosum в качестве пестичного компонента. Далее в 2021 году проводился отбор лучших форм и беккросс с Allium fistulosum в качестве повторного родителя схема скрещиваний представлена на рис.5.
также тип цитоплазмы – N – нормальная, обеспечивающая фертильность; Ga – специфичный для A. galanthum тип цитоплазмы, вызывающий мужскую стерильность.
Было проведено скрещивание растения популяции ( A. galanthum × A. fistulosum ) с ядерно-цитоплазматической мужской стерильностью и р астения популяции [ A. roylei × ( A. galanthum × A. fistulosum )] для оценки работы генов, отвечающих за устойчивость и ядерно-цитоплазмати-
2022 год
A. fistulosum
(pdpd)
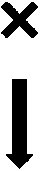
[(A roylei * A. fistulosum) * A. fistulosum]
(Pdpd)
[A. fistulosum * ((A. roylei * A. fistulosum) x A. fistulosum)]
1/2(Pdpd) / ^(pdpd)
Рис. 4. Схема беккросса межвидового гибрида [(A. roylei × A. fistulosum) × A. fistulosum] и A. fistulosum, где последний использует в качестве материнского компонента Fig. 4. Backcross scheme of the interspecific hybrid [(A. roylei × A. fistulosum) × A. fistulosum] with A. fistulosum, where the latter is used as the maternal component
Примечание: в скобках под генотипом растений обозначено предполагаемое аллельное состояние гена восстановителя фертильности Rf – доминантный аллель, восстанавливающий фертильность, rf – рецессивный аллель;
ческую мужскую стерильность в одной популяции, а также хозяйственно ценных качеств присущих луку батуну. Схема получения конечного генотипа с целевыми признаками представлена на рис. 6. Было получено 24 семени.
A. gala nth um
A. galanthum x A. fistulosum

(Ga rfrf)
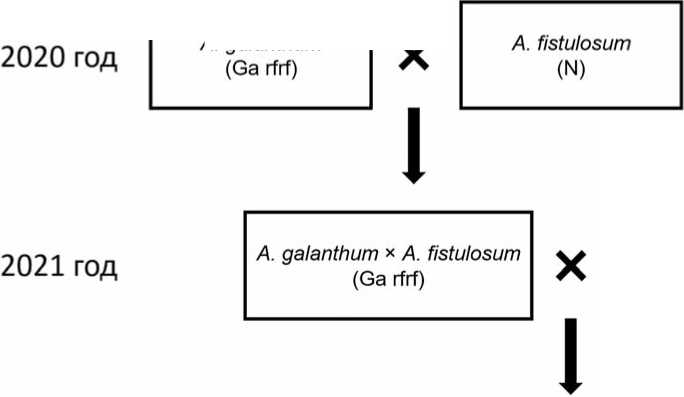
Рис. 5. Схема получения межвидовых гибридов (A. galanthum × A. fistulosum) и первого поколения беккроса
Fig. 5. Scheme for obtaining interspecific hybrids (A. galanthum × A. fistulosum) and the first backcross generation Note: In parentheses below the plant genotype, the putative allelic state of the fertility restorer gene is indicated: Rf – dominant allele restoring fertility, rf – recessive allele;
also the cytoplasm type: N – normal, ensuring fertility; Ga – A. galanthum-specific cytoplasm type inducing male sterility


