Созревание Оствальда как механизм иерархической структурной эволюции фосфата титана
Автор: Антон Дмитриевич Абрамян, Данил Андреевич Манько, Валерия Петровна Захарченкова, Олег Игоревич Большаков, Вячеслав Викторович Авдин
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Физическая химия
Статья в выпуске: 4 т.17, 2025 года.
Бесплатный доступ
Контроль роста нано- и микроструктур оксидных материалов металлов становится все более актуальным, поскольку позволяет тонко регулировать их функциональные свойства. Поэтому в области материаловедения активно разрабатывается множество методов направленного синтеза субстратов с развитой морфологией, высокой степенью кристалличности и значительной удельной поверхностью. Несмотря на значительные успехи в этой области, необходимо отметить отсутствие единого методологического подхода и, как следствие, целостного представления о структурообразовании сложных и иерархически-структурированных материалов. Фосфаты титана (TiP) – обширная группа материалов, состоящих из распространенных элементов, которые представляют собой универсальную платформу для создания материалов с регулируемой морфологией и элементным составом. Благодаря простоте синтеза и модификации на их основе получены различные сорбенты, катализаторы, электроды для накопителей энергии и полимерные добавки. Формирование иерархических структур на основе фосфатов титана, существенно превосходящих по сложности регулярные микро- и наноструктурированные, позволило получить субстраты со значительным приростом функциональности. Несмотря на перспективность исследований в этом направлении, вопросам управления механизмом формирования иерархической структуры TiP в научной литературе уделено мало внимания. В данной работе проведён анализ влияния основных термодинамических параметров гидротермальной обработки на формирование микросферического фосфата титана. Установлено, что размер микросфер TiP изменяется в соответствии с механизмом оствальдовского созревания при полном сохранении иерархической структуры. Наблюдаемые отклонения от этого механизма при высоких концентрациях фосфорной кислоты объяснены с учётом активной роли фосфат-анионов в росте микросфер. Также рассмотрены особенности изменения морфологии составляющих микросферы структурных элементов в более жёстких условиях длительной гидротермальной обработки.
Фосфат титана, иерархическая структура, оствальдовское созревание, фосфорная кислота, электронная микроскопия
Короткий адрес: https://sciup.org/147252524
IDR: 147252524 | УДК: 544, 548 | DOI: 10.14529/chem250412
Ostwald ripening as a mechanism of hierarchical structural evolution of titanium phosphate
Control over nano- and microstructure of metal oxide materials is increasingly important, as it allows for fine-tuning their functionality. Therefore, material science provided a plethora of template and template-free methods to synthesize substrates with developed morphology, high crystallinity, and large specific surface. Despite significant advances in this field, there is no unified methodology and hence gen-eral consideration about mechanisms of sophisticated and hierarchically structured materials. Titanium phosphates (TiP), a wide group of materials composed of abundant elements, are a versatile platform for development of materials with customizable morphology and elemental composition. Ease of their synthesis and modification provided multiple sorbents, catalysts, energy capacitor electrodes, and polymer additives. Elaboration of hierarchical structures in titanium phosphates beyond the regular and uniform nanocrystal-line units produced substrates with a significant surplus in functionality. Although further studies in this di-rection seem promising, too little attention was focused on control features of TiP hierarchical structure. Here, the analysis of general thermodynamic parameters of hydrothermal synthesis of microspherical titanium phosphate has been carried out. The TiP microspheres change in size according to the Ostwald ri-pening mechanism with conservation of the hierarchical structure. The deviations from this mechanism, ob-served at high concentrations of phosphoric acid, are explained in relation to an active role of phosphate anions in the microsphere growth. Besides, the features of structural elements constituting the microspheres have been considered at more severe conditions of prolonged hydrothermal treatment.
Текст научной статьи Созревание Оствальда как механизм иерархической структурной эволюции фосфата титана
Современные функциональные материалы на основе оксидов металлов являются базой для разработки промышленно значимых процессов и передовых технологий: от гетерогенного катализа и сорбентов до высокочувствительных сенсоров и транзисторов. Фосфаты титана (TiP) привлекают внимание исследователей из-за их высокой биосовместимости, термической стабильности. Перспективным представляется их применение в различных областях, таких как фотокатализ, системы накопления энергии и биомедицинские технологии [1–10]. Мезопористые TiP с контролируемой морфологией (от волокнистых до гексагональных структур) могут использоваться в фотокаталитических процессах расщепления воды, где микроструктура материала напрямую влияет на эффективность выделения водорода [6, 7, 9–12].
Универсальность свойств фосфатов титана обусловлена их способностью образовывать слоистые ( α, β, γ -фазы) и волокнистые ( π, ρ -фазы) наноструктуры. В течение последних 40 лет слоистые структуры использовали преимущественно в качестве катализаторов, ионообменных материалов и электродов для Li- и Na-аккумуляторов, в то время как волокнистые системы успешно применялись в качестве протон-проводящих материалов, супергидрофобных поверхностей и катодов для кальций-ионных батарей [13].
В настоящее время особое внимание уделяется разработке иерархически структурированных материалов, демонстрирующих различную структурную организацию в различных размерных масштабах. Сложная морфология таких продуктов обычно характеризуется высокой удельной поверхностью, мультимодальной пористостью и пространственной анизотропией свойств, что приводит к получению материалов с улучшенными механическими, полупроводниковыми, каталитическими и сорбционными характеристиками. Особый интерес представляют недавно обнаруженные иерархические структуры на основе TiP. Все они были синтезированы в гидротермальных условиях. Так продемонстрирована возможность контроля морфологии TiP через соотношение реагентов (TiO2:H2O2:H3PO4). Выдвинута гипотеза, что тип морфологических особенностей определяется энергетическими характеристиками процесса [14]. Варьируя условия гидротермальной обработки фосфорной кислотой, удалось получить тонкие плёнки фосфата титана с микроструктурой, напоминающей цветы, на поверхности никель-титанового сплава [15]. Использование глицерина в качестве низкомолекулярного темплата при гидротермальной обработке тетрахлорида титана фосфорной кислотой позволило получить микросферический фосфат титана с иерархической структурой для использования в косметике [16]. Ещё одним примером иерархически структурированных TiP, полученных с контролем микроструктуры стали микросферы, которые использованы в качестве фотоанода для сенсибилизированных красителем солнечных элементов [17].
Многочисленные примеры иерархических структур на основе TiP показали, что морфологическая изменчивость открывает возможности для тонкой настройки функциональных характеристик. Для более глубокого понимания механизмов, лежащих в основе формирования иерархической структуры, нами проведён скрининг параметров их гидротермального синтеза. Следует отметить, что не существует единой методологии изучения механизма роста и эволюции сложных сферических и цветкообразных структур. Поэтому, помимо температуры, времени и начального соотношения реагентов, в работе исследована роль среды и координирующей молекулы металла. В результате установлена связь между параметрами синтеза и морфологическими особенностями образующихся структур TiP.
Экспериментальная частьРеагенты
DL-миндальная кислота (100 %, Bingospa), NH 3 (25 %, NevaReaktiv), H 2 O 2 (40%, BiokhimReagent), титановый порошок (99 %, 400 mesh, CMP Rosatom), H 3 PO 4 (NevaReaktiv) использованы без предварительной очистки.
Аналитические инструменты и методы
Элементный анализ и морфология поверхности образцов изучены с помощью электронного микроскопа Jeol JSM 7001F. Фазовый состав и структура образцов определены на порошковом дифрактометре Rigaku Ultima IV. Дифрактограммы записаны в диапазоне углов 2θ от 5° до 90° со скоростью съёмки 5°/мин. В исследовании использовано излучение медной трубки CuKα при ускоряющем напряжении 40 кВ. Элементный состав образцов проанализирован с помощью ICP-OES Perkin Elmer ORAS OPTIMA 7300 DV для определения содержания титана и фосфора в по спектральным линиям 336,121 нм (Ti) и 213,617 нм (P). Калибровочные кривые для нижних элементов показали линейную зависимость с коэффициентом корреляции R2 = 0,9999. Перед анализом твердые пробы растворяли в 5 мл 35%-ного раствора пероксида водорода (H 2 O 2 ) при постепенном нагревании от 100 до 180 ° С. После растворения к образцам добавляли по 5 мл концентрированной серной кислоты. Полученный раствор упаривали при нагревании до появления густых паров H 2 SO 4 . После охлаждения остаток растворяли дистиллированной водой и доводили до метки в мерной колбе вместимостью 50 мл.
Синтез титанового комплекса с миндальной кислотой
Согласно ранее опубликованному методу [18], 0,41 г (8,5 ммоль) титановой пудры, 40 мл раствора H 2 O 2 (40 масс. %) и 5 мл раствора NH 3 (25 масс. %) смешивали в колбе Эрленмейера объёмом 100 мл. Реакционную смесь перемешивали до полного растворения титановой пудры (1–1,5 ч), поддерживая температуру смеси в диапазоне от 5 до 10 °С. Светло-желтый раствор пероксокомплекса титана фильтровали, после чего добавляли раствор DL-миндальной кислоты (17 ммоль, 2,5 г) растворенной в 2–3 мл дистиллированной воды. После добавления кислоты температуру в реакционной смеси поддерживали в диапазоне 15-20 ° С ещё 2-3 ч. Комплекс титана выделяли выпариванием воды на ротационном испарителе при пониженном давлении и температуре 30-40 ° С.
Получение фосфата титана гидротермальным методом
Водорастворимый комплекс титана с DL-миндальной кислотой (1,66 ммоль), растворённый в 5 мл воды, помещали в автоклав объёмом 50 мл с тефлоновой вставкой, после чего к раствору добавляли рассчитанное количество фосфорной кислоты. Полученный раствор разбавляли водой до 20 мл, герметично закрывали автоклав и нагревали при температуре от 120 до 180 ° С. Первичное мольное соотношение титанового комплекса и фосфорной кислоты в автоклаве обозначали как начальное соотношение Ti:P и варьировали от 1:8 до 1:4. Для предотвращения постепенного охлаждения автоклав, по завершении выдержки, очень быстро охлаждали в ледяной бане. Полученный белый твёрдый осадок выделяли центрифугированием .
Результаты и обсуждение
Ранее в нами показана возможность использования стабильных водорастворимых комплексов титана с органическими кислотами для получения фосфатов титана. Эти комплексы являются стабильной и безопасной альтернативой высокореакционным и токсичным прекурсорам оксида титана, таким как хлорид, оксисульфат и алкоголяты. При реакции с фосфорной кислотой (ФК) в гидротермальных условиях они образуют однородные микроструктуры с уникальной морфологией [19, 20]. Для изучения влияния условий их получения на морфологию выбрана наиболее простая из полученных микроструктур – микросферическая. Показано, что полученные микросферы правильной формы имеют узкое распределение по размерам и представляют собой агрегаты хорошо дифференцированных микрочешуек. Иерархически структурированные микросферы, образующиеся с использованием пероксокомплекса титана с миндальной кислотой, не являются новыми и ранее были получены с использованием различных прекурсоров оксида титана [14, 15, 17]. Иерархическая структура и физико-химические свойства этих материалов подробно описаны ранее. По составу они представляют собой гидратированные гидрофосфаты титана, которые при прокаливании кристаллизуются в смесь пирофосфата титана (TiP 2 O 7 ) [21, 22] и оксида фосфата титана ((TiO)2P2O7) [23]. Учитывая высокую значимость фосфатов титана с иерархической структурой, поставлена цель детального изучения эволюции их роста. Варьируя основные параметры гидротермального синтеза: время, температуру и соотношение компонентов реакции установили основные пути эволюции микросфер TiP.
Показано, что с течением времени продукты реакции, полученные в стандартных гидротермальных условиях, развиваются через три типа морфологии: аморфный осадок без структурных особенностей (Тип I), микросферы (Тип II) и микростержни (Тип III) (рис. 1а–в).

а)

б)

в)
Рис. 1. Основные типы морфологии TiP: (а) Тип I (аморфный) время обработки 1 ч, (б) Тип II (микросферы) время обработки 12 ч, (в) Тип III (микростержни) время обработки 72 ч, (г) рентгенофазовый анализ типов I–III (эволюция показана для 180 °С и начального соотношения Ti:P 1:8)
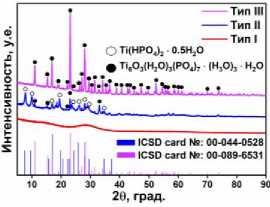
г)
Тип I представляет собой аморфный фосфат титана, который выпадает в осадок при коротком времени обработки (< 1 ч), когда мольный избыток ФК к титану меньше 4. При более низком содержании ФК продукт (осадок) не образуется (рис. 1а). Тип II образуется в широком диапазоне концентраций ФК и температур, давая однородные сферы с узким распределением по размерам (рис. 1б). Тип III представляют собой вытянутые микростержни, которые образуются в результате длительной гидротермальной обработки ( > 48 ч). Более длительное время обработки обеспечивает трансформацию микросфер в термодинамически стабильные и менее сложные микростержни (рис. 1в). Необходимо отметить, что в диапазоне 2–4 ч наблюдались продукты в виде смеси частиц I и II типов, а в диапазоне 24–48 ч – смесь частиц II и III типов, но никогда – в виде смеси частиц I и III типов.
Эволюция морфологии фосфата титана отражает переход из аморфного состояния через микросферы в стабильную кристаллическую форму в виде микростержней. Это очевидно из данных порошковой рентгеновской дифрактометрии (рис. 1г), которая показывает увеличение кристалличности с течением времени. Рентгенофазовые исследования показали, что состав иерархических структур в значительной степени зависит от времени реакции. Тип II состоит в основном из Ti(HPO 4 ) 2 ·0,5H 2 O (карта ICSD №: 00-044-0528 – гидрат гидрофосфата титана). Более длительное время синтеза переводит большую часть вещества в фазу Ti 6 O 3 (H 2 O) 3 (PO 4 ) 7 ·(H 3 O) 3 ·H 2 O (карта ICSD 00-089-6531 – гидрат оксида гидрофосфата титана) [21–24].
Микрофотографии образцов, полученных в течение первых двух часов синтеза TiP в относительно мягких условиях, выявили постепенную трансформацию морфологии типа I в тип II: сферы растут с развитой иерархической структурой с самого начала. Аморфная масса фосфата титана, наблюдаемая на первых снимках (рис. 2), по-видимому, представляет собой осажденный золь наночастиц, из которого в течение первых двух часов формируются микросферы. При более высокой температуре и большем содержании ФК рост сфер происходит быстрее, что не позволяет зафиксировать этапы трансформации золя в сферы. При меньшем содержании ФК осадок не образуется. Движущая сила формирования иерархии из аморфного геля остаётся неясной.

Рис. 2. Формирование микросфер TiP в течение первых 2 ч при 120 ° С и начальном соотношении Ti:P 1:6
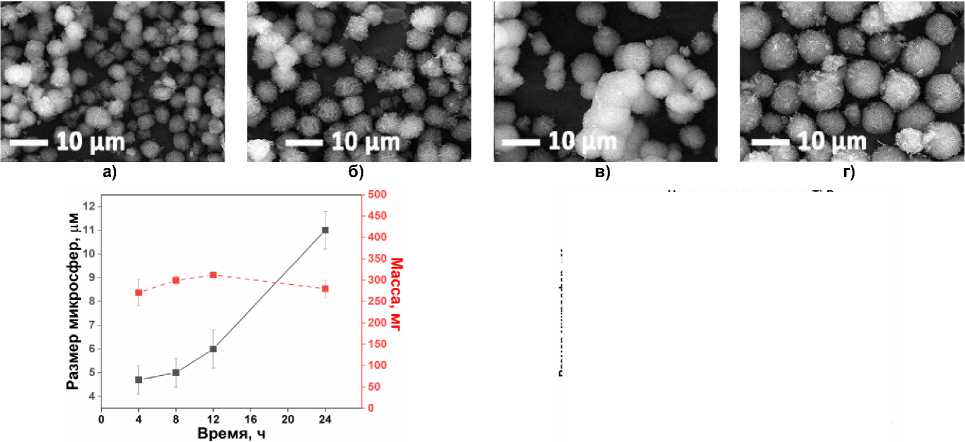
На рис. 3а–г показана динамика роста микросфер в течение первых 24 ч при температуре 140 °C и начальном соотношении Ti:P 1:5. Исходя из общей идеи роста микрочастиц как процесса, направленного на снижение общей поверхностной энергии, рост микросфер сопровождается растворением более мелких сфер с образованием более крупных, в соответствии с механизмом растворения и переосаждения по Оствальду. Этот аргумент подтверждается стабильным выходом осадка независимо от времени синтеза (рис. 3д). Вторым аргументом в пользу механизма растворения/переосаждения является геометрическая симметрия микрочастиц, которая обеспечивается равномерным внешним градиентом компонентов фосфата титана.
Другим важным наблюдением является отсутствие сфер размером <3 мкм во всех экспериментах при продолжительности обработки более 2 ч. Это свидетельствует о высокой скорости их растворения: в исследуемых условиях при достижении минимального размера они растворяются мгновенно. Это наблюдение свидетельствует об активном обмене ионами в растворе во всем исследованном диапазоне времени обработки (рис. 3а–г).
Физическая химия
Physical chemistry
д)
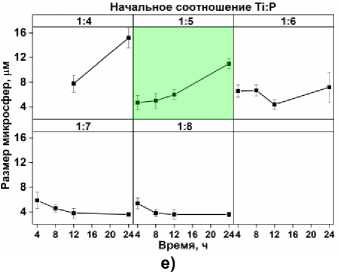
Рис. 3. (а–г) СЭМ-изображения микросфер TiP, синтезированных в течение 4, 8, 12 и 24 ч, соответственно, (д) размеры и масса продукта (начальное соотношение Ti:P 1:5, 140 ° С, (е) размер микросфер в зависимости от времени синтеза при различных начальных соотношениях Ti:P и температуре синтеза 140 ° С
Влияние ФК на изменение размера микросфер представлено графиками на рис. 3е. При исходном соотношении Ti:P в смеси выше 1:3 микросферы не формировались. При исходном соотношении Ti:P от 1:4 до 1:6 наблюдается прямая зависимость размера микросфер от времени, в соответствии с классической концепцией роста кристаллов, обсуждавшийся выше. При более высоких концентрациях ФК гидротермальный процесс приводит к образованию сфер меньшего размера. По-видимому, высокая концентрация фосфатов с одной стороны способствует увеличению числа центров роста сфер, с другой – препятствует растворению фосфатной фазы для созревания более крупных микросфер.
Постепенное снижение среднего размера микросфер – с 6 до 4 мкм – с течением времени при высоком содержании ФК (исходное соотношение Ti:P <1:6) требует отдельного объяснения. Вероятнее всего, в процессе растворения и переосаждения движущей силой процесса является снижение общей поверхностной энергии. Это может быть достигнуто за счёт существенной примитивизации морфологии: вместо множества составляющих чешуек образуются редкие, крупные и изолированные чешуйки с соответствующим уменьшением общей площади поверхности (рис. 4а–б). Таким образом, длительная выдержка микрочастиц TiP при высокой концентрация фосфатов в растворе приводит к упрощению иерархической структуры.

а)

б)
Рис. 4. СЭМ-изображения микросфер TiP, полученных при начальном соотношении Ti:P 1:8
и температуре 140 ° С в течение: (а) 4 ч, (б) 24 ч
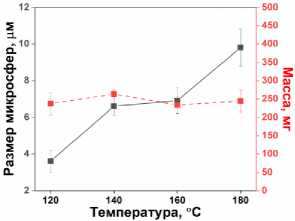
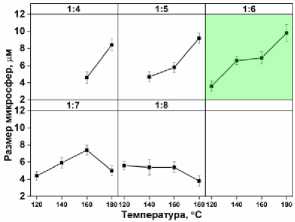
Исследование влияния температуры на размер микросфер выявило положительную ковариацию, демонстрирующую увеличение скорости оствальдовского созревания при нагревании (рис. 5а–г). Однако по мере увеличения содержания ФК (начальное соотношение Ti:P < 1:6) зависимость размера микросфер TiP от температуры имеет максимум при температуре 160 °С (начальное соотношение Ti:P 1:7). Два фактора могли уменьшить размер микросфер при большем содержании ФК. Во-первых, более высокая концентрация ФК увеличивала количество центров роста, что приводило к меньшему размеру сфер (рис. 5д). Во-вторых, высокая концентрация ФК при высокой температуре блокирует растворение фосфата титана и созревания по Оствальду, соответственно.

а)


в)

г)
д)
е)
Рис. 5. (а-г) СЭМ-изображения микросфер TiP, синтезированных при различных температурах (120-180) °C, (д) средний размер и выход продукта (начальное соотношение Ti:P 1:6, 4 ч); (е) зависимость размера микросфер TiP от температуры при различных начальных соотношениях Ti:P (4 ч)
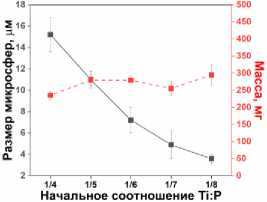
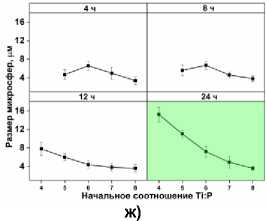
Подавление роста микросфер фосфат-анионами подтверждено отдельным исследованием, которое показало увеличение размера сфер с уменьшением содержания ФК. С ростом начального соотношения Ti:P от 1:8 до 1:4 средний размер сфер увеличивался от ~4 мкм до ~15 мкм. (рис. 6а-д). Малое время гидротермальной обработки - 4 и 8 ч - нарушает эту тенденцию при исходном соотношении Ti:P 1:6. В этой точке наблюдается излом графика и уменьшение размера микросфер. Небольшой размер микросфер в этих условиях можно объяснить меньшим содержанием фосфат-анионов. Таким образом, оптимум на первых двух графиках (рис. 6ж) отражает баланс двух противоречивых тенденций: увеличение содержания ФК в реакционной смеси способствует увеличению размера микросфер, но при этом подавляет растворение фазы TiP (рис. 6е). Предыдущее наблюдение увеличения размера микросфер во времени при меньшем содержании ФК (рис. 3е) поддерживает первую предполагаемую тенденцию.
е)
г) д)

а) б) в)
Рис. 6. (а-д) СЭМ-изображения частиц, синтезированных при различных начальных соотношениях Ti:P (1:4-1:8),
-
(е) распределения по размерам и выход продукта (24 ч., 140 ° С), (ж) зависимость размера микрочастиц от начального соотношения Ti:P при различной продолжительности синтеза (140 ° С)
Таким образом, рост микросфер хорошо объясняется механизмом, аналогичным оствальдов-скому созреванию, скорость которого при низких и средних концентрациях ФК напрямую зависит от температуры и времени. При более высокой концентрации ФК (исходное соотношение Ti:P > 1:6) наблюдается отклонение от первичного механизма. Высокая концентрация ФК увеличивает количество центров роста сфер, скорость образования которых превышает скорость роста сфер. Высокая концентрация фосфат-анионов также подавляет растворение, стабилизируя мета-стабильные сферы при меньшем размере. Длительная обработка в таких условиях упрощает иерархическую структуру и снижает удельную поверхность. На рис. 7 представлены пути эволюции микросфер в исследованных условиях.
1:4
1:5
1:5
1:7
1:8

большой размер сложная структура маленький размер простая структура
меньше центров роста сфер активное растворение-осаждение больше центров роста сфер пассивация фосфат-анионами
Температура Время
Рис. 7. Общая схема эволюции микросфер TiP в гидротермальных условиях
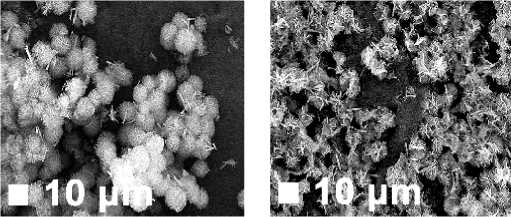
Исследована роль координирующей атом титана D/L-миндальной кислоты (рацемат) в получении микросфер. Эксперименты с пероксокомплексом Ti, не стабилизированными миндальной кислотой, привели к образованию аморфных осадков без каких-либо морфологических особенностей при всех описанных выше условиях. Это послужило доказательством активной роли органической кислоты в структурообразовании микросфер (рис. 8). Для проверки данной гипотезы предварительно синтезированные микросферы гидротермально обработали без миндальной кислоты при 140 ° С и 4-х кратном избытке ФК в течение 24 ч. По завершении эксперимента сферы не выросли в размерах, как ожидалось исходя из ранних наблюдений, представленных на рис. 3. Вместо этого они претерпели значительное ухудшение структуры с укрупнением составляющих их чешуек. Данный эксперимент доказал ключевую роль миндальной кислоты в формировании иерархической структуры: без неё растворение и переосаждение преобладают над формированием иерархической структуры, что приводит к увеличению чешуек за счёт растворения более мелких.
Механизм роста иерархической структуры выходит за рамки нашего исследования. Тем не менее, следует отметить, что предыдущие сообщения об иерархических структурах, синтезированных с использованием молекулярных темплатов, объясняют рост стабилизацией определённых граней нанокристаллов [25]. Этот подход не объясняет полученные структуры, поскольку они демонстрируют более одного уровня организации, выходящего за рамки уровня нанокристаллов.

а)
б) в)
Рис. 8. СЭМ-изображения: (а) TiP, полученный из пероксокомплекса титана, не стабилизированного миндальной кислотой, (б) предварительно сформированные микросферы, полученные после 4 ч синтеза при 140 ° C и начальном соотношении Ti:P 1:4, (в) трансформация предварительно сформированных микросфер после 24 ч обработки при 140 °C с четырехкратным избытком ФК в отсутствии миндальной кислоты
Для определения роли ионов водорода в росте микросфер проведен эксперимент с оксидом дейтерия для определения изотопного эффекта. Поскольку основным источником кислых протонов в реакции служил ФК, его варьируемые количества вводили в реакционную смесь в ходе гидротермального синтеза с использованием оксида дейтерия вместо воды. Изотопный эффект отображается в изменении размера сфер. Более тяжелые и медленные ядра дейтерия снижают скорость диссоциации ФК [26] и, как следствие, скорость образования фосфата титана. Это отражается в общем уменьшении среднего размера микросфер (рис. 9). В то же время, при начальном соотношении Ti:P 1:7–1:8 полная сходимость изотопных графиков свидетельствует о том, что при высокой концентрации ФК активности фосфатных анионов равны в обеих средах.
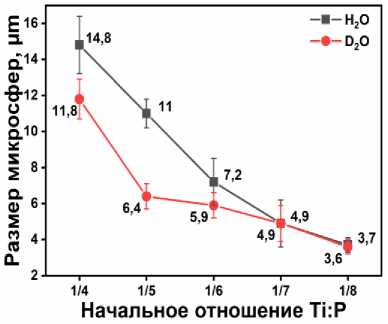
Рис. 9. Зависимость размера микросфер от начального соотношения Ti:P в протонной (чёрная кривая) и дейтерированной (красная кривая) воде (140 ° C, 24 ч)
Как указывалось ранее, более длительное время обработки, независимо от исходного соотношения Ti:P, приводит к морфологически упрощенным структурам вытянутых микрокристаллов (рис. 10а, б). Морфологическое сходство структур, полученных после более длительного времени обработки, свидетельствует о термодинамической стабильности микрокристаллов. Это означает, что микросферы представляют собой лишь промежуточную фазу, претерпевающую превращение в условиях постоянного обмена с раствором, содержащим титанатные и фосфатные соединения. В пользу такого обмена свидетельствует стабильность выхода образцов TiP, полученных при всех исследованных условиях (см. таблицу).
Исследования методом рентгеновского анализа показали, что микрокристаллические структуры, полученные через 48 ч, состоят из двух фаз: Ti(HPO 4 ) 2 ·0,5H 2 O и Ti 6 O 3 (H 2 O) 3 (PO 4 ) 7 ·(H 3 O) 3 ·H 2 O [21– 24]. Дифрактометрические профили на рис. 10в выглядят как промежуточная форма соответствующих профилей, зарегистрированных для образцов TiP типа II и типа III (рис. 1). В отличие от микросфер, эти два образца полностью утратили свою иерархическую структуру и перешли в простую и примитивную кристаллическую форму, в соответствии с общей тенденцией к снижению поверхностной энергии.

а) б)
Рис. 10. СЭМ-изображения стержней TiP, полученных в результате длительной (48 ч) гидротермальной обработки реакционных смесей при 180 °C с начальным соотношением Ti:P (а) 1:4 и (б) 1:8; (в) рентгенофазовый анализ образцов морфологии типа III, полученных при начальных соотношениях 1:4 и 1:8
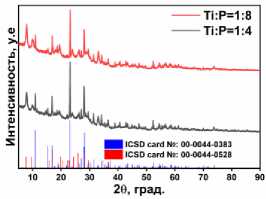
в)
Выход продукта и элементный состав соединений TiP, полученных при различных условиях синтеза
|
№ |
T, °С |
Время, ч |
Начальное соотношение Ti:P |
Масса, мг |
Соотношение Ti:P в осадке |
|
1 |
140 |
24 |
1:4 |
262 |
0,86 |
|
2 |
140 |
24 |
1:5 |
304 |
0,88 |
|
3 |
140 |
24 |
1:6 |
262 |
0,85 |
|
4 |
140 |
24 |
1:7 |
260 |
0,88 |
|
5 |
140 |
24 |
1:8 |
281 |
0,85 |
|
6 |
140 |
4 |
1:5 |
294 |
0,89 |
|
7 |
140 |
6 |
1:5 |
300 |
0,89 |
|
8 |
140 |
12 |
1:5 |
312 |
0,88 |
|
2 |
140 |
24 |
1:5 |
280 |
0,90 |
|
9 |
120 |
4 |
1:6 |
261 |
0,86 |
|
10 |
140 |
4 |
1:6 |
262 |
0,86 |
|
11 |
160 |
4 |
1:6 |
233 |
0,85 |
|
12 |
180 |
4 |
1:6 |
284 |
0,88 |
|
Тип I |
120 |
4 |
1:5 |
105 |
0,85 |
|
Тип II |
140 |
24 |
1:5 |
280 |
0,86 |
|
Тип III |
120 |
72 |
1:4 |
258 |
0,86 |
Заключение
Контроль основных термодинамических параметров гидротермального синтеза сферической иерархической структуры фосфата титана позволил тонко регулировать размер в широком диапазоне, сохраняя при этом элементный состав и выход продукта. Рост микросфер хорошо объясняется растворением и переосаждением по Оствальду, в котором фосфорная кислота выступает в качестве основного медиатора процесса. Более высокое содержание фосфорной кислоты увеличивает количество центров роста микросфер и блокирует растворение более мелких. Таким образом, высокая концентрация ФК и высокая температура приводят к уменьшению размера микросфер. При более длительном времени обработки в таких условиях микросферы теряют свою сложную иерархию и упрощаются по морфологии, что связано с тенденцией к минимизации поверхностной энергии. Механизм растворения-переосаждения отдельно подтвержден экспериментом с предварительно сформированными микросферами, которые уменьшались в размере и упрощались по морфологии после обработки фосфорной кислотой в отсутствие миндальной кислоты. Подтверждена роль D/L-миндальной кислоты (рацемат) как молекулы-темплата иерархической микроструктуры. Это первый пример адаптации ранее разработанной концепции роста кристаллических структур к иерархическим. Авторы не обнаружили существенных противоречий в эксперименте и рекомендуют его для дальнейшего изучения эволюции иерархических структур.


