Спектральное проявление взаимодействия гидроксильных групп фенолов-антиаксидантов с растворителями
Автор: Русских Ирина Владимировна, Писарева Светлана Ивановна, Рябова Наталья Викторовна
Журнал: Science for Education Today @sciforedu
Рубрика: Биологические, химические, медицинские науки
Статья в выпуске: 5 (15), 2013 года.
Бесплатный доступ
В статье исследованы спектрально-структурные характеристики пространственно-затрудненных фенолов в хлорсодержащих и ароматических растворителях методом ИК-спектроскопии. Цель работы – исследование спектральных проявлений водородных связей гидроксильных групп пространственно-затрудненных фенолов с хлорсодержащими и ароматическими углеводородами. Известно, что в фенолах экранирование объемными заместителями не позволяет гидроксильным группам образовывать межмолекулярные водородные связи. Именно этим обусловлен выбор таких структур в качестве присадок, ингибирующих окисление углеводородов. Тем не менее, введение пространственно-затрудненных фенолов в углеводородную систему может повлиять на установившийся порядок межмолекулярных взаимодействий и изменить спектральные характеристики фенолов. В работе было обнаружено, что при равных концентрациях фенолов полосы поглощения растворов в диапазоне 3700-3200 см -1 отличаются по интенсивности и по положению максимумов в зависимости от полярности и типа растворителя. Изменения спектральных характеристик обусловлены межмолекулярными взаимодействиями гидроксильных групп фенолов с растворителями.
Пространственно-затрудненные фенолы, хлорсодержащие и ароматические растворители, межмолекулярные и внутримолекулярные взаимодействия, ик-спектроскопия, водородные связи
Короткий адрес: https://sciup.org/147137492
IDR: 147137492 | УДК: 543.42
Spectral manifestation of interaction between hydroxyl groups of phenolic antioxidants and solvents
The spectral and structural characteristics of sterically hindered phenols in chlorinated and aromatic solvents are analyzed by IR spectroscopy. The spectral manifestations of hydrogen bonds of the hydroxyl groups of sterically hindered phenols in chlorinated and aromatic hydrocarbons are investigated. It is known that hydroxyl groups are not capable of forming intermolecular hydrogen bonds in phenols due to their shielding by bulky substituents. It is exactly this fact that has motivated their selection as additives inhibiting hydrocarbon oxidation. Nevertheless, an introduction of sterically hindered phenols into the hydrocarbon system may affect the established pattern of intermolecular interactions and change the phenol spectral characteristics. The intensities and peak positions in the absorption bands of solutions are shown to differ within the range 3700-3200 cm -1, depending on the solvent type and polarity, the concentrations of phenols being equal. The observed changes in the spectral characteristics are attributed to the intermolecular interactions between the phenol hydroxyl groups and solvents.
Текст научной статьи Спектральное проявление взаимодействия гидроксильных групп фенолов-антиаксидантов с растворителями
Электронный журнал «Вестник Новосибирского государственного педагогического университета» 5(15) 2013 ISSN 2226-3365
Введение.
Наиболее распространенными ингибиторами, применяемыми для предотвращения окисления различных углеводородных систем – моторных топлив, смазочных масел, пищевых продуктов, полимерных материалов и покрытий, являются соединения класса пространственно-затрудненных фенолов (ПЗФ) [1]. Известно, что в фенолах экранирование объемными заместителями не позволяет гидроксильным группам образовывать межмолекулярные водородные связи [2]. Именно этим обусловлен выбор таких структур в качестве присадок, ингибирующих окисление углеводородов. Тем не менее, введение ПЗФ в углеводородную систему может повлиять на установившийся порядок межмолекулярных взаимодействий и изменить спектральные характеристики фенолов. В работе [3] методом ИК спектроскопии изучено влияние химической природы растворителя на образование межмолекулярных водородных связей с нефтяными фенолами.
Цель работы – исследование спектральных проявлений водородных связей гидроксильных групп ПЗФ с хлорсодержащими и ароматическими углеводородами.
Объекты и методы исследования.
В качестве объектов исследования выбраны 2,6-ди- трет -бутил-4-метил-фенол
(ионол) – соединение, в котором содержится одна реакционноспособная гидроксильная группа, экранированная с двух сторон трет -бутильными заместителями, и 2,2’-метилен- бис -(4-метил-6- трет -бутил-фенол) (БФ) – соединение, в котором содержатся две реакционноспособные гидроксильные группы, экранированные с двух сторон трет -бутильными заместителями.
ИК cпектры поглощения растворов ПЗФ регистрировали на ИК-Фурье спектрометре Nicolet 5700 (разрешение 4 см-1, число сканов пробы 64) в диапазоне 3700-3200 см-1, в кюветах из NaCl c толщиной поглощающего слоя 0,216 мм. В работе использовали две группы растворителей: хлорсодержащие (четыреххлористый углерод (CCl 4 ), хлороформ (CHCl 3 ), хлористый метилен (CH 2 Cl 2 )) и ароматические углеводороды (бензол, толуол, кумол). Растворители подвергали очистке по общепринятым методикам [4]. Концентрации используемых в работе фенолов составили 0,18·10-3 моль.
Результаты и их обсуждение.
Характеристика ИК полос поглощения гидроксильных групп растворов ионола и БФ в хлорсодержащих и ароматических растворителях приведена в таблицах 1, 2.
Таблица 1.
Характеристика ИК полос поглощения гидроксильных групп растворов ионола.
|
Растворитель |
ν, см 1 |
Оптическая плотность ИК поглощения ОН (своб.) |
|
Четырёххлористый углерод (CCl 4 ) |
3649 |
0,34 |
|
Хлороформ (CHCl 3 ) |
3643 |
0,29 |
|
Хлористый метилен (СН 2 Cl 2 ) |
3638 |
0,24 |
|
Бензол (C 6 H 6 ) |
3637 |
0,23 |
|
Толуол (C 7 H 8 ) |
3637 |
0,23 |
|
Кумол (C 9 H 12 ) |
3643 |
0,19 |
|
Примечание: ν – частота максимума полосы поглощения в ИК спектрах растворов ионола в области валентных колебаний ОН-группы |
||
Все права защищены

Таблица 2.
Характеристика ИК полос поглощения гидроксильных групп растворов БФ.
|
Растворитель |
ν, см 1 |
Оптическая плотность в областях спектра ИК поглощения |
|||
|
ОН (своб.) |
ОН… π связь |
ОН (внутримол.) |
ОН (межмол.) |
||
|
Четырёххлористый углерод (CCl 4 ) |
3631, 3508, 3440 |
0,32 |
- |
0,69 |
0,31 |
|
Хлороформ (CHCl 3 ) |
3622, 3508, 3438 |
0,46 |
- |
0,33 |
0,38 |
|
Хлористый метилен (СН 2 Cl 2 ) |
3620, 3508, 3435 |
0,60 |
- |
0,42 |
0,54 |
|
Бензол (C 6 H 6 ) |
3612, 3573, 3504, 3427 |
0,39 |
0,26 |
0,59 |
0,44 |
|
Толуол (C 7 H 8 ) |
3612, 3573, 3504, 3437 |
0,35 |
0,29 |
0,58 |
0,40 |
|
Кумол (C 9 H 12 ) |
3610, 3573, 3504, 3437 |
0,31 |
0,27 |
0,63 |
0,39 |
Примечание: ν – частота максимума полос поглощения в ИК спектрах растворов БФ в области валентных колебаний ОН-группы
5(15) 2013
ISSN 2226-3365
Фрагменты ИК спектров растворов ПЗФ в четыреххлористом углероде, хлороформе, бензоле, представленные на рисунках 1, 2 демонстрируют различные виды водородной связи, о чем свидетельствуют полосы поглощения в этой области: 3649-3637 см-1 для ионола, 3631-3612, 3573, 3508-3504,
3440-3427 см-1
концентрациях
для БФ. При равных фенолов во всех растворителях полосы поглощения растворов как для ионола, так и для БФ, отличаются по интенсивности и по положению максимумов полос поглощения в зависимости от полярности и типа растворителя [5].
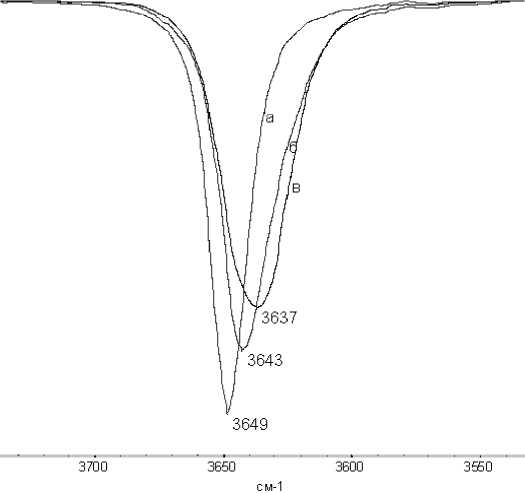
Рисунок 1.
Фрагменты ИК спектров Растворов ионола в четыреххлористом углероде (а), в хлороформе (б) и бензоле (в).
Все права защищены

5(15) 2013
ISSN 2226-3365
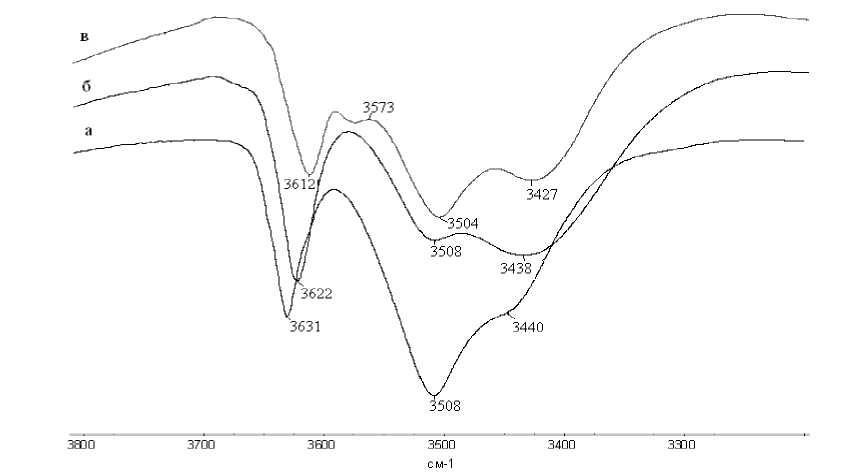
Рисунок 2.
Фрагменты ИК спектров растворов БФ в четыреххлористом углероде (а), в хлороформе (б) и бензоле (в).
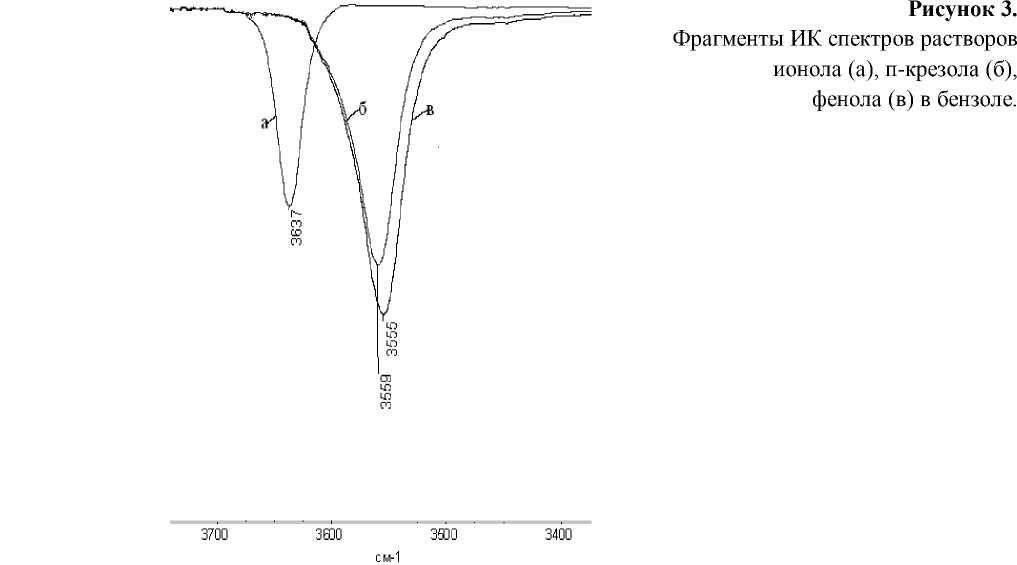
ИК спектры ионола во всех растворителях содержат одну полосу поглощения, соответствующую валентным колебаниям свободной гидроксильной группы (рис. 1, таблица 1), отличающуюся формой. Самая узкая и интенсивная полоса наблюдается в ИК спектре раствора ионола в CCl4, так как CCl4, имеющий дипольный момент, равный 0 [4], не образует межмолекулярных связей с ионолом, являясь инертной средой (рис. 1, а). Хлороформ и хлористый метилен с дипольными моментами 1,87 D (для CHCl3), 1,6 D (для CH2Cl2) [4] являются активными полярными растворителями, кислые протоны которых взаимодействуют с гидроксильными группами ионола, что проявляется на спектре в виде более широкой полосы меньшей интенсивности, смещенной в область низких частот (рис. 1, б). Наиболее широкая и менее интенсивная, еще больше смещенная в длинноволновую область, полоса поглощения, наблюдаемая на рисунке 1, в, является спектральным проявлением межмолекуляр- ного взаимодействия гидроксильных протонов ионола с π-электронной системой ароматических углеводородов (OH…π взаимодействие). В таблице 1 представлены результаты влияния заместителей в ароматических кольцах растворителей на интенсивность и положение максимумов полос поглощения гидроксильной группы ионола. Для бензола и толуола эти значения равны, а для кумола наблюдается уширение и сдвиг полосы поглощения в высокочастотную область, что обусловлено пространственным эффектом метильных групп изопропилбензола. Влияние метильных групп в ароматических кольцах фенолов (на примере фенола, п-крезола, ионола) на межмолекулярное взаимодействие гидроксильных групп с π-электронной системой бензола представлено на рисунке 3. Как следует из рисунка, для п-крезола и фенола наблюдается существенное увеличение интенсивности и сдвиг полосы поглощения в область низких частот, что свидетельствует о более прочном OH…π взаимодействии.
Все права защищены

5(15) 2013 ISSN 2226-3365
ИК спектр раствора БФ в CCl4 содержит узкую полосу поглощения свободной гидроксильной группы в области 3631 см-1. Полоса поглощения 3508 см-1, более интенсивная, чем при 3631 см-1, свидетельствует о том, что большую долю водородной связи БФ в растворе CCl4 составляет внутримолекулярная водородная связь между двумя гидроксильными группами. Положение максимума этой полосы не зависит от полярности растворителя (таблица 2). Полоса поглощения, смещенная в область низких частот - 3440 см-1, характеризует валентные колебания гидроксильных групп в межмолекулярной водородной связи, так как при межмолекулярном взаимодействии влияние пространственного фактора меньше (больше степеней свободы во взаимном расположении двух молекул БФ относительно друг друга и связь О…Н прочнее). Положение максимума полосы межмолекулярной водородной связи зависит от полярности растворителя (таблица 2) [4].
Так, в инертном растворителе CCl 4 , полоса 3440 см-1 проявляется только в виде плеча на полосе 3508 см-1 (рис. 2, а).
ИК спектры растворов БФ в CHCl3 и CH2Cl2 содержат узкие интенсивные полосы поглощения гидроксильной группы при 3622 и 3620 см-1, соответственно (рис. 2 б, таблица 2). Увеличение интенсивности и сдвиг максимума полос поглощения гидроксильных групп в область низких частот, по сравнению с CCl4 (3631 см-1), с повышением полярности растворителя объясняется взаимодействием их с кислыми протонами CHCl3 и CH2Cl2. В этих растворах также присутствуют полосы поглощения в области 3508 см-1, которые характеризуют внутримолекулярную водородную связь между гидроксильными группами. Увеличение интенсивности полос при 3438 и 3435 см-1, отвечающих за межмолекулярную водородную связь гидроксильных групп БФ, а также стабильность максимума полос поглощения внутримолекулярной водородной связи вполне соответствуют
Все права защищены

5(15) 2013
ISSN 2226-3365
классическим представлениям о том, что увеличение полярности растворителя усиливает интенсивность процесса образования межмолекулярных водородных связей [5, 6].
В ИК спектрах БФ в ароматических растворителях наряду с вышеуказанными полосами поглощения появляется новая полоса 3573 см-1 меньшей интенсивности, которая является спектральным проявлением межмолекулярного взаимодействия гидроксильных протонов БФ с π-электронной системой ароматических углеводородов (OH…π взаимодействие) (рис. 2, в, таблица 2). Теоретически эта связь должна усиливаться с увеличением подвижности р-электронов в ряду: C 6 H 6 < C 7 H 8 < C 9 H 12 [5], однако влияние пространственного эффекта в изопропилбензоле меняет вышеуказанный теоретический ряд: C 6 H 6 < C 9 H 12 < C 7 H 8 , что подтверждается значениями оптических плотностей полос поглощения (таблица 2).
Заключение.
Анализ спектральных характеристик растворов пространственно-затрудненных фенолов показал, что на проявление межмолекулярных взаимодействий влияет тип и полярность растворителя. Так, CCl4 не способствует образованию межмолекулярных водородных связей в растворах фенолов, являясь инертной средой. С повышением полярности хлорсодержащих растворителей наблюдается увеличение интенсивности и сдвиг максимума полос поглощения гидроксильных групп в область низких частот, что объясняется межмолекулярным взаимодействием их с кислыми протонами CHCl3 и CH2Cl2. В растворах ароматических углеводородов обнаружено межмолекулярное взаимодействие гидроксильных протонов фенолов с π-электронной системой ароматических углеводородов. В полярных хлорсодержащих и ароматических растворителях БФ содержит смесь соединений с внутримолекулярной (3504 см-1) и межмолекулярной (3573, 3427 см-1) водородных связей, находящихся в лабильном динамическом равновесии.
Список литературы Спектральное проявление взаимодействия гидроксильных групп фенолов-антиаксидантов с растворителями
- Рогинский В. А. Фенольные антиоксиданты. Реакционная способность и эффективность. -М.: Наука, 1988. -247 с.
- Четкина Л. А., Соболев А. Н., Бельский В. К., Заводник В. Е., Арзаманова И. Г.,Гурвич Я. А., Старикова О. Ф. Строение фенольных стабилизаторов полимеров. VIII. Структура кристаллов моноакрилата 2,2’-метилен-бис-(4-метил-6-трет-бутил-фенола)//Журнал структурной химии. -1991. -Т. 32. -№ 5. -С. 162-164.
- Писарева С. И., Русских И. В. Влияние природы растворителя на образование ассоциатов с внутри-и межмолекулярными водородными связями в растворах нефти//Нефтехимия. -2012. -Т. 52. -№ 3. -С. 191-195.
- Гордон А., Форд Р. Спутник химика. -М.: Мир, 1976. -541 с.
- Беллами Л. Новые данные по ИК-спектрам сложных молекул/пер. с англ. В. М. Акимова, Э. Г. Тетерина//под ред. Ю. А. Пентина. -М.: Мир, 1971. -318 с.
- Наканиси К. Инфракрасные спектры и строение органических соединений/пер. с англ. Н. Б. Куплетской и Л. М. Эпштейн//под ред. А. А. Мальцева. -М.: Мир, 1965. -21 с.


