Способ комплексного ведения лапаротомного доступа при операциях на органах брюшной полости
Автор: Тонеева С.Н., Мартынова Е.В., Мидленко О.В., Тонеев Е.А., Мартынов А.А., Хамидов А.В.
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Статья в выпуске: 4, 2025 года.
Бесплатный доступ
Лапаротомия – это наиболее распространенный способ доступа при проведении хирургических операций на органах брюшной полости и малого таза. Однако после операции у пациентов зачастую диагностируется выраженный болевой синдром, а также появляется высокий риск возникновения инфекционных осложнений в области хирургического вмешательства, которые способствуют развитию внутрибольничных инфекций и могут значительно увеличивать смертность пациентов. Цель. Оценка эффективности нового метода профилактики, направленного на снижение риска развития инфекционных осложнений в области хирургического вмешательства и уменьшение болевого синдрома в раннем послеоперационном периоде. Материалы и методы. Способ профилактики инфекций в области хирургического вмешательства применен у 10 больных. Метод предполагает использование двух перфорированных микроирригаторов, которые размещаются на различных уровнях раневой поверхности. В первый катетер, установленный в предбрюшинное пространство, в качестве анестетика непрерывно при помощи дозатора-помпы со скоростью 5 мл/ч в течение 3 сут вводится 0,2 % ропивакаин. Во второй микроирригатор, установленный в подкожно-жировой клетчатке, в качестве антисептика болюсно по 20 мл 3 р./сут с интервалом 8 ч на протяжении 3 сут вводится раствор повидон-йода. Оценивали болезненность в области лапаротомной раны и развитие послеоперационных осложнений. Результаты. У всех пациентов наблюдалось ускорение заживления раны и отмечено отсутствие болевых ощущений в области хирургического вмешательства, что позволило обойтись без применения наркотических анальгетиков. Также не было зарегистрировано послеоперационных осложнений, связанных с использованием данного метода. Выводы. Применение предложенного метода в клинической практике способствует снижению риска развития инфекционных осложнений после плановой лапаротомии и обеспечивает эффективное обезболивание.
Ацетозоламид, сердечная недостаточность, комбинированная диуретическая терапия
Короткий адрес: https://sciup.org/14134207
IDR: 14134207 | УДК: 616.381-089.48 | DOI: 10.34014/2227-1848-2025-4-15-26
A method for integrated management of laparotomy access during abdominal surgery
Laparotomy is the most common approach for surgical procedures involving abdominal and pelvic organs. However, after surgery, patients often experience severe pain and a high risk of surgical site infection. These complications contribute to the development of hospital-acquired infections and can significantly increase patient mortality. Objective. The purpose of the study is to evaluate the efficacy of a new prophylactic method aimed at reducing the risk of developing surgical site infections and alleviating pain in the early postoperative period. Materials and Methods. A method for the prevention of surgical site infections was used in 10 patients. The method involves the use of two perforated micro-irrigators, which are placed at different levels of the wound surface. A 0.2 % ropivacaine anesthetic was continuously injected into the first catheter, inserted into the preperitoneal space, using a pump dispenser at a rate of 5 ml/hour for 3 days. A povidone-iodine solution was administered as an antiseptic via a bolus injection into the second micro-irrigator, inserted into the subcutaneous tissue, (20 ml t.i.d. at 8-hour intervals for 3 days). Pain after a laparotomy wound and the development of postoperative complications were assessed. Results. All patients experienced accelerated wound healing and absence of pain at the surgical site, which eliminated the need for narcotic analgesics. Furthermore, no postoperative complications associated with this method were reported. Conclusion. The use of the proposed method in clinical practice reduces the risk of infectious complications after elective laparotomy and provides effective pain relief.
Текст научной статьи Способ комплексного ведения лапаротомного доступа при операциях на органах брюшной полости
Введение. На сегодняшний день лапаротомия является наиболее распространенным способом доступа при проведении хирургических операций на органах брюшной полости и малого таза. Однако после операции высок риск возникновения инфекционных осложнений в области хирургического вмешательства (ИОХВ), которые способствуют развитию внутрибольничных инфекций и могут значительно увеличивать смертность пациентов [1].
Согласно данным зарубежных исследований частота ИОХВ после плановых лапаротомий может достигать 25 % [2]. Риски возникновения ИОХВ разнообразны и могут быть разделены на две основные категории: индивидуальные и связанные с самим хирургическим вмешательством. К первым относятся возраст, алиментарная недостаточность, ожирение, сахарный диабет, длительный стаж курения, ослабленный иммунитет; ко вторым – срок предоперационной госпитализации и неполное соблюдение правил асептики и антисептики в операционном блоке и перевязочном кабинете [3, 4].
Профилактика риска развития инфекционных осложнений является важной и экономически целесообразной мерой для системы здравоохранения в целом, поскольку она снижает расходы на лечение пациентов и уменьшает продолжительность их пребывания в стационаре [5].
Отметим, что соблюдение правил асептики и антисептики в ходе хирургического вмешательства, использование антибиотико-профилактики перед операцией позволяют минимизировать риск возникновения ИОХВ, предотвращая контаминацию инфекционными агентами раневой поверхности передней брюшной стенки [6]. Однако даже эти профилактические меры не могут полностью исключить риск инфекции в области хирургического вмешательства.
Другим осложнением, возникающим в раннем послеоперационном периоде и связанным с лапаротомией, является выраженный болевой синдром, который способствует увеличению сроков реабилитации и фармакологической коррекции, а также обуславливает применение опиоидных анальгетиков, что влечет за собой возможное развитие психосоматических расстройств [7].
Таким образом, болевой синдром и инфекция области хирургического вмешательства негативно влияют на репаративные процессы организма в целом, так как приводят к возникновению других проблем, связанных с оказанием медицинской помощи.
Следовательно, несмотря на достижения современной хирургии и фармакологии, профилактика развития ИОХВ после плановой лапаротомии и обеспечение адекватного обезболивания остаются актуальными задачами.
Цель исследования. Оценка эффективности нового метода профилактики, направленного на снижение риска развития инфекционных осложнений в области хирургического вмешательства и уменьшение болевого синдрома в раннем послеоперационном периоде.
Материалы и методы. На базе двух лечебных учреждений (ГУЗ Ульяновская областная клиническая больница, ГУЗ Областной клинический онкологический диспансер) проведено проспективное исследование.
Критерии включения:
-
• плановое хирургическое вмешательство;
-
• операции по поводу злокачественного новообразования I–IIIстадии.
Критерии исключения:
-
• операции, выполненные по экстренным и срочным показаниям;
-
• хирургические вмешательства у паллиативных и декоменсированных пациентов с злокачественными новообразованиями IV стадии.
Протокол ведения пациентов в послеоперационном периоде был единым. Антибактериальная терапия проводилась согласно рекомендациям СКАТ. Стратификация послеоперационных инфекционных осложнений проводилась по классификации CDC [8]. Степень их тяжести определялась по классификации Cvaien – Dindo [9].
Все пациенты предоставили добровольное информированное согласие на использование методики. Исследование получило одобрение этических комитетов ГУЗ ОКОД и ГУЗ УОКБ.
Болевой синдром оценивался с помощью визуально-аналоговой шкалы (ВАШ). Кроме того, измерялся уровень кортизола до операции, в 1-е и на 5-е сут после хирургического вмешательства.
Обезболивание в послеоперационном периоде себя включало использование НПВС либо инфузионных форм ингибиторов ЦОГ-2 (парацетамол 500 мг) 1–2 раза в день. При возникновении прорывных болей применялись опиоидные анальгетики (промедол 20 мг/мл – 1 мл).
Ведение послеоперационной лапаротом-ной раны осуществлялось по следующему алгоритму.
После завершения оперативного пособия производится ушивание лоскутов брюшины непрерывным узловым швом атравматичной иглой. Далее через контрапертуру, расположенную в 3 см от основного лапаротомного разреза, на ушитую брюшину устанавливается перфорированный микроирригатор (рис. 1).
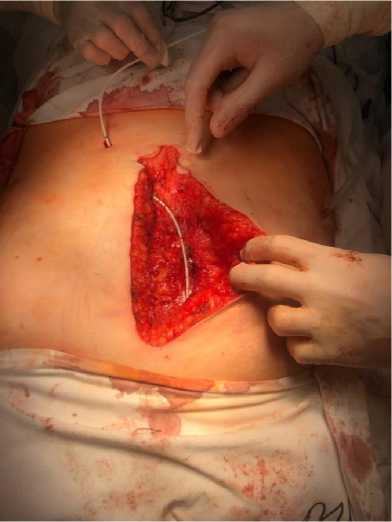
Рис. 1. Установленный преперитонеально перфорированный катетер
Fig. 1. Preperitoneally placed perforated catheter
Выполняется ушивание апоневроза либо узловым капроновым швом, либо непрерывной петлей из полидиоксанона. Затем в подкожножировую клетчатку передней брюшной стенки через контрапертуру, расположенную в 3 см от основного лапаротомного разреза, устанавливается 2-й перфорированный микроирригатор (с противоположной стороны от 1-го) (рис. 2).
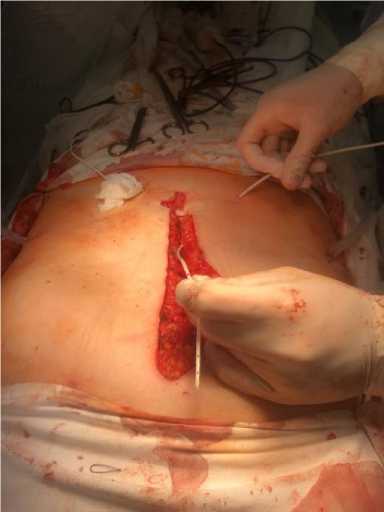
Рис. 2. Введение второго катетера в один из слоев раны
Fig. 2. Placement of a second catheter into a wound layer
Подкожно-жировая клетчатка также ушивается отдельными узловыми швами атравматичной иглой. Микроирригаторы должны быть расположены на всем протяжении раневой поверхности (рис. 3, 4). Такое расположение катетеров позволяет обеспечивать непре- рывную инфузию анестетика и периодическое введение антисептика, что создает оптимальные условия для обезболивания и предотвращения инфекционных осложнений. Далее кожа ушивается отдельными узловыми швами (рис. 5).
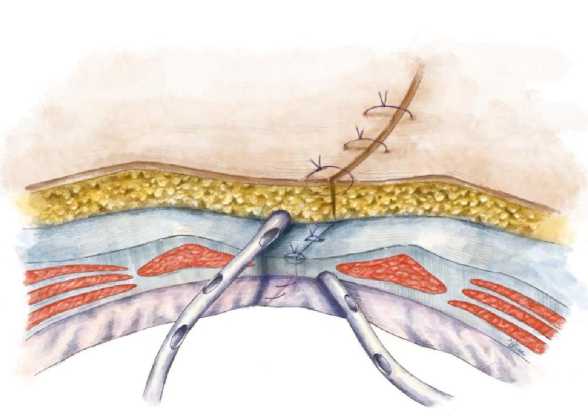
Рис. 3. Расположение катетеров в ране (поперечный срез)
Fig. 3. Cross-sectional view of a wound with a catheter
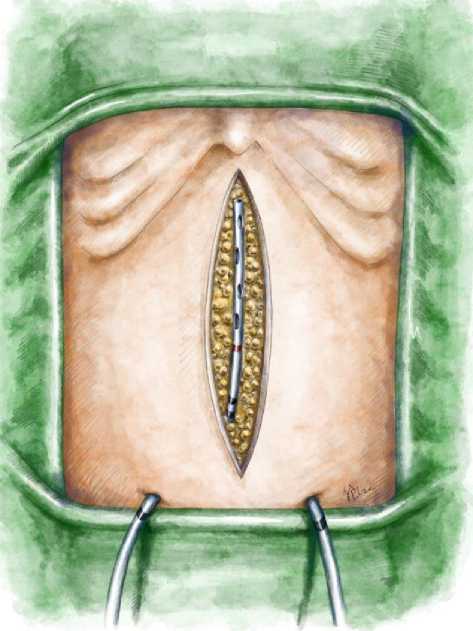
Рис. 4. Расположение катетера в подкожно-жировой клетчатке
Fig. 4. Catheter placement in the subcutaneous tissue
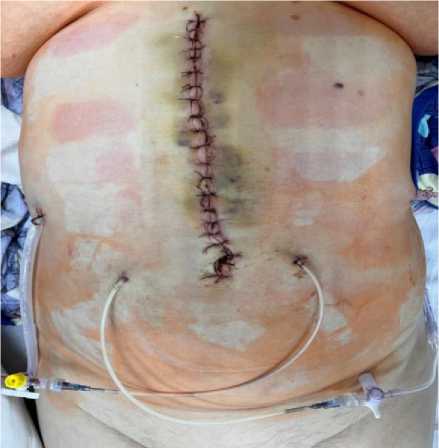
Рис. 5. Вид послеоперационной раны с введенными катетерами
Fig. 5. Postoperative wound with indwelling catheters
В первый установленный в предбрюшин-ное пространство катетер в качестве анестетика непрерывно при помощи дозатора-помпы со скоростью 5 мл/ч в течение 3 сут вводится 0,2 % ропивакаин. Во второй микро- ирригатор, установленный в подкожно-жировой клетчатке, в качестве антисептика бо-люсно по 20 мл 3 р./сут с интервалом 8 ч на протяжении 3 сут вводится раствор повидон-йода (рис. 6).
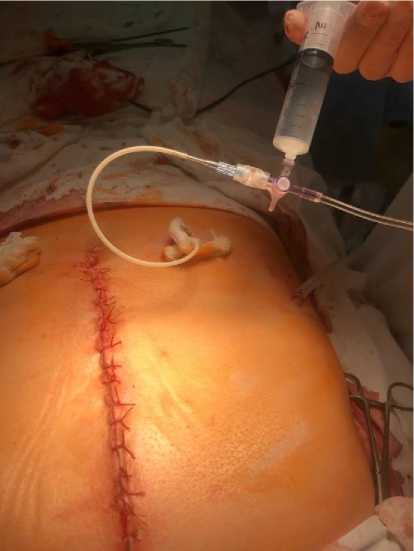
Рис. 6. Введение лекарственного средства в рану
Fig. 6. Introduction of a drug into the wound
Результаты. Предлагаемый метод был применен у 10 больных. Структура исследуе- мых пациентов представлена в табл. 1 и на рис. 7.
Таблица 1
Table 1
Clinical Data of the Studied Patients
|
Показатель Parameter |
M±SD / Me |
95 % ДИ (Q₁–Q₃) 95 % CI (Q₁–Q₃) |
|
Возраст, лет Age, years old |
66,50 |
64,25–68,75 |
|
Пол, абс. Gender, abs. (%) |
Жен. / Female |
2 (20) |
|
Муж. / Male |
8 (80) |
|
|
Продолжительность операции, мин Operating time, min |
190,00±42,75 |
159,42–220,58 |
|
Кровопотеря, мл Blood loss, ml |
400,00 |
400,00–400,00 |
|
Уровень кортизола, нг/мл Cortisol level, ng/ml |
96,20±12,95 |
86,94–105,46 |
Клинические данные исследуемых пациентов
2 (20 %)
3 (30 %)
(50 %)
-
■ Резекции ободочной кишки / Intestinal resections
-
■ Гастрэктомия / Gastrectomy
-
■ Гистерэктомия / Hysterectomy
Рис. 7. Типы операций
Fig. 7. Types of operations
В табл. 2 представлены результаты оценки также динамика уровня кортизола в процессе болевого синдрома у пациентов по ВАШ, а лечения.
Оценка болевого синдрома
Таблица 2
Table2
Pain assessment
|
Показатель / Parameter |
M±SD / Me |
95 % ДИ (Q₁–Q₃) 95 % CI (Q₁–Q₃) |
|
ВАШ в 1-е сут, баллов VAS, Day 1, score |
8,50±1,27 |
7,59–9,41 |
|
ВАШ на 5-е сут, баллов VAS, Day 5, score |
4,50 |
4,00–5,00 |
|
Уровень кортизола в 1-е сут, нг/мл Cortisol level, Day 1 (ng/ml) |
179,50±7,63 |
174,04–184,96 |
|
Уровень кортизола на 5-е сут, нг/мл Cortisol level, Day 5, (ng/ml) |
147,10±4,12 |
144,15–150,05 |
Примечание. ВАШ – визуально-аналоговая шкала.
Note. VAS – Visual Analog Scale.
У всех пациентов наблюдалось ускоренное заживление раны и отмечено отсутствие болевых ощущений в области хирургического вмешательства, что позволило обойтись без наркотических анальгетиков. Случаев развития ИОХВ не отмечалось. Возникшие осложнения относились 1-му и 2-му типам по классификации Clavien – Dindo, т.е. определялись как малые, и не были связаны с побочными эффектами предлагаемой методики.
Обсуждение. Существует множество методов профилактики развития инфекций области хирургического вмешательства. Одним из них является превентивная обработка раны антисептиком. По данным зарубежных исследований, интраоперационное орошение раневой поверхности раствором повидон-йода перед ушиванием значительно снижает риск развития ИОХВ по сравнению с применением других антисептиков или полным отсутствием воздействия [10, 11]. Также было установлено, что повидон-йод является наиболее эффективным и безопасным антисептическим средством по сравнению с хлоргексидином и раствором пероксида водорода [12]. Кроме того, продемонстрировано, что применение антисептических растворов для промывания ран может снизить потребность в использовании антибактериальных препаратов [13].
Согласно некоторым исследованиям непрерывная инфузия местного анестетика в ткани области хирургического вмешательства через катетер со множеством небольших отверстий позволяет значительно снизить послеоперационную боль, сократить потребление наркотических анальгетиков и сроки пребывания в стационаре. Это в свою очередь способствует более быстрому началу послеоперационной реабилитации и уменьшает риск возникновения инфекционных осложнений. У пациентов, которым проводили инфузии местного анестетика через катетер, установленный в рану, уже в первые сутки после операции отмечалось значительное снижение болевых ощущений и потребности в наркотических анальгетиках [14]. В различных исследованиях были предложены разнообразные методы установки катетеров, однако наиболее эффективной была признана установка в предбрюшинное пространство
Недостатком данного метода является размещение катетера в углу обширной раны, что может затруднить процесс регенерации тканей. Кроме того, используется только один катетер.
Авторы способа профилактики нагноения послеоперационных ран С.Н. Щерба и В.В. Половинкин предложили методику, которая заключается в том, что на дне раневой полости устанавливают перфорированную трубку, выводя ее концы наружу через заранее подготовленные контрапертуры на коже пациента, после чего фиксируют трубку к коже и герметично закрывают. Начиная со следующего дня после операции и в течение первых 2–3 послеоперационных дней ежедневно вводят 100–150 мл антисептического раствора через один из концов трубки, при этом второй конец остается закрытым. Это создает внутрираневую гидравлическую компрессию антисептика. Давление увеличивается до тех пор, пока раствор не начнет частично просачиваться между кожными швами. Затем закрытый конец трубки открывают и удаляют весь антисептик из раны. После этого полностью аспирируют оставшееся содержимое как в дренажной трубке, так и в ране. С 3–4-го по 9–10-й дни продолжают ежедневное промывание раны проточным способом без использования гидравлической компрессии [19].
Эта методика предполагает аспирацию содержимого дренажной трубки после введения большого объема антисептика, что усложняет процедуру и может увеличить вероятность развития осложнений. Кроме того, как и в первом методе, применяется только один катетер.
Ключевой особенностью нашего метода является комплексный подход, который гарантирует как эффективное обезболивание, так и про- филактику ИОХВ. В отличие от ранее существующих методик предложенный способ подразумевает использование двух перфорированных микроирригаторов, размещенных на различных уровнях послеоперационной раны.
Заключение. Разработанный метод значительно улучшает течение раннего послеоперационного периода, обеспечивает более эффективное и безопасное лечение пациентов. Его применение в клинической практике может снизить риск развития инфекций после плановых хирургических вмешательств при использовании лапаротомного доступа, а также обеспечить адекватное обезболивание, что позволит отказаться от наркотических анальгетиков, избежать нежелательных осложнений и сократить сроки госпитализации пациента.


