Способ обнаружения антител класса IgA к деамидированным пептидам глиадина у пациентов с IgA-нефропатией
Автор: Манцаева М.Е., Корабельников Д.И., Борисов А.Г.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.20, 2025 года.
Бесплатный доступ
Обоснование: IgA-нефропатия (IgA-H) – одна из ведущих причин развития терминальной почечной недостаточности, требующей проведения заместительной почечной терапии. Этиопатогенез болезни до конца не изучен. По результатам некоторых исследований предполагается связь с заболеваниями и состояниями, которые сопровождаются воспалением и повышенной проницаемостью кишечной стенки. Ряд исследований указывает на высокую распространенность определённых антител (АТ) в крови, специфичных и чувствительных для целиакии, у больных IgA-H. Предполагается, что эти АТ класса IgA влияют на активность и риски прогрессирования гломерулярного заболевания. Цель: разработать прогностическую модель для определения вероятности обнаружения АТ ДПГ IgA в сыворотке крови у пациентов с IgA-H. Методы: в исследовании приняло участие 105 пациентов в возрасте от 18 до 64 лет (мужчины – 92 (87,6%), женщины – 13 (12,4%)) с морфологически подтвержденной IgA-Н. Медиана длительности заболевания до проведения нефробиопсии составила 17 [6–48] месяцев. Результаты: на основании полученных при комплексном обследовании данных методом бинарной логистической регрессии построена прогностическая модель определения вероятности обнаружения АТ ДПГ IgA в сыворотке крови у пациентов с IgA-H в зависимости от протеинурии, систолического артериального давления и общего IgA. Полученная регрессионная модель имеет высокую статистическую значимость (площадь под ROC-кривой составила 0,860; 95% ДИ: 0,744–0,976; p<0,001). Чувствительность и специфичность модели составили 82,4% и 83,1%, соответственно. Заключение: разработанная прогностическая модель может снизить стоимость диагностики при отборе пациентов для тестирования на АТ; улучшить оценку рисков прогрессирования IgA-Н и создать новые возможности для персонифицированного клинического подхода и оптимизации лечебных стратегий, что, в свою очередь, может привести к улучшению почечных исходов для пациентов с IgA-H.
IgA-нефропатия, хронический гломерулонефрит, целиакия, антитела к деамидированным пептидам глиадина, прогностическая модель
Короткий адрес: https://sciup.org/140310624
IDR: 140310624 | DOI: 10.25881/20728255_2025_20_3_96
Method for determining the probability of detection of IgA antibodies to deamidated gliadin peptides in patients with IgA nephropathy
Backgraund: IgA nephropathy (IgA-N) is one of the leading causes of terminal renal failure requiring renal replacement therapy. The etiopathogenesis of the disease is not fully understood. Some studies suggest an association with diseases and conditions that are accompanied by inflammation and increased permeability of the intestinal wall. A number of studies indicate a high prevalence of certain antibodies (AB) in the blood specific and sensitive for celiac disease in IgA-N patients. These IgA AB are thought to influence the activity and risks of glomerular disease progression. Aims: to develop a tool (predictive model) to determine the probability of detecting of IgA AB to deamidated gliadin peptides (IgA DGP AB) in IgA-N patients serum. Materials and methods: the study included 105 patients aged 18 to 64 years with morphologically confirmed IgA-N. The median duration of the disease before nephrobiopsy was 17 (6–48) months. Distribution by sex: men – 92 (87.6%), women – 13 (12.4%). All patients underwent a complex clinical examination. Results: on the basis of the obtained data a prognostic model for determining the probability of detecting IgA DGP AB in IgA-N patients serum depending on proteinuria, systolic blood pressure and total IgA was constructed by the method of binary logistic regression. The regression model obtained has high statistical significance (the area under the ROC curve was 0.860; 95% CI: 0.744 to 0.976; p<0.001). The sensitivity and specificity of the model were 82.4% and 83.1%, respectively. Conclusions: the developed predictive model for determining the probability of detecting IgA DGP AB in IgA-N patients serum, which has high sensitivity and specificity, may reduce the cost of diagnostic measures in selecting patients for AB testing; improve risk assessment of IgA-N progression; and create new opportunities for personalized clinical approach and optimization of treatment strategies, which in turn may lead to improved renal outcomes for IgA-N patients.
Текст научной статьи Способ обнаружения антител класса IgA к деамидированным пептидам глиадина у пациентов с IgA-нефропатией
Обоснование
Иммуноглобулин A-нефропатия (IgA-H) – хроническая гломерулярная болезнь, связанная с воспалительным поражением почечных клубочков, опосредованным депозицией иммунных комплексов, содержащих аберрантный секреторный иммуноглобулин А и приводящая к развитию необратимых фибропластических изменений органа.
IgA-H является одной из ведущих причин терминальной почечной недостаточности, требующей проведения дорогостоящей заместительной почечной терапии [1; 2].
Этиопатогенез болезни остается недостаточно изученным. Существование потенциальной патогенетической энтероренальной оси позволяет предполагать, что развитие IgA-Н может быть ассоциировано с заболева-

ниями или состояниями, которые сопровождаются клинически очевидным или субклиническим воспалением с повышенной проницаемостью стенки кишечника и активацией MALT-системы кишечника [3–6].
В свете ранее проведенных исследований особое внимание следует уделять значению пищевых антигенов, в частности глютену, способных изменять иммунный ответ слизистой оболочки тонкой кишки и приводить к выработке специфических антител (АТ) [7–10]. Так, согласно экспериментальным данным пероральная иммунизация глиадином (фракция белка клейковины некоторых злаковых растений) способна приводить к отложению IgA в мезангии клубочков [8; 11].
Ассоциация IgA-H и целиакии (ЦК), где основным этиологическим фактором развития болезни является глютен, а также эффективность аглютеновой диеты у некоторых больных IgA-H [12; 13], вызывает необходимость уточнить значение специфических АТ, характерных для ЦК, у пациентов с IgA-H.
Принимая во внимание результаты ряда ранее проведенных исследований о распространенности АТ, характерных для ЦК [14–19], а также собственные данные о распространенности АТ класса IgA к деамидированным пептидам глиадина (АТ ДПГ IgA) среди больных IgA-H [20] и высокую активность гломерулярной болезни в данной группе больных мы предполагаем, что определенные целиакийные АТ могут служить дополнительным предиктором ускоренного прогрессирования заболевания и прогнозирования почечных исходов. Поскольку стандартные протоколы диагностики и лечения IgA-H не включают в себя скрининговое определение целиакийных АТ, возникает необходимость создания специального инструмента для выявления пациентов, нуждающихся в данном скрининге.
Цель
Разработать прогностическую модель для определения вероятности обнаружения АТ ДПГ IgA в сыворотке крови у пациентов с IgA-H.
Методы
Дизайн исследования
В одноцентровом проспективном сравнительном когортном контролируемом исследовании приняло участие 105 пациентов в возрасте от 18 до 64 лет.
Критерии соответствия
Критерии включения пациентов в исследование : пациенты обоего пола старше 18 лет; морфологически подтвержденная IgA-H; подписанное информированное согласие пациента на участие в исследовании.
Критерии невключения пациентов в исследование: CКФ по CKD-EPI <15 мл/мин/1,73 м2; атипичные формы IgA-H; пациенты на заместительной почечной терапии (программный гемодиализ, перитонеальный диализ, трансплантация почки); наличие у пациента тяжелых соматиче- ских заболеваний в стадии декомпенсации или обострения, онкологических и психических заболеваний; отсутствие подписанного больным информированного согласия.
Критерии исключения : положительный тест на беременность и период лактации; отказ пациента от дальнейшего участия в исследовании.
Условия проведения
Исследование проводилось среди пациентов, которые находились на обследовании и лечении в нефрологическом отделении Главного военного клинического госпиталя имени академика Н.Н. Бурденко Минобороны России (ГВКГ).
Продолжительность исследования
Исследование проводилось в период с сентября 2020 г. по апрель 2025 г.
Описание медицинского вмешательства
Всем пациентам проведено комплексное клиническое обследование. Выполнены клинический анализ крови и мочи, биохимический и иммунологический анализы крови, расчёт скорости клубочковой фильтрации по формуле CKD-EPI для оценки функционального состояния почек, определение суточной экскреции белка с мочой, измерение артериального давления (АД) стандартным методом и ультразвуковое исследование почек.
Антитела IgA к тканевой трансглютаминазе (АТ ТТГ IgA) и АТ ДПГ IgA определены в венозной крови иммуноферментным методом с применением набора реагентов Euroimmun и Orgentec (Германия). Антитела к эндомизию (АЭМ IgA) определены методом непрямой иммунофлюоресценции с применением набора реагентов Euroimmun (Германия).
Диагноз IgA-Н был установлен на основании прижизненной нефробиопсии с морфологическим исследованием почечной ткани методами световой микроскопии и иммунофлюоресцентного исследования.
Части серопозитивных пациентов (n = 12) выполнена фиброгастродуоденоскопия с биопсией из залукович-ного отдела двенадцатиперстной кишки с последующим морфологическим исследованием слизистой оболочки тонкой кишки.
Анализ в подгруппах
На основании полученных результатов обследования были сформированы две группы: в основную группу I (n = 20) вошли больные IgA-H с выявленными АТ ДПГ IgA, в контрольную группу II (n = 85) – пациенты с IgA-H, серонегативные по АТ ДПГ IgA, АТ ТТГ IgA и АЭМ IgA.
Этическая экспертиза
Исследование проводилось с одобрения независимого этического комитета при ГВКГ и независимого этического комитета при АНО ДПО «Московский медико-социальный институт им. Ф.П. Гааза» при соблюдении

действующего законодательства РФ и в соответствии с этическими принципами, принятыми Всемирной медицинской ассоциацией (Хельсинкская декларация).
Статистический анализ
Статистический анализ полученных данных проведен с использованием программы StatTech v. 4.8.0 (ООО «Статтех», Россия). Рассчитывали медиану (Me) с межквартильным размахом [Q1–Q3], среднее со стандартным отклонением (M±SD) и 95% доверительным интервалом (ДИ). Построение прогностической модели вероятности определенного исхода выполнялось при помощи метода логистической регрессии. Мерой определенности, указывающей на ту часть дисперсии, которая может быть объяснена с помощью логистической регрессии, служил коэффициент детерминации R2 Найджелкерка (Nagelkerke). Для оценки диагностической значимости количественных признаков при прогнозировании определенного исхода, применялся метод анализа ROC-кривых. Разделяющее значение количественного признака в точке cut-off определялось по наивысшему значению индекса Юдена (Youden’s index). Различия считались статистически значимыми при p<0,05.
Результаты
Объекты (участники) исследования
Средний возраст больных составил 35,48±9,68 лет. Медиана возраста дебюта IgA-H 30 [24–36] лет. Средний возраст на момент нефробиопсии 33,19±8,46 лет. Медиана длительности заболевания до проведения нефробиопсии составила 17 [6–48] месяцев. Распределение по полу: мужчины – 92 (87,6%), женщины – 13 (12,4%). 94 (89,5%) пациента получали нефропротективную терапию блокаторами ренин-ангиотензин-альдостероновой системы в максимально переносимых дозировках. Из них 80 (76,2%) больным терапия проводилась в течение более 3 месяцев. У 13 (12,4%) пациентов в анамнезе был шестимесячный курс лечения глюкокортикостероидами.
Основные результаты исследования
С целью определения вероятности обнаружения АТ IgA к ДПГ у пациентов с IgA-H нами была разработана прогностическая модель методом бинарной логистической регрессии в зависимости от протеинурии (ПУ, г/л), систолического артериального давления (САД, мм рт. ст.) и общего иммуноглобулина A (IgA, г/л). Число наблюдений составило 105. Наблюдаемая зависимость описывается следующим уравнением:
P = 1 / (1 + e-z) x 100% z = -13,396 + 1,020XПУ + 0,813XIgA + 0,055XСАД (1)
где: P – оценка вероятности обнаружения АТ IgA к ДПГ (%), z – значение логистической функции, XПУ – протеинурия (г/л), XIgA – IgA (г/л), XСАД – систолическое артериальное давление (мм рт. ст.).
Табл. 1. Характеристики связи предикторов модели с вероятностью выявления АТ IgA к ДПГ
|
Предикторы |
Unadjusted |
Adjusted |
||
|
COR; 95% ДИ |
p |
AOR; 95% ДИ |
p |
|
|
Протеинурия, г/л |
3,618; 1,562–8,373 |
0,003* |
2,774; 1,111–6,931 |
0,029* |
|
IgA, г/л |
2,344; 1,366–4,023 |
0,002* |
2,255; 1,271–3,999 |
0,005* |
|
САД, мм рт. ст. |
1,058; 1,016–1,102 |
0,007* |
1,057; 1,005–1,112 |
0,030* |
САД, мм рт. ст. - Н^
Протеинурия, г/л - = -----------------------■-----------------------
IgA, г/л - i ---------------------------------------
—i-------------------------------------1-----------------1-----------
1 3 5
ОШ; 95% ДИ
Рис. 1. Оценки отношения шансов с 95% ДИ для изучаемых предикторов.
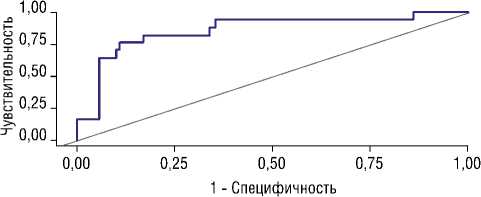
Рис. 2. ROC-кривая, характеризующая зависимость вероятности выявления АТ IgA к ДПГ от значения логистической функции P.
Полученная регрессионная модель с точки зрения соответствия прогнозируемых значений наблюдаемым при включении предикторов по сравнению с моделью без предикторов является статистически значимой (p <0,001). Псевдо-R2 Найджелкерка составил 40,3%.
Так, при увеличении ПУ на 1 г/л шансы выявления АТ IgA к ДПГ увеличивались в 2,774 раза. При увеличении IgA на 1 г/л шансы выявления АТ IgA к ДПГ увеличивались в 2,255 раза. При увеличении САД на 1 мм рт. ст. шансы выявления АТ IgA к ДПГ увеличивались в 1,057 раза.
Характеристики связи каждого из предикторов с шансами выявления АТ IgA к ДПГ представлены в таблице 1.
На рис. 1 сопоставлены значения скорректированного отношения шансов с 95% ДИ для изучаемых факторов, вошедших в модель (1).
При оценке дискриминационной способности регрессионной модели с помощью ROC-анализа была получена следующая кривая (Рис. 2).
Площадь под ROC-кривой составила 0,860; 95% ДИ: 0,744–0,976, p<0,001). Полученная модель была статистически значимой (p<0,001).
Пороговое значение оценок вероятности P в точке cut-off, которому соответствовало наивысшее значение
индекса Юдена (Youden’s index), составило 19,5%. Наличие АТ IgA к ДПГ прогнозировалось при значении оценок вероятности P выше данной величины или равном ей. Чувствительность и специфичность полученной прогностической модели составили 82,4% и 83,1%, соответственно.
Обсуждение
Резюме основного результата исследования
Скорректированная прогностическая модель, обладающая высокой чувствительностью и специфичностью, подтверждает возможность использования АТ IgA ДПГ в качестве дополнительного предиктора для оценки рисков прогрессирования IgA-H. С помощью данного инструмента появится возможность проводит целенаправленный отбор больных IgA-H для тестирования на предмет выявления АТ IgA ДПГ.
Обсуждение основного результата исследования
Основываясь на данных мировой литературы, факт выявления специфических АТ, характерных для ЦК у пациентов с IgA-H, позволил сформулировать гипотезу о связи IgA-H и ЦК. На уровне отдельных клинических наблюдений подтверждается вышеуказанная ассоциация, при этом назначение аглютеновой диеты положительно влияет на течение гломерулярного заболевания [21–23].
Авторы других исследований отметили высокую распространенность специфических целиакийных АТ среди пациентов с IgA-H без указания на морфологически подтвержденную глютеновую энтеропатию [14-20].
Общепринятого объяснения этому феномену не дано до сих пор. Рассматривая патогенез IgA-H с позиций энтероренальной оси, Coppo R. c соавт. отметили, что ключевую роль в образовании «патогенного» IgA играет усиленный иммунный ответ слизистых оболочек кишечника под воздействием различных антигенов, включая пищевые, такие как глютен.
Важным аспектом является роль MALT-системы кишечника, поскольку нарушение иммунологической толерантности, возникающее вследствие повреждения кишечного барьера и увеличенной абсорбции пищевых антигенов, может приводить к усилению иммунного ответа, субклиническому воспалению кишечника и избыточному синтезу галактозодефицитного IgA (Gd-IgA1). Gd-IgA1 откладывается в мезангии почечных клубочков, образуя депозиты, которые формируют характерную морфологическую картину IgA-H [3].
В экспериментальных условиях Papista K. c соавт. продемонстрировали, что глиадин участвует в образовании нефротоксичного циркулирующего комплекса IgA1-sCD89 не только за счёт взаимодействия с IgA1, но и посредством связывания с sCD89 (растворимая форма рецептора IgA). Исключение глютена из рациона приводило к снижению экспрессии CD71 (рецептор к трансферрину) и тканевой трансглутаминазы 2, уменьшению уровня мезангиального IgA1 и степени выраженности гематурии, а также к отсутствию иммунных комплексов IgA1-sCD89 в сыворотке крови и мезангии почек. Авторы отметили, что тяжесть и клиническая картина IgA-H зависели от прямого связывания глиадина с CD89. Кроме того, глютен вызывал увеличение секреции IgA1 в кишечнике, что способствовало воспалению и атрофии ворсинок слизистой оболочки тонкого кишечника. При этом уровень АТ к глиадину в крови коррелировал с выраженностью ПУ [11].
Использование антиглиадиновых АТ (АГА) в качестве дополнительного прогностического предиктора для пациентов с IgA-H впервые предложили Ots M. с соавт. В своём исследовании авторы отметили, что уровень АГА коррелировал с продолжительностью заболевания, возрастом и уровнем артериального давления. В группе АГА концентрация креатинина крови была выше, а СКФ, соответственно, ниже. Морфологические изменения в пределах площади нефробиоптата статистически значимо не отличались в группах, однако у пациентов с АГА выраженность интерстициального фиброза была выше и коррелировала с уровнем артериального давления и суточной ПУ [17].
Для отбора пациентов с IgA-H – возможных носителей АТ IgA ДПГ для тестирования нами ранее была разработаны прогностическая модель и программа для ЭВМ на ее основе, которая позволяет эффективно отбирать больных для скрининга на наличие АТ IgA ДПГ [24]. При продолжении исследования с увеличением количества пациентов мы скорректировали прогностическую модель на основании дополнительных данных.
Ограничения исследования
Исследование, выполненное на базе одного центра и относительно небольшой размер выборки, могут ограничивать воспроизводимость результатов в других условиях и возможности экстраполяции результатов на более крупные когорты. Разница в размерах групп (n = 20 vs n = 85) может снижать статистическую мощность сравнения.
Заключение
Разработанная прогностическую модель определения вероятности обнаружения АТ ДПГ IgA в сыворотке крови у пациентов с IgA-H, обладающая высокой чувствительностью и специфичностью, может снизить стоимость диагностических мероприятий при отборе пациентов для тестирования на АТ; улучшить оценку рисков прогрессирования IgA-Н и создать новые возможности для персонифицированного клинического подхода и оптимизации лечебных стратегий, что, в свою очередь, может привести к улучшению почечных исходов для пациентов с IgA-H.


