Способ получения и свойства препарата VIII фактора свертывания плазмы крови человека
Автор: Ямкин А.В., Стронин О.В., Никитина Л.Н., Семенова Н.А., Епанчинцев А.А.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Оригинальные исследования
Статья в выпуске: 2-2 т.24, 2009 года.
Бесплатный доступ
Разработан способ получения вирусинактивированного препарата VIII фактора свертывания из плазмы крови человека. Метод включает стадии криофракционирования, вирусной инактивации, эксклюзионной хроматографии, концентрирования и лиофилизации. При использовании разработанного способа выход фактора VIII после эксклюзионной хроматографии в среднем составлял 82±7%, удельная активность - 15±2 МЕ/мг белка. В готовом препарате активность фактора VIII составляла 13±2 МЕ/мл, удельная активность - 1,5±0,3 МЕ/мг белка. Данный способ сопоставим с зарубежными по экономическим показателям и позволяет получать препарат со стандартным качеством.
Фактор свертывания viii, эксклюзионная хроматография
Короткий адрес: https://sciup.org/14919054
IDR: 14919054 | УДК: 612.115.4:615.012.8
Preparation method and characteristics of a human blood plasma coagulation factor VIII
Method of preparing virus-inactivated human blood plasma coagulation factor VIII is presented in the article. The preparation was developed aimed at isolating coagulation factor VIII from human plasma. Economic parameters of the given method are comparable with those of world manufacturers which allows to receive the preparation of standard quality.
Текст научной статьи Способ получения и свойства препарата VIII фактора свертывания плазмы крови человека
СПОСОБ ПОЛУЧЕНИЯ И СВОЙСТВА ПРЕПАРАТА VIII ФАКТОРА СВЕРТЫВАНИЯ ПЛАЗМЫ КРОВИ ЧЕЛОВЕКА
Филиал ФГУП «НПО Микроген» МЗ РФ в г. Томск «НПО «Вирион»
Очищенные препараты VIII фактора свертывания плазмы крови человека применяются для лечения гемофилии А, и их получение является одной из основных целей промышленного фракционирования плазмы крови во всем мире [1-3]. В России такие препараты не производятся [1, 4], тогда как минимальная ежегодная потребность отечественного здравоохранения в препаратах VIII фактора свертывания составляет 300 миллионов международных единиц (МЕ) [5]. В связи с этим изучение возможностей различных способов производства данного препарата является актуальной задачей.
Целью настоящей работы являлась оценка эффективности оригинального способа получения и изучение свойств препарата VIII фактора свертывания плазмы крови, полученного этим способом.
Разработанный оригинальный способ (патент №2324495 «Способ получения препарата VIII фактора свертывания крови человека») является комбинированным и включает криофракционирование плазмы крови для получения криопреципитата, растворение криопреципитата, вирусинактивирующую обработку раствора криопреципитата, хроматографию, ультрафильтрацию и лиофилизацию. Криопреципитат получали из свежезамороженной плазмы крови, соответствующей ФС 42-0091-02, путем ее разморозки при температуре 3-4°С до полного исчезновения льда и формирования отчетливо видимого осадка. Затем проводили центрифугирование размороженной плазмы на проточной центрифуге ОТР101-К1
(Россия) при 15000 об/мин в течение (40±10) мин. Сразу после извлечения из ротора центрифуги полученный из плазмы осадок – криопреципитат – замораживали при температуре (–60±10)°С. Для получения очищенного фактора VIII криопреципитат растворяли в рабочем буфере при соотношении 0,4-2,0 мл рабочего буфера/г криопреципитата при (25±2)°С в течение 30 минут, затем полученный раствор криопреципитата подвергали осветляющей фильтрации с использованием префильтров с диаметром пор 5 мкм (NCG 29325, ООО «Палл Евразия», Москва). Вирусинактивирующую обработку раствора криопреципитата проводили сольвент-де-тергентным методом с использованием в качестве вирусинактивирующих агентов три-н-бутилфосфата и Тритона Х-100 (Sigma-Aldrich Chemie GmbH, Германия) в конечных концентрациях 0,3 и 1% соответственно. Инкубацию с вирусинактивирующими агентами проводили в течение 6 часов при температуре (27±2)°С при постоянном перемешивании. Затем проводили основную стадию очистки методом эксклюзионной хроматографии, для чего вирусинак-тивированный раствор криопреципитата наносили на хроматографическую колонну XK 50/90 (GE Healhcare Bio-Sciences AB, Швеция) с сорбентом Sepharose 4FF (GE Healhcare Bio-Sciences AB, Швеция) на скорости 60 см/ч при давлении в хроматографической системе (2,5±0,5) Бара. В полученный элюат, содержащий фактор VIII, добавляли стабилизаторы, а затем концентрировали его методом ультрафильтрации на полых волокнах с использованием аппаратов разделительных АР-0,1-100 ПС (г. Кириши) до получения необходимых значений активности фактора VIII на мл концентрируемого раствора. Затем проводили стерилизующую фильтрацию концентрированного элюата с использованием фильтров с диаметром пор 0,45 мкм (NXG 29325, ООО «Палл Евразия», Москва) и 0,22 мкм (NRG 29325, ООО «Палл Евразия», Москва), разливали продукт во флаконы, замораживали при температуре (– 45±5)°С и лиофилизировали. Лиофилизацию проводили в сублимационной установке ТГ-15 («Хохвакуум», Германия). Начальная температура в сублимационной установке составляла (–40±5)°С, конечная температура продукта составляла (45±5)°С. Общая длительность процесса лиофилизации продукта составляла (75±5) ч. Активность (количество) VIII фактора свертывания определяли методом измерения активированного частичного тромбопластинового времени (АЧТВ) с использованием коммерческих наборов («НПО Ренам», г. Москва), в качестве стандарта использовали плазму с аттестованной активностью фактора VIII («НПО Ренам», г. Москва). Содержание общего белка определяли биуретовым методом и методом Лоури [7]. Удельную активность фактора VIII оценивали как отношение активности фактора VIII к количеству общего белка в единице объема. Количество три-н-бутилфосфата определяли мето-17
дом газовой хроматографии [8], количество Тритона Х-100 определяли методом обращенно-фазовой хроматографии [9]. Белковый спектр раствора криопреципитата и хроматографического элюата изучали методом электрофореза в полиакриламидном геле в присутствии додецил-сульфата натрия [10].
Пробы не были нормированы по содержанию белка. Денситометрию геля проводили с помощью программы Phoretix.1.0.
Результаты представлены в виде среднего значения с указанием стандартного отклонения по выборке.
В таблице 1 представлены обобщенные данные, полученные при производстве 46 экспериментальных серий при загрузках 10-12 литров плазмы, и показаны активность и степень очистки фактора VIII на основных этапах. Полученные результаты показывают, что основная очистка фактора VIII происходит на стадии эксклюзионной хроматографии. Так, после криофракционирования и вирусинактивирую-щей обработки удельная активность фактора VIII в растворе криопреципитата составляла 0,19 МЕ/мг (табл. 1). Оценка молекулярно-массового состава методом электрофореза в полиакриламидном геле показала, что на данном этапе криопреципитат содержал 87% белков с молекулярным весом 50-80 кДа и 7% белков с молекулярным весом 330 кДа (рис. 1). Следует отметить, что, по данным литературы, почти 90% всех белков криопреципитата составляет фибриноген, имеющий молекулярную массу 340 кДа [11], который при электофорезе в редуцирующих условиях распадается на составляющие его альфа-бе-та-гамма-цепи с молекулярными массами 53-79 кДа [12]. Молекула фактора VIII в плазме крови в норме связана с молекулами фактора фон Виллебранда и
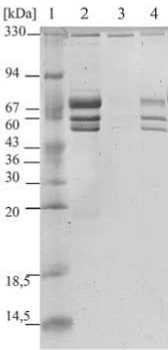
Рис. 1. Молекулярно-массовый состав исходного раствора криопреципитата и хроматографических пиков при эксклюзионной хроматографии.
1 - маркеры молекулярных весов, [кДа]; 2 - исходный раствор криопреципитата, загружаемый на колонну; 3 - элюат первого пика; 4 - элюат второго пика образует крупнейший белковый комплекс плазмы крови, молекулярная масса которого может достигать 20x103 кДа [13]. При электрофорезе в редуцирующих условиях комплекс фактор VIII – фактор фон Виллебранда также распадается на субъединицы с молекулярной массой порядка 240 кДа [12]. В связи с этим можно предположить, что в нашем исследовании молекулярно-массового состава (рис. 1) белки с молекулярным весом в области 50-80 кДа – это субъединицы фибриногена и другие балластные белки, а белки с молекулярным весом в области 330 кДа – это субъединицы комплекса фактора VIII, являющегося целевым белком в процессе очистки. Разница в молекулярных весах целевого белка и основного балластного белка – фибриногена обосновала выбор метода очистки эксклюзионной хроматографией с использованием сорбента, в гранулах которого радиус пор меньше, чем стоксовский радиус, отражающий
Таблица 1
Характеристика активности фактора свертывания VIII и концентрация вирусинактивирующих агентов в процессе получения препарата (M±m)
|
Наименование объекта исследования |
Активность VIII фактора свертывания [МЕ/мл] |
Содержание общего белка [мг/мл] |
Удельная актив -ность VIII фактора свертывания [МЕ/мг] |
Три-н-бу-тилфосфат, мкг/мл |
Тритон Х-100, мкг/мл |
Выход фактора VIII, % |
|
Вирусинактивирован-ный криопреципитат |
9±2* n=46 |
50±12* n=46 |
0,19±0,05 n=46 |
3000 |
100000 |
35±7° n=46 |
|
Элюат, содержащий |
5±1 |
0,33±0,02 |
15±2 |
0,3±0,1 |
0,5±0,2 |
82±7+ |
|
фактор VIII |
n=46 |
n=46 |
n=46 |
n=46 |
n=46 |
n=46 |
|
Препарат после |
13±2 |
8,5±1,3** |
1,5±0,3** |
0,8±0,2 |
0,6±0,2 |
35±5*** |
|
лиофилизации |
n=46 |
n=46 |
n=46 |
n=46 |
n=46 |
n=46 |
Примечание:
M – среднее арифметическое значение по выборке; m – стандартное отклонение по выборке; n – объем выборки;
° – по отношению к свежезамороженной плазме; * – замороженный криопреципитат разводили в 4 раза;
** – после добавления стабилизаторов; + – по отношению к раствору криопреципитата, наносимого на хроматографическую колонну;
*** – по отношению к содержанию фактора VIII в растворе криопреципитата.
молекулярный вес комплекса VIII фактора свертывания, но больше, чем стоксовский радиус молекул балластных белков [13]. Поэтому фактор VIII не проникает в гранулы сорбента и, оставаясь в свободном объеме колонны, элюируется первым пиком, а балластные белки проникают в поры гранул сорбента и элюируются медленнее, то есть вторым пиком. Этот механизм подтверждается при исследовании полученного хроматографического элюата. Так, методом АЧТВ было выявлено, что активность фактора VIII определялась только в элюате первого хроматографического пика (рис. 2).
Оценка молекулярно-массового состава также показала, что первый пик на 95% состоял из фракции с молекулярным весом не менее 320 кДа, к которой, предположительно, принадлежит фактор VIII (рис. 1). Во втором пике активность фактора VIII не определялась (рис. 2). По-видимому, это связано с тем, что второй пик на 93% состоял из белков и белковых субъ-
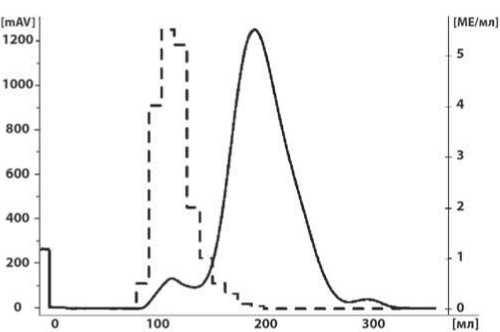
Рис. 2. Профиль элюции раствора криопреципитата при эксклюзионной хроматографии и активность фактора VIII в разных хроматографических пиках.
– активность фактора VIII [МЕ/мл]
– оптическая плотность при длине волны 280 нм [mAU]
единиц с молекулярной массой 50-80 кДа (рис. 1), к которым, предположительно, принадлежат балластные белки. По активности выход фактора VIII после эксклюзионной хроматографии в среднем составлял 82% от количества фактора VIII, содержавшегося в растворе криопреципитата, наносимого на хроматографическую колонну (табл. 1). При этом удельная активность фактора VIII в элюате составляла (15±2) МЕ/мг (табл. 1). Следует отметить, что хроматографический элюат, содержащий фактор VIII, является последним полупродуктом разработанного способа, где можно корректно оценить удельную активность фактора VIII как основного показателя степени очистки целевого белка, последующие показатели удельной активности оцениваются после добавления альбумина в качестве стабилизатора и не могут являться критерием степени очистки. Остаточное содержание три-н-бутилфосфата и тритона X-100 в элюате было 0,3±0,1 мкг/мл и 0,5±0,2 мкг/мл соответственно (табл. 1). Это в 10 раз меньше минимально допустимого остаточного количества три-н-бутилфосфата и в 20 раз меньше минимально допустимого остаточного количества тритона X-100 в препаратах крови согласно требованиям Всемирной организации здравоохранения [14]. После добавления стабилизаторов, концентрирования, стерилизующей фильтрации и лиофилизирования содержание общего белка в конечном препарате повысилось в 26 раз, тогда как активность фактора VIII только в 2,6 раза, что, соответственно, уменьшило удельную активность фактора VIII в конечном препарате в 10 раз. Это связано с тем, что добавление стабилизаторов, в частности альбумина, снижало удельную активность фактора VIII, повышая содержание общего белка. Кроме этого, в процессе обработки элюата (концентрирование, стерилизующая фильтрация, лиофилизация) терялось в среднем 58% от активности фактора
Таблица 2
Результаты контроля стабильности препарата VIII фактора свертывания
|
№ серии препарата |
17 |
17 |
17 |
19 |
19 |
19 |
22 |
22 |
22 |
|
Месяц/год исследования |
04/05 |
07/06 |
10/06 |
05/05 |
08/06 |
11/06 |
06/05 |
09/06 |
12/06 |
|
Описание |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
|
Подлинность |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
|
Растворимость |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
|
Прозрачность |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
|
Цветность |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
|
Механические включения |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
|
Содержание общего белка [мг/мл] |
7,7 |
7,2 |
7,5 |
8,9 |
9,1 |
9,3 |
8,1 |
8,4 |
7,8 |
|
Активность фактора VIII [МЕ/мл] |
12 |
11 |
12 |
13 |
14 |
12 |
14 |
13 |
13 |
|
Удельная активность фактора VIII [МЕ/мг] |
1,6 |
1,5 |
1,6 |
1,5 |
1,5 |
1,3 |
1,7 |
1,5 |
1,7 |
|
Пирогенность |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
|
Токсичность |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
|
Стерильность |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
соотв. |
VIII, содержащейся в хроматографическом элюате (табл. 1). При этом ориентировочно 20% активности фактора VIII в полупродукте терялось, предположительно, из-за денатурации молекул фактора VIII за счет гидродинамических сдвигов в процессах концентрирования и стерилизующей фильтрации, а 38% активности фактора VIII терялось при температурном воздействии в процессе лиофилизации (данные не представлены в таблицах).
Качество препарата контролировали согласно проекту фармакопейной статьи предприятия (ФСП), которая была составлена с учетом требований Европейской фармакопеи.
Как видно из таблицы 1, показатели активности фактора свертывания VIII и выход произведенных серий препарата стандартны и повторяемы. В отношении экономических показателей следует отметить, что выход фактора VIII при использовании разработанного способа составлял 8-18% от исходного содержания фактора свертывания VIII в плазме крови. По данным литературы, он колеблется в пределах 18-22% [15]. При этом, как по нашим (табл. 1), так и по данным литературы, до 70% целевого продукта терялось на стадии криофракционирования плазмы крови для получения криопреципитата [15, 16]. Соответственно выход активности фактора VIII относительно содержания в криопреципитате при получении по разработанному способу составлял 30-40% (табл. 1), что сопоставимо с общемировыми показателями (19-57%) [15-17].
Выборочный контроль стабильности серий препарата, проведенный через 3 и 6 месяцев после окончания срока хранения, составляющего 1 год согласно проекту ФСП, показал, что значения наиболее чувствительных к хранению параметров не изменились за исследуемый период (табл. 2).
Разработанный способ получения препарата VIII фактора свертывания сопоставим с подобными зарубежными способами по экономическим показателям и позволяет получать препарат стандартного качества.
-
1. Русанов В.М., Левин И. Лечебные препараты крови. – М.: Медпрактика, 2004. – 283 с.
-
2. Burnouf T. Plasma fractionation in the world: current status // Transfus Clin Biol. – 2007. – Vol. 14 (1). – P. 41-50.
-
3. Burnouf T. Modern plasma fractionation // Transfus Med Rev. – 2007. – Vol. 21 (2). – P. 101-17.
-
4. Государственный реестр лекарственных средств: Официальное издание (по состоянию на 1 сентября 2004): в 2 т. – М.: «Научный центр экспертизы средств медицинского применения» Минздрава России, 2004. – Т. 1-2.
-
5. 17 апреля – Международный день гемофилии: Электронный журнал «Медицинские ведомости». Выпуск №4 (47) 2002. Доступен по URL: http://www.medcom . spb.ru/archiv/mv_n47/current_articles.html/
-
6. Burnouf T. at al. A minipool process for solvent-detergent treatment of cryoprecipitate at blood centres using a
disposable bag system // Vox Sang. – 2006. – Vol. 91(1). – P. 56-62.
-
7. Досон Р., Эллиот Д., Эллиот У., Джонс К. Справочник биохимика. – М.: Мир, 1991. – С. 466-467.
-
8. Nellaiappan K. at al. Validation of simple and sensitive gas chromatographic method for the analysis of tri-n-bytyl phosphate from virally inactivated human immunoglobulin // J. of Chromatography B. – 2001. – Vol. 757. – P. 181-189.
-
9. Strancar А.at al. Extraction of Triton X-100 and its determination virus-inactivated human plasma by the solventdetergent method // J. of Chromatography A. – 1994. – Vol. 658. – P. 475-481.
-
10. Weber K., Osborn M. The reliability of molecular weight determinations by dodecylsulfate-polyacrylamide gel electrophoresis // J. Biol. Chem. – 1969. – Vol. 244. – P. 4406.
-
11. Lefebvre et al. Severe hypodysfibrinogenemia in compound heterozygotes of the fibrinogen A_IVS4_1G_T mutation and anA_Gln328 truncation (fibrinogen Keokuk) // Blood. – 2004. – Vol. 103, num. 7. – P. 2571-2576.
-
12. Sally L. at al. Studies on the Purification and Characterization of Human Factor VIII // The Journal of Clinical Investigation. – 1972. – Vol. 51. – P. 2151-2161.
-
13. Kaersgaard P., Barington K.A. Isolation of the factor VIII-von Willebrand factor complex directly from plasma by gel filtration // Journal of chromatography B. – 1998. – Vol. 715. – P. 357-367.
-
14. Guidelines on viral inactivation and removal procedures intended to assure the viral safety of human blood plasma products: Annex 4. – WHO Technical Report, Series No. 24, 2004. – P. 177.
-
15. Josic D. at. al Purification of factor VIII and von Willebrand factor from human plasma by anion-exchange chromatography // Journal of chromatography B. – 1994. – Vol. 662. – P. 181-190.
-
16. Brockway W.J. et al Gel filtration of factor VIII United States Patent. Num.5,177,191 Jan. 5, 1993. Доступен по URL: http://www.freepatentsonline.com/5177191.html ? query=PN%2F5177191+OR+5177191&stemming=on
-
17. Farrugia A.,Robert P. Plasma protein therapies: current and future perspectives // Best Pract Res Clin Haemotol. – 2006. – Vol. 19(1). – P. 243-58.
PREPARATION METHOD
AND CHARACTERISTICS OF A HUMAN
BLOOD PLASMA COAGULATION
FACTOR VIII
A.V. Yamkin, O.V. Stronin, L.N. Nikitina, N.A. Semenova, A.A. Epanchintsev
Список литературы Способ получения и свойства препарата VIII фактора свертывания плазмы крови человека
- Русанов В.М., Левин И. Лечебные препараты крови. -М.: Медпрактика, 2004. -283 с.
- Burnouf T. Plasma fractionation in the world: current status//Transfus Clin Biol. -2007. -Vol. 14 (1). -P. 41-50.
- Burnouf T. Modern plasma fractionation//Transfus Med Rev. -2007. -Vol. 21 (2). -P. 101-17.
- Государственный реестр лекарственных средств: Официальное издание (по состоянию на 1 сентября 2004): в 2 т. -М.: «Научный центр экспертизы средств медицинского применения» Минздрава России, 2004. -Т. 1-2.
- апреля -Международный день гемофилии: Электронный журнал «Медицинские ведомости». Выпуск №4 (47) 2002. Доступен по URL: http://www.medcom.spb.ru/archiv/mv_n47/current_articles.html/
- Burnouf T. at al. A minipool process for solvent-detergent treatment of cryoprecipitate at blood centres using a disposable bag system//Vox Sang. -2006. -Vol. 91(1). -P. 56-62.
- Досон Р., Эллиот Д., Эллиот У., Джонс К. Справочник биохимика. -М.: Мир, 1991. -С. 466-467.
- Nellaiappan K. at al. Validation of simple and sensitive gas chromatographic method for the analysis of tri-n-bytyl phosphate from virally inactivated human immunoglobulin//J. of Chromatography B. -2001. -Vol. 757. -P. 181-189.
- Strancar А.at al. Extraction of Triton X-100 and its determination virus-inactivated human plasma by the solvent-detergent method//J. of Chromatography A. -1994. -Vol. 658. -P. 475-481.
- Weber K., Osborn M. The reliability of molecular weight determinations by dodecylsulfate-polyacrylamide gel electrophoresis//J. Biol. Chem. -1969. -Vol. 244. -P. 4406.
- Lefebvre et al. Severe hypodysfibrinogenemia in compound heterozygotes of the fibrinogen A_IVS4_1G_T mutation and anA_Gln328 truncation (fibrinogen Keokuk)//Blood. -2004. -Vol. 103, num. 7. -P. 2571-2576.
- Sally L. at al. Studies on the Purification and Characterization of Human Factor VIII//The Journal of Clinical Investigation. -1972. -Vol. 51. -P. 2151-2161.
- Kaersgaard P., Barington K.A. Isolation of the factor VIII-von Willebrand factor complex directly from plasma by gel filtration//Journal of chromatography B. -1998. -Vol. 715. -P. 357-367.
- Guidelines on viral inactivation and removal procedures intended to assure the viral safety of human blood plasma products: Annex 4. -WHO Technical Report, Series No. 24, 2004. -P. 177.
- Josic D. at. al Purification of factor VIII and von Willebrand factor from human plasma by anion-exchange chromatography//Journal of chromatography B. -1994. -Vol. 662. -P. 181-190.
- Brockway W.J. et al Gel filtration of factor VIII United States Patent. Num.5,177,191 Jan. 5, 1993. Доступен по URL: http://www.freepatentsonline.com/5177191.html? query=PN%2F5177191+OR+5177191&stemming=on
- Farrugia A.,Robert P. Plasma protein therapies: current and future perspectives//Best Pract Res Clin Haemotol. -2006. -Vol. 19(1). -P. 243-58.


