Сравнение биологической эффективности импульсного и непрерывного нейтронного излучения с энергией 14 МэВ на культуре клеток мышиной меланомы В-16
Автор: Исаева Е.В., Бекетов Е.Е., Корякин С.Н., Лычагин А.А., Ульяненко С.Е.
Рубрика: Научные статьи
Статья в выпуске: 2 т.21, 2012 года.
Бесплатный доступ
Исследовано влияние импульсного (10, 50 и 75 Гц) и непрерывного нейтронного излучения с энергией 14 МэВ на клоногенную активность клеток мышиной меланомы В-16 в диапазоне доз 0,5-5 Гр. По результатам исследований не выявлено различий в биологической эффективности импульсного излучения в исследованном диапазоне частот и доз. По тесту клоногенной активности клеток мышиной меланомы В-16 не обнаружено также различий между облучением в импульсном и непрерывном режимах в указанном дозовом диапазоне.
Импульсное и непрерывное нейтронное облучение, меланома в-16
Короткий адрес: https://sciup.org/170170070
IDR: 170170070
Comparison of biological effectiveness of pulse and continuous radiation of 14 MeV neutrons on murine melanoma B-16 cell culture
The effect of pulse (10, 50, 75 Hz) and continuous radiation of 14 MeV neutrons in 0.5-5 Gy dose range on melanoma B-16 cells clonogenic growth was studied. Obtained results show no difference in biological effectiveness of pulse radiation of different frequencies. Clonogenic assay of murine melanoma B-16 cells did not show a difference between effects of pulse and continuous radiation modes within studied dose range.
Текст научной статьи Сравнение биологической эффективности импульсного и непрерывного нейтронного излучения с энергией 14 МэВ на культуре клеток мышиной меланомы В-16
В лучевой терапии злокачественных новообразований используются редко- и плотноио-низирующие излучения, генерируемые, как правило, источниками непрерывного действия. Для обеспечения локального противоопухолевого эффекта необходимо достичь высоких поглощённых доз облучения в мишени, однако, с повышением дозы начинают нарастать побочные эффекты действия излучений на нормальные ткани, попадающие в зону облучения. Одним из возможных способов уменьшения такого негативного действия ионизирующих излучений в настоящее время является разработка методов низкодозовой лучевой терапии с сохранением противоопухолевого эффекта, что становится возможным при использовании импульсно-периодического режима облучения с определёнными частотами повторения импульсов [4].
Представленные в литературе результаты исследований по сопоставлению биологического действия облучения в импульсном и непрерывном режимах на различные тест-системы, а также облучения в импульсном режиме с различной частотой импульсов в большинстве случаев противоречивы. Одни авторы наблюдали увеличение радиопоражаемости клеток с уменьшением частоты импульсов рентгеновского излучения [12, 13], в то время как по данным других авторов биологический эффект не зависел от частоты импульсов в широких её пределах [8, 15]. Повышение биологической эффективности пучка протонов (энергия 1000 МэВ) с уменьшением частоты импульсов с 45,9 до 4,5 с-1 наблюдали в работе [3] в экспериментах по общему равномерному облучению животных. В работе [4] показано, что импульсно-периодическое рентгеновское излучение (ИПРИ) способно проявлять антипролиферативную активность в системе in vitro на культуре опухолевых клеток. При этом цитостатический эффект ИПРИ в значительной степени зависел от используемой частоты повторения импульсов («частотное окно» – 8, 10, 13, 16, 25 Гц), поглощённой дозы («дозовый коридор» от 0,003 до 0,1 Гр) и линии опухолевых клеток. Цитостатический эффект, отмеченный для ИПРИ в системе in vitro , сохранялся и при локаль-
Исаева Е . В . – ст. науч. сотр., к.б.н.; Бекетов Е . Е . – аспирант; Корякин С . Н . – вед. науч. сотр., к.б.н.; Ульяненко С . Е . * – зав. отделом, д.б.н.
ном облучении опухоли (карциномы легких Льюис) в системе in vivo [1]. При изучении дозовой зависимости выхода аберраций хромосом в культуре лимфоцитов человека при облучении нейтронами со средней энергией 0,7 МэВ в импульсном режиме в работе [7] не обнаружено достоверных различий в цитогенетическом эффекте при частоте импульсов 1 и 5 Гц, однако, авторы отметили его повышение при частоте 100 Гц. Также противоречивы и результаты исследований по сопоставлению биологического действия смешанного гамма-нейтронного излучения импульсного реактора БАРС-6 (средняя энергия нейтронов 1,44 МэВ), работающего в двух режимах: одиночный импульс длительностью ~ 65 мкс и непрерывное излучение длительностью 1 ч. В зависимости от используемой тест-системы отмечалась большая эффективность или импульсного режима облучения [6], или непрерывного [5], или авторы не наблюдали достоверных различий в действии обоих режимов облучения [2, 5, 6, 9, 10].
Из анализа литературных данных следует, что в настоящее время вопрос о биологическом действии импульсного ионизирующего излучения, и в частности импульсного нейтронного воздействия, далеко не решен. В связи с этим цель настоящей работы состояла в исследовании биологической эффективности импульсного нейтронного излучения с энергией 14 МэВ в зависимости от частоты импульсов (10, 50 и 75 Гц). Также интересовал вопрос, как соотносятся данные по выживаемости клеток млекопитающих, полученные при облучении импульсным нейтронным излучением, с результатами облучения в непрерывном режиме.
Материалы и методы
В качестве источников нейтронного излучения использовали импульсный генератор ИНГ-031 и генератор НГ-14 непрерывного действия, разработанные во ВНИИ автоматики им. Н.Л. Духова (Москва). Средний выход нейтронов из мишени с энергией ~ 14 МэВ, образующихся в результате реакции 3Н(d,n)4Не, составлял для ИНГ-031 6,6·109 н/с и для НГ-14 1,4·1010 н/с. Длительность импульса – 1 мкс, возможный диапазон изменения частоты следования импульсов от 1 до 100 Гц (для ИНГ-031). В экспериментах использовали частоты – 10, 50 и 75 Гц. Вклад сопутствующего гамма-излучения находился в пределах 10-17 %, в зависимости от расстояния до мишени. Для уменьшения вклада сопутствующего гамма-излучения в общую дозу облучения верхнюю чашку экранировали свинцовой пластиной толщиной 2 мм.
Недостатком работы генератора ИНГ-031 была нестабильность потока нейтронов во время облучения, довольно быстрый спад выхода нейтронов по мере проведения серии последовательных облучений и ограничение в длительности одного сеанса (15 мин при частоте импульсов 50 Гц). Поэтому для получения требуемых доз в заданном диапазоне от 0,5 до 5 Гр была применена схема облучения, представленная на рисунке 1. Опытные образцы облучали в чашках Петри диаметром 35 мм, которые располагали стопкой по 4-5 чашек. Расстояние от мишени генератора ИНГ-031 до дна верхней чашки в разных экспериментах составляло: 2,3, 2,5 и 2,8 см. Усреднённые по ряду опытов дозы облучения, мощности доз, дозы за импульс на одних и тех же расстояниях от мишени приведены в таблице 1.
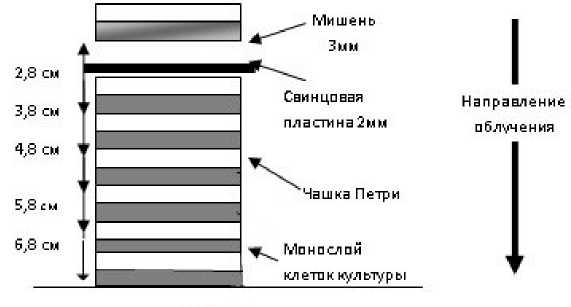
Рис . 1. Схема облучения культуры клеток меланомы В-16 в монослое на ИНГ-031.
Таблица 1
Параметры нейтронного облучения клеток меланомы В -16 в монослое на генераторе ИНГ -031
|
Расстояние от мишени генератора , см |
Среднее время облучения , с |
Доза , Гр |
Мощность дозы , Гр ·10-4/ с |
Доза за импульс , Гр ·10-4 |
|
Частота 10 Гц |
||||
|
2,3 |
2,3 |
12,2 |
1,2 |
|
|
2,8 |
1890 |
1,9 |
10,1 |
1,0 |
|
3,3 |
1,4 |
7,4 |
0,7 |
|
|
3,8 |
1,1 |
5,8 |
0,6 |
|
|
Частота 50 Гц |
||||
|
2,3 |
4,6 |
51,1 |
1,0 |
|
|
2,8 |
3,4 |
37,7 |
0,8 |
|
|
3,3 |
2,7 |
30,0 |
0,6 |
|
|
3,8 |
900 |
2,2 |
24,4 |
0,5 |
|
4,5 |
1,7 |
18,9 |
0,4 |
|
|
5,5 |
1,2 |
13,3 |
0,3 |
|
|
6,5 |
0,7 |
7,7 |
0,2 |
|
|
Частота 75 Гц |
||||
|
2,5 |
3,3 |
68,8 |
0,9 |
|
|
3,5 |
2,0 |
41,6 |
0,6 |
|
|
4,8 |
480 |
1,3 |
27,1 |
0,4 |
|
5,3 |
1,0 |
20,8 |
0,3 |
|
|
5,3 |
0,9 |
18,8 |
0,3 |
|
|
6,3 |
0,8 |
16,7 |
0,2 |
|
На генераторе НГ-14 чашки с культурой клеток также облучали стопкой. Расстояние до мишени от дна верхней чашки в стопке составляло 4,6 см. Исследованный диапазон доз 0,6-4,9 Гр. Мощность дозы уменьшалась с 41,7·10-4 Гр/с на расстоянии от мишени 4,6 см (верхняя чашка) до 7,4·10-4 Гр/с на расстоянии 9,6 см (нижняя чашка). Длительность облучения составляла 14-20 мин.
Дозиметрию осуществляли с помощью «Измерителя импульсного потока нейтронов автоматизированного» (ИНПА), поставляемого вместе с генератором, а также дозиметров ДКС-101 и Unidos. Погрешность определения дозы составляла около 10 %.
В качестве экспериментальной биологической тест-системы использовали культуру клеток мышиной меланомы В-16, полученную из РОНЦ им. Н.Н. Блохина, приспособленную к выращиванию в монослое. Клетки культивировали в среде RPMI-1640 с добавлением антибиотиков
(канамицин 100 мг/мл), 10 % фетальной сыворотки в атмосфере, содержащей 5 % СО 2 , при температуре 37 ° С. Облучали культуру в поздней лог-фазе в монослое в чашках Петри (Corning, США) диаметром 35 мм при комнатной температуре. После облучения выживаемость клеток определяли по методу Puck T. и Marcus P. [14], модифицированному для наших условий. Для этого облучённые клетки снимали со дна чашек Петри раствором трипсина-ЭДТА, ресуспенди-ровали до получения одиночных клеток и подсчитывали в камере Горяева. Высевали (от 1000 до 100 000 клеток на флакон в зависимости от дозы облучения) в чашки Петри (Corning, США) диаметром 100 мм в среду RPMI-1640 с добавлением 10 % фетальной сыворотки и выдерживали в СО 2 -инкубаторе при температуре 37 ° С в течение 8-11 дней до формирования видимых невооруженным глазом колоний. По окончании инкубации культуральную среду удаляли, колонии окрашивали 2 % раствором метиленового синего в 50 % этаноле по методике, описанной Guda K. et al. [11]. Подсчёт вели на счётчике Scan 100 (Interscience, Франция), учитывая колонии, содержащие 50 и более клеток. Фракцию клоногенных клеток выражали в процентах по отношению к высеянным. Полученные значения соотносили с выживаемостью в контроле.
Статистическую обработку результатов и определение параметров кривых доза-эффект осуществляли с помощью пакета программ «Origin 6.1». Аппроксимацию экспериментальных данных проводили по линейно-квадратичной модели:
- InS = aD + ро2, где S - доля выживших клеток; D - доза облучения, Гр; а, в - коэффициенты, отражающие вероятность образования летальных повреждений в треках одной или нескольких частиц.
Соответствие экспериментальных данных указанной модели оценивали с помощью критерия % 2.
Результаты и обсуждение
Экспериментальные результаты зависимости клоногенной активности клеток меланомы В-16 от дозы и частоты импульсного нейтронного излучения представлены на рисунке 2 в виде кривых доза-эффект.
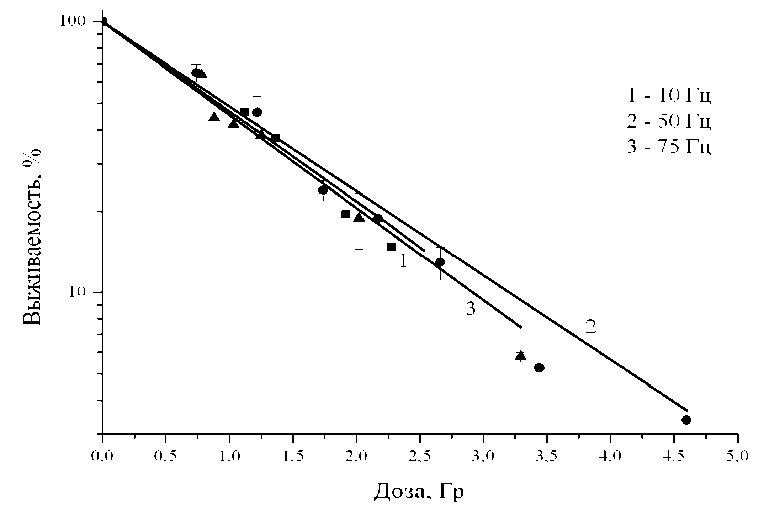
Рис . 2. Кривые доза-эффект для мышиной меланомы В-16, облучённой импульсным нейтронным излучением (14 МэВ) с частотой импульсов 10 Гц (кривая 1, квадраты), 50 Гц (кривая 2, круги) и 75 Гц (кривая 3, треугольники). Коэффициенты а кривых: 1) 0,76271 ± 0,03485;
2) 0,71867 ± 0,03527; 3) 0,79058 ± 0,04825.
Как следует из приведённых данных, эта зависимость носит линейный характер при всех исследованных частотах следования импульсов в указанном диапазоне доз (соответственно уравнение, описывающее линейную зависимость, принимает вид: - In S = a D ). Вследствие ограниченного выхода нейтронов генератора ИНГ-031 для кривой 10 Гц были получены данные в основном на начальном участке.
Используемая в наших экспериментах схема облучения, когда воздействию подвергается сразу стопка чашек, приводит к изменению мощности дозы в каждой последующей чашке. Однако, на одних и тех же расстояниях от мишени генератора, при разных частотах доза за импульс и, соответственно, мощность дозы в импульсе имеют близкие значения (табл. 1). Таким образом, одна и та же доза может быть «набрана» разным количеством импульсов, и конечный эффект облучения клеток зависит от частоты, а не от мощности дозы. Сопоставление между собой данных по выживаемости клеток меланомы В-16, полученных после воздействия при частотах 10, 50 и 75 Гц, не выявило значимых отличий между ними, из чего следует заключение: изменение частоты следования импульсов нейтронного излучения как в сторону уменьшения, так и в сторону увеличения от 50 Гц (базовой частоты для ИНГ-031) не приводит к уменьшению или увеличению количества выживших клеток. Эффект облучения в данном случае не зависит от частоты импульсов. Этот вывод совпадает с данными работы [7], где исследовали дозовую зависимость выхода аберраций хромосом в культуре лимфоцитов человека при импульсном нейтронном облучении с частотой 1 и 5 Гц. Возможно, биологический эффект облучения определяется как раз тем, какие именно частоты следования импульсов применяются. Так, в работах [1, 4] при исследовании антипролиферативного действия ИПРИ на опухолевые клетки, показано, что эффект проявлялся только при определённых частотах и в определённом диапазоне доз. Одновременно авторы пришли к выводу, что фактор длительности импульсов в проведённых экспериментах существенным не является. Возможные механизмы анти-пролиферативного действия ИПРИ на опухолевые клетки связаны, по мнению авторов, с индукцией активных форм кислорода, выходом цитохрома С из митохондрий, активацией экспрессии р53 и, в конечном счёте, с индукцией процесса апоптоза. Поскольку как редко-, так и плотноио-низирующие излучения инициируют в клетках одни и те же первичные физико-химические процессы, указанные механизмы могут иметь место и при действии нейтронного излучения. Вопрос заключается в том, какой дозовый и частотный диапазон следует исследовать в этом случае.
Следующим этапом наших исследований было сравнение биологической эффективности импульсного нейтронного излучения генератора ИНГ-031 при частоте 50 Гц с эффективностью непрерывного нейтронного излучения генератора НГ-14. Результаты представлены на рисунке 3.
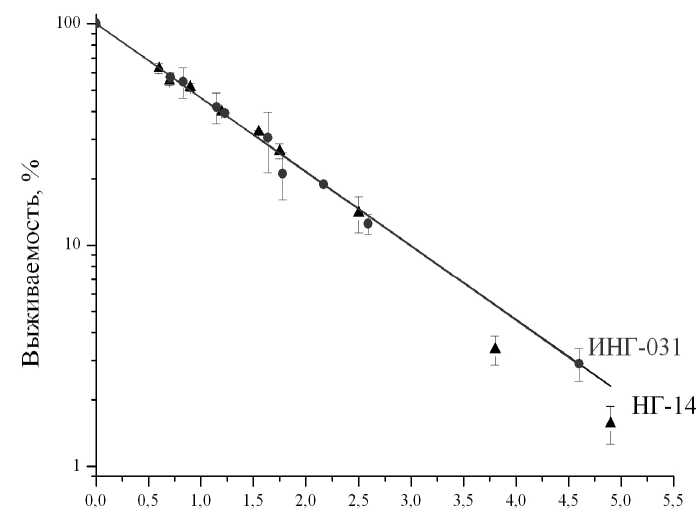
Доза, Гр
Рис . 3. Кривые доза-эффект клоногенной активности клеток мышиной меланомы В-16, облучённой импульсным (ИНГ-031, 50 Гц) (круги) и непрерывным (НГ-14) (треугольники) нейтронным излучением с энергией 14 МэВ.
Как видно из рисунка, кривые доза-эффект, построенные на основе данных, полученных в ряде экспериментов на двух установках, в исследованном диапазоне доз имеют линейный характер с одинаковыми коэффициентами α , равными 0,769 ± 0,013 и 0,771 ± 0,014 для НГ-14 и ИНГ-031 соответственно. Обычно различия в действии излучения в импульсном и непрерывном режимах связывают с различиями в мощности дозы. Действительно, особенностью импульсного режима облучения является то, что в момент прохождения импульса мощность дозы может достигать очень высоких значений. Например, в проведённых экспериментах на ИНГ-031 она доходила до 1,2·102 Гр/с в импульсе, в то время как минимальная мощность дозы для НГ-14 (непрерывный режим) составляла всего 7,4·10-4 Гр/с. Однако нами по тесту клоногенной активности клеток мышиной меланомы В-16 не обнаружено различий между облучением в импульсном и непрерывном режимах в указанном дозовом диапазоне.
Заключение
Таким образом, в проведённых нами исследованиях не выявлено различий в биологической эффективности импульсного нейтронного излучения с энергией 14 МэВ при различной частоте следования импульсов (10, 50 и 75 Гц). Возможно, для выявления закономерностей, характерных, по данным других авторов, для редкоионизирующих излучений, требуется исследовать другой дозовый или частотный диапазон. Также по тесту клоногенной активности клеток мышиной меланомы В-16 не обнаружено эффекта мощности дозы для нейтронного излучения с энергией 14 МэВ. Это позволяет нам в последующем использовать обе установки как взаимозаменяемые при исследовании одновременного действия гамма- и нейтронного излучений.
Список литературы Сравнение биологической эффективности импульсного и непрерывного нейтронного излучения с энергией 14 МэВ на культуре клеток мышиной меланомы В-16
- Булдаков М.А., Литвяков Н.В., Климов И.А. и др. Влияние низкодозового импульсно-периодического рентгеновского излучения на рост и метастазирование карциномы легких Льюис//Сибирский онкологический журнал. 2011. Т. 48, № 6. С. 47-51.
- Исаева Е.В., Корякин С.Н., Ульяненко С.Е. и др. Клоногенная активность клеток мышиной меланомы В-16 после облучения на импульсном реакторе БАРС-6//Медицинская радиология и радиационная безопасность. 2010. Т. 55, № 3. С. 5-10.
- Коннов Б.А., Карлин Д.Л., Коннова Л.А. и др. Влияние ультрафракционирования на эффект общего равномерного облучения протонами с энергией 1000 МэВ//Радиобиология. 1988. Т. 28, № 6. С. 822-827.
- Литвяков Н.В., Ростов В.В., Булдаков М.А. и др. Ингибирование пролиферации опухолевых клеток импульсно-периодическим рентгеновским излучением//Сибирский онкологический журнал. 2006. Т. 17, № 1. С. 24-31.
- Рябченко Н.И., Ульяненко С.Е., Рябченко В.И. и др. Радиолиз липосом, растворов ферросульфата и альбумина смешанным γ-нейтронным излучением с различной мощностью дозы//Радиационная биология. Радиоэкология. 2005. Т. 45, № 5. С. 571-575.
- Рябченко Н.И., Ульяненко С.Е., Антощина М.М. и др. Действие смешанного γ-нейтронного излучения с различной мощностью дозы на содержание клеток в тимусе и хромосомы костного мозга мышей и лимфоцитов человека//Радиационная биология. Радиоэкология. 2005. Т. 45, № 5. С. 592-598.
- Севанькаев А.В., Герасименко В.Н. Сравнительная частота аберраций хромосом в культуре лимфоцитов человека в зависимости от режима нейтронного облучения//Радиобиология. 1989. Т. 29. С. 264-266.
- Стяжкина Т.В., Хаймович Т.И. Действие импульсного ионизирующего излучения на лимфоциты крови человека in vitro//Медицинская радиология. 1982. Т. 27, № 5. С. 68-69.
- Цыб Т.С., Комарова Е.В., Потетня В.И. и др. Биологическая эффективность импульсного и непрерывного нейтронного излучения для клеток дрожжей Saccharomyces//Радиационная биология. Радиоэкология. 2001. Т. 41, № 3. С. 290-294.
- Цыб Т.С., Комарова Е.В., Малинова И.В. и др. Изучение эффектов действия нейтронного излучения с различной мощностью дозы на клетках дрожжей Saccharomyces различного генотипа//Радиационная биология. Радиоэкология. 2007. Т. 47, № 5. С. 598-607.
- Guda K., Natale L., Markowitz S.D. An improved method for staining cell colonies in clonogenic assays//Cytotechnology. 2007. V. 54. P. 85-88.
- Merz T., Michelsen A. Radiat. Res. 1972. V. 51. P. 513.
- Prempree T., Michelsen A., Merz T. The repair time of chromosome breaks induced by pulsed x-rays on ultra-high dose-rate//Int. J. Radiat. Biol. 1969. V. 15, N. 6. P. 571-574.
- Puck T.T., Marcus P.I. Action of X-rays on mammalian cells//J. Exp. Med. 1956. V. 103. P. 653-666.
- Purrott R.J., Reeder E.J. Chromosome aberration yields induced in human lymphocytes by 15 MeV electrons given at a conventional dose-rate and in microsecond pulses//Int. J. Radiat. Biol. 1977. V. 31, N. 3. P. 251-256.


