Сравнение двух комбинированных режимов лекарственной терапии по почечному повреждению у пациентов с метастатическим раком почки, ранее перенёсших одностороннюю нефрэктомию
Автор: Титов К.С., Епифанова М.В., Алимов А.А., Нестерова О.Ю., Шутов Е.В., Лебедев С.С., Запиров Г.М.
Журнал: Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье @vestnik-reaviz
Рубрика: Клиническая медицина
Статья в выпуске: 2 т.15, 2025 года.
Бесплатный доступ
Актуальность. Ежегодно выявляется почти 450 новых случаев почечно-клеточного рака и почти 160 случаев летальных исходов от онкологических заболеваний. Особый интерес для пациентов с метастатическим почечно-клеточным раком (ПКР), которые часто переносят радикальную нефрэктомию до назначения комбинированной иммунотерапии, вызывает оценка дальнейшего почечного повреждения, возникающего на фоне приёма ингибиторов тирозинкиназ и блокаторов контрольных точек иммунитета. Тем не менее, исследований, посвящённых данному вопросу, на сегодняшний день нет. Цель: сравнение почечного повреждения у пациентов с метастатическим ПКР с единственной почкой, принимающих два режима лекарственной терапии: ипилимумаб + ниволумаб и пембролизумаб + акситиниб. Объект и методы. В ретроспективное исследование было включено 100 пациентов (мужчин – 73, женщин – 27) с метастатическим почечно-клеточным раком группы неблагоприятного прогноза, которым ранее была выполнена односторонняя радикальная нефрэктомия по поводу основного заболевания. 50 пациентов получали комбинированную иммунотерапию по схеме ипилимумаб + ниволубаб, в то время как другие 50 пациентов – по схеме пембролизумаб + акситиниб. В данных группах хроническая болезнь почек отмечалась у 83,0% и 77,3% пациентов соответственно (80,2% общей выборки). Пациенты, получающие пембролизумаб + акситиниб, были несколько старше (медиана 63,0 года и 57,0 года, р = 0,019). Повреждение единственной почки оценивалось на протяжении 28–36 недель комбинированной терапии, что соответствовало 12-ти введениям препаратов в каждой группе. Результаты. Острое почечное повреждение (ОПП) после 1-го введения ипилимумаба + ниволумаба отмечалось в 10% случаев, в то время как после 1-го введения пембролизумаба + акситиниба – в 11% случаев (р = 1,000). Максимальная разница ОПП между изучаемыми группами отмечалась после 10-го введения: ОПП встречалось в 25% и 6% случаев в группах пациентов, получающих ипилимумаб + ниволумаб и пембролизумаб + акситиниб соответственно, однако различия также были статистически незначимыми (р = 0,513). Несмотря на более старший возраст пациентов, получающих пембролизумаб + акситиниб, в среднем за всё время терапии креатинин в группе ипилимумаб + ниволумаб был на 23,4 мкмоль/л выше, чем в группе пембролизумабом + акситиниб (р = 0,006) при исходно сопоставимых показателях. Максимальная разница креатинина между группами отмечалась после 3-го введения препаратов: креатинин в группе ипилимумаб + ниволумаб был на 43,0 мкмоль/л выше, чем у пациентов в группе пембролизумаб + акситиниб (р < 0,001). Мочевина за всё время терапии в группе ипилимумаб + ниволумаб была на 1,7 ммоль/л выше (р = 0,010), чем в группе пембролизумабом + акситиниб при исходно сопоставимых показателях. Максимальная разница мочевины между группами отмечалась после 5-го и 12-го введения препаратов, составляя 2,6 ммоль/л и 2,7 ммоль/л соответственно (р = 0,009 и р = 0,032 соответственно). Выводы. На фоне комбинированной иммунотерапии ипилимумабом + ниволумабом при метастатическом ПКР у пациентов с единственной почкой отмечается более выраженное ухудшение показателей почечной функции по сравнению с комбинированной иммунотаргетной терапией пембролизумабом + акситинибом.
Метастатический рак почки, Комбинированная лекарственная терапия, Нефротоксичность, Односторонняя нефрэктомия, Почечное повреждение, Сравнительное исследование
Короткий адрес: https://sciup.org/143184252
IDR: 143184252 | УДК: 616.61-006.6-033.2-085-06:616.61-008.64]-089.87 | DOI: 10.20340/vmi-rvz.2025.2.CLIN.2
Comparison of two combined drug therapy regimens for renal damage in patients with metastatic kidney cancer after previously performed unilateral nephrectomy
Relevance. Almost 450 new cases of renal cell carcinoma and almost 160 deaths from cancer are detected annually. Of particular interest to patients with metastatic renal cell carcinoma who often undergo radical nephrectomy prior to the appointment of combined immunotherapy is the assessment of further renal damage that occurs while taking tyrosine kinase inhibitors and immune checkpoint blockers. Objective: to compare renal damage in patients with metastatic RCC with a single kidney taking two drug therapy regimens: ipilimumab + nivolumab and pembrolizumab + axitinib. Object and methods. A retrospective study included 100 patients (73% men and 27% women) with metastatic renal cell carcinoma of the unfavorable prognosis group who had previously undergone unilateral radical nephrectomy for the underlying disease. 50 patients received ipilimumab + nivolubab combined immunotherapy, while 50 patients received pembrolizumab + axitinib. In these groups, CKD was observed in 83.0% and 77.3% of patients, respectively (80.2% of the total sample). Patients receiving pembrolizumab + axitinib were slightly older (median 63.0 years and 57.0 years, p = 0.019).Damage to a single kidney was assessed during 28-36 weeks of combination therapy, which corresponded to 12 drug injections in each group. Results. Acute renal injury (AKI) after the 1st administration of ipilimumab + nivolumab was observed in 10%, while after the 1st administration of pembrolizumao + axitinib - in 11% (p = 1,000). The maximum difference in AKI between the studied groups was noted after the 10th administration: AKI occurred in 25% and 6% of cases in the groups of patients receiving ipilimumab + nivolumab and pembrolizumab + axitinib, respectively, but the differences were also statistically insignificant (p = 0.513). Despite the older age of patients receiving pembrolizumab + axitinib, the average creatinine in the ipilimumab + nivolumab group was 43.0 mmol/L higher than in patients in the pembrolizumab + axitinib group (p < 0.001). Over the entire duration of therapy, urea in the ipilimumab + nivolumab group was 1.7 mmol/L higher (p = 0.010) than in the pembrolizumab + axitinib group with initially comparable parameters. The maximum difference in urea between the groups was observed after the 5th and 12th administration of the drugs, amounting to 2.6 mmol/l and 2.7 mmol/l, respectively (p = 0.009 and p = 0.032, respectively). Conclusion. Combined immunotherapy with ipilimumab + nivolumab in patients with metastatic RCC in patients with a single kidney has a more pronounced deterioration in renal function compared with combined immunotherapy with pembrolizumab + axitinib.
Текст научной статьи Сравнение двух комбинированных режимов лекарственной терапии по почечному повреждению у пациентов с метастатическим раком почки, ранее перенёсших одностороннюю нефрэктомию
Competing interests. The authors declare no competing interests.
Funding. This research received no external funding.
Compliance with ethical principles. The authors confirm that they respect the rights of the people participated in the study, including obtaining informed consent when it is necessary.
Cite as: Titov K.S., Epifanova M.V., Alimov A.A., Nesterova O.Yu., Shutov E.V., Lebedev S.S., Zapirov G.M. Comparison of two combined drug therapy regimens for renal damage in patients with metastatic kidney cancer after previously performed unilateral nephrectomy. Bulletin of the Medical Institute "REAVIZ": Rehabilitation, Doctor and Health. 2025;15(2):68-77. 0.20340/
Актуальность
Почечно-клеточный рак (ПКР) занимает 16-е место в структуре распространённости онкологических заболеваний и 17-е место в структуре смертности во всем мире. В РФ он входит в десятку самых распространённых онкологических заболеваний, занимая 8-е место в структуре распространённости и 12-е место в структуре смертности, превышая тем самым общемировые показатели [1]. Отмечается, что около трети пациентов с ПКР на момент постановки диагноза имеют метастазы [2, 3]. По данным Каприна А.Д. и др. (2023) в нашей стране в 2023 году ПКР III-IV стадии выявлялся в 32,2% случаев, что также подтверждало мировые тенденции [4]. При этом следует отметить, что даже в случае выявления локализованных форм ПКР, после выполнения первичного радикального оперативного лечения примерно в 40% случаев в последующем выявляются метастазы [5, 6]. Внедрение в клиническую практику ингибиторов тирозинкиназ и контрольных точек иммунитета (ИКТИ) изменило парадигму лечения метастатического рака почки. При этом проведённые за последние два десятилетия исследования показали, что комбинированная терапия обладает большей эффективностью по сравнению с монотерапией [7]. Так, комбинированная терапия ипили-мумаб + ниволумаб была впервые одобрена FDA как первая линия терапии метастатического ПКР промежуточного/неблагоприятного риска в 2018 г. на основании результатов исследования CheckMate 214. Было показано, что комбинированная иммунотерапия ипилимумабом + ниволумабом по сравнению с сутинибом была ассоциирована с более высокой общей выживаемостью пациентов, выживаемостью без прогрессирования и более частым объективным ответом на терапию [8]. Позднее, в апреле 2019 года, по данным исследования KEYNOTE-426 была одобрена ещё одна схема - пембролизумаб + акситиниб, включающая, помимо ингибитора PD-1, новый препарат - мощный и селективный ингибитор тирозинкиназы рецепторов фактора роста эндотелия сосудов (VEGF). По данным KEYNOTE-426 комбинированная иммунотаргетная терапия пемброли-зумабом + акситинибом по сравнению с ингибитором VEGF сутинибом у пациентов с метастатическим ПКР ассоциирована с повышением общей выживаемости и выживаемости без прогрессирования, а также с более высоким количеством пациентов с полным и частичным ответом на лечение. Такая закономерность отмечалась для пациентов всех групп прогноза по IMDC [9]. Комбинированная иммунотерапия ипилимумабом + ниволумабом рекомендована в качестве первой линии терапии для пациентов с метастатическим ПКР промежуточного и неблагоприятного прогноза по IMDC, в то время как комбинированная иммунотаргетная терапия, к которой относится пембролизумаб + акситиниб, для всех прогностических групп [10]. Тем не менее, данные варианты комбинированной терапии сопряжены с рядом осложнений. При этом исследователи описывают, что в некоторых случаях отмечается почечное повреждение, характеризующееся повышением креатинина, появлением протеинурии, развитием острого почечного повреждения (ОПП) или нефритов [8, 9]. С одной стороны, такие осложнения могут быть следствием ранее перенесённой нефрэктомии, которая выполнялась большинству пациентов, по поводу метастатического ПКР. С другой стороны, почечные осложнения могут быть связаны с непосредственным приёмом комбинированных схем препаратов, прямое сравнение которых в данном аспекте для однородной выборки пациентов с единственной почкой ранее не выполнялось.
Таким образом, особый интерес для пациентов с метастатическим ПКР, которые часто переносят радикальную нефрэктомию до назначения комбинированной иммунотерапии, вызывает оценка дальнейшего почечного повреждения, возникающего на фоне приёма ингибиторов тирозинкиназ и блокаторов контрольных точек иммунитета. Тем не менее, исследований, посвящённых данному вопросу, на сегодняшний день нет. В связи с этим, целью настоящей работы стало сравнение почечного повреждения у пациентов метастатическим ПКР с единственной почкой, принимающих два режима лекарственной терапии: ипилимумаб + ниволумаб и пембролизумаб + акситиниб.
Объект и методы
В ретроспективное исследование было включено 100 пациентов (73 мужчины и 27 женщин) с метастатическим почечно-клеточным раком группы неблагоприятного прогноза, которым ранее была выполнена односторонняя радикальная нефрэктомия по поводу основного заболевания.
50 пациентов получали комбинированную иммунотерапию по схеме ипилимумаб + ниволубаб, в то время как другие 50 пациентов - по схеме пембро-лизумаб + акситиниб. Средний возраст пациентов общей выборки составил 59,7 года (по медиане 60,5 года). Сравнительная характеристика параметров пациентов в зависимости от группы лечения до начала иммунотерапии представлена в таблице 1.
Как видно из представленной таблицы 1, единственным параметром, статистически значимо отличающимся у пациентов в группах ипилимумаб + ни-волумаб и пембролизумаб + акситиниб был возраст. Пациенты, получающие пембролизумаб + аксити-ниб, были несколько старше. Состояние почечной функции до начала иммунотерапии было известно у 73 пациентов: 39 пациентов из группы ипилимумаб + ниволумаб и 34 пациента из группы пембролизумаб + акситиниб. В данных группах хроническая болезнь почек (ХБП) отмечалась у 83,0% и 77,3% пациентов соответственно (80,2% общей выборки).
Ипилимумаб вводился 1 раз в 3 недели исходя из расчета 1 мг на кг совместно с ниволумабом исходя из расчета 3 мг на кг - 4 раза. Время внутривенной капельной инфузии составляло 90 минут. Для разведения рекомендуется использовать физиологический раствор 0,9% хлорида натрия или 5% раствор глюкозы (декстрозы) до концентрации от 1 до 4 мг/дл. После 4-х совместных введений ниволумаб вводился в режиме 1 раз в 2 недели в той же дозе. Для инфузии использовали систему со стерильным, апирогенным фильтром с диаметром пор от 0,2 до 1,2 мкм и низким коэффициентом связывания белка. Акситиниб принимался перорально 2 раза в день по 5 мг. Пембролизумаб вводился в/в капельно 1 раз в 3 недели исходя из расчета 2 мг на кг или 200 мг единоразово. Время внутривенной капельной инфузии составляло 30 минут.
Для оценки почечного повреждения в процессе комбинированной иммунотерапии у пациентов с единственной почкой нами были выбраны следующие критерии:
-
• Развитие ОПП в ходе лечения. ОПП определяется как повышение уровня креатинина сыворотки в ≥ 1,5 раза от исходного уровня, которое известно или предположительно произошло в течение предыдущих 7 дней; или повышение уровня креатинина сыворотки на ≥ 26,5 мкмоль/л в течение 48 часов; или олигурия (объём мочи < 0,5 мл/кг в час в течение 6 часов [11].
-
• Снижение скорости клубочковой фильтрации (СКФ) ниже 60 у пациентов с исходным уровнем СКФ более 60 мл/мин/1,73 м2: СКФ определяли по формуле CKD-EPI [12].
-
• Ухудшение степени ранее присутствовавшей ХБП в соответствии с классификацией стадий ХБП по уровню СКФ.
-
• Повреждение единственной почки оценивалось на протяжении 28-36 недель комбинированной терапии после каждого курса введения препаратов и также дополнительно оценивался уровень креати-
- нина, мочевины, СКФ, гемоглобина. Данный временной интервал соответствовал 12-ти введениям препаратов в каждой группе.
Таблица 1. Сравнительная характеристика параметров пациентов в зависимости от группы лечения до начала иммунотерапии Table 1. Comparative characteristics of patient parameters depending on the treatment group before the start of immunotherapy
|
Параметр |
Ипилимумаб + ниволубаб |
Пембролизумаб + акситиниб |
р* |
|
Возраст, медиана, (Q1–Q3) |
57,0 (52,0-64,5) |
63,0 (57,5-67,0) |
0,019 |
|
Пол |
0,499 |
||
|
Мужчины, % (n) |
76,0% (38) |
70,0% (35) |
|
|
Женщины, % (n) |
24,0% (12) |
30,0% (15) |
|
|
рТ |
0,846 |
||
|
рТ1, % (n) |
2,1% (1) |
2,3% (1) |
|
|
рТ2, % (n) |
8,3% (4) |
11,4% (5) |
|
|
рТ3, % (n) |
75,0% (36) |
77,3% (34) |
|
|
рТ4, % (n) |
14,6% (7) |
9,1% (4) |
|
|
рN |
0,575 |
||
|
рN0, % (n) |
76,6% (36) |
74,4% (32) |
|
|
pN1, % (n) |
23,4% (11) |
23,3% (10) |
|
|
pN2, % (n) |
0% |
2,3% (1) |
|
|
pM |
0,398 |
||
|
рМ0, % (n) |
38,0% (19) |
30,0% (15) |
|
|
рМ1, % (n) |
62,0% (31) |
70,0% (35) |
|
|
Стадия |
0,509 |
||
|
III, % (n) |
32,0% (16) |
26,0% (13) |
|
|
IV, % (n) |
68,0% (34) |
74,0% (37) |
|
|
Гистологический тип |
0,261 |
||
|
светлоклеточный |
98,0% (49) |
88,0% (44) |
|
|
саркоматоидный |
2,0% (1) |
2,0% (1) |
|
|
папиллярный |
0% |
6,0% (3) |
|
|
транслокационный |
0% |
2,0% (1) |
|
|
хромофобный |
0% |
2,0% (1) |
|
|
Хронические заболевания, % (n) |
0,157 |
||
|
Нет заболеваний |
36,0% (18) |
50,0% (25) |
|
|
АГ или СД или АГ и СД |
64,0% (32) |
50,0% (25) |
|
|
Наличие ХБП |
83,0% (39) |
77,3% (34) |
0,495 |
|
Стадия ХБП |
0,976 |
||
|
ХБП 3а, % (n) |
64,1% (25) |
61,8% (21) |
|
|
ХБП 3б, % (n) |
30,8% (12) |
32,4% (11) |
|
|
ХБП 4, % (n) |
5,1% (2) |
5,9% (2) |
Примечание: АГ - артериальная гипертензия; СД - сахарный диабет; ХБП - хроническая болезнь почек; *критерий Манна - Уитни для количественных переменных; Хи-квадрат для номинальных переменных; Q1-Q3 - межквартильный интервал.
Статистическая обработка данных проводилась с использованием программного обеспечения RStudio на языке программирования R. Номинальные переменные были представлены в виде абсолютных значений (n) и частотных характеристик (%). Сравнение номинальных переменных проводилось с использованием критериев Хи-квадрат или Хи-квадрат с поправкой Йейтса. Изменяющиеся в динамике показатели почечной функции (креатинин, мочевина, СКФ), а также гемоглобин и гематокрит были представлены в виде совокупных средних (LS-means, LS-средние) и 95% доверительных интервалов (ДИ) на графиках. В таблицах представлены разницы данных показателей между сравниваемыми группами (Δ) и стандартные ошибки для △ (SE). При сравнении динамики показателей между группами использовались обобщённые линейные смешанные модели (Generalized linear mixed model) с дальнейшим дисперсионным анализом моделей (anova). Различия считались статистически значимыми при p < 0,05.
Результаты
В соответствие с выбранными критериями, повреждение единственной почки после начала комбинированной иммунотерапии ипилимумаб + ниво-лумаб и пембролизумаб + акситиниб (1-е введение) отмечалось у 23% и 19% пациентов с метастатическим ПКР, ранее перенёсших нефрэктомию, соответственно (р = 0,944). Максимальная разница почечного повреждения между изучаемыми группами отмечалась после 11-го введения: почечное повреждение в группах пациентов, получающих ипилиму-маб + ниволумаб и пембролизумаб + акситиниб, встречалось в 36% и 21% случаев соответственно, однако различия также были статистически незначимыми (р = 0,706).
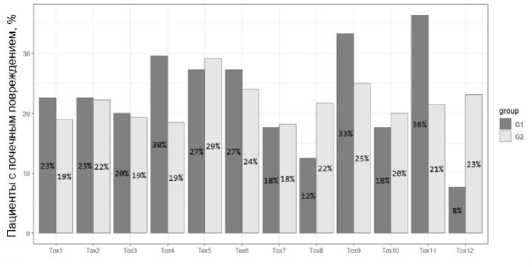
Рисунок 1. Сравнительная частота развития повреждения единственной почки на фоне 12 введений комбинированной иммунотерапии (ипилимумаб + ниволумаб (G1) и пембролизумаб + акситиниб (G2)) у пациентов с метастатическим почечноклеточным раком, ранее перенёсших нефрэктомию
Figure 1. Comparative incidence of solitary kidney injury during 12 administrations of combination immunotherapy (ipilimumab + nivolumab (G1) and pembrolizumab + axitinib (G2)) in patients with metastatic renal cell carcinoma who previously underwent nephrectomy
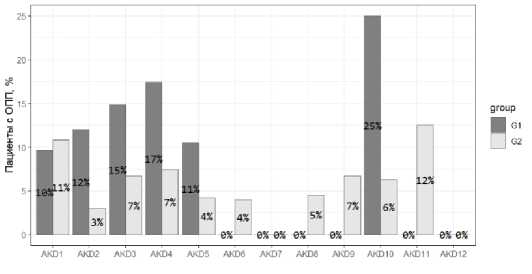
Рисунок 2. Сравнительная частота развития острого почечного повреждения на фоне 12-ти введений комбинированной иммунотерапии (ипилимумаб + ниволумаб (G1) и пембролизумаб + акситиниб (G2)) у пациентов с метастатическим почечноклеточным раком, ранее перенёсших нефрэктомию
Figure 2. Comparative incidence of acute kidney injury during 12 administrations of combination immunotherapy (ipilimumab + nivolumab (G1) and pembrolizumab + axitinib (G2)) in patients with metastatic renal cell carcinoma who previously underwent nephrectomy
При сравнении почечного повреждения между группами после каждого введения статистически значимых различий не отмечалось. Визуальное представление развития почечного повреждения представлено на рисунке 1.
ОПП отмечалось после 1-го введения комбинированной иммунотерапии ипилимумаб + ниволумаб у 10% при метастатическом ПКР у пациентов с единственной почкой, в то время как после 1-го введения комбинированной иммунотаргетной терапии пембролизумаб + акситиниб - у 11% (р = 1,000). Максимальная разница ОПП между изучаемыми группами отмечалась после 10-го введения: ОПП в группах пациентов, получающих ипилимумаб + ни-волумаб и пембролизумаб + акситиниб, встречалось в 25% и 6% случаев, однако различия также были статистически незначимыми (р = 0,513). При сравнении ОПП между группами после каждого введения статистически значимых различий не от- мечалось. Визуальное представление развития почечного повреждения представлено на рисунке 2.
На следующем этапе исследования мы сравнили динамику изменения показателей почечной функции (креатинина, мочевины и СКФ) на фоне иммунотерапии ипилимумаб + ниволумаб и пембролизу-маб + акситиниб в общей выборке пациентов с метастатическим ПКР с единственной почкой. Показатели были представлены в виде разницы LS-средних значений и стандартных ошибок между пациентами, пролеченными по схеме ипилимумаб + ниволумаб и пембролизумаб + акситиниб (Δ) (табл. 2). Положительное значение Δ указывает на то, что у пациентов из группы ипилимумаб + ниволумаб данный показатель (в среднем по группе) был выше, чем у пациентов из группы пембролизумаб + акситиниб. Отрицательное значение, наоборот, показывает, что данный показатель у пациентов из группы ипилимумаб + ниволумаб (в среднем по группе) был ниже, чем у пациентов из группы пембролизумаб + акситиниб.
Таблица 2. Сравнительная динамика различий в изменении показателей почечной функции и гемоглобина на фоне комбинированной иммунотерапии после каждого введения ипилимумаба + ниволумаба и пембролизумаба + акситиниба
Table 2. Comparative dynamics of differences in changes in renal function parameters and hemoglobin during combination immunotherapy after each administration of ipilimumab + nivolumab and pembrolizumab + axitinib
|
№ введения препарата |
Креатинин мкмоль/л |
р |
Мочевина ммоль/л |
р |
СКФ мл/мин/1,73м2 |
р |
Гемоглобин г/л |
р |
|
(Ипи+Ниво) – (Пембро+Акси), ΔLS–средние ± SE |
||||||||
|
До введения |
3,6 ± 10,7 |
0,740 |
0,3 ± 0,8 |
0,732 |
1,2 ± 3,5 |
0,736 |
-1,6 ± 4,1 |
0,704 |
|
1 |
13,0 ± 11,3 |
0,253 |
1,6 ± 0,9 |
0,068 |
0,2 ± 3,6 |
0,951 |
-11,9 ± 4,2 |
0,005 |
|
2 |
39,8 ± 11,4 |
< 0,001 |
2,1 ± 0,9 |
0,019 |
-3,7 ± 3,6 |
0,306 |
-13,7 ± 4,2 |
0,001 |
|
3 |
43,0 ± 11,7 |
< 0,001 |
1,7 ± 0,9 |
0,069 |
-6,1 ± 3,7 |
0,099 |
-15,1 ± 4,3 |
< 0,001 |
|
4 |
31,1 ± 12,1 |
0,011 |
1,8 ± 0,9 |
0,054 |
-5,1 ± 3,7 |
0,177 |
-10,8 ± 4,4 |
0,014 |
|
5 |
25,6 ± 12,6 |
0,043 |
2,6 ± 1,0 |
0,009 |
-6,4 ± 3,9 |
0,097 |
-10,1 ± 4,5 |
0,026 |
|
6 |
20,4 ± 12,7 |
0,108 |
2,0 ± 1,0 |
0,041 |
-4,3 ± 3,9 |
0,271 |
-9,1 ± 4,5 |
0,046 |
|
7 |
24,8 ± 13,4 |
0,065 |
2,5 ± 1,1 |
0,021 |
-5,0 ± 4,0 |
0,218 |
-10,0 ± 4,7 |
0,034 |
|
8 |
23,1 ± 13,7 |
0,092 |
1,9 ± 1,1 |
0,092 |
-4,8 ± 4,1 |
0,238 |
-8,6 ± 4,7 |
0,072 |
|
9 |
28,6 ± 15,3 |
0,062 |
1,4 ± 1,2 |
0,277 |
-6,3 ± 4,4 |
0,158 |
-6,6 ± 5,1 |
0,193 |
|
10 |
33,2 ± 14,1 |
0,019 |
1,9 ± 1,1 |
0,095 |
-7,8 ± 4,2 |
0,061 |
-6,5 ± 4,8 |
0,176 |
|
11 |
29,4 ± 15,0 |
0,051 |
1,6 ± 1,2 |
0,198 |
-6,2 ± 4,4 |
0,159 |
-8,5 ± 5,1 |
0,092 |
|
12 |
22,7 ± 15,2 |
0,135 |
2,7 ± 1,2 |
0,032 |
-3,6 ± 4,4 |
0,414 |
-9,3 ± 5,1 |
0,072 |
Визуальное представление динамики изменения показателей почечной функции и гемоглобина показано на рисунке 3. Как видно из представленной таблицы 2 и рисунка 3, креатинин в среднем по выборке на протяжении иммунотерапии ипилимума-бом + ниволумабом был статистически значимо выше, чем у пациентов из группы пембролизум + акситиниб (р = 0,006), что проявлялось более высоким подъёмом данного показателя после каждого введения. В среднем за всё время терапии креатинин в группе ипилимумаб + ниволумаб был на 23,4 мкмоль/л выше, чем в группе пембролизу-мабом + акситиниб. Самому высокому значению разницы креатинина между группами соответствовали показатели после 3-го введения препаратов: креатинин в группе ипилимумаб + ниволумаб был на 43,0 мкмоль/л выше, чем у пациентов в группе пембролизумаб + акситиниб (р < 0,001).
Аналогичная динамика была характерна и для мочевины, которая на протяжении всей иммунотерапии ипилимумабом + ниволумабом была статистически значимо выше, чем у пациентов из группы пембролизум + акситиниб (р = 0,010). В среднем в указанный промежуток мочевина в группе ипили-мумаб + ниволумаб была на 1,7 ммоль/л выше, чем в группе пембролизумабом + акситиниб. Максимальная разница мочевины между группами отмечалась после 5-го и 12-го введения препаратов, составляя 2,6 ммоль/л и 2,7 ммоль/л соответственно (р = 0,009 и р = 0,032 соответственно).
Для СКФ, несмотря на явную тенденцию более высоких значений у пациентов из группы пемброли-зум + акситиниб, статистически значимых различий не отмечалось. Дополнительно была оценена сравнительная динамика гемоглобина, так как почка также играет важную роль в регуляции эритропоэза. Было установлено, что у пациентов, получающих пембролизум + акситиниб, средние значения гемоглобина на протяжении всей иммунотерапии статистически значимо выше, чем у пациентов, получающих ипилимумаб + акситиниб (р = 0,010). В среднем в указанный промежуток гемоглобин в группе пембролизумаб + акситиниб был на 10,0 г/л выше, чем в группе ипилимумаб + ниволумаб. Максимальная разница гемоглобина между группами отмечалась после 3-го введения препаратов, составляя 15,2 г/л (р < 0,001).
Обсуждение
Побочные эффекты терапии ипилимумаб + ниво-лумаб чаще всего связаны с иммуноопосредован-ным повышением активности иммунной системы организма. Среди почечных иммуноопосредован-ных побочных эффектов, помимо ОПП, в литературе описаны случаи острого интерстициального нефрита, острого тубулярного некроза и гломерулярных нарушений [13]. Сообщалось, что распространённость ОПП на фоне применения ниволумаба у пациентов с другими онкологическими заболеваниями (не ПКР) составляет 2%, в то время как при комбинации с ипилимумабом повышается до 4,5% [14-16]. Тем не менее, как показали результаты работы Alejandro Meraz-Munoz и соавт. (2020), ОПП на фоне ИКТИ может возникать гораздо чаще, достигая 16,5% случаев, в то время как у 3,9% пациентов возникала нефротоксичность, подтверждённая результатами биопсии, показавшей возникновение интерстициального нефрита (1,9%), мембранозной нефропатии (0,6%), болезнь минимальных изменений (0,6%) и тромботическую микроангиопатию (0,6%) [13].
Двойная иммунотерапия ИКТИ (ипилимумаб + ниволумаб) была одобрена в качестве первой линии терапии у пациентов с метастатическим ПКР промежуточного и неблагоприятного прогноза, которые часто переносят радикальную нефрэктомию до начала иммунотерапии. Так, по данным исследования CheckMate-214, 82% пациентов, получающих ипилимумаб + ниволумаб имели единственную почку. При этом связанные с терапией почечные побочные эффекты отмечались у 10,1% пациентов (55 из 547 пациентов), 1,3% почечных осложнений были классифицированы как осложнения 3-4 степени. Повышение уровня креатинина (любой степени по CTCAE) отмечалось у 7,3% пациентов (из них у 2,5% - 3-4 степени), в то время как ОПП - у 2,2% (из них у 33,3% - 3-4 степени). В пересчёте на общую выборку пациентов повышение креатинина 3-4 степени и ОПП 3-4 степени отмечалось в 0,2% и 0,7% случаев [8]. Из 436 пациентов с иммуноопосредованными побочными эффектами терапии ипилимумаб + ниволумаб (включая кожные, гастроинтестинальные, лёгочные и почечные) 35% требовали назначения высоких доз глюкокортикостероидов (40 мг и выше преднизолона в сутки) [17]. В рамках настоящей работы на фоне комбинированной иммунотерапии ОПП развивалась максимально у 25% пациентов после 10-го введения препаратов. Дополнительно нами было показано, что на фоне введения ипилимумаба + ниволумаба у пациентов в среднем по выборке отмечается повышение уровня креатинина и мочевины, что указывает на усиление повреждения единственной почки.
Побочные эффекты комбинированной иммуно-таргетной терапии, включающей ингибитор PD-1 пембролизумаб и ингибитор тирозинкиназы VEGF акситиниб, связаны как с активацией собственной иммунной системы, так и с опосредованными эффектами блокады VEGF. Так, в физиологических условиях VEGF-сигналлинг ингибирует продукцию мощного эндогенного вазоконстриктора, эндотелина-1 (ET-1), стимулирует выработку вазодилататора NO и про- стациклина [18, 19]. В результате, на фоне назначения акситиниба, повышается системная вазоконстрикция, что приводит к развитию артериальной гипертензии, которая, как наиболее частый побочный эффект анти-VEGF терапии, сама по себе, может ухудшать состояние почечной функции. Помимо этого, ингибирование сигналлинга VEGF в эндотелиальных клетках клубочка предотвращает их пролиферацию, приводя к истончению гломерулярных капилляров, что ещё более способствует вазоконстрикции в ответ на снижение концентрации натрия с последующим выбросом ангиотензина II [19].
Учитывая такое влияние ИКТИ и анти-VEGF-терапии, почечные осложнения выявлялись также и в исследовании KEYNOTE-426, доказавшем возможность успешного использования комбинированной иммунотаргетной терапии (пембролизумаб + акси-тиниб) у пациентов с метастатическим ПКР [9]. Было показано, что на фоне лечения пембролизумабом + акситинибом в 17,5% случаев (75 из 429 пациентов) отмечалась протеинурия любой степени тяжести по CTCAE, из них у 16% - 3 степени тяжести и выше (или 2,8% от общей выборки пациентов - 12 из 429). У 11,2% пациентов (48 из 429) отмечалось повышение креатинина любой степени тяжести по CTCAE, из них у 4,2% - 3 степени тяжести и выше (или 0,5% от общей выборки пациентов - 2 из 429). У 1,4% общей выборки (6 из 429 пациентов) описано развитие нефрита любой степени тяжести по CTCAE, из них в 16,7% случаев - 3 степени тяжести и выше (или 0,2% от общей выборки пациентов - 1 из 429). При этом ни в одном случае не было описано развития ОПП. Следует отметить, что в 82,6% случаев пациентам, получающим пембролизумаб + акситиниб, до начала иммунотаргетной терапии выполнялась радикальная нефрэктомия [9]. В рамках настоящего исследования радикальная нефрэктомия до назначения пембролизумаба + акситиниба выполнялась всем пациентам, что, тем самым, заранее компрометировало почечную функцию. Нами было показано, что ОПП после 1-го введения препаратов отмечалась у 11% пациентов, достигая максимальных значений после 11-го введения (12%). Однако при этом, в среднем по выборке, повышения креатинина и мочевины, как основных показателей почечной функции, не возникало, что, тем самым, позволило сделать вывод о безопасности комбинированной иммунотаргетной терапии пембролизумабом + ак-ситинибом в отношении дальнейшего ухудшения функции единственной почки.
Согласно данным нескольких систематических обзоров и мета-анализов, в которых проводится оценка отдельных клинических исследований, посвящённых эффективности и безопасности различных вариантов иммунотерапии и иммунотаргетной терапии, отмечается, что схема ипилимумаб + ниво- лумаб характеризуется меньшей частотой побочных эффектов 3 степени и выше по сравнению с терапией пембролизумаб + акситиниб [20-23]. Тем не менее, как отмечалось в систематическом обзоре и мета-анализе Fahad Quhal и соавт. (2021), ипилиму-маб + ниволумаб обладают наибольшей частотой иммуноопосредованных побочных эффектов [23]. В последнем мета-анализе Xiangyu Chen и соавт., опубликованном в феврале 2024 года, было показано, что суммарные побочные эффекты у пациентов, получающих ипилимумаб + ниволумаб и пемброли-зумаб + акситиниб, сопоставимы при более высокой эффективности последней схемы [6]. Однако следует отметить, что все проводимые в систематических обзорах и мета-анализах сравнения являются непрямыми и основаны на данных, полученных в различных исследованиях, в то время как прямое сравнение двух вариантов терапии (ипилимумаб + ниво-лумаб и пембролизумаб + акситиниб) в одной работе отсутствует.
Крупнейшее исследование, посвящённое прямому сравнению двух режимов комбинированной иммунотерапии и иммунотаргетной терапии, носило ретроспективный характер и было выполнено Neil J. Shah и соавт. (2023). Исследование включало более 1,5 тысяч человек с метастатическим ПКР. Отмечалось, что при исходно сопоставимых клинических показателях пациенты дольше находились на терапии пембролизумабом + акситинибом по сравнению с пациентами, получающими лечение по схеме ипилимумаб + ниволумаб (16,4 месяца и 8,3 месяца соответственно). Это могло указывать, с одной стороны, на большую эффективность терапии пембролизумабом + акситинибом, а с другой стороны, на лучшую переносимость данной схемы пациентами, однако сравнительной оценки безопасности в исследовании не проводилось [24].
Единственным исследованием, в котором выполнялось прямое сравнение профиля эффективности и безопасности между комбинированной иммунотерапией (ипилимумаб + ниволумаб) и иммуно-таргетной терапией, является работа Hiroki Ishihara с соавт. (2024), включающая 175 пациентов с метастатическим ПКР, ранее не переносившими радикальную нефрэктомию (критерий исключения). При этом только 25% из группы иммунотаргетной терапии получали пембролизумаб + акситиниб, в то время как у остальных пациентов использовались другие комбинации ИКТИ и ингибиторов тирозин-киназ. Исследователи показали, что суммарно побочные эффекты любой степени тяжести развиваются у 100% и 80,5% пациентов в группах комбинированной иммунотаргетной терапии и иммунотерапии соответственно (р = 0,0001). При этом отмечалось, что осложнения 3 степени и выше в изучаемых группах статистически значимо не отличались
(46,2% и 53,9% соответственно, р = 0,336). Одновременно, пациенты из группы ипилимумаб + ниво-лумаб более чем в 2 раза чаще требовали назначения глюкокортикостероидов по сравнению с пациентами на иммунотаргетной терапии (43,3% и 20,3% соответственно, р = 0,001) [25]. Сравнительного анализа почечного повреждения на фоне терапии исследователями не проводилось. Такой анализ был сделан в рамках настоящего исследования. Нами было показано, что, несмотря на отсутствие статистически значимых различий в развитии почечного повреждения и ОПП между пациентами, получающими ипилимумаб + ниволумаб и пембро-лизумаб + акситиниб, в первой группе отмечалась отчётливая тенденция более частого возникновения данных осложнений, которые достигали максимальных значений после 11-го и 10-го введения препаратов (36% и 25% соответственно). В группе пембролизумаб + акситиниб почечное повреждение и ОПП имели максимальную распространённость после 5-го и 11-го введения препаратов (29% и 12% соответственно). Тем не менее, нами было показано, что на фоне терапии ипилимумабом + ниволумабом отмечается более выраженное ухудшение показателей почечной функции по сравнению с терапией пембролизумабом + акситинибом при исходно сопоставимых показателях. Так, за время терапии средние значения креатинина в группе ипилимумаб + ниволумаб были на 23,4 мкмоль/л выше, чем в группе пембролизу-мабом + акситиниб (р = 0,006). Показатели мочевины за всё время терапии в группе ипилимумаб + ниволумаб были также на 1,7 ммоль/л выше (р = 0,010), чем в группе пембролизумабом + акси-тиниб, что указывало на более выраженное повреждение почечной паренхимы на фоне комбинированной иммунотерапии ипилимумаб + ниволумаб, которая, на основании полученных нами данных, является менее безопасной для пациентов с метастатическим ПКР и единственной почкой.
Заключение
На фоне комбинированной иммунотерапии ипи-лимумабом + ниволумабом при метастатическом ПКР у пациентов с единственной почкой отмечается более выраженное ухудшение показателей почечной функции (креатинина и мочевины) по сравнению с комбинированной иммунотаргетной терапией пембролизумабом + акситинибом. Тем самым, полученные нами данные показывают, что схема пембролизумаб + акситиниб для данной категории пациентов является наиболее безопасной с точки зрения дальнейшего повреждения единственной почки и может быть рекомендована в качестве первой линии терапии.


