Сравнение кинетических свойств различных циклодекстринглюканотрансфераз
Автор: Федорова Полина Юрьевна, Гильванова Елена Альбертовна, Усанов Николай Глебович
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Биотехнология
Статья в выпуске: 5-3 т.13, 2011 года.
Бесплатный доступ
Приводятся данные, указывающие на факт высокой частоты встречаемости способности к образованию циклодекстринов среди бактерий рода Paenibacillus (Ash et al. 1994 emend. Behrendt et al. 2010). Проведено сравнение физико-химических и каталитических свойств циклодекстринглюканотрансфераз четырех штаммов, выделенных из почвы тремя различными методами и охарактеризованных филогенетически в качестве представителей P.macerans, P.ehimensis, P.illinoisensis и P.campinasensis.
Циклодекстрины, цд, циклодекстринглюанотрансфераза, цгтаза
Короткий адрес: https://sciup.org/148205560
IDR: 148205560 | УДК: 577.151.64
Cyclodextrin glycosyltransferases of different paenibacillus species
The data presented point to the fact the high frequency of ability to form cyclodextrins among bacteria of the species Paenibacillus. Made comparison of physico-chemical and catalytic properties CGTases four strains isolated from soil by three different methods and characterized as representative of the phylogenetic P.macerans, P.ehimensis, P.illinoisensis and P.campinasensis.
Текст научной статьи Сравнение кинетических свойств различных циклодекстринглюканотрансфераз
Циклодекстринглюканотрансфераза (ЦГТаза, КФ 2.4.1.19) – фермент, катализирующий реакции межмолекулярного трансгликозилирования, в своей сумме приводящие к деполимеризации крахмала и образованию циклодекстринов (ЦД) – нередуцирующих макроциклических олигосахаридов, широко используемых в пищевой промышленности, фармацевтике, косметике, органическом синтезе [1].
Наиболее распространены и известны, альфа-( a ), бета-( β ) и гамма-( γ ) ЦД, молекулы которых состоят из 6, 7 и 8 остатков D-глюкопиранозы, связанных a -1→4-D связями. При действии ЦГТазы на крахмал в реакционной смеси одновременно образуются и накапливаются все три гомолога, ингибирующие действие фермента.
В зависимости от того, какой продукт доминирует в продуктах конверсии, различают ( a )-, ( β )- и ( γ )-ЦГТазы, природа которых в свою очередь зависит от генетическо-видовых особенностей штамма-продуцента.
Не смотря на об илие публикаций о выделении новых бактерий, способных к синтезу ЦГТаз, накопленный материал зачастую оторван от современных таксономических описаний, названия изолятов бактерий не соответствуют действительности, а сами публикации фактически лишены смысла. Филогенетически изучены лишь единичные штаммы аэробных спорообразующих бактерий, таких как Paenibacillus macerans [2], P.illinoisensis [10], P.graminis [19], P.stellifer [17], P. campinasensis [20], Bacillus agaradhaerens [14]. Единичные продуценты позиционированы на физиологобиохимическом уровне на уровне родов Klebsiella [9].
Несмотря на перечисленные факты, даже в последних обзорах [16, 18], посвященных сравнительному описанию продуцентов ЦД, в качестве основной родовой группы продолжает фигурировать род Bacillus, Cohn 1872.
Практически не имеется работ, в которых бы в рамках одной лаборатории проводилось сравнение свойств нескольких ЦГТаз бактерий различных видовых групп, прошедших филогенетическую идентификацию. Целью настоящего исследования является восполнение пробелов в данной тематике.
МАТЕРИАЛ И МЕТОДЫ
В работе использовали лиофильно высушенные препараты циклодекстринглюканотрансфераз продуцентов из коллекции лаборатории прикладной микробиологии Института биологии УНЦ РАН: Paenibacillus ehimensis ВКМB-2680D (IB-739), P.illinoisensis IB-1087, P.campinasensis IB-417, P.macerans IB-14 (IB-1053).
Выращивание бактерий Paenibacillus ehimensis осуществляли в 250 мл качалочных колбах содержащих 50 мл среды, при скорости 180 об/мин при 37÷390С в течение 68÷72 ч, на среде, содержащей (в граммах): крахмал – 10,0; пептон – 4,0; дрожжевой экстракт – 5,0; КH 2 PO 4 – 1,0; СaСО 3 – 1,0; дистиллированную воду до 1000 мл, при стартовых рН 7,0-7,2.
Наработку ЦГТазы P.illinoisensis IB-1087 проводили в вышеописанных условиях на среде K1, содержащей (в граммах): крахмал – 10,0; пептон – 5,0; дрожжевой экстракт – 5,0; КH 2 PO 4 – 2,0; Na 2 HPO 4 – 2,0; дистиллированную воду до 1000 мл, при стартовых рН 7,2^7,4.
Наработку ЦГТазы P.campinasensis IB-417 проводили на среде К1 с добавлением 0,8÷1,0% Na2CO3, при стартовых рН 9,2^9,8.
Наработку препарата ЦГТазы P.macerans IB-I4 проводили на среде, содержащей (в граммах): крахмал – 10,0; пептон – 3,0; дрожжевой экстракт – 3,0; кукурузный экстракт – 3,0; (NH 4 ) 2 SO 4 – 0,2; CaCO 3 – 1,0; дистиллированную воду до 1000 мл, при стартовых рН 7,4^7,8.
ЦГТазную активность растворов и препаратов измеряли фенолфталеиновым методом [3], используя для разбавления фермента 50 мМ ацетатный буфер рН 6,0÷6,1, содержащий 10 мМ CaCl 2 . За 1 единицу активности принимали количество ЦГТазы, катализирующее образование 1 мкМ в -ЦД в течение 1 мин при 40 0 С.
Для выделения ЦГТазы из культуральной жидкости бактериальные клетки отделяли центрифугированием при 6000 мин-1 в течение 30 мин, фильтрат культуральной жидкости концентрировали методом ультрафильтрации на полых волокнах ВПУ-50. Для получения сухого не очищенного препарата концентрат подвергали лиофильной сушке в аппарате «ИНЕЙ-6».
Аналитическое определение специфичности ЦГТаз осуществляли следующим методом. Пробы (5 мл) реакционной смеси, состоящей из клейсте-ризованного картофельного крахмала в 50 мМ ацетатном буфере (рН 6,0), ЦГТазы и 10 мМ CaCl 2 , помещали в биологический термостат и выдерживали при 400С в течение 24 часов. По истечении указанного интервала времени, из пробирок извлекали по 900 мкл образцов, которые помещали в 2,0 мл пробирки Эппендорф. В каждую из проб вносили по 90 мкл 10%-ного раствора ксилозы, игравшей роль внутреннего стандарта. После завершения указанных манипуляций в пробирки дозировали по 990 мкл ацетонитрила ОСЧ для хроматографии и отделяли образовавшийся осадок крахмала центрифугированием при 8000 мин-1 в течение 10 минут. Порции супернатанта, соответствующие условиям реакции, анализировали с помощью ВЭЖХ на колонке «SEPARON-NH 2 »-5мкм (3х150 мм), используя в качестве элюента смесь ацетонитрил – вода в объемном соотношении 63:37. Подачу растворителя осуществляли насосом НРР-5001 со скоростью 0,7 мл/мин, а в качестве детектора использовали рефрактометр RIDK-102. Регистрацию и оцифровку аналогового сигнала, последующую обработку хроматограмм проводили с помощью программно-вычислительного комплекса «Мультихром 1.59». Калибровку прибора осуществляли методом внутреннего стандарта, используя индивидуальные ЦД производства «Wacker Chemie» (США).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Для получения ферментных препаратов использованы культуры из коллекции лаборатории прикладной микробиологии Института биологии УНЦ РАН Paenibacillus illinoisensis (IB-1087), P.ehimensis ВКМ B-2680D (IB-739), P.macerans (IB-1053), P.campinasensis (IB-417). Три первых штамма были выделены из почвы с помощью аэробной и анаэробной накопительной среды на основе растворов 0,5% β -циклодекстрина [4, 5]. Алкалотоле-рантный штамм P.campinasensis IB-417 обнаружен в процессе скрининга продуцентов щелочных бактериальных целлюлаз на щелочной элективной среде, содержавшей в своем составе 0,5% КМЦ-Na и 1% Na 2 CO 3 (рН=10,0÷11,0).
Способность к синтезу ЦД, была обнаружена лишь после выполнения 16S рРНК анализа и обнаружения близкого сходства прочитанной последовательности гена с таковыми, описанными ранее бразильскими авторами у культур P.campinasensis
JCM11200 (№ NCBI=AB073187) и P.campinasensis BL11 (DQ232773) [7-8; 20].
Для наработки образцов ферментов использовали среды и режимы культивирования, приведенные в материалах и методах.
Препараты подвергали частичной очистке пере-осаждением, высаливанием, хроматографическими и абсорбционными методами.
Используя стандартные процедуры, исследовали физико-химические свойства выделенных белков, их молекулярную массу.
Результаты описаний ЦГТаз 4-х видов бактерий, выделенных в нашей лаборатории и охарактеризованных филогенетическими методами, сведены в таблице.
Суммируя полученные результаты, можно указать на тот факт, что описания ЦГТаз P.macerans IB-1053 и P.campinasensis IB-417, P.illinoisensis IB-1087 были близки к описанным ранее для культур тех же видов.
Весьма важной характеристикой ЦГТаз является их специфичность в отношении спектра ЦД, накапливающихся в продуктах конверсии крахмала [1]. По преобладающему продукту реакции дают название ЦГТазе, указывая что она, например, относится к β -типу. По доминантному продукту реакции принято разделять циклизующие ферменты на a -[11], β -[8] и γ -ЦГТазы [12; 13].
Вместе с тем, в расчет не берется тот факт, что само соотношение [ a -ЦД]:[ β -ЦД]:[ γ -ЦД] в продуктах реакции динамично меняется во времени, и зачастую, весьма существенно. Например для a -ЦГТаз P.macerans описаны серьезные вариации соотношения a -ЦД: β -ЦД: γ -ЦД, возникающие в течение реакции, равно как и при вариациях стартового соотношения субстрат/фермент (E/S).
Учитывая, что условия выбора режима реакции зависит, как от воли автора исследования, так и от использованных им методов измерения циклизующей активности, сравнение ЦГТаз, кинетические свойства которых были исследованы в разных лабораториях зачастую не возможно.
В этой связи для изучения кинетических особенностей ЦГТаз, имевшихся в нашем распоряжении, был применен собственный подход, основанный на определении безразмерных коэффициентов, являющихся отношениями молярных концентраций KU α =[ β -ЦД]/[ a -ЦД] и KU γ =[ β -ЦД]/[ γ -ЦД] в продуктах суточной конверсии крахмала.
Измерения велись в широком диапазоне стартового соотношения (E/S), а в качестве единицы характеризующей количество ЦГТазы, была использована ее активность в мкКат, измеренная фенолфталеиновым методом.
На рис. представлены результаты сравнения каталитических свойств четырех штаммов циклодекстриногенных бактерий относящихся к роду Paeni-bacillus .
Таблица. Сравнение свойств ЦГТаз четырех видов бактерий рода Paenibacillus
|
Источник ЦГТазы |
S* |
ММ** |
pH о пт |
рН стаб. |
т „ опт. |
τ τ 50% *** |
pI |
16S рРНК NCBI |
|
|
А |
P.illinoisensis IB-1087 |
β - |
68 |
7,0 |
5-9 |
55 |
19 мин |
5.1 |
FN422001.1 |
|
Б |
P.macerans IB-1053 |
a - |
70 |
5,5 |
7-9,5 |
55 |
6,2 мин |
4.9 |
AM406669.1 |
|
В |
P.ehimensis IB-739 |
β - |
75 |
6,0 |
5,5-8,2 |
40 |
5,3 мин |
Н.д |
FN582329.1 |
|
Г |
P.campinasensis IB-417 |
β - |
82 |
7,0 |
6-10 |
60 |
3 часа 15 мин |
Н.д |
FN429977.1 |
Прим.: S* – специфичность (дозировка 10 ед/г крахмала, 40оС, 1 ч); ММ** – молекулярная масса; τ 50% *** – время экспозиции образца ЦГТазы при 550С, вызывающее 50% снижение его активности при рН 6,0 без субстрата
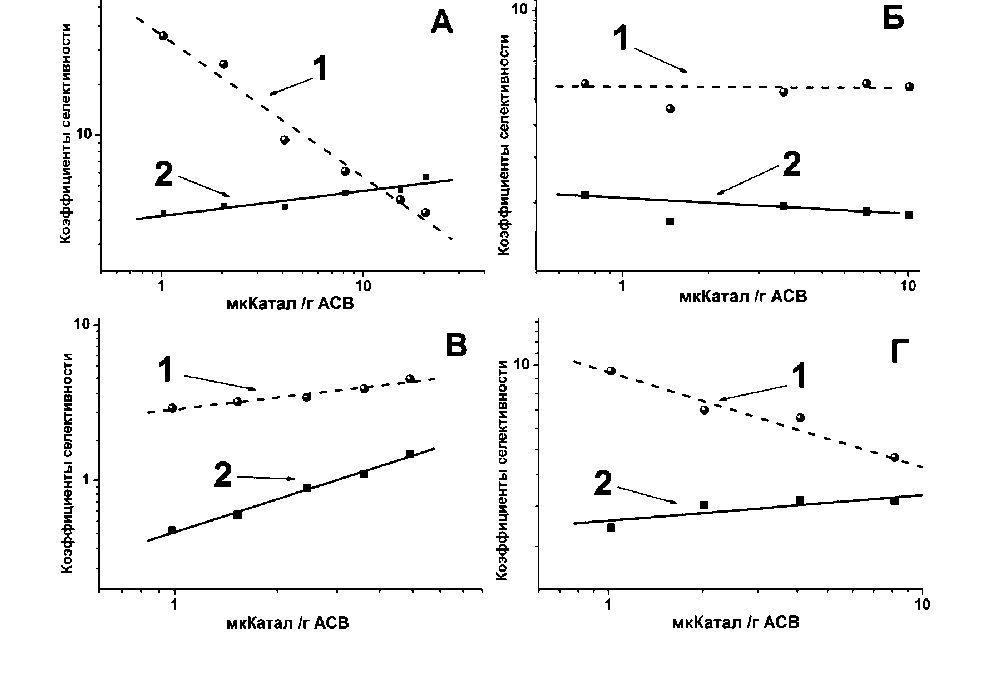
Рис. Зависимость выхода циклодекстринов от концентрации ЦГТаз, выделенных из бактерий различных видов в течение 24 ч трансформации 2,75% крахмала: А – Paenibacillus campinasensis IB-417; Б – Р.ehimensis IB-739; В – P.macerans IB-I4; Г – P.illinoisensis IB-1087. Кривые (1) и (2) обозначают величины безразмерных коэффициентов равных молярным отношениям [ β -ЦД]/[ a -ЦД] и [ β -ЦД]/ [ γ -ЦД] в продуктах реакции соответственно
Обнаружено, что во всех 4-х случаях зависимость молярных соотношений KUα=[β-ЦД]/[a-ЦД] и KUγ=[β-ЦД]/[γ-ЦД] от величины (E/S) в двойных логарифмических координатах вырождаются в линейные (рис.1). Полученная информация позволяет подробно описывать и сравнивать динамику накопления различных форм ЦД, а также ее зависимость от дозы внесенного фермента для разных типов ЦГТаз. Например, при использовании β-ЦГТазы алкалотолерантной P.campinasensis (А), накопление β-ЦД относительно a-ЦД падает с увеличением относительной дозировки фермента и этот процесс сопровождается ростом отношения KUα, из чего следует, что удельный выход γ-ЦД также снижается по мере продолжения реакции. Схожими кинетическими особенностями обладает бета-ЦГТаза P.illinoisensis (Г). Оба фермента, на ранних стадиях реакции (что адекватно низким удельным дозировкам ЦГТаз) катализируют преимущественное образование длинноцепочечных β-ЦД и γ-ЦД, которые по мере накопления начинают изомеризоваться в a-ЦД (6 глюкозных остатков). ЦГТаза P.macerans (В) катализирует трансформацию крахмала иным образом: сначала в среде накапливается a-ЦД, который по мере увеличения (E/S) трансформируется в β-ЦД. Каталитическая «ретрансформация» a- и γ-ЦД в β- форму, по мере нарастания их концентраций в ходе реакции явля- ется типичной и хорошо известной особенностью ферментов данного типа [15]. Бактерии вида P.ehimensis секретируют ЦГТазу широкой специфичности (Б), инициирующую превращение крахмала до смесей, пригодных для одновременного синтеза одновременно трех циклических декстринов. Для этого фермента характерно образование относительно постоянных соотношений a-, β- и γ-ЦД, мало зависящих от дозы внесенной ЦГТазы. ЦГТаза P.campinasensis в первые моменты реакции отличается ярко выраженной β-специфичностью, (А) но по мере трансформации субстрата в среде накапливается значительное количество a-формы. Оптимальными для трансформации крахмала в ЦД для всех четырех типов ЦГТаз можно считать их удельные дозировки на уровне 8÷10 мкКат/1г субстрата.
Таким образом, 4 культуры бактерий, секретирующие ЦГТазу и выделенные 3-мя различными методами, с использованием бета-ЦД и КМЦ-Na в качестве субстрата накопительных сред, принадлежат к роду Paenibacillus. ЦГТазы P.illinoisensis IB-1087; P.macerans IB-1053; P.campinasensis IB-417 по своим физико-химическим свойствам близки к описанным в литературе. Описание ЦГТазы P.ehimensis IB-739 (ВКМ B-2680D) выполнено впервые. Также впервые обнаружено, что при действии ЦГТаз на крахмал зависимость отношений [ β -ЦД]/[ a -ЦД] и [ β -ЦД]/[ γ -ЦД] от величины (E/S) в двойных логарифмических координатах вырождаются в линейную.
Николай Глебович Усанов, один из авторов, скоропостижно скончался при подготовке статьи к публикации.
Список литературы Сравнение кинетических свойств различных циклодекстринглюканотрансфераз
- Абелян В.А. и др. Сравнительная характеристика циклодекстрингликозилтрансфераз различных групп микроорганизмов//Биохимия. 1992. Т. 57. № 3. С. 430-437.
- Абелян В.А., Афян К.Б., Манукян Л.С. Новые циклодекстринглюканотрансферазы, продуцируемые Bacillus macerans//Прикладная биохимия и микробиология. 2000. Т. 36. № 4. С. 395-401.
- Усанов Н.Г. и др. Усовершенствованный метод фотометрического определения активности циклодекстринглюканотрансферазы//Прикладная биохимия и микробиология. 2007. Т. 43. № 1. С. 118-124.
- Усанов Н.Г., Логинов О.Н., Мелентьев А.И. Синтез циклодекстринглюканотрансфераз микроорганизмами, утилизирующими циклодекстрины в качестве единственного источника углерода//Докл. АН СССР. 1989. Т. 310. № 6. С. 1489-1492.
- А.с. 1703681 СССР. Способ выделения бактерий Bacillus macerans из почвы/Усанов Н.Г. и др. Опубл. 1991.
- Abelyan V.H. Cyclodextrines: Production and uses. Kuala Lumpur, 2005. 511 p.
- Alves-Prado H.F., Gomes E., Da Silva R. Evaluation of solid and submerged fermentations for the production of cyclodextrin glycosyltransferase by Paenibacillus campinasensis H69-3 and characterization of crude enzyme//Appl. Biochem. Biotechnol. 2006. V. 129. № 1. Р. 234-246.
- Alves-Prado H. F., Gomes E., Da Silva R. Purification and characterization of a cyclomaltodextrin glucanotransferase from Paenibacillus campinasensis strain H69-3//Appl. Biochem. Biotechnol. 2007. V. 137. Р. 41-55.
- Binder F., Huber O., Bock A. Cyclodextrin-glycosyltransferase from Klebsiella pneumoniae M5a1: Cloning, nucleotide sequence and expression//Gene Lehrstuhl fur Mikrobiologie. 1986. V. 47. № 3. Р. 269-277.
- Doukyu N., Kuwahara H., Aono R. Isolation of Paenibacillus illinoisensis that produces cyclodextrin glucanotransferase resistant to organic solvents//Biosci., Biotechnol. Biochem. 2003. V. 67. № 2. Р. 334-340.
- Gawande B., Patkar A. Alpha-cyclodextrin production using cyclodextrin glycosyltransferase from Klebsiella pneumoniae AS-22//Starch/Staerke. 2001. V. 53. № 2. Р. 75-83.
- Hirano K. et al. Molecular cloning and characterization of a novel gamma-CGTase from alkalophilic Bacillus sp.//Appl. Microbiol. Biotechnol. 2006. V. 70. № 2. Р. 193-201.
- Kato T., Horikoshi K. A new gamma-cyclodextrin forming enzyme produced by Bacillus subtilis No.313//Starch Sci. 1986. V. 33. № 2. Р. 137-143.
- Martins R.F., Hatti-Kaul R. A new cyclodextrin glycosyltransferase from an alkaliphilic Bacillus agaradhaerens isolate: Purification and characterisation//Enzyme and Microbial Technology. 2002. V. 30. № 1. Р. 116-124.
- Patrick Lee K.C., Tao B.Y A kinetic study of cyclodextrin glycosyltransferase: Substrate and product inhibitions//Biotechnol. Appl. Biochem. 1995. V. 21. № 1. Р. 111-121.
- Sivaramakrishnan S. и др. a-Amylases from microbial sources-An overview on recent developments//Food Technol. Biotechnol. 2006. V. 44. № 2. Р. 173-184.
- Suominen I. и др. Paenibacillus stellifer sp. nov., a cyclodextrinproducing species isolated from paperboard//Intern. J. System. Evolution. Microbiology. 2003. V. 53. № 5. Р. 1369-1374.
- Tonkova A. Bacterial cyclodextrin glucanotransferase//Enzyme and Microbial Technology. 1998. V. 22. № 8. Р. 678-686.
- Vollu R.E. et al. Cyclodextrin production and genetic characterization of cyclodextrin glucanotranferase of Paenibacillus graminis//Biotechnol. Lett. 2008. V. 30. № 5. Р. 929-935.
- Yoon J.H. et al. Paenibacillus campinasensis sp. nov., a cyclodextrin-producing bacterium isolated in Brazil//Intern. J. System. Bacteriology. 1998. V. 48. №. 3. Р. 833-837.


