Сравнение трансперинеальной и трансректальной биопсии предстательной железы в амбулаторных условиях: рандомизированное контролируемое исследование
Автор: Воробьев В.А., Акперов Г.Р., Бакланова О.В., Мицкевич Д.С., Ковалев Е.В., Попов И.П., Кернер Д.В., Азизов З.С.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Клинические исследования
Статья в выпуске: 1 т.25, 2026 года.
Бесплатный доступ
Цель исследования – сравнить диагностическую эффективность, безопасность и переносимость трансперинеальной (ТП) и трансректальной (ТР) биопсий предстательной железы, выполняемых амбулаторно под местной анестезией. Материал и методы. В рандомизированное контролируемое исследование включено 106 мужчин с подозрением на рак простаты. Пациенты случайным образом распределены в группы ТП (n=54) и ТР (n=52). Всем выполнена систематическая 12-точечная биопсия; при наличии очагов PI-RADS ≥3 – таргетная биопсия. Антибиотикопрофилактика назначалась только в ТР-группе. Первичной конечной точкой была частота выявления клинически значимого рака (ISUP ≥2). Вторичные исходы: общая детекция рака, осложнения (Clavien–Dindo), болевой синдром (ВАШ), длительность процедуры и удовлетворенность. Результаты. Рак обнаружен у 74,1 % пациентов группы ТП и у 55,8 % – группы ТР (p=0,066). Клинически значимый рак – у 44,4 и 34,6 % соответственно (p=0,33). Инфекционные осложнения отмечены только после ТР-биопсии (11,5 vs 0 %; p=0,012); тяжелых осложнений не зарегистрировано. Легкие осложнения (гематурия, гематоспермия) встречались одинаково часто (30 %). Боль по ВАШ была ниже при ТП (медиана 3 vs 5, p<0,01); сильная боль (ВАШ ≥6) – у 6 % ТП против 33 % ТР. Длительность процедуры составила 20 мин для ТП и 8 мин для ТР (p<0,001). Удовлетворенность пациентов была высокой в обеих группах (85 и 75 %, p=0,20). Заключение. ТПбиопсия показала сопоставимую с ТР диагностическую эффективность при меньшем риске инфекций и более низком уровне боли. Несмотря на большую длительность процедуры, удовлетворенность пациентов оставалась высокой. Полученные данные поддерживают применение трансперинеальной биопсии как более безопасного метода в амбулаторной практике.
Трансперинеальная и трансректальная биопсия предстательной железы, осложнения, рандомизированное контролируемое исследование
Короткий адрес: https://sciup.org/140314343
IDR: 140314343 | УДК: 616.65-076 | DOI: 10.21294/1814-4861-2026-25-1-5-17
Comparison of transperineal and transrectal prostate biopsy in the outpatient setting: a randomized controlled trial
Objective: to compare transperineal (TP) versus transrectal (TR) prostate biopsy under local anesthesia in terms of diagnostic yield, safety, and patient tolerability in an outpatient randomized trial. Material and Methods. A total of 106 men with suspected prostate cancer were randomized 1:1 to TP (n=54) or TR (n=52) biopsy. All patients underwent 12-core systematic sampling; MRI-targeted cores were added for PI-RADS ≥3. Antibiotic prophylaxis was given only in the TR group. The primary endpoint was detection of clinically signifcant prostate cancer (csPCa, ISUP ≥2). Secondary outcomes included overall cancer detection, complications (Clavien–Dindo), pain scores (VAS), procedure time, and satisfaction. Results. Cancer was detected in 74.1 % of TP vs 55.8 % of TR patients (p=0.066). csPCa was found in 44.4 % vs 34.6 % (p=0.33). Infectious complications occurred only after TR biopsy (11.5 % vs 0 %; p=0.012). No severe (grade III–V) events were observed. Minor events (hematuria, hematospermia) occurred in 30 % of both groups. Median VAS pain was lower in TP (3 vs 5, p<0.01); severe pain (VAS ≥6) was reported by 6 % in TP vs 33 % in TR. Median procedure time was longer with TP (20 vs 8 min, p<0.001). Patient satisfaction was high in both arms (85 % vs 75 %, p=0.20). Conclusion. Outpatient TP biopsy provided equivalent diagnostic performance to TR, with markedly fewer infectious complications and lower pain scores. Despite longer procedure time, satisfaction remained high. These fndings support TP biopsy as a safer alternative to TR in routine practice.
Текст научной статьи Сравнение трансперинеальной и трансректальной биопсии предстательной железы в амбулаторных условиях: рандомизированное контролируемое исследование
Биопсия предстательной железы является ключевым методом диагностики рака простаты. Начиная с 1989 г., когда K.K. Hodge et al. [1] впервые описали систематическую трансректальную биопсию под контролем УЗИ, трансректальный доступ (через прямую кишку) стал стандартом благодаря своей относительной простоте и возможности выполнения под местной анестезией в амбулаторных условиях. Трансректальная (ТР) ультразвуковая биопсия обычно включает забор 10–12 столбиков через стенку прямой кишки и характеризуется высокой диагностической точностью выявления опухолей простаты [1]. Однако очевидным недостатком трансректального пути является необходимость прохождения биопсийной иглы через микофлору прямой кишки, что создает риск заноса фекальной бактерии в простату и кровь [2]. Несмотря на профилактическое применение фторхинолонов или других антибиотиков перед процедурой, инфекционные осложнения (вплоть до сепсиса) после ТР биопсии продолжают отмечаться и даже участились за последние деся- тилетия из-за роста антибиотикорезистентности микрофлоры [3]. По данным ряда современных исследований, частота инфекций после ТР биопсии составляет 2–5 %, а случаи сепсиса – до 2,4 % [3], причем подавляющее большинство возбудителей при постбиопсийных инфекциях являются резистентными к фторхинолонам (88–91 %) [3]. В редких случаях возможны жизнеугрожающие осложнения; летальность от сепсиса после ТР биопсии оценивается около 0,1 % [4].
Трансперинеальный (ТП) доступ к простате был исторически первой методикой биопсии (предлагались пункции через промежность еще в 1920-х гг.), однако до недавнего времени применялся реже, т.к. традиционно требовал спинальной или общей анестезии из-за болезненности процедуры [4]. Современное развитие методик местного обезболивания (включая блокаду нервов простаты) возродило интерес к трансперинеальной биопсии как к более безопасной альтернативе без трансколониальной контаминации [4]. При трансперинеальной биопсии иглы проводятся через стерильно обработанную кожу промежности и не проходят через кишечник, поэтому риск инфекционного обсеменения практически отсутствует [5]. В крупных сериях сообщается о нулевой частоте госпитализаций по поводу инфекций после трансперинеальной биопсии [6], тогда как при трансректальном методе этот показатель достигает 2–5 % [6]. Таким образом, ТП метод позволяет вовсе обходиться без антибиотикопрофилактики, что особенно важно в контексте глобальной стратегии сохранения эффективности антибиотиков (antibiotic stewardship) [4]. Европейские урологические руководства в последние годы отдают предпочтение трансперинеальному доступу именно из-за более низкого риска инфекционных осложнений [7]. Некоторые эксперты призывают к «TREXIT» – полному отказу от трансректальной биопсии в пользу трансперинеальной [4, 5].
Помимо безопасности, актуальным является вопрос диагностической эффективности разных подходов. Считается, что ТП биопсия обеспечивает лучший доступ к передним отделам и верхушке простаты, которые труднее охватить при стандартной трансректальной схеме [8, 9]. Теоретически это может повысить выявляемость рака, особенно в труднодоступных зонах. Ранние метаанализы 2010-х гг. не показывали существенных различий в частоте выявления рака между ТР и ТП подходами, хотя отмечали сниженную частоту лихорадки и ректальных кровотечений при трансперинеальной биопсии [10]. Однако недавно опубликованное крупное многоцентровое исследование TRANSLATE (2025) на биопсий-наивных пациентах продемонстрировало значимое увеличение выявления клинически значимого рака (ISUP ≥2) при трансперинеальной биопсии по сравнению с трансректальной (60 vs 54 %, OR=1,32, p=0,031) [11]. При этом в группе ТР отмечалось больше госпитализаций по поводу инфекций (9 случаев против 2 при ТП) и несколько более низкий комфорт процедуры [11]. Другое крупное рандомизированное контролируемое исследование (PREVENT, 2024) не выявило различий в частоте значимого рака (53 vs 50 %) между методами, но подтвердило отсутствие инфекций после ТП биопсии без антибиотиков против 4 инфекций (1,4 %) после ТР биопсии с таргетной антибиоти-копрофилактикой (p=0,059) [12]. В исследовании ProBE-PC (2024, n=718) также не найдено различий ни в инфекционных (2,7 % в обеих группах), ни в геморрагических осложнениях между ТР и ТП подходами [13]. Таким образом, текущие данные противоречивы: одни работы указывают на сопоставимую онкологическую результативность методов [10], другие – на преимущество ТП по выявлению значимого рака [11]. Различия могут объясняться дизайном исследований (использование МРТ-наведения, критерии включения) и опытом операторов. В то же время в части безопасности консенсус постепенно склоняется в пользу транс- перинеального доступа, позволяющего практически исключить серьезные инфекции [6].
Цель исследования – провести прямое сравнение трансперинеальной и трансректальной биопсии простаты, выполняемых в амбулаторных условиях под местной анестезией, с акцентом как на диагностические показатели (общая и клинически значимая выявляемость рака), так и на профиль осложнений, болевой синдром и восстановление. Исследование проведено в соответствии со стандартами CONSORT для рандомизированных контролируемых испытаний, что отражено в структуре представления результатов.
Материал и методы
Проведено проспективное одноцентровое рандомизированное контролируемое исследование. Критерии включения: мужчины ≥18 лет с показаниями к первичной или повторной биопсии предстательной железы (уровень ПСА >4 нг/мл и/или подозрение на опухоль по данным цифрового ректального исследования или МРТ, категория PIRADS ≥3). Критерии исключения: ранее подтвержденный рак простаты, острый простатит, тяжелые сопутствующие состояния, делающие биопсию рискованной (не скорректированные нарушения свертываемости, выраженные геморроидальные узлы и пр.), а также невозможность наблюдения пациента в течение 30 дней после процедуры.
Всего с января по декабрь 2024 г. оценено 120 пациентов, из них 14 исключены (10 – не соответствовали критериям, 4 – отказались). В исследование рандомизировано 106 пациентов. Схема рандомизации – 1:1 в две группы: трансперинеальная биопсия (группа ТП, n=54) и трансректальная биопсия (группа ТР, n=52). Распределение осуществляли с помощью компьютерной генерации случайных чисел в блоках по 4–6, с сокрытием последовательности (запечатанные конверты). Из-за характера вмешательства были ослеплены только пациенты (не обсуждался метод биопсии, процедура выполнялась за ширмой); оценка исходов осложнений проводилась независимым врачом на контрольных визитах.
Все биопсии выполнялись амбулаторно в условиях процедурного кабинета под местной анестезией. В положении лежа на спине с разведенными ногами выполнялась местная анестезия 1 % раствором лидокаина: для ТП биопсии – инфильтрация кожи промежности и выполнение перипроста-тической блокады (введение 5 мл лидокаина по ходу NV-связок у основания простаты с каждой стороны под контролем ультразвука); для ТР биопсии – стандартная перипростатическая блокада под контролем трансректального УЗИ (10 мл 1 % лидокаина в латеральные края простаты у основания). Дополнительно пациентам группы ТП за 5 мин до пункции на кожу промежности наносился анестетический крем лидокаин/прилоксаин.
Трансректальная биопсия выполнялась в литотомическом положении с ТРУЗИ-контролем (датчик 7,5 МГц, вводимый в прямую кишку). Брали 12 систематических биоптатов из периферической зоны (схема секстант + дополнительные боковые образцы у основания и средней трети справа/сле-ва). При наличии подозрительных зон по МРТ также выполняли прицельную биопсию этих очагов (когнитивная фьюжн-навигация). Иглы 18G, автоматический биопсийный пистолет, длина выстрела 17 мм. Каждый столбик помещался в отдельный контейнер с формалином и маркировался.
Трансперинеальная биопсия проводилась в литотомическом положении, через два прокола кожи в проекции правой и левой половины промежности. Использовалась шаговая сетка-трафарет, прикрепленная к трансректальному ультразвуковому датчику (оборудование для шаблонной биопсии). Выполнялось от 12 до 18 пункций в зависимости от объема простаты: систематически охватывались периферическая и передняя зоны каждой половины простаты (шаблон распределения по секторам через промежность). При наличии МРТ-очагов выполнялись целевые биопсии путем отклонения трафарета под соответствующим углом (фьюжн по изображению МРТ/УЗИ осуществлялась когнитивно). Таким образом, ТП биопсия сочетала систематический шаблон и таргетные образцы, при общем числе столбиков, как правило, 14–18 (в среднем – 16).
После биопсии пациенты обеих групп наблюдались в клинике 2 ч. Профилактически всем назначались НПВП (кеторолак 10 мг per os однократно) и рекомендовалось обильное питье. Антибиотико-профилактика: в группе ТР биопсии стандартно вводился ципрофлоксацин 500 мг перорально за час до процедуры и еще 500 мг вечером в день биопсии (при аллергии – триметоприм/сульфаме-токсазол); группе ТП биопсии профилактический антибиотик не назначался (исходя из низкого риска инфекции при данном методе). Однако при развитии симптомов инфекции после биопсии пациентам обеих групп была предусмотрена возможность раннего начала антибактериальной терапии.
Переменные и исходы
Первичная конечная точка – частота обнаружения клинически значимого рака простаты, определенного как наличие аденокарциномы Gleason Grade Group ≥2 (соответствует сумме баллов Глисона ≥7 (3 + 4 и выше)). Эта категория отражает опухоли, имеющие клиническое значение и обычно требующие активного лечения, в отличие от Gleason 6 (ISUP 1), которые могут наблюдаться. Диагноз рака и градация по ISUP устанавливались патоморфологом, не знавшим о методе биопсии, по гистологическим препаратам стандартным образом.
Вторичные исходы включали: (1) общую часто- ту выявления рака простаты (любой Gleason ≥6); (2) распределение пациентов по категориям ISUP 1–5 в каждой группе; (3) число положительных биоптатов (количество столбиков с опухолью) на пациента; (4) показатели безопасности в течение 30 дней после процедуры – инфекционные осложнения (определены как лихорадка ≥38 °С, диагноз: инфекция мочевых путей или простатит, сепсис) и неинфекционные осложнения (гематурия, ге-моспермия, острая задержка мочи, кровотечение из прямой кишки и др.), классифицированные по шкале Clavien–Dindo; (5) болевой синдром во время и сразу после биопсии по визуальной аналоговой шкале (ВАШ 0–10, где 0 – нет боли, 10 – невыносимая боль); (6) длительность процедуры (время от ввода датчика до извлечения последней иглы, мин); (7) необходимость госпитализации или обращения за неотложной помощью в связи с осложнениями; (8) время восстановления трудоспособности (количество дней до возвращения к работе или обычной активности); (9) удовлетворенность пациента процедурой (оценивалась на контрольном визите через 1 мес, двоичный ответ: доволен/не доволен результатом и переносимостью биопсии).
Пациенты наблюдались амбулаторно: обязательный осмотр уролога на 1-е сут (для удаления катетера, если установлен, и оценки ранних осложнений), затем повторный визит через 7–10 дней (оценка состояния, обсуждение гистологии) и телефонный контакт или визит через 30 дней (фиксация поздних осложнений). Далее осуществлялось стандартное онкологическое наблюдение (результаты лечения за рамками данной работы). При любом недомогании пациенты могли внепланово обратиться; серьезные осложнения регистрировались вплоть до 90 сут.
Размер выборки (n=106) был ограничен, поскольку исследование носит проспективный характер. Постфактум мощность для выявления различий в частоте значимого РПЖ оценивалась в 30 % (для разницы 10–15 % между группами при α=0,05). Статистический анализ выполнен с использованием пакета SPSS v.27. Переменные с нормальным распределением описаны средним ± стандартное отклонение, с ненормальным – медианой и межквартильным размахом. Для межгруппового сравнения использованы критерий Стьюдента или Mann–Whitney (непарные данные) для количественных показателей и χ2 или точный тест Фишера – для категориальных данных. Двусторонние значения p<0,05 считались статистически значимыми.
Анализ проводился по принципу intention-to-treat: все рандомизированные пациенты включены в итоговый анализ соответствующей группы, вне зависимости от незначительных отклонений (в нашем случае все пациенты получили назначенную интервенцию, потерь для анализа не было).
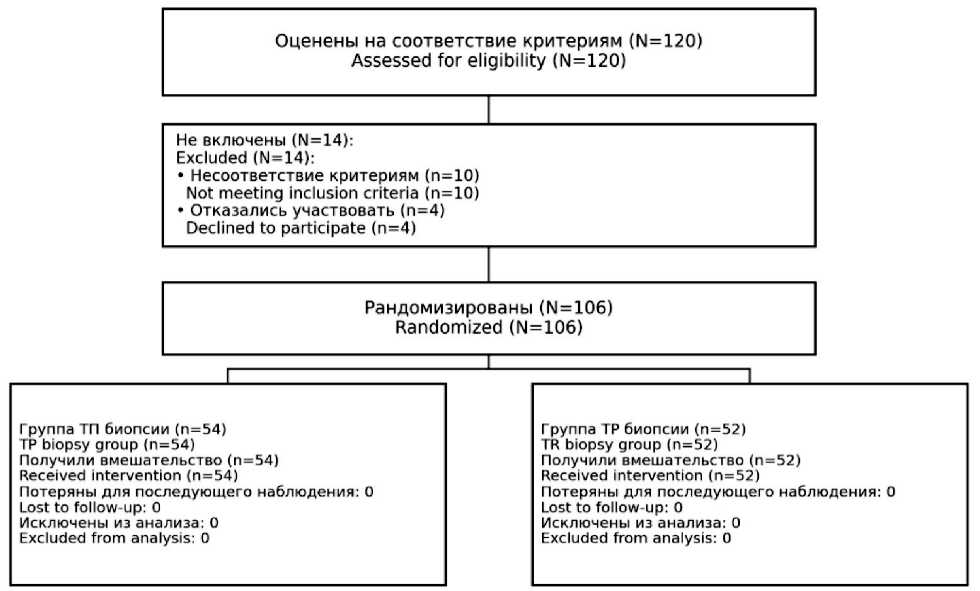
Рис. 1. CONSORT-блок-схема исследования. Примечание: рисунок выполнен авторами Fig. 1. CONSORT flow diagram of the study. Note: created by the authors
Данные об осложнениях оценивались в совокупности и по отдельным категориям. Для первичной конечной точки (выявление значимого РПЖ) дополнительно рассчитан относительный риск (RR) с 95 % доверительным интервалом. Представлена CONSORT-блок-схема прохождения участников через исследование (рис. 1).
Результаты
В табл. 1 представлены исходные характеристики двух групп. Группы статистически не различались по возрасту, уровню ПСА, объему предстательной железы и другим факторам. Средний возраст пациентов составил 67 лет (диапазон 45–78), медиана ПСА – 8,0 нг/мл (IQR 6,1–12,5). У 58 % пациентов при пальцевом ректальном исследовании пальпировался подозрительный узел в простате, равномерно в обеих группах (p=0,44). МРТ перед биопсией была выполнена у 97 % пациентов; в 72 % случаев выявлены очаги PIRADS 4–5 (по 39 пациентов в каждой группе, p=0,87). Доля ранее перенесших биопсию пациентов (повторная биопсия) составила 15 % (8/54) в группе ТП и 17 % (9/52) в группе ТР (p=0,78); медиана времени от предыдущей биопсии – 24 мес. Таким образом, группы были хорошо сбалансированы по ключевым параметрам.
Все пациенты успешно перенесли назначенную процедуру без интраоперационных осложнений. Ни один пациент не был переквалифицирован в другую группу. Продолжительность процедуры оказалась значительно больше при трансперинеальном доступе: медиана –20,0 мин (IQR 18–28 мин) против 7,9 мин (IQR 7–9 мин) при трансректальной биопсии (p<0,001). У 87 % пациентов группы ТП процедура длилась >15 мин (против 4 % в группе ТР). Этот результат объясняется большим числом проколов и необходимостью смены позиций иглы при шаблонной биопсии.
Среднее количество взятых биоптатов в группе ТП составило 14,8 ± 2,9, в группе ТР – 12,2 ± 0,8 (p<0,001). У 90,7 % пациентов ТП группы было взято ≥14 столбиков (у 51 % – 16 и более), тогда как у 100 % пациентов ТР группы выполнялось ровно 12 пункций (согласно протоколу). Таким образом, ТП подход позволял более обширное исследование тканей простаты, включая передние зоны. Все взятые столбики были достаточного качества для гистологической оценки; артефактов, мешающих анализу, не отмечено.
В группе ТР всем пациентам было профилактически введено по 1–2 дозы ципрофлоксацина; в группе ТП планово антибиотики не применялись. Фактически лишь 8 (14,8 %) пациентов группы ТП получили антибиотики в раннем послеоперационном периоде, эти случаи связаны с подозрением на инфекцию (повышение температуры или симптомы простатита) и будут рассмотрены ниже. Остальные 46 (85,2 %) пациентов перенесли ТП биопсию без антибиотикотерапии.
Показатели, характеризующие переносимость процедуры, приведены в табл. 2. Средний уровень
Таблица 1/table 1
Исходные характеристики пациентов в группах трансперинеальной (ТП) и трансректальной (ТР) биопсии
Baseline characteristics of patients in the transperineal (tP) and transrectal (tR) biopsy groups
|
Показатель/Parameter |
ТП биопсия/ TP biopsy (n=54) |
ТР биопсия/ TR biopsy (n=52) |
p-value |
|
Возраст, лет/Age, years |
66,8 ± 7,1 |
66,1 ± 8,3 |
0,62 |
|
ПСА, нг/мл (медиана, IQR)/PSA, ng/mL (median, IQR) |
8,4 (6,0–13,0) |
7,8 (5,9–12,1) |
0,74 |
|
Объем простаты, мл/Prostate volume, mL |
46,5 ± 12,3 |
48,2 ± 15,0 |
0,53 |
|
Пальпируемое уплотнение простаты/Palpable prostate nodule |
31/54 (57 %) |
30/52 (58 %) |
0,88 |
|
PIRADS 4–5 по МРТ (%)/PI-RADS 4–5 on MRI (%) |
39 (72 %) |
38 (73 %) |
0,91 |
|
Предшествующая биопсия в анамнезе/Previous biopsy history |
8 (14,8 %) |
9 (17,3 %) |
0,78 |
|
Сопутствующая патология/Comorbidities* |
|||
|
Артериальная гипертензия/Hypertension |
24 (44 %) |
21 (40 %) |
0,68 |
|
Сахарный диабет/Diabetes mellitus |
6 (11 %) |
5 (10 %) |
0,88 |
|
Хронический простатит (анамнез)/Chronic prostatitis (history) |
7 (13 %) |
8 (15 %) |
0,77 |
|
Антикоагулянты/антиагреганты/Anticoagulants/antiplatelet agents** |
5 (9 %) |
4 (8 %) |
0,85 |
|
Индекс массы тела, кг/м² (M)/Body mass index, kg/m² (M) |
27,5 |
28,0 |
0,56 |
Примечания: * – значимых различий по другим сопутствующим заболеваниям (ИБС, ХОБЛ и др.) между группами не отмечено: ** – прием антикоагулянтов прерывался согласно протоколу за 5–7 дней до биопсии; все биопсии прошли без геморрагических инцидентов; таблица составлена авторами.
Notes: * – no statistically significant differences were observed between the groups with regard to other comorbidities (including coronary artery disease, chronic obstructive pulmonary disease, etc.); * – anticoagulant therapy was discontinued in accordance with the study protocol 5–7 days prior to biopsy; all biopsies were performed without hemorrhagic complications; created by the authors.
Таблица 2/table 2
Ход процедуры и переносимость (сравнение групп)
Procedure course and tolerability (comparison between groups)
|
Показатель/ Parameter |
ТП биопсия/ TP biopsy (n=54) |
ТР биопсия/ TR biopsy (n=52) |
p-value |
|
Время процедуры, мин/Procedure time, min |
20,96 ± 7,4 |
8,16 ± 3,1 |
<0,001 |
|
>15 мин (доля пациентов)/>15 min (proportion of patients) |
47 (87,0 %) |
2 (3,8 %) |
<0,001 |
|
Число биоптатов/Number of core |
14,8 ± 2,9 |
12,2 ± 0,8 |
<0,001 |
|
ВАШ боль (0–10)/VAS pain (0–10) |
2,74 ± 2,11 |
4,96 ± 2,45 |
<0,001 |
|
Боль умеренная/сильная (ВАШ ≥6)/Moderate/severe pain (VAS ≥6) |
3 (5,6 %) |
17 (32,7 %) |
<0,001 |
|
Дополнительный анальгетик потребовался/Additional analgesic required |
3 (5,6 %) |
17 (32,7 %) |
<0,001 |
|
Катетеризация мочевого пузыря после/Post-procedure bladder catheterization |
5 (9,3 %) |
4 (7,7 %) |
0,79 |
|
Госпитализация в день биопсии/Hospitalization on the day of biopsy |
0 |
0 |
– |
|
Удовлетворен процедурой (через 1 мес)/ Satisfied with the procedure (at 1 month)* |
53 (98,1 %) |
49 (94,2 %) |
0,88 |
|
Возврат к обычной активности, дней/Return to usual activities, days |
2 (IQR 1–3) |
3 (IQR 2–4) |
0,08 |


