Сравнительная характеристика эффективности и гематологической токсичности двух режимов противоопухолевой химиотерапии (CVC и CVCV) у больных мелкоклеточным раком легкого
Автор: Матяш М.Г., Феденко М.Г., Гольдберг В.Е., Жданов В.В., Симолина Е.И., Высоцкая В.В.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Клинические исследования
Статья в выпуске: 2 (14), 2005 года.
Бесплатный доступ
В проведенном исследовании сравнивалась эффективность и гематологическая токсичность двух режимов противо- опухолевой химиотерапии CVC и CVCV (CVC - вепезид). Показано, что при практически равной токсичности режим CVCV обладает значимо большей эффективностью, чем режим CVC.
Короткий адрес: https://sciup.org/14054205
IDR: 14054205
Comparative characteristics of efficiency and hematological toxicity of two regimens of anti-tumor chemotherapy (CVC and CVCV) in patients with small cell lung cancer
Efficiency and hematological toxicity of 2 regimens of anti-tumor chemotherapy (CVC and CVC-vepeside) were compared in the study. Having nearly the same toxicity, CVCV regimen was shown to have a significantly higher efficiency compared to CVC regimen.
Текст научной статьи Сравнительная характеристика эффективности и гематологической токсичности двух режимов противоопухолевой химиотерапии (CVC и CVCV) у больных мелкоклеточным раком легкого
COMPARATIVE CHARACTERISTICS OF EFFICIENCY AND HEMATOLOGICAL TOXICITY OF TWO REGIMENS OF
ANTI-TUMOR CHEMOTHERAPY (CVC AND CVCV) IN PATIENTS WITH SMALL CELL LUNG CANCER
M.G. Matyash1, M.G. Fedenko3, V.E, Goldberg1, V.V. Zhdanov2, E.I. Simolina1, V.V. Vysotskaya1
Cancer Research Institute, Tomsk Scientific Center, SB RAMS'
Pharmacology Research Institute, Tomsk Scientific Center, SB RAMS2 Oncologic Dispensary3, Tyva Republic, Kyzyl
Efficiency and hematological toxicity of 2 regimens of anti-tumor chemotherapy (CVC and CVC+vepeside) were compared in the study. Having nearly the same toxicity, CVCV regimen was shown to have a significantly higher efficiency compared to CVC regimen.
Рак легкого на протяжении многих лет занимает ведущее место в структуре онкологической патологии [3] и остается одной из основных причин смертности онкологических больных в большинстве стран мира. При этом в 15-30 % случаев диагностируется мелкоклеточный рак легкого (МРЛ) [12,15], который относится к категории наиболее злокачественных опухолей, поскольку характеризуется скрытым течением, быстрым развитием (среднее время удвоения объема опухоли колеблется от 30 до 80 дней), ранним метастазированием и плохим прогнозом [1,7,8,9]. Вследствие вышеназванных причин основным для лечения больных МРЛ был и остается метод проти-. воопухолевой химиотерапии [11]. Достигнут значительный прогресс: современные схемы цитостатической терапии позволяют добиться общего эффекта в среднем у 90% [ 14], а полных регрессий - у 30-50 % больных МРЛ. Стало возможным и излечение данного заболевания в 2-4 % случаев [6].
В настоящее время являются бесспорными ряд положений, которыми руководствуются онкологи, занимающиеся лечением МРЛ.
Для комбинированной химиотерапии обычно подбирают противоопухолевые препараты, совпадающие по противоопухолевой активности, но различающиеся (на молекулярном, клеточном уровнях или на уровне организма) по механизму действия [4]. Исходя из токсикологического принципа в комбинацию включают препараты, которые при монотерапии активны в отношении данной опухоли, но'обла-дают разным профилем токсичности.
Выигрыш от выбора лечения больного на основании известных научных фактов имеет ряд преимуществ, среди которых не последнее место занимают следующие: для многих онкологических больных излечение недостижимо, поэтому большую роль играет снижение токсичности проводимой терапии; даже небольшой выигрыш в результатах имеет значение при лечении наиболее распространенных опухолевых заболеваний [5].
Проблему составляет выбор рациональной схемы химиотерапии, которая смогла бы обеспечить высокие показатели выживаемости при сохранении качества жизни больных.
СИБИРСКИЙ ОНКОЛОГИЧЕСКИЙ ЖУРНАЛ. 2005. №2 (14)
Руководствуясь вышеизложенными принципами, нами была поставлена цель исследования: провести сравнительную оценку эффективности и токсичности двух режимов противоопухолевой химиотерапии С VC и С VC V (С VC+вепезид) и на основе полученных результатов определить целесообразность включения Вепезида в программу лечения больных МРЛ.
Материалы и методы
В настоящую работу включены результаты изучения эффективности и токсичности двух режимов противоопухолевой химиотерапии - С VC и С VC V - у больных мелкоклеточным раком легкого, находившихся на обследовании и лечении в отделении химиотерапии НИИ онкологии ТНЦ СО РАМН с 1999 по 2004 г., не получавших ранее специальной терапии. Материалом исследования являлись костный мозг, капиллярная и венозная кровь. Диагноз в каждом случае устанавливался на основании данных клинического, эндоскопического, рентгенологического и ультразвукового методов обследования и был верифицирован морфологически. Программа лечения включала в себя проведение 3 курсов лекарственного лечения с интервалом между ними в 3 нед.
Противоопухолевую химиотерапию в режиме С VC получали 16 пациентов: винкристин 1,4 мг/м2 - в 1 -й день; циклофосфан 600 мг/м2- в 1 -й день; карбоплатин 300 мг/м2 - во 2-й день.
В режиме CVCV лечение проведено 41 пациенту: винкристин 1,4 мг/м2 - в 1-й день; циклофосфан -600 мг/м2- в 1 -й день; карбоплатин - 300 мг/м2 - во 2-й день; вепезид - по 120 мг/м2 - с 3-го по 5-й день.
Определение показателей периферической крови (гемоглобин, эритроциты, лейкоциты, гемограмма, тромбоциты) производили стандартными гематологическими методами [2]. Полученные результаты обрабатывали методами вариационной статистики.
Результаты и обсуждение
Прежде всего необходимо было определить эффективность названных режимов химиотерапии. Оценка эффекта проводилась нами через 3 нед после окончания 3 курсов химиотерапии. При проведении полихимиотерапии в режиме CVC после завершения всей программы лечения у 10 из 16 пациентов была зарегистрирована частичная регрессия (ЧР) опухолевого процесса, что составило 62,5 %. Полная регрессия (ПР) не была достигнута ни у одного боль ного. У пяти пациентов, получавших лечение по данной программе, отмечалась стабилизация опухолевого процесса (31,25 %), и у одного больного было выявлено прогрессирование процесса (6,25 %). Общая эффективность программы CVC, таким образом, составила 62,5 %.
При проведении цитостатического лекарственного лечения по программе CVCV общая эффективность составила 87,8 % за счет достижения ПР у 2 больных (4,9 %) и ЧР - у 34 пациентов (82,9 %). Стабилизация процесса была отмечена в 4 случаях (9,8 %), прогрессирование процесса определялось у одного больного (2,4 %).
Результаты проведенных нами исследований показали прирост общей эффективности (ОЭ) на 25,3% при применении режима CVCV в сравнении с режимом CVC, что является весьма существенным.
Применение эпиподофиллотоксинов, к которым относится Вепезид, совместно с цисплатином или карбоплатином является частью терапии 1 -й линии, и эти комбинации большинством исследователей признаются стандартными [10,13]. По данным литературы, полные и частичные регрессии составляют 80-90 % от числа всех леченных по названным программам больных. Таким образом, общая эффективность 87,8 %, отмеченная нами при проведении режима CVC V, находится в соответствии с установленными показателями. Кроме того, следует учесть и тот факт, что оценка эффективности проводилась нами в более ранние сроки, чем это делается в большинстве исследований. Возможно, при проведении большего количества курсов число полных регрессий выросло бы за счет достигнутых частичных регрессий. К сожалению, оценить эффективность на более поздних сроках не представлялось возможным, так как пациенты после завершения программы лечения в рамках данного исследования получали противоопухолевую терапию по разным схемам, а также лучевую терапию.
Второй, не менее важной частью исследования было определение безопасности режимов химиотерапии CVC и CVCV (CVC+вепезид).
Поскольку для Этопозида (Вепезида) характерным является угнетение миелопоэза [4], мы сочли необходимым оценить его гематологическую токсичность.
При анализе содержания эритроцитов в периферической крови больных, получавших химиотерапию по программе CVC, отмечена тенденция к последовательному уменьшению данного показателя от курса, к курсу цитостатического лечения: от 4,07+0,09 Т/л перед началом лечения до 3,80±0,21 Т/л после окончания 3-го курса. Однаш достоверных различий между значениями данного показателя выявлено не было .
Средние значения концентрации гемоглобина в периферической крови также изменялись незначительно в течение всего периода наблюдения, при этом минимальное значение данного показателя (130,50+5,55 г/л) было зарегистрировано после 2-го курса химиотерапии, а затем отмечалось повышение содержания гемоглобина практически до первоначального уровня (138,67+11,62 г/л и 140,04±3,05 г/л соответственно). Выявленные отклонения были недостоверными.
Таким образом, было установлено, что проведение цикловой полихимиотерапии в режиме CVC не вызывает статистически достоверного снижения показателей красной крови.
При проведении химиотерапии по программе CVC V была отмечена тенденция к уменьшению содержания эритроцитов в периферической крови от курса к курсу цитостатического лечения: от 4,10±0,07 Т/л перед началом лечения до 3,57±0,10 Т/л после окончания 3-го курса, при этом начиная с контрольной точки до 2-го курса химиотерапии снижение содержания эритроцитов было статистически достоверным.
Средние значения концентрации гемоглобина в периферической крови изменялись незначительно в течение всего периода наблюдения, при этом отмечалось уменьшение данного показателя к окончанию каждого из 3 курсов химиотерапии, а наименьший уровень содержания гемоглобина был зарегистрирован после 2-го курса химиотерапии (124,79±4,56 г/ л) — в сравнении с первоначальным его значением — 135,40±2,74 г/л. Необходимо отметить, что достоверной разницы в значениях данного показателя не выявлялось в течение всего периода наблюдения.
Анализируя динамику двух показателей красной крови, можно заключить, что, несмотря на статистически достоверное снижение содержания эритроцитов в процессе противоопухолевой химиотерапии, уровень гемоглобина менялся незначительно, а это свидетельствует о минимальном воздействии цитостатиков программы CVCV на эритропоэз.
При изучении количества лейкоцитов и лейкоцитарной формулы в периферической крови больных МРЛ было установлено, что проведение химиотерапии как в режиме CVC, так и в режиме CVCV вызывает снижение общего числа лейкоцитов периферической крови за счет содержания сегментоядерных нейтрофилов.
Для того чтобы провести более адекватный анализ влияния СVC и CVCV на лейкопоэз и тромбоци- топоэз, абсолютные цифры показателей тромбоцитов, лейкоцитов и лейкоцитарной формулы были переведены в процентное отношение к исходному уровню. Полученные нами данные (рис. 1) выявили отсутствие статистически значимых различий в количественном содержании тромбоцитов и лейкоцитов в течение всего периода наблюдения при проведении химиотерапии в режимах CVC и CVCV. Что касается показателей лейкоцитарной формулы, то при проведении режима CVCV было зафиксировано статистически значимо большее снижение числа только моноцитов и только в одной точке - после 1-го курса химиотерапии.
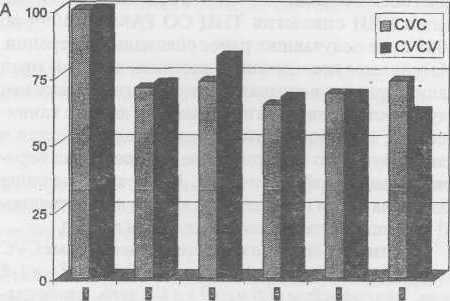
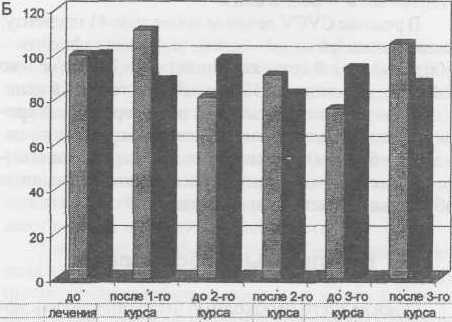
Рис. 1 Изменения общего количества лейкоцитов (А) и тромбоцитов (Б) в периферической крови у больных раком легкого III-IV стадии в динамике проведения противоопухолевой терапии по схемам CVC либо CVCV. По оси абсцисс - сроки исследования, по оси ординат -содержание отдельных морфологических форм (в % от исходного уровня)
* - различия между группами достоверны (р<0,05)
На основании вышеизложенного анализа показателей периферической крови можно сделать вывод, что добавление к режиму С VC четвертого цитостатика - Вепезида - не приводит к значимому усилению токсического действия химиотерапии на эрит-ро-, лейко- и тромбоцитопоэз.
Таким образом, проведенные исследования, свидетельствующие о большей эффективности режима CVCУ(СУС+вепезид) при практически равной его токсичности с режимом CVC, позволяют считать протокол CVCV более предпочтительным для лечения больных мелкоклеточным раком легкого в качестве химиотерапии 1-й линии.


