Сравнительная характеристика методов извлечения золота (цианид, тиосульфат, тиомочевина, хлорид)
Автор: Холов Х.И.
Журнал: Журнал Сибирского федерального университета. Серия: Техника и технологии @technologies-sfu
Рубрика: Исследования. Проектирование. Опыт эксплуатации
Статья в выпуске: 2 т.19, 2026 года.
Бесплатный доступ
В статье выполнен сравнительный анализ гидрометаллургических методов извлечения золота – цианидного, тиосульфатного, тиомочевинного и хлоридного – по критериям эффективности, токсичности, стоимости и утилизации отходов. Рассмотрены технологические ограничения, связанные с минералогией руд (упорность, углистое вещество, сульфидная матрица), и показано, что выбор растворителя должен определяться не только предельной степенью извлечения, но и скоростью процесса, чувствительностью к примесям и необходимостью предварительного вскрытия минералов. Систематизированы данные о диапазонах извлечения: для легкообогатимых руд типичны 90–95 % при цианировании; тиосульфатные и тиомочевинные схемы обеспечивают сравнимые показатели на углистых и сурьмяных рудах; хлоридные системы достигают высоких значений при строгом контроле окислительно-кислотных условий. Отмечено, что наименьшие прямые реагентные затраты характерны для цианида за счёт малого расхода и отработанности оборудования, тогда как тиосульфат требует заметно большей дозировки и специфической регенерации, а тиомочевина и хлорсодержащие реагенты удорожают очистку сточных вод и материалов. Рассмотрены блоки обезвреживания: INCO‑процесс для цианида, осаждение и биодеструкция для аммиачно-тиосульфатных растворов, окислительная деструкция и нейтрализация для тиокарбамида, а также газо- и водоочистка с солевым балансом для хлоридных схем. Показано, что комбинированные маршруты (гравитация/флотация + выщелачивание) позволяют адаптировать технологию к конкретной руде, минимизируя экологический риск и себестоимость при заданной металлургической извлекаемости. Сформулированы практические ориентиры по выбору растворителя: цианид – для «простых» руд при наличии строгой экологической дисциплины; тиосульфат – для углистых и «preg-robbing » систем; тиомочевина – для сурьмянистых и высокореакционных концентратов; хлоридные системы – как нишевый вариант при наличии герметичных коррозионностойких аппаратов и замкнутых водных контуров.
Золото, цианидное выщелачивание, тиосульфатное выщелачивание, тиомочевина, хлоридное выщелачивание, упорные руды, эффективность, токсичность, утилизация отходов, экологические риски, стоимость процесса, комбинированные схемы, регенерация реагента, очистка сточных вод
Короткий адрес: https://sciup.org/146283264
IDR: 146283264 | УДК: 669.21:669.053.4
Comparative Characteristics of Gold Extraction Methods (Cyanide, Thiosulfate, Thiourea, Chloride)
This paper presents a comparative assessment of four hydrometallurgical routes for gold recovery–cyanide, thiosulfate, thiourea, and chloride–benchmarked by extraction efficiency, toxicity, costs, and waste management requirements. Mineralogical constraints (refractoriness, carbonaceous matter, sulfide locking) are highlighted to show that solvent selection must consider not only final extraction levels but also dissolution rate, impurity sensitivity, and the need for pre-treatment. Typical performance windows are summarized: 90–95 % for amenable ores under cyanidation; comparable results for thiosulfate and thiourea flowsheets on carbonaceous and stibnite-rich feeds; and high recoveries for chloride systems when redox and acidity are tightly controlled. Direct reagent costs are generally lowest for cyanide because of low dosage and mature equipment, whereas thiosulfate demands higher make-up and specific regeneration; thiourea and chlorine-bearing reagents increase effluent treatment costs and materials requirements. Detox and cleanup blocks are outlined: SO2 / air (INCO) for cyanide, precipitation and biodestruction for ammoniacal thiosulfate, oxidative destruction and neutralization for thiourea, and gas/liquid treatment with salt balance for chloride circuits. Hybrid routes (gravity/ flotation + leaching) help tailor the process to ore type while controlling environmental risk and unit cost.
Текст научной статьи Сравнительная характеристика методов извлечения золота (цианид, тиосульфат, тиомочевина, хлорид)
Цитирование: Холов Х. И. Сравнительная характеристика методов извлечения золота (цианид, тиосульфат, тиомочевина, хлорид) / Х. И. Холов // Журн. Сиб. федер. ун-та. Техника и технологии, 2026, 19(2). С. 182–201. EDN: AREQLN низкой стоимости реагента цианидный метод доминирует в промышленности на протяжении десятилетий [3]. Химическая реакция растворения золота в цианидном растворе в присутствии кислорода до получения дицианоаурата натрия выглядит следующим образом [4, 5]:
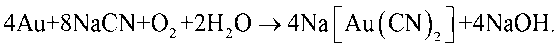
Как отмечают Т. Ю. Никитина и Г. В. Петров [6], в настоящее время более 90 % мирового годового производства золота осуществляется с применением цианидного выщелачивания, что фактически делает эту технологию отраслевым стандартом. Вместе с тем, по данным Н. Т. Ша-рифбоева [7], столь широкое распространение цианидного метода сопровождается серьезными экологическими и социальными рисками, что стимулирует поиск альтернативных, менее токсичных реагентов.
Цианид – чрезвычайно токсичный реагент, представляющий смертельную опасность для человека и экосистем [8]. Исторически утечки цианидов на золотоизвлекательных предприятиях приводили к экологическим катастрофам [9]. Классическим примером, подробно описанным в работе Х. И. Холова и соавт. [10], является авария на румынском предприятии «Бая-Маре» (2000 г.), когда разрыв дамбы хвостохранилища вызвал выброс более 100 000 м³ цианидсодержащих сточных вод, приведший к массовой гибели рыбы и длительному загрязнению рек бассейна Дуная. Подобные инциденты обострили внимание общественности к проблемам экологической безопасности горнодобывающей отрасли [11]. В результате в ряде стран мира введены законодательные запреты на использование цианидных технологий добычи золота, а во многих регионах действуют строгие нормативы хранения и нейтрализации цианидсодержащих отходов [12]. Действительно, помимо острого токсического воздействия цианидная технология требует значительных затрат на обезвреживание и надежное хранение отходов [13]: перед складированием хвостов необходима химическая детоксикация цианидных растворов (например, диоксидом серы) для снижения риска утечек.
Как подчеркивают Н. Ю. Самсонов с соавт. [14, 15] и О. Н. Кононова с соавт. [16], цианидный метод также имеет ряд технико-экономических ограничений: он не обеспечивает полного извлечения металла из упорных руд, содержащих углеродистые и сульфидные минералы, из-за эффекта сорбционного поглощения золота ( preg- robbing ) и затруднённого взаимодействия с реагентом. В итоге значительная часть золота остаётся в твёрдых хвостах, что снижает эффективность и усложняет утилизацию отходов.
Следовательно, как справедливо отмечают Б. Х. Тусупова и Ж. Д. Байгурин [17], несмотря на широкое распространение цианидного выщелачивания благодаря его эффективности и экономичности, растущие экологические риски и технологические ограничения делают актуальным поиск альтернативных, менее токсичных методов извлечения золота.
В последние десятилетия ведутся интенсивные исследования, направленные на разработку альтернативных реагентов для извлечения золота, которые были бы менее опасными для окружающей среды, но сохраняли бы высокую селективность и степень извлечения металла [18]. Среди традиционных нецианидных выщелачивателей наибольшее внимание привлекли тиосульфатные [19], тиомочевинные [20] и хлоридные методы выщелачивания золота [21]. Каждая из этих технологий обладает своими преимуществами и недостатками с точки зрения эффективности, безопасности и экономических издержек по сравнению с цианидным процессом.
В данной статье рассмотрены методы гидрометаллургического извлечения золота из руд: классическое цианидное выщелачивание, а также альтернативные безцианидные методы – на основе тиосульфата, тиомочевины (тиокарбамида), ацетилтиомочевины и хлоридного (галоидного) выщелачивания. Сравнение проведено по основным ключевым аспектам: токсичность применяемых реагентов, эффективность извлечения золота, стоимость и ресурсозатраты процесса, экологические риски, а также сложность утилизации отходов. В табл. 1 приведено обобщённое сравнение и последующий анализ по каждому из указанных аспектов.
Методы исследования
Исследование носит обзорный характер и основано на систематизации опубликованных данных по современным гидрометаллургическим методам извлечения золота. Использованы сравнительно-аналитические подходы с привлечением результатов лабораторных и промышленных испытаний, отражённых в научных статьях, отчетах, патентах и книгах. Проведён критический анализ эффективности, стоимости, токсичности и экологической безопасности процессов цианидного, тиосульфатного, тиомочевинного и хлоридного выщелачивания. При подготовке обзора применены методы контент-анализа, обобщения и сопоставления технологических параметров. Полученные выводы имеют обобщающий характер и служат основой для выбора рациональной схемы выщелачивания золота из руд различного минералогического типа.
Таблица 1. Сравнение основных характеристик методов извлечения золота
Table 1. Comparison of the main characteristics of gold extraction methods
|
Аспект |
Цианидное выщелачивание |
Тиосульфатное выщелачивание |
Тиомочевина (тиокарбамид) |
Хлоридное выщелачивание |
|
Токсичность |
Очень высокая, смертельно ядовит NaCN; требует строгой безопасности |
Низкая, реагенты нетоксичны, экологичны [6] |
Умеренная, возможна канцерогенность; требует защиты |
Высокая, хлор и HCl опасны, нужны герметичные реакторы [22] |
|
Эффективность извлечения |
90–95 % (легкие руды), ниже для упорных [24] |
85–90 %, эффективен при углистых рудах [23] |
>90 %, быстрое растворение, устойчив к As, Sb [7] |
До 95 %, но требует сильного окислителя и контроля среды |
|
Стоимость процесса |
Низкая, реагенты дешёвые, технология отработана |
Средняя, большой расход реагента, сложная схема (Cu, NH 3 ) [23] |
Относительно высокая, расход 5–10 кг/т, кислая среда [24] |
Средне-высокая, недорогие реагенты, но дорогое оборудование |
|
Экологические риски |
Очень высокие, частые аварии и токсичные стоки [24] |
Низкие, но нужно очищать от Cu²⁺ и NH 3 [24] |
Средние, требует нейтрализации и утилизации [10] |
Высокие, опасность выброса хлора и кислотных стоков [22] |
|
Утилизация отходов |
Детоксикация (SO2/ воздух, H 2 O 2 ), контроль CN⁻ < 10 мг/л |
Простая нейтрализация и окисление до сульфатов [10] |
Специальная щёлочная и окислительная обработка [23] |
Нейтрализация кислот, осаждение гидроксидов, солевые стоки |
Токсичность и экологическая опасность
Цианидный метод отличается крайне высокой токсичностью основного реагента и продуктов [25]. Цианид натрия (NaCN) – сильнодействующий яд, смертельный для человека в дозах порядка нескольких миллиграммов на килограмм массы [6, 10]. При проведении процессов цианидного выщелачивания золота необходимо поддерживать щелочную среду (pH > 10,5), что достигается добавлением извести Ca(OH) 2 . Это предотвращает протекание реакции разложения цианида с образованием летучего и высокотоксичного синильного газа HCN [26]:
NaCN+H2O ^ HCN T +NaOH.
Исследования К. К. Размахнина и П. А. Василюка [27] подтверждают, что нарушение данного режима способно привести к выделению HCN и острому отравлению рабочих или загрязнению атмосферы. При этом, как отмечает Н. В. Воробьёв-Десятовский [28], даже незначительные утечки цианистых соединений представляют угрозу живым организмам, а их высокая реакционная активность требует особых мер безопасности на всех стадиях технологического процесса.
При pH ниже 10,5, как подчёркивают М. Н. Макарова и др. [26], а также авторы [27], равновесие смещается в сторону образования летучего и крайне токсичного HCN; тогда как при поддержании щелочной среды (pH > 10,5) ион цианида (CN⁻) остаётся в устойчивой форме. Тем не менее любые утечки цианида немедленно создают угрозу живым организмам: цианид быстро блокирует дыхательные ферменты и вызывает гибель людей и животных. По сведениям Н. Т. Шарифбоева [7], к крупным авариям, связанным с цианидами, относится разлив на румынском руднике Бая-Маре (2000 г.), когда в реки попало порядка 100 т цианидсодержащих стоков, что уничтожило биоту на десятки километров. Высокая токсичность вызвала общественный резонанс и регуляторные меры: как отмечают С. С. Тимофеева с соавт. [29] и А. Е. Воробьёв с соавт. [30], а также авторы [31], в ряде стран Европы и США введены запреты на применение цианидных технологий, тогда как в мировой практике их используют лишь при строгом соблюдении требований промышленной безопасности (включая положения Международного кодекса по цианиду). Существенные экологические риски обусловлены не только прямой токсичностью CN⁻, но и долговременным воздействием производных: по данным М. К. Хочиена [32], цианаты и тиоцианаты могут сохраняться в окружающей среде годами. Дополнительно, как показывают Л. В. Бикетова с соавт. [33], присутствие CN⁻ способствует мобилизации тяжёлых металлов из минеральной матрицы, усиливая их миграцию и распространение в экосистемах. В совокупности это делает цианидный метод наиболее экологически опасным среди альтернативных технологий.
Альтернативные безцианидные подходы существенно выигрывают по показателям экологической безопасности, хотя и не лишены рисков. Так, по данным А. Е. Воробьёва и соавт. [33] и Х. И. Холова с соавт. [24], тиосульфатное выщелачивание считается более «мягким»: сам тиосульфат-ион нетоксичен для человека и большинства организмов, а рабочие растворы аммиачного тиосульфата не содержат летучих ядов. Исследования CSIRO показывают [34], что применение тиосульфата заметно снижает экологические риски по сравнению с цианидом [35]. Основные опасности тиосульфатного метода связаны с присутствием в рабочем растворе аммиака и меди: аммиак токсичен для рыб и способствует эвтрофикации водоёмов, а ионы Cu2+ – 186 – тоже ядовиты для водной среды. Поэтому сточные воды после тиосульфатного выщелачивания требуют обработки (удаления Cu, нейтрализации аммония) перед сбросом. Общий экологический риск тиосульфата ощутимо ниже, чем у цианида, а по оценке специалистов – “низкий” при должной эксплуатации [10, 24].
Тиомочевинный метод с точки зрения острой токсичности выгоднее цианида [36]: тиомочевина, или тиокарбамид, не вызывает мгновенной гибели при малых дозах (летальная доза порядка 8–14 г/кг для животных), то есть в тысячи раз менее токсична, чем цианиды. Однако у этого реагента имеются отсроченные вредные эффекты [37]. Тиомочевина признана подозреваемым канцерогеном (группа 2B IARC) – опыты показали развитие опухолей щитовидной железы у крыс при длительном воздействии вещества. У человека явной канцерогенности не выявлено, но обращаться с тиомочевиной следует как с потенциальным канцерогеном (в производстве она отнесена к токсичным веществам, требующим ограниченного контакта) [38, 39]. В рабочих зонах нужно предотвращать вдыхание аэрозоля тиомочевины и прямой контакт с кожей, применять средства защиты (респираторы, перчатки и т.д.). С точки зрения окружающей среды тиомочевина менее губительна при разовом выпуске, чем цианид (не убивает мгновенно всё живое), но может накапливаться и вредить экосистемам и людям при хроническом присутствии. В частности, слив даже разбавленных растворов тиомочевины строго запрещён – они подлежат сбору и специальной утилизации как опасные отходы [39]. Попадание тиомочевины в водоёмы может нарушать размножение и рост организмов, а продукты её разложения (тиолы, сероводород, аммиак) также нежелательны [40]. Данный метод требует тщательной изоляции и очистки отходов, хотя непосредственная угроза жизни при авариях ниже, чем у цианида.
Хлоридное (хлорное) выщелачивание по характеру опасностей стоит особняком, так как использует крайне агрессивные реагенты [41]. Основной реагент – газообразный хлор (Cl2) или его производные (гипохлорит NaOCl + кислота) – представляет высокую опасность для здоровья: хлор токсичен при вдыхании (вызывает отёк лёгких), а контакты с концентрированной соляной кислотой вызывают ожоги. В промышленной практике зафиксированы многочисленные случаи отравлений и взрывов, связанных с применением хлорсодержащих технологий, поэтому прямое хлорирование руд в настоящее время практически не используется [42, 43]. Вместо него исследуются более мягкие и контролируемые методы окисления, основанные на применении гипохлоритов, пероксидов и других безопасных источников активного хлора. Однако и при таких подходах экологический риск остаётся значительным: утечки хлорсодержащих газов способны вызвать гибель водных организмов и поражение дыхательных путей у человека, а попадание кислых растворов в окружающую среду приводит к кислотному загрязнению почв и водных экосистем.
Согласно Д. В. Гордееву с соавт. [44], исследуются более контролируемые варианты на базе гипохлоритов и пероксидов; однако, как подчёркивают А. Г. Секисов и соавт. [45] и М. И. Фаз-луллин и соавт. [46], даже при таких подходах ключевой стратегией остаётся предотвращение выбросов: герметичные, коррозионно-стойкие реакторы, эффективная газо- и водоочистка и полная нейтрализация стоков. При соблюдении этих требований воздействие на окружающую среду может быть контролируемым, но суммарный риск по-прежнему сопоставим с цианидным, хотя и имеет иную природу (ожогово-токсическое действие хлора вместо ферментной блокировки при CN⁻).
Эффективность извлечения золота
Все рассмотренные методы способны обеспечить высокую степень извлечения – порядка 85–95 % золота при оптимальных условиях; их показатели представлены на рис. 1. Цианидный метод остается популярным благодаря очень высокой эффективности: ещё в 1890-е годы разработчики добивались извлечения до 96 % золота из руды с помощью цианистого раствора [47, 48].
В современных условиях, по данным А. А. Самсалиева и С. С. Ларина [49], для легкообога-тимых руд типично достигается около 90 % при цианидном выщелачивании. Даже на упорных (сульфидных, углистых) рудах комбинированные схемы с включением стадий цианирования дают > 90 %: так, для месторождения Пакрут суммарное извлечение составило 92,2 % при добавлении флотации и довыщелачивания хвостов (Х. И. Холов и соавт. [50]). По результатам А. Г. Михайлова и соавт. [51], тиомочевина как растворитель золота не уступает цианиду по максимально достижимому извлечению: в лабораторных испытаниях получали > 90 % за 6–8 ч выщелачивания концентратов. В промышленной практике тиокарбамид применялся для руд, трудных для цианида (например, с высокой примесью сурьмы), и показал высокие выходы золота [52]. Тиосульфатный метод также способен вынимать золото не хуже цианида: так, в одном из испытаний на упорном сырье получили 87,8 % извлечения на тиосульфате против 87,3 % на цианиде [53, 54]. Компания Barrick сообщала, что на руднике Goldstrike переход на тиосульфат позволил извлекать золото из углистых руд, которые не поддавались цианиду, причём итоговые выходы сравнимы с цианидными [10, 55]. Хлорное выщелачивание в теории может дать даже более высокий процент, близкий к 100 %, так как хлор окисляет и растворяет золото полностью. В XIX веке хлорный метод конкурировал с цианидом [41, 44]. Современные исследования показывают, что при сочетании окислительного автоклавирования и хлоридно-го выщелачивания можно извлечь >95 % золота из упорного концентрата [56]. Например, при выщелачивании концентрата в 6 часов с 20 % HCl и большим расходом хлора достигнуто 97 % извлечения. Однако средние показатели хлорных методов на реальных рудах часто ниже из-за побочных реакций: часть реагента тратится на растворение других минералов. Без автоклавной подготовки и высокой дозы окислителя золото может извлекаться неполно (есть данные о 58 % за 46 часов на гипохлорите без оптимизации). Потенциал метода остаётся высоким.
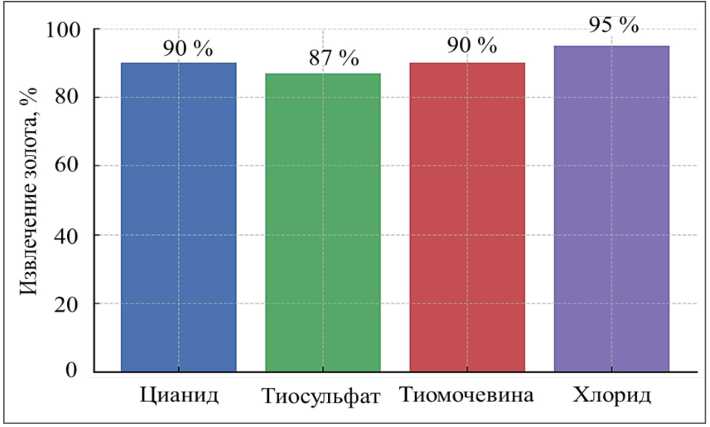
Рис. 1. Сравнение доли извлечённого золота при различных методах выщелачивания
Fig. 1. Comparison of the proportion of gold recovered using different leaching methods
Следует подчеркнуть, что, как показано у К. Янг [57] и Дж. Б. Мошер и соавт. [58], эффективность любого метода критично зависит от минералогии руды. Цианид хуже всего справляется с так называемыми упорными рудами, где золото мелко связано в сульфидах (пирит, арсенопирит) или в углистом веществе: такие руды требуют либо окислительного обжига или автоклава, либо альтернативных растворителей. Тиосульфат как раз эффективен для углистых руд – в них цианид “воруется” органическим углеродом ( preg- robbing эффект), а тиосульфат нет [59]. В то же время тиосульфатная выщелачивающая система более чувствительна к присутствию растворённых ионов: повышенные концентрации некоторых металлов (например, Cu2+, Zn2+) катализируют разложение тиосульфата и могут снижать степень извлечения [19]. Тиомочевина лучше выносит наличие примесей As, Sb, Cu – они меньше мешают ей комплек-сировать золото. К тому же тиомочевина особенно быстра: она растворяет даже крупное золото намного скорее цианида, который славится медлительностью (стандартное цианирование длится 24 часа) [60]. В реальных схемах часто используют комбинации: гравитация + флотация с последующим цианированием либо цианирование с последующим выщелачиванием хвостов альтернативным реагентом (Ю. А. Мамаев и соавт. [61]; П. К. Федотов и соавт. [62]). В целом, по обзорам Х. И. Холова и соавт. [63] и В. А. Бочарова и соавт. [64], при оптимизации режимов любой из методов способен обеспечить 85–95 % извлечения; различия же проявляются преимущественно в скорости растворения, устойчивости к примесям и объёме требуемой предварительной подготовки руды.
Стоимость процесса и утилизация отходов
Затраты на применение того или иного метода зависят от стоимости реагентов, их необходимого количества, а также сложности технологической схемы [65, 66]. Цианидный метод традиционно считается наиболее экономичным для крупных производств. Главные причины – высокая эффективность (меньше потерь золота) и сравнительно невысокая цена самого реагента. По оценкам Н. А. Казаковой и соавт. [67] и С. С. Тимофеевой и соавт. [68], промышленный NaCN стоит порядка 2000–3000 $/т, при этом типичный расход составляет 0,5–2 кг/т руды, что даёт всего «несколько долларов» реагентных затрат на тонну сырья. Технология цианирования хорошо отработана: применяются доступные материалы (например, сталь с резиновой футеровкой для чанов), а вспомогательные реагенты – известь, цементирующий цинк, активированный уголь – широко доступны по цене. Хотя капитальные вложения в золотоизвлекательные фабрики значительны, их величина, как отмечают А. О. Василькова и соавт. [69], слабо зависит от выбора растворителя; напротив, альтернативные схемы нередко требуют более сложного и дорогого оборудования. В итоге себестоимость извлечения при цианировании остаётся минимальной – пока не действуют дополнительные экологические сборы и ограничения.
Для сравнения, альтернативные методы могут потребовать большего количества реагентов или более дорогих компонентов. На рис. 2 приведён ориентировочный сравнительный расход основного реагента на 1 тонну руды для рассматриваемых методов.
Цианид потребляется в малом количестве (обычно 1 кг/т), тогда как тиосульфатные растворы требуют значительно больших доз – порядка десятков кг/т [18]. Тиомочевинное и хлоридное выщелачивание занимают промежуточное положение по расходу реагентов – их потребность обычно составляет лишь несколько килограммов на тонну руды [70, 71]. Повышенный рас- – 189 –
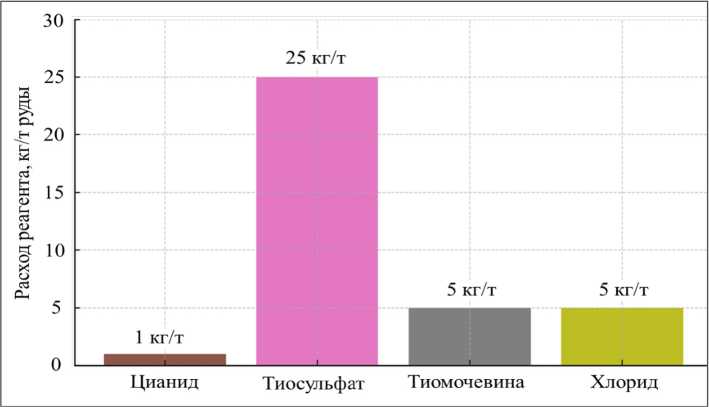
Рис. 2. Оценочный удельный расход ключевого реагента для разных методов
Fig. 2. Estimated specific consumption of the key reagent for different methods ход тиосульфата связан с его частичным разложением в процессе выщелачивания – например, в опытах отмечают 25 кг/т руды расхода тиосульфата аммония [24,72], что увеличивает расходы на реагенты. В промышленной установке Barrick Goldstrike для удешевления процесса пришлось построить установку регенерации тиосульфата и его повторного использования [73, 74], иначе эксплуатационные затраты были бы слишком высоки. Тиомочевина является сравнительно недорогим реагентом (ориентировочная стоимость составляет около $ 1000 за тонну, хотя в некоторых источниках упоминается цена порядка $ 100 за тонну сырья [75]). Однако её удельный расход достаточно велик – обычно 5–10 кг на тонну руды, при этом дополнительно требуется около 5–10 кг серной кислоты (H₂SO₄) и не менее 1 кг ионов Fe3+, вводимых в виде Fe2(SO4)3, для окислительного растворения золота [76]. В результате суммарные реагентные затраты у тиомочевинного метода выше, чем у цианида, хотя и не астрономические. Хлорный метод по реагентам может быть сравнительно экономичен: технический хлор дешев, а при правильной технике его нужно 5 кг/т руды для полного извлечения золота (с учётом частичной регенерации хлора) [77]. Однако следует учитывать, что главная статья затрат при хлорировании – это материалы оборудования и безопасность. Необходимы кислотоупорные реакторы (дороже обычных), системы нейтрализации газов, дорогие сплавы или покрытия, что удорожает процесс. Кроме того, хлорный метод чаще реализуется при повышенных температурах и давлениях (например, совмещение с автоклавным окислением) [78], что требует дополнительной энергии.
С точки зрения утилизации отходов, по практическим оценкам Х. И. Холова и соавт. [10] и технологических регламентов, наименее затратной остаётся цианидная схема – вопреки токсичности CN⁻. Технологии детоксикации хорошо отработаны и опираются на недорогие реагенты: процесс SO₂/воздух (INCO) эффективно переводит цианид в менее опасные формы (тиоцианат, цианат) с использованием метабисульфита (источник SO₂) и медного катализатора [7]. Также применяются пероксид, гипохлорит и др.; подобные операции закладываются проектом фабрики. К 2008 г. в ЕС действовал норматив WAD-CN < 10 мг/л (10 ppm) в хвостохра-– 190 – нилище [10], которого достигают комбинацией поддержания pH, дозирования разрушителей и рециклинга воды. Благодаря дешёвым реагентам и тиражируемым схемам эксплуатационные расходы на детоксикацию обычно составляют «сенты» на тонну руды.
Для тиосульфатных хвостов требуется своя система очистки, но она также не слишком сложна. Основная задача – удалить из раствора ионы тяжелых металлов (медь, возможно, мышьяк, свинец, которые могли перейти в раствор) и нейтрализовать аммиак [19]. Это достигается осаждением гидроксидов при повышении pH и последующей фильтрацией осадка. Сам тиосульфат при длительном контакте с воздухом окисляется до сульфата, который уже не представляет опасности. Иногда применяют метод биологической очистки: бактерии де-нитрификаторы могут усваивать азот аммония, а сульфат-восстанавливающие – остатки серы [79]. Расходы на утилизацию тиосульфатных растворов оцениваются как умеренные и сопоставимы с обычной очисткой шахтных сточных вод [80]. Отсутствие дорогостоящих ядохимикатов упрощает обращение с отходами: например, нет строгих требований по хранению хвостов под слоем воды, как для цианида.
Тиомочевинные отходы – напротив, требуют повышенного внимания и затрат на обезвреживание [81]. Несмотря на отсутствие мгновенной токсичности, классификационно их относят к опасным отходам. Как указывалось, запрещено сбрасывать их без обработки. Утилизация включает несколько стадий: сначала деструкция тиомочевины в отходах – обычно окислителями (озон, гипохлорит, перманганат) в щелочной среде, что переводит тиокарбамид в менее токсичные вещества (например, в мочевину и сульфат). Параллельно или после проводят осаждение растворённых металлов (в том числе ценного золота, которое могло остаться в растворе). Осадок фильтруют, а очищенный раствор нейтрализуют [82]. Все эти операции – стандартные химводоочистные, но их себестоимость выше, чем у цианидной схемы, ввиду необходимости реагентов на окисление органики. Кроме того, приходится утилизировать больший объём твёрдых отходов (осадок серы, гипса, гидроксидов металлов) – их захоронение также требует расходов. Утилизация отходов тиомочевины добавляет заметную долю к расходам процесса, делая его экономически оправданным лишь при высоком содержании золота или в условиях, где цианид недопустим [83].
Для хлоридного метода наибольшие сложности – коррозия и минеральный состав стоков [41]. Сами реагенты (хлор, кислоты) в отходах не сохраняются при правильном ведении процесса – хлор полностью реагирует, а кислота нейтрализуется. Однако остаются очень солёные растворы (NaCl, CaCl 2 ) с растворёнными металлами [42]. Их нельзя просто сбросить в воду – высокая минерализация погубит экосистему. Обычно практикуют следующую схему: кислый раствор после выщелачивания отправляют в нейтрализацию известью, при этом металлы (Fe, Cu, Pb и др.) выпадают в осадок гидроксидов. Осадок отделяют и отправляют на хранение (как токсичный шлам). Остаётся солевой раствор, который либо повторно используют в технологическом процессе (идеально – замкнутый цикл хлоридов), либо подвергают дополнительной очистке. Возможна выпарка и кристаллизация соли с последующим складированием – это дорого, но уменьшает объём жидких отходов. Некоторые схемы предлагают переводить часть хлора в гипохлорит и возвращать в процесс. В любом случае система очистки при хлорном выщелачивании – это существенный дополнительный блок оборудования (нейтрализационные реакторы, фильтры, газоочистка), который увеличивает капитальные и операционные затраты – 191 –
-
[43]. Без него эксплуатация метода невозможна по экологическим соображениям. По совокупности затрат на реагенты и утилизацию отходов хлоридный и тиомочевинный методы обычно уступают цианидному – это подтверждается тем фактом, что они внедряются лишь там, где использование цианида невозможно либо законодательными ограничениями, либо по технологическим причинам (неэффективность на данном сырье).
Заключение
Сопоставление четырёх гидрометаллургических подходов показывает, что универсального растворителя не существует: оптимальная технология определяется минералогией, требованиями к экологии и совокупной стоимостью владения процессом. При «простых» рудах экономически целесообразно цианирование при строгом контроле pH и последующей детоксикации WAD-CN (INCO, H 2 O 2 ). Для углистых и preg-robbing систем рационален аммиачно-тиосульфатный режим с обязательной регенерацией тиосульфата и удалением NH4+ и Cu2+ из стоков. Для сурьмянистых и высокореакционных концентратов целесообразны тиомочевин-ные схемы с окислительной деструкцией органики. Хлоридные схемы остаются нишевыми: они требуют герметичных коррозионностойких аппаратов, газо- и водоочистки и замкнутого солевого контура. Во всех случаях повышается результативность комбинированных маршрутов (гравитация/флотация + выщелачивание), а также предварительного вскрытия сульфидной матрицы обжигом, био- или автоклавным окислением. Практическая рекомендация: начинать с минералого-технологического профилирования руды, сопоставлять чувствительность процесса к примесям (уход реагента, каталитическое разложение), затем выбирать растворитель с минимальным риском при требуемом извлечении и очистке стоков. Такой последовательный выбор снижает неопределённость проектных решений, уменьшает экологические риски и обеспечивает устойчивую металлургическую эффективность.


