Сравнительная эффективность аутовенозного трансплантата с разрушенными клапанами и биологического протеза в бедренно-подколенной позиции при лечении критической ишемии нижних конечностей
Автор: Суковатых Б.С., Сидоров Д.В., Беликов Л.Н., Боломатов Н.В.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.11, 2016 года.
Бесплатный доступ
Представлен анализ комплексного обследования и хирургического лечения 60 пациентов с критической ишемией нижних конечностей на почве атеросклеротического поражения бедренно-подколенно-берцового сегмента. Мужчин было 51, женщин - 9, возраст пациентов варьировал от 51 до 77 лет. Пациенты по технологии бедренно-подколенного шунтирования были разделены на 2 статистически однородные группы по 30 человек в каждой. Пациентам первой группы операция проводилась по оригинальной технологии - свободным аутовенозным трансплантатом с разрушенными клапанами, а во второй группе в качестве шунта использовался биологический протез из внутренней грудной артерии быка.
Бедренно-подколенное шунтирование, свободный аутовенозный трансплантат, биологический протез
Короткий адрес: https://sciup.org/140188583
IDR: 140188583 | УДК: 617.58-005.4-089.819.843:616.137.83/.86
Comparative effectiveness of autovenous trans-plantat with destructed valves and biological prostheses in femoral-popliteal positions in the critical ischemia of lower extremities treatment
60 patients (male - 51, female - 9; aged from 51 to 77 years) with critical lower limb ischemia were examined and surgically treated. The cohort was divided into two groups : the patients of the 1st group were operated by the original technology - free autovenous graft with valves destroyed, the patients of the 2nd group were operated with biological graft prosthesis of the internal thoracic artery bull.
Текст научной статьи Сравнительная эффективность аутовенозного трансплантата с разрушенными клапанами и биологического протеза в бедренно-подколенной позиции при лечении критической ишемии нижних конечностей
Одной из основных причин развития критической ишемии является атеросклеротическое поражение артерий инфраингвинальной зоны [4, 7]. Известно, что вид пластического материала (аутовена, биологический или синтетический протез) не влияет на результаты проксимального бедренно-подколенного шунтирования. Через 4–5 лет функционирует от 36% до 78% шунтов, избежать ампутации конечности удается в 70–91% случаев [8, 10]. Результаты дистального бедренно-подколенного шунтирования ниже щели коленного сустава оставляют желать лучшего. Через 5 лет проходимость аутовенозного трансплантата колеблется от 15% до 43%, конечность удается сохранить не более чем у 50% больных [6, 9].
В настоящее время существует 2 способа выполнения аутовенозного дистального бедренно-подколенного шунтирования: путем применения в качестве шунта реверсированной большой подкожной вены или по методике «in situ». Как первая, так и вторая методика имеют существенные недостатки.
В результате ряда причин (малый диаметр большой подкожной вены на бедре менее 3,5 мм, варикозной ее трансформации, ранее выполненной венэктомии) произвести аутовенозное бедрено-подколенное шунтирование не представляется возможным. В этих случаях в качестве шунта применяются синтетические или биологические протезы. Синтетический политетрафторэтиленовый протез в бедренно-подколенной позиции ниже щели коленного сустава функционирует в среднем не более года [11]. Для удлинения сроков функционирования синтетического имплантата применяется комбинированный протез, состоящий на проксимальном конце из синтетического протеза, а на дистальном из аутовены [3]. Эффективность применения в качестве шунта биологического протеза в бедренно-подколенной позиции ниже щели коленного сустава изучена недостаточно [1].
Цель исследования: улучшить результаты лечения пациентов с критической ишемией нижних конечностей на фоне облитерирующего атеросклероза сосудов ин-фраингвинальной зоны путем оптимизации методики аутовенозного бедренно-подколенного шунтирования.
Материалы и методы
Проведен анализ комплексного обследования и хирургического лечения 60 пациентов с критической ишемией нижних конечностей на почве атеросклеротического поражения бедренно-подколенно-берцового сегмента. Мужчин было 51, женщин – 9, возраст пациентов варьировал от 51 до 77 лет. Пациенты по технологии бедренно-подколенного шунтирования были разделены на 2 статистически однородные группы по 30 человек в

каждой. Группы были сопоставимы по полу, возрасту, сопутствующим заболеваниям, степени поражения бедренно-подколенно-берцового сегмента, состоянию дистального сосудистого русла (р > 0,05). В 1 группе применяли оригинальную технологию (патент РФ на изобретение №2556605 от 16.06.2015) – рис. 1. Производили оперативное обнажение бифуркации бедренной артерии в паховой области и дистального отдела подколенной артерии в верхней трети голени традиционным образом. Через отдельные кожные разрезы (2–4) по медиальной поверхности бедра выделяли большую подкожную вену, впадающие притоки перевязывали и пересекали.
Большую подкожную вену отсекали по ее устью, дефект в бедренной вене ушивали монофиламентной нитью 6/0. Пересекали вену чуть ниже коленного сустава, дистальный конец лигировали. Большая подкожная вены иссекалась на всем протяжении бедра и верхней трети голени. Под визуальным контролем, выворачивая вену, острым путем при помощи микрохирургических ножниц иссекали устьевой и приустьевой клапаны в подкожной вене. Для разрушения клапанного аппарата вены применяли инструмент для разрушения клапанов свободного аутовенозного трансплантата (заявка на патент № 2015129895 от 2.07.2015). Инструмент состоит из насадки для шприца, полого проводника с каналом для подачи промывной жидкости и рабочей части, по форме соответствующей венозному синусу (рис. 2).
Разрушение клапанов осуществлялось следующим образом: в проксимальный отдел трансплантата вводили инструмент, диаметром, соответствующим калибру вены. Его продвигали в дистальном направлении, предварительно нагнетая физиологический раствор в просвет трансплантата. Под визуальным контролем определяли створки клапана. Рабочей частью инструмента, имеющей форму венозного синуса, под контролем зрения, разрушали сначала створку аутовенозного клапана с одной стороны, а затем с противоположной стороны (рис. 3).
Вначале в проксимальный конец трансплантата вводили инструмент диаметром 6 мм, с помощью которого разрушали клапаны до его средней трети. Для разрушения клапанов в средней трети трансплантата применяли инструмент диаметром 5 мм, а в дистальной трети – 4 мм. Инструментом последовательно разрушали клапаны аутовенозного трансплантата, проводя их по вене в ретроградном направлении. Затем к инструменту подсоединяли шприц, объемом 100 мл. Трансплантат промывали физиологическим раствором и убеждались в полном разрушении клапанов по хорошему напору промывной жидкости, выходившей из шунта. Дебет промывной жидкости при полном разрушении клапанов должен быть не менее 100 мл за 12 с, что в перерасчете за 1 мин. соответствует оптимальной пропускной способности шунта 500 мл/мин. При сохранении проходимости поверхностной бедренной артерии в верхней трети, проксимальный анастомоз между проксимальным концом аутовенозного трансплантата формировали по типу конец в бок бедрен-
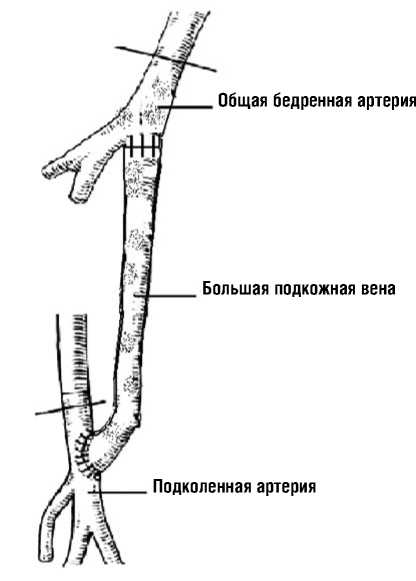
Рис. 1. Бедренно-подколенное шунтирование свободным аутовенозным траснплантатом

Рис. 2. Инструмент для разрушения клапанов аутовенозного трастантата ной артерии. В случае полной окклюзии поверхностной бедренной артерии, ее отсекали от общей бедренной артерии, дистальный конец перевязывали и накладывали анастомоз с общей бедренной артерией конец в конец. Трансплантат проводили по ходу сосудистого-нервного пучка до подколенной ямки и формировали дистальный анастомоз между дистальным концом трансплантата и конечным отделом подколенной артерий конец в бок. Во 2 группе выполняли дистальное бедренно-подколенное шунтирования с использованием биологического протеза из внутренней артерии быка – «Кемангиопротеза», диаметром 6 мм в проксимальном отделе, 4 мм в дистальном отделе, длинной 50 ± 6 см.
Суковатых Б.С., Сидоров Д.В., Беликов Л.Н., Боломатов Н.В.
СРАВНИТЕЛЬНАЯ ЭФФЕКТИВНОСТЬ АУТОВЕНОЗНОГО ТРАНСПЛАНТАТА С РАЗРУШЕННЫМИ КЛАПАНАМИ И БИОЛОГИЧЕСКОГО ПРОТЕЗА В БЕДРЕННО-ПОДКОЛЕННОЙ ПОЗИЦИИ ПРИ ЛЕЧЕНИИ КРИТИЧЕСКОЙ ИШЕМИИ НИЖНИХ КОНЕЧНОСТЕЙ
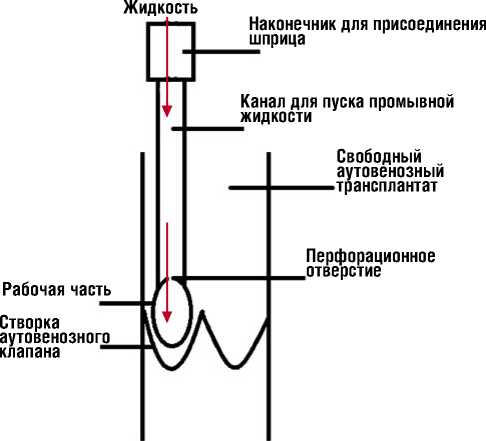
Рис. 3. Методика разрушения клапанов аутовенозного трасплантата
Диагностическая программа была традиционной и включала функциональные (реовазография, фотоплетизмография), ультразвуковые (допплерография, ангиосканирование) и рентгенологические (артериография) методы исследования. Кроме этого в предоперационном, во время операции и в послеоперационном периодах оценивался диаметр большой подкожной вены и объемный кровоток по шунту. Изменение интенсивности артериального кровотока после операции регистрировали по динамике реовазографического индекса (РИ) и лодыжечно-плечевого индекса (ЛПИ); а микроциркуляции – по динамике фотоплетизмографического индекса (ФИ). Состояние путей оттока (дистального русла) и результаты лечения оценивались по шкалам Ruterford et al., которые рекомендованы в качестве стандарта Российским обществом ангиологов и сосудистых хирургов [6]. В соответствии с международными рекомендациями проведена оценка «качества жизни» пациентов до и через 12 месяцев после лечения, на основании анкетного обследования пациентов с помощью опросника MOS SF-36, нормированного для сосудистых больных. Для сравнения использовались показатели «качества жизни» лиц (n = 30) без хронической ишемии нижних конечностей, сопоставимых по полу, возрасту и сопутствующей патологии больным первой, второй и третьей групп. Качество жизни оценивали сами больные по 8 шкалам: физическое функционирование (ФФ), физическая роль (ФР), физическая боль (ФБ), общая оценка здоровья (003), жизненная активность (ЖА), эмоциональная роль (ЭР), социальное функционирование (СФ), психическое здоровье (ПЗ). Шкалы группировали в 2 интегральных показателя: физический компонент здоровья (ФКЗ) и психический компонент здоровья (ПКЗ).
Статистическая обработка материала проводилась с использованием методов однофакторного дисперсного и корреляционного анализа. Вычисляли средние величины количественных показателей, стандартные ошибки и критерий согласия у2 Пирсона. Полученные данные представлены в виде М ± m. Существенность различий средних величин оценивали с помощью t-критерия Стьюдента. Различия считали статистически значимыми при р < 0,05.
Результаты
Состояние путей оттока по артериям голени представлены в таблице 1.
Из таблицы видно, что хорошее состояние дистального артериального русла до операции было у 36 (60%), а удовлетворительное – у 24 (40%). Индекс путей оттока в первой группе составил 5,2 ± 1,1, а во второй группе 5,8 ± 1,4 балла (р > 0,05 между группами).
Показатели объемного кровотока, по данным ре-овазографии, магистрального кровотока, по данным допплерографии, микроциркуляции по данным фотоплетизмографии, в ближайшем послеоперационном периоде представлено в таблице 2.
Из таблицы видно, что применение для лечения критической ишемии нижних конечностей свободного аутовенозного трансплантата с разрушенными клапанами позволяет увеличить объемный кровоток в конечности по данным РИ в 1,5 раза, магистральный кровоток по данным ЛПИ – в 1,6 раза, уровень микроциркуляции по данным ФИ – в 1,3 раза. Статистически достоверных различий между показателями после операции у больных первой и второй групп нет. Объемный кровоток по шунту во время операции по свободному аутовенозному трансплантату с разрушенными клапанами 570 ± 70 мл/мин., а по биологическому протезу 510 ± 40 мл/мин.
Табл. 1. Характеристика состояния дистального русла при выполнении бедренноподколенного шунтирования
|
Характеристика дистального русла |
Оценка дистального русла |
Группа 1 (n = 30) |
Группа 2 (n = 30) |
||
|
Абс |
% |
Абс |
% |
||
|
Подколенная и артерии голени проходимы без стенозирования |
Хорошо |
19 |
63,3 |
17 |
56,7 |
|
Стеноз подколенной артерии не более 50%, проходимы 1–2 артерии голени |
Удовлетворительно |
11 |
36,7 |
13 |
43,3 |
Табл. 2. Динамика показателей артериального кровотока и микроциркуляции после операции
|
Диагностические критерии |
Группа 1 (п = 30) |
Группа 2 (п = 30) |
||
|
До операции |
После операции |
До операции |
После операции |
|
|
РИ |
0,23 ± 0,03 |
0,9 ± 0,3* ** |
0,22 ± 0,06 |
0,81 ± 0,04 * |
|
ЛПИ |
0,3 ± 0,1 |
0,8 ± 0,2* ** |
0,28 ± 0,05 |
0,60 ± 0,06 * |
|
ФИ, % |
25 ± 5% |
80 ± 10%* ** |
23 ± 5% |
65 ± 6% * |
Примечание : * – р < 0,05 по сравнению с показателями до операции, ** – р < 0,05 по сравнению с показателями первой группы после операции.

Частота и виды осложнений в ближайшем послеоперационном периоде (до 1 месяца после операции) представлены в таблице 3.
У 2 (6,6%) пациентов первой группы развилось по одному осложнению. На начальном периоде разработки технологии операции у 1 пациента развился тромбоз шунта вследствие неполного разрушения клапанов аутовенозного трансплантата. Больной был повторно оперирован, произведена тромбэктомия и дополнительное разрушение клапанов в вене. Проходимость шунта восстановлена. Лимфорея из операционной раны на бедре имела место у 1 пациента второй группы и была ликвидирована консервативными мероприятиями.
Во 2 группе у 2 (6,6%) пациентов возник тромбоз шунта. Причиной тромбоза была не удалённая атеросклеротическая бляшка в дистальном отделе анастомоза между протезом и подколенной артерией, которая суживала соустье. Пациенты были повторно оперированы, произведена эндартерэктомия из подколенной артерии, тромбэктомия. Проходимость шунта была восстановлена. У 1 (3,3%) больного после операции развилось кровотечение из места наложения дистального анастомоза в ближайшие часы после операции. Больной был повторно оперирован. Кровотечение остановлено наложением дополнительных швов. Лимфорея из операционной раны на бедре имела место у 1 (3,3%) пациента и была ликвидирована консервативными мероприятиями.
Отдаленные результаты оценивались через 12 и 36 месяцев. К концу 1 года наблюдений проходимость протезов в 1 группе у 30 (100%) пациентов, а во 2 группе – у 19 (63,3%) больных. Через 3 года шунт функционировал в 1 группе у 25 (83,3%) пациентов, а во 2 группе – у 5 (16,7%) больных.
В первой группе поздние тромбозы шунта развились у 5 (16,7%) пациентов. Во всех случаях их причиной было прогрессирование атеросклеротического процесса в артериях голени, у пациентов с удовлетворительным состоянием дистального сосудистого русла. У 3 (10%) ишемия конечности прогрессировала и этим пациентам выполнена высокая ампутация конечности. У 2 (6,7%) пациентов после тромбоза шунта критическая ишемия конечности не рецидивировала. У 25 (83,3%) протезы продолжают функционировать. При контрольных ультразвуковых исследованиях объемный кровоток по ним колебался в пределах 360 ± 50 мл/мин. Следует подчеркнуть, что проксимальный конец шунта у этих пациентов превышал 7 мм в диаметре.
Во второй группе поздние тромбозы шунта развились у 25 (83,3%) пациентов. Причиной их было прогрессирование атеросклеротического процесса в берцовых артериях у 5 (16,7%), варикозная трансформация биологического протеза у 8 (26,7%) и неопластическая гиперплазия в области анастомозов у 12(40%) пациентов. У 11 (36,7%) пациентов ишемия конечности прогрессировала и этим пациентам выполнена высокая ампутация
Табл. 3. Частота послеоперационных осложнений в раннем послеоперационном периоде
Результаты оценки степени изменения клинического статуса пациентов по отношению к периоду до операции представлены в таблице 4.
В 1 группе у 83,3% пациентов достигнуто значительное улучшение клинического статуса, что свидетельствует о лучшей перфузии ишемизированных тканей, чем у пациентов во 2 группе.
Результаты оценки «качества жизни» пациентов представлены в табл. 5.
Из таблицы видно, что критическая ишемия снижает все показатели качества жизни пациентов. При этом интегральный показатель физический компонент здоровья снижается в 2,9 раза, а психический – в 2,2 раза. Применение свободного аутовенозного трансплантата позволяет повысить физический компонент здоровья на 27,6, а психический компонент на 26,68 балла по сравнению с группой больных, которым в качестве шунта применялся биологический протез.
Табл. 4. Динамика клинического статуса пациентов после проведенного лечения
|
Баллы |
Эффективность |
Первая группа (п = 30) |
Вторая группа (п = 30) |
|
+3 |
Значительное улучшение |
25 (83,3%)* |
3 (10%) |
|
+2 |
Умеренное улучшение |
– |
2 (6,7%) |
|
+1 |
Минимальное улучшение |
2 (6,7%)* |
14 (46,7%) |
|
0 |
Без изменений |
– |
– |
|
-1 |
Минимальное ухудшение |
– |
– |
|
-2 |
Умеренное ухудшение |
– |
– |
|
-3 |
Значительное ухудшение |
3 (10%)* |
11 (36,7%)* |
Примечание : * – р < 0,05 в сравнению со второй группой по критерию у 2 Пирсона.

Суковатых Б.С., Сидоров Д.В., Беликов Л.Н., Боломатов Н.В.
СРАВНИТЕЛЬНАЯ ЭФФЕКТИВНОСТЬ АУТОВЕНОЗНОГО ТРАНСПЛАНТАТА С РАЗРУШЕННЫМИ КЛАПАНАМИ И БИОЛОГИЧЕСКОГО ПРОТЕЗА В БЕДРЕННО-ПОДКОЛЕННОЙ ПОЗИЦИИ ПРИ ЛЕЧЕНИИ КРИТИЧЕСКОЙ ИШЕМИИ НИЖНИХ КОНЕЧНОСТЕЙ
Табл. 5. Оценка «качества жизни» пациентов до и через 12 месяцев после лечения
|
Шкала SF-36 |
Здоровая популяция жителей России (п = 30) |
Пациенты до лечения (п = 60) |
Группа 1 (n = 30) |
Группа 2 (n = 30) |
|
ФФ |
90,1 ± 1,7 |
30,1 ± 2,3# |
62,0 ± 3,8* ** |
34,33 ± 6,79* |
|
РФ |
90,2 ± 1,8 |
19,1 ± 2,1# |
57,5 ± 3,2* ** |
10,00 ± 4,92* |
|
ФБ |
86,4 ± 2,1 |
45,5 ± 3,1# |
64,2 ± 3,6* ** |
40,73 ± 5,65* |
|
ООЗ |
79,7 ± 1,9 |
38,4 ± 1,2# |
52,1 ± 2,9* ** |
38,87 ± 3,14* |
|
ЖА |
60,2 ± 2,3 |
15,2 ± 3,2# |
60,1 ± 4,1* |
41,33 ± 4,24* |
|
СФ |
84,2 ± 2,4 |
47,7 ± 2,3# |
72,3 ± 3,5* ** |
62,50 ± 7,72* |
|
ПЗ |
62,4 ± 1,2 |
18,7 ± 3,2# |
61,2 ± 2,3* |
59,20 ± 3,81* |
|
ЭР |
61,2 ± 1,9 |
30,3 ± 4,5# |
60,3 ± 4,5* |
24,44 ± 3,94* |
|
ФКЗ |
86,6 ± 1,9 |
29,5 ± 2,3# |
58,9 ± 3,9* ** |
31,3 ± 2,00* |
|
ПКЗ |
67,0 ± 2,0 |
30,2 ± 1,5# |
63,5 ± 3,6* |
36,82 ± 2,01* |
Примечание : # – р < 0,001 в сравнении с показателями больных до лечения и здоровыми лицами; * – р < 0,05 в сравнении с показателями больных до лечения;** – р < 0,05 в сравнении с показателями больных второй группы.
Обсуждение
При хорошем состоянии дистального сосудистого русла оптимальным способом лечения критической ишемии является использование свободного аутовенозного трансплантата с разрушенными клапанами. Методика позволяет сохранить естественную геометрию потока крови и избежать стеноза кондуита. Применение оригинальной технологии бедрено-подколенного шунтирования позволяет в ближайшем послеоперационном периоде снизить количество ранних послеоперационных осложнений по сравнению с биологическим протезом -на 6,7%, поздних тромбозов шунта на 66,6%; ампутаций конечности на 26,7%.
В случаях рассыпного типа строения венозной системы нижних конечностей, когда диаметр ствола большой подкожной вены на бедре 3,5 мм и менее, возможно применение в качестве шунта биологического протеза из внутренних грудных артерий быка. Биологический протез при бедренно-подколенном шунтировании ниже щели коленного сустава функционирует в среднем 18 ± 6 месяцев, что значительно уступает длительности функционирования аутовенозного кондуита [14]. Отрицательными свойствами протеза являются более быстрое развитие гиперплазии интимы в области анастомозов и аневризматической трансформации шунта.
Выводы
-
1. Применение в качестве шунта свободного аутовенозного трансплантата с разрушенными клапанами при бедренно-подколенных шунтированиях патогенетически обосновано: позволяет избежать стеноза кондуита, сохранить естественную геометрию потока крови, замедлить развитие неоинтимальной гиперплазии в области проксимального анастомоза.
-
2. В случае невозможности использовать аутовену при дистальном бедренно-подколенном шунтировании целесообразно применять биологический протез в качестве трансплантата.
-
1. Барбараш Л.С., Бурков Н.Н., Кудрявцева Ю.А. и др. Сравнительный анализ применения биопротезов артерий с различной антитромботической модификацией // Ангиология и сосудистая хирургия 2012. – Т. 18., №2. – С. 21–25.
-
2. Гавриленко А.В., Котов А.Э., Кочетов С.В., и др. Хирургическое лечение больных с критической ишемией нижних конечностей в зависимости от спектра вегетирующей флоры // Хирургия. – 2012. – №2. – С.19–25.
-
3. Казаков Ю.И., Лукин И.Б., Казаков А.Ю. и др. Выбор метода реконструкции сосудов при критической ишемии нижних конечностей // Ангиология и сосудистая хирургия. – 2015. – Т. 21, №2. – С. 152–158.
-
4. Майстренко Д.Н., Жеребцов Ф.К., Осовских В.В. и др. Современные диагностические технологии в определении тактики лечения больных с облитерирующим атеросклерозом сосудов нижних конечностей // Вестник хирургии. – 2009. – №2. – С. 41–46.
-
5. Российский консенсус «Диагностика и лечение пациентов с критической ишемией нижних конечностей». – М.: Медицина, 2002. – 40 с.
-
6. Сажинов А.П., Лукинский А.В., Чупин А.В. Пути улучшения проходимости бедренно-подколенных-берцовых шунтов // Ангиология и сосудистая хирургия. – 2014. – Т. 20, №1. – С. 141–145.
-
7. Червяков Ю.В., Староверов И.Н., Борисов А.В. и др. Отдаленные результаты до 3 лет использования непрямых способов реваскуляризации у больных с хронической ишемией нижних конечностей // Вестник хирургии. – 2015. – №2. – С. 84–88.
-
8. Bradbury A.W., Adam D.J., Bell J., et al. Bypass versus Angioplasty in Severe Ischaemia of the Leg (BASIL) trial: Analysis of amputation free and overall survival by treatment received // J. Vasc. Surg. – 2010. – Vol. 51 (Suppl. S). – P. 18–31.
-
9. Conte M.S. Bypass versus Angioplasty in Severe Ischaemia of the Leg (BASIL) and the (hoped for) dawn of evidence-based treatment for advanced limb ischemia // J. Vasc. Surg. – 2010. – Vol.51 (Suppl. S). – P. 69–75.
-
10. Pereira C.E., Albers M., Romiti M., et al. Meta-analysis of femoropopliteal byp-as grafts for lower extremity arterial insufficiency // J. Vasc. Surg. – 2006. – Vol. 44, №3. – P. 510–517.
-
11. Rychlik I.J., Davey P., Murphy J., et al. A meta-analysis to compare Dacron versus polytetrafluroethylene grafts for above-knee femoropopliteal artery bypass // J. of Vascular Surg. – 2014. – Vol. 61, №2. – Р. 506–513.
Список литературы Сравнительная эффективность аутовенозного трансплантата с разрушенными клапанами и биологического протеза в бедренно-подколенной позиции при лечении критической ишемии нижних конечностей
- Барбараш Л.С., Бурков Н.Н., Кудрявцева Ю.А. и др. Сравнительный анализ применения биопротезов артерий с различной антитромботической модификацией//Ангиология и сосудистая хирургия 2012. -Т. 18., №2. -С. 21-25.
- Гавриленко А.В., Котов А.Э., Кочетов С.В., и др. Хирургическое лечение больных с критической ишемией нижних конечностей в зависимости от спектра вегетирующей флоры//Хирургия. -2012. -№2. -С.19-25.
- Казаков Ю.И., Лукин И.Б., Казаков А.Ю. и др. Выбор метода реконструкции сосудов при критической ишемии нижних конечностей//Ангиология и сосудистая хирургия. -2015. -Т. 21, №2. -С. 152-158.
- Майстренко Д.Н., Жеребцов Ф.К., Осовских В.В. и др. Современные диагностические технологии в определении тактики лечения больных с облитерирующим атеросклерозом сосудов нижних конечностей//Вестник хирургии. -2009. -№2. -С. 41-46.
- Российский консенсус «Диагностика и лечение пациентов с критической ишемией нижних конечностей». -М.: Медицина, 2002. -40 с.
- Сажинов А.П., Лукинский А.В., Чупин А.В. Пути улучшения проходимости бедренно-подколенных-берцовых шунтов//Ангиология и сосудистая хирургия. -2014. -Т. 20, №1. -С. 141-145.
- Червяков Ю.В., Староверов И.Н., Борисов А.В. и др. Отдаленные результаты до 3 лет использования непрямых способов реваскуляризации у больных с хронической ишемией нижних конечностей//Вестник хирургии. -2015. -№2. -С. 84-88.
- Bradbury A.W., Adam D.J., Bell J., et al. Bypass versus Angioplasty in Severe Ischaemia of the Leg (BASIL) trial: Analysis of amputation free and overall survival by treatment received//J. Vasc. Surg. -2010. -Vol. 51 (Suppl. S). -P. 18-31.
- Conte M.S. Bypass versus Angioplasty in Severe Ischaemia of the Leg (BASIL) and the (hoped for) dawn of evidence-based treatment for advanced limb ischemia//J. Vasc. Surg. -2010. -Vol.51 (Suppl. S). -P. 69-75.
- Pereira C.E., Albers M., Romiti M., et al. Meta-analysis of femoropopliteal byp-as grafts for lower extremity arterial insufficiency//J. Vasc. Surg. -2006. -Vol. 44, №3. -P. 510-517.
- Rychlik I.J., Davey P., Murphy J., et al. A meta-analysis to compare Dacron versus polytetrafluroethylene grafts for above-knee femoropopliteal artery bypass//J. of Vascular Surg. -2014. -Vol. 61, №2. -Р. 506-513.


