Сравнительная оценка гемодинамики до и после оперативного лечения у пациентов с нейроваскулярным синдромом
Автор: Асланов А.Д., Калибатов Р.М., Логвина О.Е., Бетуганова А.Л., Дунаев С.А., Тлупова Л.М., Карданова Л.Ю., Готыжев М.А., Кагазежева Л.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Сердечно-сосудистая хирургия
Статья в выпуске: 2 (88), 2024 года.
Бесплатный доступ
Введение. В подходе к показаниям при решении вопроса о хирургическом вмешательстве существуют различные мнения о целесообразности его использования и эффективности данного метода лечения больных с нейроваскулярным синдромом.Цель исследования. Улучшение результатов хирургического лечения больных с нейроваскулярным синдромом на основе сравнительного анализа гемодинамики по данным ультразвуковой допплерографии до и после различных методов оперативного вмешательства.Материалы и методы исследования. Исследование проводилось среди 155 пациентов с нейроваскулярным синдромом. Сформированы две группы: 88 пациентов (56,8 %), перенёсших операции, и 67 пациентов (43,2 %), проходивших консервативное лечение. На подгруппы по типам операции распределились аналогично: 24 (27,3 %) больных, которым изначально были проведены операции на симпатическом стволе (шейная и грудная симпатэктомия), и 64 (72,7 %) поэтапно проходили симпатэктомию. Кровоток оценивался ультразвуковой допплерографией.Результаты лечения. Периоперационные осложнения после 1 и 2 этапов были минимальными и редкими - в основном в виде ограниченных гематом в области хирургического доступа. Непосредственные результаты, сравнивая шейную или грудную симпатэктомию с периартериальной, не имели значимых различий в линейной скорости кровотока на артериях кисти.Заключение. Шейная или грудная симпатэктомия не является предпочтительным вариантом первичного хирургического вмешательства для лечения пациентов с нейроваскулярным синдромом, так как она более травматична, чем периферическая периартериальная симпатэктомия.
Нейроваскулярный синдром, синдром рейно, симпатэктомия, ультразвуковая допплерография
Короткий адрес: https://sciup.org/142241730
IDR: 142241730 | УДК: 617-089.844 | DOI: 10.17238/2072-3180-2024-2-28-37
Comparative assessment of hemodynamics before and after surgical treatment of patients with neurovascular syndrome
Introduction. In the approach to indications when deciding on surgical intervention, there are different opinions about the expediency of its use and the effectiveness of this method of treating patients with neurovascular syndrome.The purpose of the study. Improving the results of surgical treatment of patients with neurovascular syndrome based on a comparative analysis of hemodynamics according to ultrasound dopplerography before and after various surgical methods.Materials and methods of research. The study was conducted among 155 patients with neurovascular syndrome. Two groups were formed: 88 patients (56,8 %) who underwent surgery, and 67 patients (43,2 %) who underwent conservative treatment. The subgroups were divided similarly by type of surgery: 24 (27,3 %) patients who initially underwent surgery on the sympathetic trunk (cervical and thoracic sympathectomy), and 64 (72,7 %) underwent sympathectomy in a different levels (from distal to proximal). Blood flow was assessed by ultrasound dopplerography.Treatment results. Perioperative complications after stages 1 and 2 were minimal and rare, mainly in the form of limited hematomas in the area of surgical access. The immediate results, comparing cervical or thoracic sympathectomy with periarterial, had no significant differences in the linear velocity of blood flow on the arteries of the hand.Conclusion. Cervical or thoracic sympathectomy is not the preferred option for primary surgery for the treatment of patients with neurovascular syndrome, as it is more traumatic than peripheral periarterial sympathectomy.
Текст научной статьи Сравнительная оценка гемодинамики до и после оперативного лечения у пациентов с нейроваскулярным синдромом
С тех пор, как французский врач Морис Рейно (1862) впервые описал диагностику ангиотрофопараспастического синдрома, ученые всего мира из различных областей медицины продолжают исследовать эту проблему [1].
В большом количестве публикаций авторы указывают на то, что эта патология встречается у 4–5 % населения, а в регионах с холодным и умеренным климатом ее проявления отмечаются у 10–15 % населения [2].
По гендерному составу в этой патологии преобладают женщины (до 80 %) [3]. Как правило, первые проявления заболевания начинаются у людей в возрасте до 35 лет [4], даже в детском возрасте [5]. У 44,4 % детей при этом выявили наследственную предрасположенность [6, 7].
Вследствие прогрессирования нейроваскулярного синдрома, больные все больше теряют трудоспособность, не только временно, но и нередко становятся инвалидами. При этом они являются людьми трудоспособного возраста. Нейроваскулярный синдром имеет широкое распространение среди населения до 10 %, причем частота поражения у женщин выше [8].
Если хирурги в сосудистых отделениях обладают широким арсеналом методов лечения заболеваний магистральных сосудов, то в выборе вариантов лечения поражения периферического русла они ограничены [9, 10]. Диагностика нейроваскулярного синдрома затруднительна из-за многообразия его форм, отсутствия единых взглядов на причины возникновения, а также деления на первичную нозологию и вторично возникший синдром [11]. Проведение лечения только консервативными мероприятиями позволяет уменьшить количество спастических атак лишь у половины больных. А при ряде форм заболевания, которые сопровождаются необратимыми трофическими изменениями с выраженным болевым синдромом, возникла необходимость использовать хирургические методы лечения нейроваскулярного синдрома [12].
В подходе к показаниям при решении вопроса о хирургическом вмешательстве существуют полярные мнения о целесообразности его использования и эффективности такого подхода к лечению больных [13]. Хотя в большинстве работ исследователи утверждают, что только выполнение симпатэктомии, с целью «выключения» активных импульсов, приводящих к спазму артерий, позволяет добиться выздоровления или стойкой ремиссии, но это не является гарантией от рецидивов [14, 15].
Цель исследования. Улучшить результаты хирургического лечения больных с нейроваскулярным синдромом на основании сравнительного анализа гемодинамики до и после различных методов оперативного лечения.
Материалы и методы
Исследование проведено у 155 больных с нейроваскулярным синдромом. Вначале всем лицам осуществляли консервативное лечение, в которое входило приём фармпрепаратов включая: спазмолитики, антиагреганты, нестероидные противовоспалительные и десенсибилизирующие препараты, транквилизаторы. Дополнительно им проводили различные физиотерапевтические процедуры. У целого ряда больных проводимая терапия не имела положительного эффекта в течение одного года. В дальнейшем у части из них в случае необходимости выпол- нили хирургическое лечение. В связи с этим из них выделили 2 группы. Первую из них составили 88 (56,8 %) больных, которые перенесли хирургическое вмешательство и вторую – 67 (43,2 %) лиц, которым провели только консервативное лечение. Первую группу больных, в свою очередь, разделили на две подгруппы с учётом тактики хирургического лечения. В первую подгруппу вошли 24 (27,3 %) человека, которым изначально были проведены операции на симпатическом стволе (шейная и грудная симпатэктомия), во вторую подгруппу включили остальных 64 (72,7 %) больных, которым поэтапно осуществляли симпатэктомию.
Хирургический этап лечения осуществили в отделении хирургии сосудов Республиканской клинической больницы МЗ Кабардино-Балкарской республики в период 2000–2018 гг.
Мужчины составили 71 (45,8 %) человек, женщины – 84 (54,2 %). Средний возраст – 24,9±9,7 лет. Средний возраст мужчин – 25,4±10,3 лет, женщин – 24,9±9,2 года. Молодые люди до 30 лет составили 122 (78,7 %) человека. Давность заболевания менее 5 лет имели 95 (61,7 %) больных. Следует отметить, что клиническую картину в виде хронической ишемии верхних конечностей наблюдали у всех пациентов. Среди вошедших в исследование лиц 57 (36,8 %) был диагностирован первичный ФР, а у 98 (63,2 %) – вторичный. Больные, с учётом стадии заболевания, представлены для анализа в таблице 1.
Таблица 1
Распределение лиц по стадиям заболевания
Distribution of persons by stage of the disease
Table 1
|
Стадия / Stage |
Количество больных/ Number of patients |
% |
|
I фаза (ангиоспастическая)/ Phase I (angiospastic) |
15 |
9,7 |
|
II фаза (ангиопаралитическая)/ Phase II (angioparalytic) |
113 |
72,9 |
|
III фаза (трофическая)/ Phase III (trophic) |
27 |
17,4 |
Примечание: процент указан от общего количества больных Note: the percentage is indicated from the total number of patients
Наибольшее количество пациентов, обратившихся за помощью, и которым, проводили лечение, были уже во II (ангио-паралитической) и III (трофической) фазах нейроваскулярного синдрома.
При оценке ишемии верхней конечности использовали классификацию хронической ишемии, принятую в нашей клинике, основанную на классификации А.В. Покровского 1978 года. Классификация была основана на выраженности ишемических проявлений в верхней конечности в зависимости от степени её физической нагрузки. Преобладали пациенты со 2-й (43,9 %) и 3-й (38,7 %) степенью ишемии кистей. Меньше было больных с 4-й и 1-й степенью ишемии – 25 (16,1 %) и 2 (1,3 %) лица, соответственно (табл. 2).
Проводили оценку состояния кровотока методом ультразвуковой допплерографии на уровне лучевой артерии, артериях кисти и пальцев как до, так и после проведения провокации. С помощью этой методики были обследованы 108 больных как до, так и после операции, а также 47 человек, которым провели консервативную терапию.
Таблица 2
Распределение больных по степени ишемии руки (n=155)
Table 2
Distribution of patients by degree of arm ischemia (n=155)
|
Степень Stage |
Количество больных/ Number of patients |
% |
|
1 |
2 |
1,3 |
|
2 |
68 |
43,9 |
|
3 |
60 |
38,7 |
|
4 |
25 |
16,1 |
Примечание: процент указан от общего количества больных Note: the percentage is indicated from the total number of patients
РезультатыРезультаты консервативного лечения
Всем больным с НС изначально проводили консервативную терапию. При анализе результатов консервативного лечения выявили, что на фоне постоянного приема медикаментозной терапии периодически уменьшалась степень проявления хронической ишемии верхних конечностей. Исключением явились 2 больных, которым, в связи с быстрым началом прогрессирования некрозов кистей на фоне ранее относительно стабильного течения заболевания, была выполнена ампутация на уровне предплечья.
Остальные больные находились под постоянным медицинским контролем и обращались за медицинской помощью при учащении вазоспастических атак или усугублении тяжести хронической ишемии конечности. Таким больным выполняли различные варианты хирургического лечения. При анализе отдаленных результатов наблюдения за больными выявили, что в течение 5 лет усугубление клинических проявлений, требующих хирургического лечения, возникло у 105 (67,7 %) больных (рис. 1).
Таким образом, за период наблюдения больных с НС, которым проводили консервативную терапию, необходимость в хирургическом лечении возникла у большинства наблюдаемых лиц.
Хирургические методы лечения
Учитывая ранее приобретённый опыт лечения больных с НС (до 2008 г.) сотрудниками кафедры госпитальной хирургии Кабардино-Балкарского государственного университета им. Х.М. Бербекова была разработана и внедрена в практическую работу тактика хирургического лечения на разных уровнях симпатической нервной системы, подразумевающая последовательность выполнения вмешательств:
-
1 этап – периартериальная симпатэктомия, которую проводили на уровне бифуркации плечевой артерии (64 больных);
-
2 этап – периартериальная симпатэктомия выполняли на уровне подмышечной артерии (38 больных);
3-й этап –грудная симпатэктомия (18 больных).
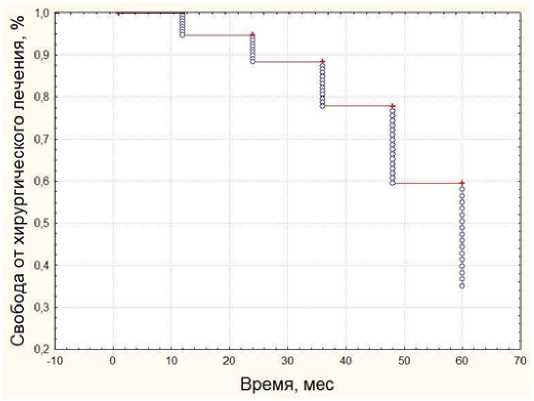
Рис. 1. Продолжительность положительного эффекта консервативной терапии у больных с нейроваскулярным синдромом Fig. 1. Duration of the positive effect of conservative therapy in patients with neurovascular syndrome
Данные тактические подходы использовали в нашей клинике на протяжении последних десяти лет. Периоперационные осложнения на 1-м и 2-м этапах были минимальные и проявляли себя достаточно редко, преимущественно в виде ограниченных гематом в области хирургического доступа, своевременное устранение которых никак не сказывалось на удлинение послеоперационного пребывания в стационаре. Поэтому в данной части исследования оценивали только отдаленные результаты и динамику ультразвуковых показателей кровотока после хирургического вмешательства.
Периартериальная симпатэктомия бифуркации плечевой артерии
Периартериальную симпатэктомию бифуркации плечевой артерии провели 64 больным, как 1-й этап хирургического вме- шательства. У основной части больных (98,4 %) после операции провели УЗДС для оценки состояния гемодинамики после операции на 1-ом этапе лечения. До операции отмечали резкое снижение скорости кровотока и индекса сопротивления, а после вмешательства данные показатели в течение первых суток достигали физиологической нормы (табл. 3). Клинически это выражалось в повышении кожной температуры кисти, исчезновении ишемической боли в ней и восстановление трофических нарушений.
Таблица 3
Сравнительная характеристика ультразвуковых показателей кровотока на ладонной дуге до и после периартериальной симатэктомии на уровне плечевой артерии, n = 64
Table 3
Comparative characteristics of ultrasound parameters of blood flow in the palmar arch before and after periarterial symatectomy at the level of the brachial artery, n = 64
|
Параметр/ Parameter |
До операции/ Before the operation |
После операции/ After the operation |
Р |
|
Vps, см/с / cm/s |
15,7±4,2 |
25,9±4,9 |
<0,0001 |
|
PI |
8,8±1,7 |
3,1±1,2 |
<0,0001 |
|
RI |
0,8±0,3 |
0,7±0,1 |
0,01 |
Таким образом, до операции по данным УЗДС отмечали резкое снижение скорости кровотока и индекса сопротивления. При этом степень снижения этих показателей была прямо пропорциональна степени выраженности ишемии верхней конечности. После хирургического вмешательства эти показатели в целом достигли референсных значений. Причём наибольший прирост показателей кровотока отмечен у больных со II-й степенью ишемии верхней конечности, а наименьшей среди лиц с IV степенью. То есть, чем ниже степень ишемии верхней конечности при ФР, тем более эффективнее был результат хирургического лечения с клинической стороны, а это достоверно подтвердили и объективные методы обследования.
Стабильный положительный отдалённый результат наблюдали у 26 (40,6 %) пациентов в течение 68,3±8,2 месяцев. Остальным 38 (59,4 %) больным в дальнейшем возникла необходимость повторного хирургического вмешательства – периартериальной симпатэктомии, только уже на уровне подмышечной артерии.
Периартериальные симпатэктомии подмышечной артерии
Показанием к последующему этапному хирургическому лечению на уровне подмышечной артерии были, как правило, рецидив боли в кисти и её похолодание, появление трофических изменений на пальцах. Возобновление клиники фиксировали через 31,4±9,1 месяц после ранее выполненной периартериальной десимпатизации на уровне плечевой артерии. Необходимость в дистальной ампутации пальцев на уровне концевых фаланг из-за глубоких некротических изменений возникла только у 2 (5,3 %) женщин. После ампутации раны на пальцах быстро зажили первичным натяжением. Ещё у 4 (10,6 %) больных, у которых имели место неглубокие трофические нарушения кожных покровов, процесс заживления и проходил самопроизвольно. У пациентов без некротических изменений наблюдали исчезновение вазоспастических проявлений при контакте с провоцирующими факторами или же заметное уменьшение проявлений заболевания. По результатам ультразвуковой допплерографии во всех случаях отмечали увеличение ЛСК (табл. 4).
Таблица 4
Сравнительная характеристика ультразвуковых показателей кровотока на ладонной дуге до и после периартериальной симатэктомии на уровне подмышечной артерии, n =38
Table 4
Comparative characteristics of ultrasound parameters of blood flow in the palmar arch before and after periarterial symatectomy at the level of the axillary artery, n =38
|
Параметр/ Parameter |
До операции/ Before the operation |
После операции/ After the operation |
Р |
|
Vps, см/с / cm/s |
16,3±3,1 |
26,2±4,7 |
<0,0001 |
|
PI |
8,3±1,9 |
3,6±1,4 |
<0,0001 |
|
RI |
0,8±0,5 |
0,7±0,1 |
<0,01 |
Результаты лечения после 2-го этапа периартериальной симпатэктомии были стабильные положительные. В дальнейшем у 25 (65,8 %) больных начала проявляться отрицательная динамика, которая привела к рецидиву ишемии верхней конечности в различной степени выраженности через 13,3±3,2 месяцев наблюдения (рис. 2). На фоне вазотропной терапии им удавалось поддерживать относительно удовлетворительное состояние конечности кроме 18 (47,4 %) человек. У остальных 13 (34,2 %) пациентов сохранился стойкий положительный результат.
Таким образом, при оценке результатов лечения больных НС после разработанной тактики этапного лечения отметили положительную динамику у всех пациентов в раннем послеоперационном периоде. В отдаленном же периоде у части больных всё-таки развились явления рецидива заболевания.
Так, при вмешательстве на дистальных отделах (бифуркация плечевой артерии) получили удовлетворительные данные безрецидивного состояния у ряда больных. В течение 68,3±8,2 месяцев 40,6 % пациентов не имели никаких проявлений хронической ишемии верхней конечности. Однако остальным 59,4 % больным в последующем потребовалось повторное хирургическое вмешательство (рис. 3).
В группе больных после проксимальной периартериальной симпатэктомии (на уровне подмышечной артерии) результаты оказались менее обнадёживающие. Через 5 лет наблюдения у них была отмечена отрицательная динамика заболевания. Относительно удовлетворительные результаты наблюдали до 13,3±3,2 месяцев наблюдения. В дальнейшем рецидива не было только у 34,2 % больных при небольших сроках наблюдения. Необходимость в 3-ем этапе хирургического лечения возникла у 47,4 % лиц из-за угрозы нарастания гангренозных изменений пальцев руки. У остальных, несмотря на отрицательную динамику, угрозы необратимых нарушений кровообращения не возникало и им проводили комплексную консервативную терапию.
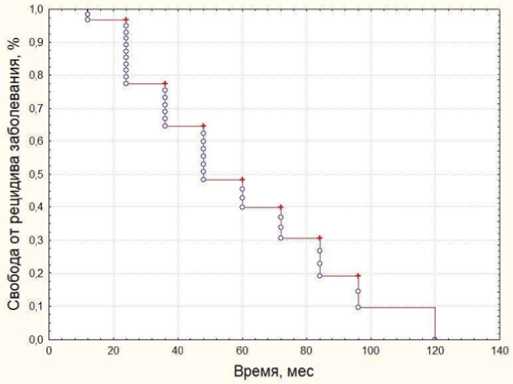
Рис. 2. Отдаленные результаты безрецидивного состояния больных после дистальной периартериальной симпатэктомии Fig. 2. Long-term results of relapse-free condition of patients after distal periarterial sympathectomy
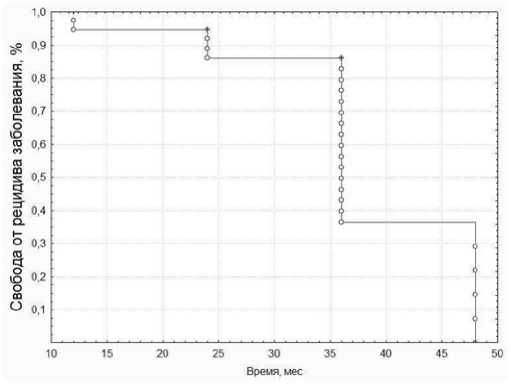
Рис. 3. Отдаленные результаты безрецидивного состояния больных после проксимальной периартериальной симпатэктомии
Fig. 3. Long-term results of relapse-free condition of patients after proximal periarterial sympathectomy
Подводя итог этапных периартериальных вмешательств можно отметить, что стабильный положительный результат получен в 40,6 % случаях после 1- ого этапа хирургического лечения и 52,6 % случаев после 2-ого этапа. Если суммировать эти результаты, то получается, что необходимость в 3-ем, наиболее травматическом этапе хирургического лечения, отпала у большинства, а именно, у 46 (72,8 %) пациентов.
Грудная симпатэктомия
В целом удаление симпатических ганглиев в шейном и грудном отделах выполнили 42 больным. В качестве первичного вмешательства данную операцию провели у 24 (56,1 %) больных, но от данного подхода отошли в последние 10 лет, когда начали применять разработанную схему лечения. Применение таких симпатэктомий мы посчитали целесообразным только в тех случаях, когда другие возможности хирургического подхода (периартериальные десимпатизации) были исчерпаны.
Первоначальный опыт, основанный на 24 больных, показал то, что отдаленные результаты как шейной, так и грудной симпатэктомий были хуже того, что мы наблюдали непосредственно после операции. Следует отметить и то, что в раннем послеоперационном периоде в 33,3 % случаев мы отмечали те или иные осложнения, которые доставляли неудобство для больных, и это продолжалось от 1 месяца до года пока пациенты не отмечали полного восстановления. Также можно обратить внимание на то, что количество ампутаций в этой группе больных было больше, чем в остальных: на уровне пальцев у 4 (16,7 %) лиц, а на уровне предплечья – у 2 (8,3 %).
Можно выделить специфические осложнения в виде малого гемоторакса, брахиоплексита, синдрома Горнера, кровотечения в месте доступа. Неспецифическими осложнениями были: нагноение раны, лимфорея (1 больной), гематома в области шва (2 больных).
Эффективность первичной шейной или грудной симпатэктомии была только сразу после операции. В дальнейшем 9 (37,5 %) лиц обратились к хирургу через несколько лет. Весь указанный период их руки не беспокоили. У остальных 15 (62,5 %) больных были рецидивы основных признаков НС, и они регулярно посещали хирурга и получали лечение. Существенное прогрессирование рецидива НС с развитием некрозов и даже гангрены пальцев было отмечено у 7 (29,2 %) из 24 наблюдавшихся больных в отдаленном периоде.
Если оценивать в целом результаты лечения как первичных, так и повторных шейных и грудных симпатэктомий (42 пациента), то в ближайшее время после операции наблюдали положительный гемодинамический эффект. Сразу уже в первые сутки после операции наблюдали гиперваскуляризацию. По данным УЗДГ у большинства больных фиксировали уровень кровотока, превышающий показатели здоровой конечности. Затем постепенно наступала стабилизация кровообращения верхней конечности на уровне референсных значений с последующим исчезновением клиники НС.
В таблице 5 приведено сравнение усреднённых показателей УЗДГ, которые были рассчитаны как до, так и после операции. Скорость кровотока только в плечевой артерии после шейной или грудной симпатэктомии, а также подмышечной артерии достоверно не изменилась. В артериях же на других дистальных уровнях прирост ЛСК был достоверным, включая лиц, которым первым этапом была проведена десимпатизация на уровне плечевой артерии, особенно в поверхностной ладонной дуге (р <0,05), что и обусловливало первичный положительный эффект от операции.
Таблица 5
Характеристика динамики ЛСК (см/сек) при УЗДГ артерий руки
Table 5
Characteristics of the dynamics of LSC (cm/sec) in ultrasound of the arteries of the arm
|
Артерия/ Artery |
До операции/ Before the operation |
После/ After the operation |
Нормальные значения/ Normal values N |
|
Плечевая/ Brachial |
34,1±5,1 |
38,9±5,7 |
35,8±6,2 |
|
Локтевая/ Ulnar |
18,7±5,4 |
27,1±5,3 |
24,7±2,12 |
|
Лучевая/ Radial |
19,8±6,2 |
28,4±6,4 |
21,3±1,61 |
|
Поверхностная ладонная дуга/ Superficial palmar arch |
15,7±4,2 |
23,2±5,1 |
22,1±1,6 |
Примечание: жирным шрифтом выделены статистически достоверные различия с показателями до операции (р <0,05) Note: statistically significant differences with indicators before surgery are highlighted in bold (p <0,05)
Также провели анализ динамики показателей УЗДГ и у 17 больных с 4-й ст. ишемии кисти до и после хирургического вмешательства (табл. 6). В артериальном русле верхней конечности на всех уровнях исследования (кроме плечевой артерии) отметили достоверный прирост ЛСК после симпатэктомии. У 5 пациентов после операции определить кровоток в общепальцевых артериях не смогли, возможно из-за развившейся облитерации артерий.
Таким образом, после малотравматичных этапных десим-патизаций плечевой и подмышечной артерий у большинства, а именно у 46 (72,8 %) больных, отпала необходимость в грудной симпатэктомии, которые были гораздо травматичнее, чем периферическая десимпатизация.
Таблица 6
Характеристика динамики ЛСК (см/сек) при УЗДГ у больных с 4 степенью ишемии
Table 6
Characteristics of the dynamics of LSC (cm/sec) in UZD in patients with grade 4 ischemia
|
Артерия/ Artery |
До операции/ Before the operation |
После/ After the operation |
Нормальные значения/ Normal values N |
|
Плечевая/ Brachial |
35,5±4,4 |
41,2±5,4 |
35,8±6,2 |
|
Локтевая/ Ulnar |
17,7±5,0 |
24,6±3,1 |
24,7±2,12 |
|
Лучевая/ Radial |
18,3±4,3 |
25,4±2,9 |
21,3±1,61 |
|
Поверхностная ладонная дуга/ Superficial palmar arch |
13,6±4,5 |
19,8±3,8 |
22,1±1,6 |
Примечание: жирным шрифтом выделены статистически достоверные показатели (р <0,05)
При сравнительном анализе непосредственных результатов лечения между методом шейной или грудной и периферическими симпатэктомиями не обнаружили достоверных различий линейной скорости кровотока на артериях кисти. На основании этого можно утверждать, что шейная или грудная симпатэктомия не целесообразна как первичное хирургическое вмешательство в лечении больных с нейроваскулярным синдромом ввиду большей травматичности чем периферическая периартериальная симпатэктомия.
Обсуждение
Для оценки эффективности операций проводились исследования гемодинамики на догоспитальном и предоперационном этапах с помощью ультразвуковой допплерографии. Важным методом было применение методов периартериальной десимпатизации и шейно-грудной симпатэктомии, включая анализ УЗДГ для измерения скорости кровотока и индекса сопротивления в различных артериях верхней конечности. После операции было отмечено увеличение скорости кровотока и индекса сопротивления, сопровождающееся повышением кожной температуры кисти, исчезновением болей и нормализацией трофических нарушений. Несмотря на положительную динамику у большинства пациентов, в отдаленном периоде наблюдались рецидивы заболевания. После подмышечной симпатэктомии у некоторых пациентов наблюдалась менее утешительная динамика в течение 5 лет. Необходимость в дальнейших этапах хирургического вмешательства возникала в 47,4 % случаев. Положительный результат отмечен у 40,6 % после первого и 52,6 % после второго этапов хирургической помощи после поэтапных периартериальных вмешательств. В группе, где шейно-грудная симпатэктомия выполнялась как первичное вмешательство, кровоток улучшился, а скорость кровотока в дистальных артериях повысилась. У 5 пациентов, возможно, из-за облитерации артерий, кровоток после операции не был обнаружен. Сравнительный анализ результатов операции показал, что шейная и грудная симпатэктомии не показали существенных различий в скорости кровотока, однако второй вариант был менее инвазивным и, таким образом, предпочтительным как первичное вмешательство в лечении нейроваскулярного синдрома.
Выводы
-
1. При нейроваскулярном синдроме наблюдается снижение линейной скорости кровотока по артериям предплечья и кисти, при этом чем выраженнее степень ишемии конечности, тем эти показатели ниже.
-
2. Разработанный этапный подход малотравматичных периартериальных симпатэктомий при лечении нейроваскулярного синдрома (дистальный, проксимальный) и только потом грудной симпатэктомии даёт возможность сохранить безрецидивное течение заболевания в срок до 5 лет после каждого этапа лечения. После каждого этапа лечения на период указанного срока увеличивается скорость кровотока по артериям предплечья и кисти (р < 0,05).
-
3. Наилучшие показатели объективного прироста кровоснабжения после операции периартериальной десимпатизации или симпатэктомии следует ожидать при II степени, наихудшие — при IV степени ишемии верхней конечности (р < 0,05).
-
4. Для решения вопроса о выборе тактики лечения больных с нейроваскулярным синдромом необходимо оценивать скорости кровотока на артериях предплечья и кисти, уровень транскутанного напряжения кровотока в дистальных отделах верхней конечности. На основании полученных данных можно корректировать схемы проводимого лечения.
-
5. Для продления эффекта безрецидивного течения заболевания следует выполнять этапное лечение, начиная от консервативного, затем периартериальная симпатэктомия сначала на уровне плечевой, при возникновении рецидива – на уровне подмышечной артерии, а если и после этого возникнет рецидив, только тогда выполнять грудную симпатэктомию.
-
6. Выполнение шейной или грудной симпатэктомии на первом этапе хирургического лечения нецелесообразно из-за травматичности вмешательства, необходимости применения наркоза, а также блокирования дальнейшей возможности продлить эффект от хирургического вмешательства. Целесообразно начинать хирургическое лечение с менее травматичных периартериальных симпатэктомий.
Список литературы Сравнительная оценка гемодинамики до и после оперативного лечения у пациентов с нейроваскулярным синдромом
- Letamendia A., López-Román J., Bustamante-Munguira J., Herreros J. Digital periarterial sympathectomy in the management of post-traumatic Raynaud syndrome. J Vasc Surg., 2016, Feb; № 63(2), рр. 459-465. https://orcid.org/10.1016/j.jvs.2015.08.102
- Рахматуллаев Р., Абдувахидов Б.У., Пулатов О.Н. и соавт. К вопросу о десимпатизации верхней конечности при феномене Рейно. Вестник Авицены, 2018. Т. 20. № 1. С. 113-119. https://orcid.org/10.25005/2074-0581-2018-20-1-113-119
- Fardoun M.M., Nassif J., Issa K., Baydoun E., Eid A.H. Raynaud’s Phenomenon: A Brief Review of the Underlying Mechanisms. Front Pharmacol., 2016, Nov 16; № 7, рр. 438. https://orcid.org/10.3389/fphar.2016.00438
- Fraenkel L., Zhang Y., Chaisson C.E., Evans S.R., Wilson P.W., Felson D.T. “The Association of Estrogen Replacement Therapy and the Raynaud Phenomenon in Postmenopausal Women.” Annals of Internal Medicine, 1998, № 129, рр. 208-211. https://doi.org/10.7326/0003-4819-129-3-199808010-00009
- Qiu O., Chan T., Luen M., Cruz J.E., Hermes-DeSantis E.R. Use of nitroglycerin ointment to treat primary and secondary Raynaud’s phenomenon: a systematic literature review. Rheumatol Int., 2018, Dec; № 38(12):2209-2216. https://orcid.org/10.1007/s00296-018-4119-9
- Ter Borg E.J., Piersma-Wichers G., Smit A.J., Kallenberg C.G., Wouda A.A. Serial nailfold capillary microscopy in primary Raynaud’s phenomenon and scleroderma. Semin Arthritis Rheum., 1994, Aug; № 24(1), рр. 40-47. https://orcid.org/10.1016/0049-0172(94)90098-1. PMID: 7985036
- Lamprecht P. Aktuelle Aspekte ANCA-assoziierter Vaskulitiden [New aspects in ANCA-associated vasculitides]. Med Klin (Munich), 2004, Sep 15, № 99(9), рр. 518-522. German. https://orcid.org/10.1007/s00063-004-1078-6
- Bürgi B., Otten U.H., Ochensberger B., Rihs S., Heese K., Ehrhard P.B., Ibanez C.F., Dahinden C.A. Basophil priming by neurotrophic factors. Activation through the trk receptor. J Immunol., 1996. Dec 15; № 157(12), рр. 5582-5588.
- Михайличенко В.Ю., Орлов А.Г., Иваненко А.А. Методы хирургической коррекции хронической акральной ишемии верхних конечностей. Современные проблемы науки и образования., 2016. № 4. URL: https://science-education.ru/ru/article/view?id=25074
- Рахмонов Д.А., Султанов Д.Д., Гаибов А.Д., Неъматзода О., Сайдалиев Ф.Дж. Шейно-грудная симпатэктомия в лечении хронической акральной ишемии. Кардиология и сердечно-сосудистая хирургия, 2023. № 16(5). С. 474-480. https://doi.org/10.17116/kardio202316051474
- Путилина М.В. Феномен Рейно в практике врача-интерниста. Фарматека, 2015. № 20. C. 24-31. https://journals.eco-vector.com/2073-4034/article/view/288383
- Михайличенко В.Ю., Орлов А.Г. Эффективность применения периартериальной симпатэктомии у больных с акральной ишемией верхних конечностей. Международный журнал прикладных и фундаментальных исследований, 2016. № 11(5). С. 906-908. URL: https://applied-research.ru/ru/article/view?id=10557
- Yasser Aljehani, Rahma ShahBahai, Alaa Turkistani. BILATERAL UNIPORTAL VIDEO-ASSISTED THORACOSCOPIC SURGERY SYMPATHECTOMY FOR MANAGING RAYNAUDS DISEASE. Int. J. of Adv. Res., 2019, № 7, рр. 788-789. https://doi.org/10.21474/IJAR01/9424
- Jeon S.B., Ahn H.C., Ahn Y.S., Choi M.S. Two-Step Incision for Periarterial Sympathectomy of the Hand. Archives of Plastic Surgery, 2015 Nov; № 42(6), рр. 761-768. https://doi.org/10.5999/aps.2015.42.6.761
- Асланов А.Д., Логвина О.Е., Бетуганова А.Л., Карданова Л.Ю., Дунаев С.А., Готыжев М.А., Куготов А.Г., Куготов А.Х., Эдигов А.Т., Таукенова Л.И., Жириков А.В., Хашев А.Ч. Эффективность применения этапного лечения нейроваскулярного синдрома. Московский хирургический журнал, 2022. № 3. С. 15-24. https://doi.org/10.17238/2072-3180-2022-3-15-24


