Сравнительная оценка результатов хирургического и эндоваскулярного методов лечения аневризмы брюшной аорты у пациентов с низкими и средними факторами риска
Автор: Чарчян Эдуард Рафаэлович, Абугов Сергей Александрович, Степаненко Анна Борисовна, Генс Андрей Павлович -, Пурецкий Михаил Владимирович, Поляков Роман Сергеевич, Карапетян Айк Хачатурович, Скворцов Алексей Алексеевич
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Сосудистая хирургия
Статья в выпуске: 2 т.19, 2015 года.
Бесплатный доступ
Цель По данным различных авторов частота заболеваемости аневризм брюшной аорты колеблется от 8 до 12%, а летальность составляет 7,2-9,0%. В настоящее время определены два основных альтернативных метода лечения: хирургический и эндоваскулярный. Материал В исследование включены 98 пациентов с атеросклеротическими аневризмами инфраренального отдела и методы брюшной аорты с невыраженной сочетанной и сопутствующей патологией (без клиники ишемической болезни сердца, легкая степень хронической обструктивной болезни легких и др.). Первая группа - 38 пациентов, подвергшиеся эндоваскулярному лечению аневризм брюшной аорты. Во вторую группу вошли 60 больных, которым выполнена резекция аневризмы с линейным или бифуркационным протезированием стандартным хирургическим методом. Результаты В группе эндоваскулярного протезирования наблюдались достоверно лучшие показатели течения интра- и раннего послеоперационного периодов (отсутствие выраженного болевого синдрома, короткий койко-день). Однако в отдаленном послеоперационном периоде имелись осложнения: эндолика, n = 7 (18,4%), тромбоз графта в области подвздошных артерий, n = 3 (7,9%), снижение потенции в связи с перекрытием внутренних подвздошных артерий, n = 3 (7,9%). Некоторые осложнения требовали сложных повторных операций. У пациентов после хирургических вмешательств по поводу аневризм брюшной аорты в течение пятилетнего послеоперационного периода осложнений, связанных непосредственно с аортальной реконструкцией, не выявлено. Выводы Эндоваскулярное протезирование аневризм брюшной аорты - высокоэффективный и малотравматичный метод лечения. Однако у пациентов с низкими и средними факторами риска приоритетным следует считать хирургическое лечение.
Инфраренальная аневризма, хирургическое лечение, эндоваскулярное лечение
Короткий адрес: https://sciup.org/142140672
IDR: 142140672 | УДК: 616.136.007-386-089
Comparative evaluation of the results of surgical and endovascular methods of abdominal aortic aneurysm repair in patients with low and medium risk factors
Background. According to the data by various authors the incidence of abdominal aorta aneurysms varies from 8 to 12%, with the mortality rate reaching 7.2-9,0%. At present, two alternative methods of repair exist: surgical and endovascular procedures. Methods. The study involved 98 patients with athero-sclerotic aneurysms of an infrarenal part of the abdominal aorta with unexpressed concomitant pathology (without signs of ischemic heart disease, a light degree of chronic obstructive lung disease, etc.). The first group of 38 patients underwent endovascular repair of abdominal aorta aneurysms. The second group involved 60 patients who underwent open resection of the aneurysm followed by conventional implantation of a linear or bifurcational prosthesis. Results. In the endovascular repair group significantly better intraoperative and early postoperative indicators were observed (absence of marked pain syndrome, shorter hospital stay). However, in the late postoperative period complications were recorded: endoleak n=4 (10.8%), graft thrombosis in the region of iliac arteries n=2 (5.3%), decrease of sexual potency because of the involvement of internal iliac arteries n=3 (7.9%). Some complications required complex repetitive surgical interventions. No complications directly related to aortic repair were observed in those patients who underwent surgical treatment during 5-year follow-up. Conclusions. Endovascular abdominal aortic aneurysm repair is a highly effective and less traumatic method of treatment. However, in patients with low and medium risk factors surgical treatment should be considered as a priority.
Текст научной статьи Сравнительная оценка результатов хирургического и эндоваскулярного методов лечения аневризмы брюшной аорты у пациентов с низкими и средними факторами риска
абвг
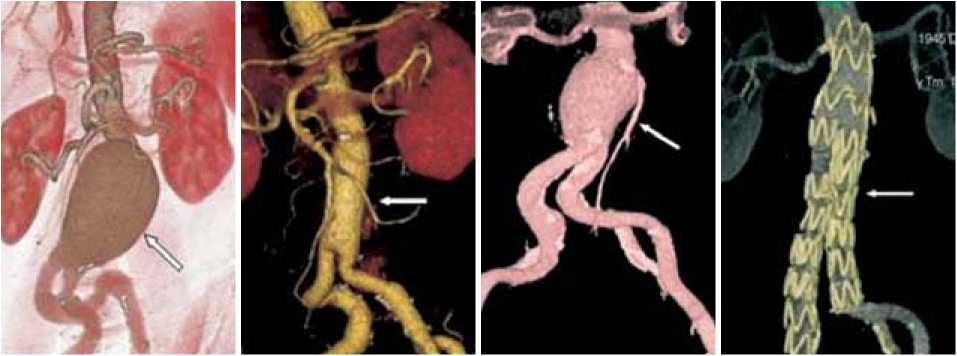
Рис. 1. Спиральная компьютерная томография до и после вмешательств на брюшной аорте по поводу аневризм: а – инфра-ренальная аневризма (стрелкой указана аневризма); б – состояние после протезирования брюшной аорты через 5 лет после операции (стрелкой указан линейный протез аорты); в – инфраренальная аневризма до стентирования; г – через год после стентирования брюшной аорты (стрелкой указан стент)
40% [3, 4]. Высокая смертность тяжелых соматических больных, травматичность и частота развития осложнений после классических операций на аорте способствуют появлению новых альтернативных методов лечения, одним из которых является рентгенэндоваскулярная хирургия [5].
В РНЦХ им. акад. Б.В. Петровского первая операция имплантации бифуркационного стент-графта по поводу АБА проведена в 2003 г. и в настоящее время накоплен большой опыт в данном виде лечения. Рентгеноэндоваскулярные вмешательства имеют неоспоримые преимущества перед стандартной реконструктивной хирургией брюшной аорты: миниинвазивность (отсутствие большого разреза, кровопотери и повреждения прилегающих органов и структур), возможность выполнения у пожилых пациентов при наличии тяжелой сопутствующей патологии, снижение числа ранних послеоперационных осложнений. Однако отмечается ряд ограничений в возможности проведения самого вмешательства, наблюдаются характерные осложнения в отдаленном послеоперационном периоде, требующие повторных вмешательств, а также имеется необходимость пожизненного периодического медицинского контроля и приема определенных препаратов. Все это заставляет избирательно подходить к этим двум альтернативным методам лечения, особенно у пациентов без выраженной сопутствующей патологии, где есть возможность без особо высокого риска выполнить реконструктивную операцию.
Цель работы – определение показаний для проведения эндоваскулярного или хирургического вмешательств у пациентов низкого и среднего хирургического риска.
Материал и методы
За период с января 2005 г. по март 2014 г. в отделении хирургии аорты и ее ветвей РНЦХ им. акад. Б.В. Петровского выполнено 98 вмешательств по поводу аневризмы брюшного отдела аорты у пациентов с низкими и средними факторами риска. Отбор больных для оценки факторов риска, влияющих на прогноз лечения после плановых операций по поводу АБА, проводился с помощью шкалы Рутерфорда (2005) [11]. Шкала представлена независимыми друг от друга критериями в балльном исчислении: возраст, пол, сердечная, почечная и легочная патологии. К больным, вошедшим в исследование, отнесли пациентов со следующими критериями: возраст – до 70 лет (0 , по Рутерфорду); хроническая болезнь почек – скорость клубочковой фильтрации выше 50 мл/мин (креатинин <1,8 мг/дл) (0, по Рутерфорду); ИБС – отсутствие клиники стенокардии, отсутствие ИМ в анамнезе, поражение ствола или коронарных артерий ≤50%; фракция выброса ≥40% (+3, по Рутерфорду); хроническая обструктивная болезнь лег- абвг
И^ ЯНР1М
Рис. 2. Этапы фиксации протеза баллоном Reliant: а – закрепление проксимального конца основной секции (стрелкой указан баллон Reliant); б – закрепление дистального конца основной секции (стрелкой указан баллон Reliant в дистальном конце стента основной секции); в – закрепление места соединения основной и контралатеральной секций (стрелкой указан баллон Reliant, место крепления контралатеральной секции); г – закрепление дистального конца контралатеральной секции (стрелкой указан баллон Reliant в дистальном конце стента контралатеральной секции)
ких (ХОБЛ) или одышка (+7, по Рутерфорду). Мужчин было 67 (68%) (0, по Рутерфорду), женщин – 31 (32%) (+4, по Рутерфорду). Средний возраст в группах составил 64,7±6,2 года. В исследование вошли пациенты, у которых общий балл по Рутерфорду составил не выше 10, процент летальности соответствовал 5%.
Симптомов заболевания не отмечалось у 55 пациентов (56,12%). 33 (33,6%) пациента отмечали ощущение пульсации в животе, 9 – (9,2%) жаловались на боль в животе, 19 – (19,4%) на боль в спине. У 4 (4,1%) отмечался дискомфорт со стороны желудочно-кишечного тракта.
Всем больным проводили комплексное обследование. Общеклинические методы включали сбор анамнеза, физикальное обследование, рентгенографию грудной клетки, клинический и биохимический анализы крови, ЭКГ, ультразвуковое дуплексное сканирование брюшной полости и аорты, спирометрию, коронарную ангиографию при ИБС. Основными диагностическими методами являлись ультразвуковое исследование органов брюшной полости и мультиспиральная компьютерная томография (МСКТ) (рис. 1).
Изначально больные были разделены на две группы. В 1-ю группу вошли 60 пациентов, которым выполнены открытые операции, во 2-ю – 38 пациентов, которым проведено бифуркационное стентирование брюшной аорты. Группы сопоставимы по размерам и локализации аневризм, возрасту, полу, сочетанной и сопутствующей патологиям. Средний диаметр аневризмы составил 5,78±0,62 см. В группу пациентов с хирургическим лечением отбирались пациенты, исключающие основные противопоказания, которые ограничивают применения эндоваскулярных вмешательств.
Всем больным из 1-й группы выполнены реконструктивные операции. 42 (70%) пациентам проведено линейное протезирование, 18 (30%) – бифуркационное аортоподвздошное протезирование (рис. 1).
Всем пациентам 2-й группы выполняли стентирование аневризм инфраренального отдела аорты бифуркационными самораскрывающимися стент-графтами Talent (Medtronic). Выбор стентов проводился индивидуально, по данным спиральной КТ в 3D-режиме и только тем больным, которые подходили под морфологические критерии данной методики. Для точного подбора размера стент-графта исследование проводилось от устья верхней брыжеечной артерии до общих бедренных артерий. По протоколу длина проксимальной «шейки» должна быть не менее 15 мм, ее диаметр не более 31 мм, без выраженного кальциноза стенки. Ангуляция не должна превышать 60 градусов, а диаметр подвздошных артерий должен быть не менее 8 мм, ангуляция – до 90 градусов (рис. 2).
Во время стентирования использовали 24-F основные бифуркационные системы и 18-F контралатеральные, которые до места крепления проходили через об- абвг
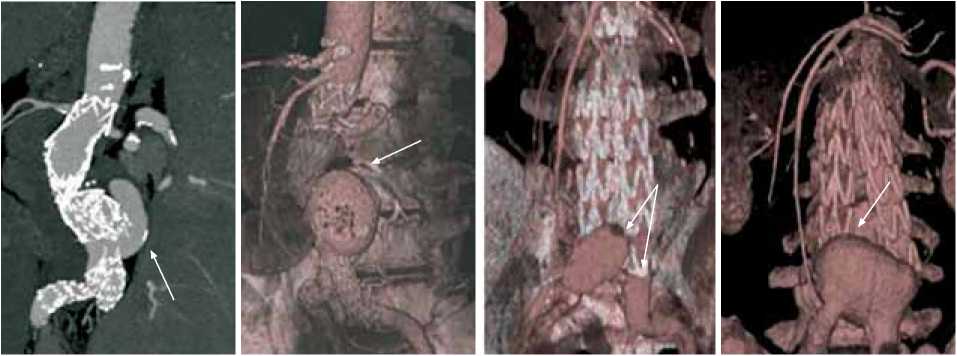
Рис. 3. Осложнения после рентгенэндопротезирования брюшной аорты по поводу инфраренальной аневризмы (данные МСКТ): а , б – увеличение аневризмы и эндолика через два года после стентирования; рост аневризмы через месяц ( в ) и год ( г ) после стентирования
щие бедренные артерии после их выделения. Сначала устанавливали основную раздвоенную секцию, затем контралатеральную подвздошную. Проксимальный и дистальные концы фиксировали с помощью дилатационного баллона Reliant (рис. 2). Стентирование проводили под контролем ангиографии. После вмешательства артерии зашивали нитью «Пролен» 6/0, раны послойно зашивали и накладывали асептические повязки.
Результаты и обсуждение
При сравнении интраоперационных показателей по продолжительности вмешательства, комбинированной эндотрахеальной и спинальноэпидуральной анестезии, интраоперационной ишемии, связанной с пережатием аорты при открытых операциях, объему инфузии и кровопотери – получены достоверное улучшение результатов у пациентов во время стентирования по сравнению с хирургической реконструкцией (табл. 1).
После хирургического лечения в ближайшем послеоперационном периоде основными осложнениями явились: пневмония – 3 (5%), раневые осложнения – 2 (3,3%) и длительный парез кишечника – 2 (3,3%). Один больной умер от кишечной непроходимости и перитонита (1,7%).
В группе стентирования в раннем послеоперационном периоде отмечены продолжительные температурные реакции без особых изменений в формуле крови, со средней температурой 37,9±0,7 °С, что, вероятно, связано с резорбцией тромботических масс в парапро-тезном пространстве у 27 (71,1%) пациентов. Одному пациенту потребовалось выполнение перекрестного бедренно-глубокобедренного шунтирования в связи с тромбозом правой бранши эндопротеза (табл. 2).
В отдаленном послеоперационном периоде после хирургического лечения из осложнений наблюдались послеоперационные грыжи у 3 (5%) пациентов и половая дисфункция у 2 (3,3%). Летальности, связанной с хирургическим вмешательством, не отмечено.
В отдаленном послеоперационном периоде после стентирования выявлены эндолики: I типа – 3 (7,9%), II – 2 (5,3%), III – 2 (5,3%). Рост аневризмы отмечался у 2 (5,3%) пациентов, разрыв аневризмы – у 3 (7,9%) (рис. 3). Тромбоз графта произошел у 3 (7,9%) больных. Половая дисфункция отмечалась в 3 (7,9%) наблюдениях. Один пациент (2,6%) умер от разрыва аневризмы (табл. 2).
При анализе послеоперационных осложнений в группах со стентированием и хирургическом лечении выявлено, что в раннем послеоперационном периоде количество осложнений в группах не отличалось. Однако в отдаленном послеоперационном периоде отмечено достоверно большее количество осложнений после стентирования (табл. 3).
При сравнении послеоперационных результатов можно утверждать, что рентгенэндоваскулярный метод лечения является достойной альтернативой от-
Таблица 1 Основные параметры интра- и послеоперационного периодов у пациентов с аневризмами брюшной аорты после хирургического и рентгенэндоваскулярного лечения
|
Параметр |
Хирургическое лечение, n = 60 |
Стентирование, n = 38 |
p |
|
Длительность операции, мин |
176,5±58,9 |
118,7±34,2 |
p<0,001 |
|
Комбинированная эндотрахеальная анестезия, n (%) |
60 (100) |
6 (15,8) |
p<0,001 |
|
Спинально-эпидуральная анестезия, n (%) |
60 (100) |
32 (84,2) |
р = 0,003 |
|
Кровопотеря, мл |
480±178 |
248±72 |
p<0,001 |
|
Длительность пребывания в кардиореанимации, сут. |
1,14±0,78 |
0,92±0,43 |
р = 0,115 |
|
Активизация больного, сут. |
2,87±0,95 |
1,87±0,58 |
р<0,001 |
|
Длительность послеоперационного стационарного лечения, сут. |
10,1±3,6 |
6,7±1,2 |
p<0,001 |
Таблица 2 Частота осложнений у больных с аневризмами брюшной аорты
Жесткие морфологические критерии и высокая стоимость этой методики ограничивают ее широкое применение [8].
При анализе отдаленных результатов лечения выявлено, что после стентирования количество осложнений достоверно выше, чем при хирургическом методе лечения. Основную часть составляют такие осложнения, как смещение стента, эндолик, рост и разрыв аневризмы. Эти осложнения имеют серьезный прогноз и, как правило, требуют сложных повторных хирургических вмешательств (n = 3; 8% ) или реинтервенций (n = 5; 13,2%). У больных с хирургической реконструкцией в
Таблица 3 Сравнительный анализ осложнений у больных с аневризмами брюшной аорты по группам
Rutherford R.B. и Krupski W.C., в 2004 г. пришли к выводу, что традиционный хирургический метод лечения предпочтительнее у молодых пациентов при низких операционных рисках – это мнение поддержано снова 2005 г. Cronenwett J.L. [6].
Mehta c соавт. проанализировали 1 768 пациентов после стентирования инфраренальной аорты, 339 из них (19,2%) потребовались повторные вмешательства из-за развития таких осложнений, как эндолик, миграция стента, формирование и разрыв аневризмы [9].
Becquemin и соавт. [10] при сравнении хирургического и рентгенэндоваскулярного методов лечения (рандомизированное исследование) заключили, что у больных с низкими и умеренными факторами риска хирургическое лечение аневризмы брюшной аорты является таким же безопасным, как и стентирование, кроме того, более радикальным методом.
Таким образом, на основании собственного опыта и литературных данных можно сделать вывод, что рен-тгенэндоваскулярное протезирование инфрареналь-ных аневризм брюшной аорты – высокоэффективный и малотравматичный метод лечения. Однако в связи с возможностью развития в отдаленном периоде осложнений, требующих сложных повторных хирургических вмешательств, у пациентов с низкими и средними факторами риска приоритетным следует считать хирургическое лечение.
Список литературы Сравнительная оценка результатов хирургического и эндоваскулярного методов лечения аневризмы брюшной аорты у пациентов с низкими и средними факторами риска
- Johnson K.W. Morbidity and mortality associated with abdominal aortic aneurysm repair: results from the Canadian aneurysm study//Current critical problem in Vascular Surgery. 1990. № 2. P. 248-255.
- Strachan D.P. Predictors of death from aortic aneurysm among middle -aged men: the Whitehall study//Br. J Surg. 1991. P. 401404.
- Дудкин Б.П., Бубкевич А.Ц., Воронцов В. В., и др. Оправдны ли одномоментные комбинированные и сочетанные операции у больных с аневризмой брюшного отдела аорты//Материалы XIII Международной конференции Российского общества ангиологов и сосудистых хирургов. М., 2005. С. 114-115.
- Покровский А.В., Дан В.Н., Златовчен А.М., Ильин С.А. Влияние кар-диального статуса и артериальной гипертензии на результаты лечения больных с аневризмами брюшной аорты старше 70 лет//Ангилогия и сосудистая хирургия. 2003. Т. 9 № 1. С. 71-75.
- Cheng S.W.K. Endovascular stent grafts: a new standart of treatment for aortic diseases//Medical Progress (Hong Kong Edition). 2005. Vol. 3. P. 115-120.
- Rutherford R.B., Krupski W.C., Current status of open, versus endovascular stent-graft repair of abdominal aortic aneurysm//J. Vasc. Surg. 2004. Vol. 39. № 5. P. 1129-1139.
- Cronenwett J.L. Endovascular aneurysm repair: important midterm results//Lancet. 2005. Vol. 365. № 9478. P. 2156-8.
- White G.H., Yu W., May J. et. al. Endoleak as a complication of endolu-minal grafting of abdominal aortic aneurysms: classification, incidence, diagnosis, and management//J. Endovasc. Surg. 1997. Vol. 4. № 2. P. 152-168.
- Mehta M., Sternbach Y., Taggert J.B., Kreienberg P.B., Roddy S.P., Paty P.S., Ozsvath K.J. J.//Vasc. Surg. 2010. № 52 (6). P. 1442.
- Becquemin J.P., Pillet J.C., Lescalie F., Sapoval M., Goueffic Y., Lermusiaux P., Steinmetz E., Marzelle J: A randomized controlled trial of endovascular aneurysm repair versus open surgery for abdominal aortic aneurysms in low-to moderate-risk patients//J. Vasc. Surg. 2011. Vol. 53. № 5. P. 1167-1173.e1.
- Rutherford R.B., Schermerhorn M.L., Cronenwett J.L. Abdominal Aortic and lliac Aneurysms//Vascular. Surgery. 2005 (6-th edition). P. 1420-1423.


