Сравнительная оценка результатов коронарного шунтирования в сочетании с методом экстракардиальной ревакуляризации миокарда у пациентов с диффузным поражением венечного русла
Автор: Борщев Г.Г., Миминошвили Л.Г., Зайниддинов Ф.А., Катков А.А., Ульбашев Д.С.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 2 т.19, 2024 года.
Бесплатный доступ
ИБС занимает главенствующее место среди сердечно-сосудистых причин смерти населения в РФ и во всем мире. У некоторых пациентов с ИБС проведение полной хирургической реваскуляризации затруднено из-за диффузного поражения коронарного русла, малого диаметра сосудов, выраженного кальциноза стенок артерий, дистального стенотически-окклюзионного поражения, высокого риска осложнений и тяжести клинического состояния по причине других сопутствующих заболеваний. Эффективность лечения таких больных до сих пор остается низкой. С целью преодоления этой проблемы Ю.Л. Шевченко разработал и внедрил в клиническую практику методику хирургической стимуляции экстракардиальной васкуляризации миокарда «ЮрЛеон». В настоящее время существуют ее разные модификации, позволяющие улучшить результаты лечения пациентов. Цель: сравнительная оценка результатов коронарного шунтирования, дополненного методикой ЮрЛеон II и ЮрЛеон III. Материалы и методы. В ретроспективное исследование включено 180 пациентов с диффузным поражением коронарного русла (мужчин — 127 (71%), женщин — 53 (29%) в возрасте от 50 до 70 лет, средний возраст — 65,6±4,65 лет), которые проходили лечение в Клинике грудной и сердечно-сосудистой хирургии имени Святого Георгия ФГБУ «НМХЦ имени Н.И. Пирогова» Минздрава России. Пациенты разделены на три группы: I группа (n = 60) — после коронарного шунтирования (КШ) (контрольная группа); II группа (n = 60) — после КШ, дополненного методикой ЮрЛеон II; III группа (n = 60) — после КШ, дополненного методикой ЮрЛеон III. Оценивалось клиническое состояние больных, данные ЭхоКГ, однофотонной эмиссионной компьютерной томографии миокарда, синхронизированной с ЭКГ (синхро-ОФЭКТ) и показатели качества жизни (опросник SF-36). Результаты. В отдаленном послеоперационном периоде во II и III группах по сравнению с I группой отмечено статистически значимое снижение функционального класса стенокардии (1 [1–2], 1 [1–2] против 2 [2–2], p<0,05); увеличение фракции выброса левого желудочка (59[54-62]% (II группа), 59[55-63]% (III группа) по сравнению с контрольной — 50 [47-53]%, p<0,05). По данным сцинтиграфии миокарда отмечено снижение показателя Summed Rest Score (4[3-7] балла (II группа), 4[2-8] балла (III группа) против 11[6-18] баллов (I группа), p<0,05); уменьшение показателя Summed Thickening Score (8[5-11] баллов (II группа), 7[5-8] баллов (III группа) по сравнению с контрольной — 10[8-14] баллов, p<0,05). Обследуемые больные через 12-36 месяцев после операции отличались по показателям качества жизни (SF-36): PF (74[66-80] балла (I группа), 86[80-92] баллов (II группа), 84 [78-90] балла (III группа), p<0,05); RP (76[70-82] баллов (I группа), 90[85-95] баллов (II группа), 92 [88-96] балла (III группа), p<0,05); BP (80[75-85] баллов (I группа), 90[85-95] баллов (II группа), 92[86-98] балла (III группа), p<0,05); PH (46[42-50] баллов (I группа), 58[54-62] баллов (II группа), 60[56-64] баллов (III группа), р<0,05). Заключение. Коронарное шунтирование, дополненное методом хирургической стимуляции экстракардиальной реваскуляризации у пациентов с ИБС и диффузным поражением коронарного русла, улучшает клиническое состояния больных, их качество жизни, повышает фракцию выброса левого желудочка, его перфузию и позволяет обеспечить дополнительное кровоснабжение миокарда в отдаленном послеоперационном периоде.
ИБС, диффузное поражение, реваскуляризация, неоангиогенез, ЮрЛеон
Короткий адрес: https://sciup.org/140307062
IDR: 140307062 | DOI: 10.25881/20728255_2024_19_2_19
Comparative evaluation of results of coronary bypass surgery in combination with extracardial myocardial revacularization in patients with diffuse coronary artery disease
Coronary heart disease (CHD) occupies a dominant place among the cardiovascular causes of death in the Russian Federation and around the world. In some patients with coronary heart disease, complete surgical revascularization is difficult due to diffuse damage to the coronary bed, small vessel diameter, pronounced calcification of the artery walls, distal stenotic-occlusive lesion, high risk of complications and severity of the clinical condition due to other concomitant diseases. The effectiveness of treatment of such patients still remains low. The effectiveness of treatment of such patients still remains low. In order to overcome this problem, Academician of the Russian Academy of Sciences Yu.L.Shevchenko developed and introduced into clinical practice the technique of surgical stimulation of extracardial myocardial vascularization «YurLeon». Currently, there are various modifications to improve the results of patient treatment. Aim: to compare the results of coronary bypass surgery, supplemented by the YurLeon II and YurLeon III. Materials and methods. The retrospective study included 180 patients with diffuse coronary artery disease (127 men (71%), 53 women (29%) aged 50 to 70 years, average age — 65.6±4.65 years) who were treated at the St. George Thoracic and Cardiovascular Surgery Clinic of the Federal State Budgetary Institution «National Medical and Surgical Center named after N.I. Pirogov» Ministry of Health of the Russian Federation. Patients were divided into three groups: Group I (n = 60) — after coronary artery bypass grafting (CABG) (control group); group II (n = 60) — after CABG supplemented by the YurLeon II; Group III (n = 60) — after CABG, supplemented by the YurLeon III. The clinical condition of patients, echocardiography data, gated-SPECT and quality of life indicators (questionnaire SF-36) were evaluated. Results. In the long-term postoperative period, in groups II and III, compared with group I, there was a statistically significant decrease in the functional class of angina pectoris (1 [1-2], 1 [1-2] versus 2[2-2], p<0.05); increased left ventricular ejection fraction (59[54-62]% (group II), 59[55-63]% (group III) compared to the control group — 50 [47-53]%, p<0.05). According to myocardial scintigraphy, there was a decrease in the «Summed Rest Score» (4[3-7] points (group II), 4[2-8] points (group III) versus 11[6-18] points (group I), p<0.05); a decrease in the «Summed Thickening Score» (8[5-11] points (group II), 7 [5-8] points (group III) compared to the control — 10 [8-14] points, p<0.05). The studied patients 12-36 months after surgery differed in terms of quality of life (SF-36): PF (74[66-80] points (group I), 86[80-92] points (group II), 84 [78-90] points (group III), p<0.05); RP (76 [70-82] points (group I), 90[85-95] points (group II), 92[88-96] points (group III), P<0.05); BP (80 [75-85] points (group I), 90[85-95] points (group II), 92[86-98] points (group III), P<0.05); PH (46[42-50] points (group I), 58[54-62] points (group II), 60 [56-64] points (group III), p<0.05). Conclusion. Coronary bypass surgery, supplemented by surgical stimulation of extracardial vascularization, in the patients with coronary artery disease and diffuse coronary artery disease improves the clinical condition of patients, their quality of life, increases the left ventricular ejection fraction, its perfusion and allows for additional blood supply to the myocardium in the long-term postoperative period.
Текст научной статьи Сравнительная оценка результатов коронарного шунтирования в сочетании с методом экстракардиальной ревакуляризации миокарда у пациентов с диффузным поражением венечного русла
Диффузное атеросклеротическое поражение коронарных артерий, выраженное изменение дистального русла, кальциноз и малый диаметр венечных сосудов у пациентов с ИБС осложняют техническое выполнение хирургической реваскуляризации миокарда, увеличивают количество послеоперационных осложнений, уменьшают выживаемость [1–5]. В целом качество жизни таких больных низкое, а медикаментозная терапия недостаточно эффективна [5]. В последние десятилетия количество пациентов с диффузным поражением венечного русла увеличивается, а их лечение по-прежнему остается ведущей проблемой современной кардиохирургии [6]. По данным многих исследований рутинное выполнение коронарного шунтирования (КШ) у таких пациентов малоэффективно и связанно с неполной реваскуляризацией [1; 5; 7]. Существует высокая вероятность ранней окклюзии трансплантата из-за плохого дистального кровотока, что приводит к периоперационным осложнениям с длительной потребностью в фармакологической и механической поддержке, а также к возможному летальному исходу [8].
Раньше такие пациенты считались неоперабельными, в настоящее время развиваются реконструктивные методики с выполнением эндартерэктомии и использованием микрохирургической техники [9]. Однако результаты подобного лечения зависят от опыта хирурга, а выполнение эндартерэктомии связано с увеличением риска периоперационного инфаркта миокарда и, как следствие, смерти от кардиальных причин в связи с тромбозом артерии в деэндотелизированном участке [10]. Многообещающими казались результаты использования трансмиокардиальной лазерной реваскуляризации миокарда (ТМЛР), предложенной M. Mirhoseini и M. Cayton ещё в 1981 г. [11], однако в более поздних исследованиях эти взгляды изменились [12; 13].
В 2007 г. Ю.Л. Шевченко внедрен в клиническую практику метод индукции непрямой реваскуляризации миокарда из околосердечных источников ( Патент на изобретение RU №2758024С1. Заявка №2021105731 ). Многими экспериментальными и клиническими исследованиями, подтверждена эффективность и безопасность подобного комплексного лечения больных ИБС с диффузным поражением коронарных артерий [14–18]. В статье продемонстрированы результаты дополнения КШ одной из основных модификаций методики ЮрЛеон в сравнении с изолированным выполнением прямой реваскуляризации у пациентов с диффузным поражением коронарного русла.
Материалы и методы
В ретроспективное исследование включено 180 пациентов с диффузным поражением коронарного русла (127 (71%) мужчин, 53 (29%) женщины, в возрасте от 50 до 70 лет, средний возраст — 65,6±4,65 лет), которые прохо- дили лечение в Клинике грудной и сердечно-сосудистой хирургии имени Св. Георгия ФГБУ «НМХЦ имени Н.И. Пирогова» Минздрава России.
Критерии включения в исследование:
-
• стенокардия напряжения III–IV ФК;
-
• резистентность к традиционной медикаментозной терапии и отсутствие возможности для эндоваскулярной реваскуляризации миокарда;
-
• отсутствие гемодинамически значимой патологии клапанного аппарата сердца;
-
• диффузное атеросклеротическое поражение коронарных артерий (задействовано два и более сегмента одной магистральной артерии, общей протяженностью поражения более 50% всей длины сосуда при наличии гемодинамически значимого сужения просвета и малым диаметром дистального русла (менее 2 мм));
-
• фракция выброса левого желудочка (ФВ ЛЖ) менее 50%.
Критерии невключения:
-
• аневризма ЛЖ;
-
• необходимость кардиальной ресинхронизирующей терапии;
-
• почечная и печеночная недостаточность;
-
• наличие тромбоза ЛЖ или предсердия;
-
• наличие онкозаболеваний.
Пациенты разделены на три группы, статистически значимо не различающиеся между собой (Табл. 1):
-
I группа (n = 60) — после КШ (контрольная группа);
-
II группа (n = 60) — после КШ, дополненного методикой ЮрЛеон II (КШ+ЮрЛеон II);
Табл. 1. Клинико-демографическая характеристика пациентов
|
Показатель |
Группа I n = 60 |
Группа II n = 60 |
Группа II n = 60 |
Значения p (критерий Краскела- Уоллиса) |
|
Пол, n (%) Мужской Женский |
41(69) 19(31) |
44(74) 16(26) |
42(70) 18(30) |
0,062 0,723 |
|
Средний возраст, лет (M±SD) |
64,8±4,2 |
66,7±4,8 |
65,8±5,7 |
0,122 |
|
Инфаркт миокарда в анамнезе, n (%) |
28(47) |
31(52) |
30(50) |
0,054 |
|
ФК стенокардии, n (%) III IV |
43(72) 17(28) |
45(76) 15(24) |
42(71) 18(29) |
0,093 0,081 |
|
SYNTAX Score, баллы (M±SD) |
29,4±5,6 |
31,2±3,4 |
30,3±4,8 |
0,322 |
|
Данные эхокардиографии |
||||
|
ФВ, % (Me [Q1–Q3]) |
40 [35-45] |
39 [36-44] |
40 [36-45] |
0,655 |
|
Данные сцинтиграфии миокарда |
||||
|
SRS, баллы (Me [Q1–Q3]) |
21 [19-22] |
19 [17-22] |
20 [18-21] |
0,605 |
|
STS, баллы (Me [Q1–Q3]) |
21 [20-23] |
22 [19-24] |
21 [19-24] |
0,899 |
Примечание : ЛЖ — левый желудочек; ФВ — фракция выброса;
ФК — функциональный класс; SRS — Summed Rest Score;
STS — Summed Thickening Score.

Борщев Г.Г., Миминошвили Л.Г., Зайниддинов Ф.А. и др.
СРАВНИТЕЛЬНАЯ ОЦЕНКА РЕЗУЛЬТАТОВ КОРОНАРНОГО ШУНТИРОВАНИЯ В СОЧЕТАНИИ С МЕТОДОМ ЭКСТРАКАРДИАЛЬНОЙ РЕВАКУЛЯРИЗАЦИИ МИОКАРДА У ПАЦИЕНТОВ С ДИФФУЗНЫМ ПОРАЖЕНИЕМ ВЕНЕЧНОГО РУСЛА
III группа (n = 60) — после КШ, дополненного методикой ЮрЛеон III (КШ+ЮрЛеон III).
Методика ЮрЛеон II
До операции выполняется заготовка обогащённой тромбоцитами плазмы крови пациента методом однократного центрифугирования. На интраоперационном этапе создается липидно-фибриновая матрица (источник мезенхимальных стволовых клеток и стимуляторов неоангиогенеза) по разработанной оригинальной методике. Проводится механическая обработка эпикарда и перикарда абразивным материалом с целью создания асептического воспаления. Полученная липидно-фибриновая матрица фиксируется на эпикарде. На 2 сутки в перикардиальную полость вводится стерильный дренажный аспират, полученный в течение первых 12 часов после операции и содержащий факторы стимуляции неоангиогенеза (Рис. 1).
Методика ЮрЛеон III
На интраоперационном этапе проводится обработка перикарда и эпикарда абразивным материалом (специальной перчаткой), выполняется субтотальная пери-кардэктомия, формируется медиастинальный жировой лоскут и фиксируется на поверхности сердца. На 2 сутки после операции через дополнительный перикардиальный дренаж вводится стерильный дренажный аспират, полученный в течение первых 12 часов после реваскуляризации и содержащий факторы стимуляции неоангиогенеза (Рис. 2).
Учитывались данные исследований, проведенных перед реваскуляризацией миокарда и в послеоперационном периоде через 6, 12, 24, 36 месяцев. Оценивались жалобы, данные анамнеза, клиническое состояние больных, результаты трансторакальной ЭхоКГ, синхронизированной с электрокардиограммой однофотонной эмиссионной компьютерной томографии миокарда с 99mTc-технетрилом (синхро-ОФЭКТ). Для изучения качества жизни был применен опросник SF-36.
Статистический анализ
Статистические расчеты проведены в программе Statistica 12 (StatSoft). Оценено соответствие данных нормальному распределению (критерии Шапиро-Уилка, Колмогорова-Смирнова). Показатели описательной статистики включали число наблюдений (n), среднее значение (М), стандартное отклонение (SD), медиану (Ме), нижний и верхний квартили [Q1–Q3]. При распределении, близком к нормальному, использован однофакторный дисперсионный анализ. В случаях, когда распределение отличалось от нормального, анализ выполнялся с помощью непараметрических критериев: Фридмана для связанных выборок, U-критерия Краскела-Уоллиса для независимых. Различия считали статистически значимыми при p<0,05.
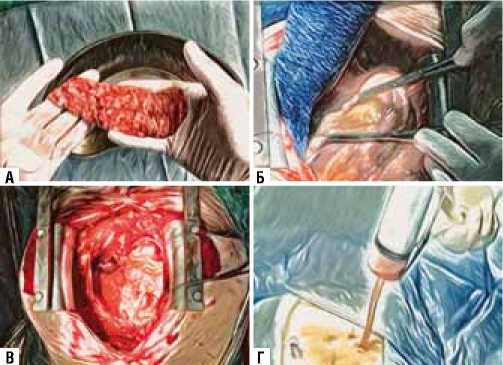
Рис. 1. Техника выполнения методики ЮрЛеон II. А — формирование липидно-фибриновой матрицы; Б — абразивная обработка перикарда и эпикарда; В — позиционирование и фиксация липидно-фибриновой матрицы на сердце; Г — введение стерильного дренажного аспирата в перикардиальную полость на 2 сутки после операции.
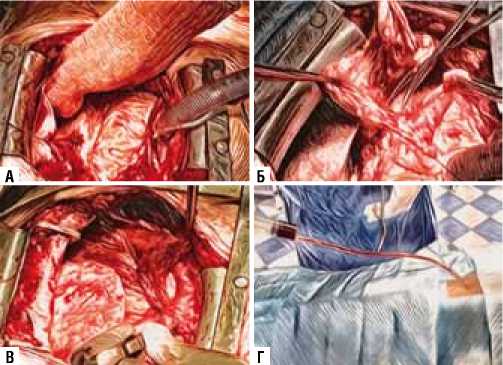
Рис. 2. Техника выполнения методики ЮрЛеон III. А — абразивная обработка перикарда и эпикарда; Б — формирование медиастинального жирового лоскута и субтотальная перикардэктомия; В — фиксация медиастинального жирового лоскута на сердце; Г — введение стерильного дренажного аспирата в перикардиальную полость на 2 сутки после операции через специальный дренаж.
Результаты
У всех пациентов отмечено улучшение клинического состояния в послеоперационном периоде. Через 6 месяцев ФК стенокардии уменьшился во всех группах с 3[3–4] до 2[2–2] (p<0,01). Через год отмечены статистические различия между группами: в I группе ФК стенокардии не изменился — 2[2–2], во II и III группах отмечено улучшение клинического состояния — 1[1–2] (p<0,01). В отдалённые сроки после операции в контрольной группе, по сравнению с другими, наблюдалась отрицательная динамика — увеличение ФК (через 36 месяцев: 2[2–2] класс (I группа), 1[1–2] класс (II группа), 1[1–2] класс (III группа), p<0,05), чаще отмечались случаи возврата стенокардии (Табл. 2).
Табл. 2. Изменение ФК стенокардии напряжения, (Me [Q1–Q3])
|
Сроки |
I группа |
II группа |
III группа |
Значение р между группами |
Значение р внутри групп |
|
Исходно |
3 [3–4] |
3 [3–4] |
3 [3–4] |
I–II–III 0,722; I–II 0,432; II–III 0,825; I–III 0,722 (критерий Краске-ла–Уоллиса) |
I <0,05 II <0,05 III <0,05 (критерий Фридмана) |
|
6 мес. |
2 [2–2] |
2 [2–2] |
2 [2–2] |
I–II–III 0,321; I–II 0,214 II–III 0,528; III 0,345 (критерий Краске-ла–Уоллиса) |
|
|
12 мес. |
2 [1–2] |
1 [1–2] |
1 [1–2] |
I–II–III <0,05; I–II <0,05 II–III 0,438; I–III <0,05 (критерий Краске-ла–Уоллиса) |
|
|
24 мес. |
2 [1–2] |
1 [1–2] |
1 [1–2] |
I–II–III <0,05; I–II <0,05 II–III 0,802; I–III <0,05 (критерий Краске-ла–Уоллиса) |
|
|
36 мес. |
2 [2–2] |
1 [1–2] |
1 [1–2] |
I–II–III <0,05; I–II <0,05 II–III 0,858; I–III <0,05 (критерий Краске-ла–Уоллиса) |

Изменение ФВ ЛЖ (по данным эхокардиографии)
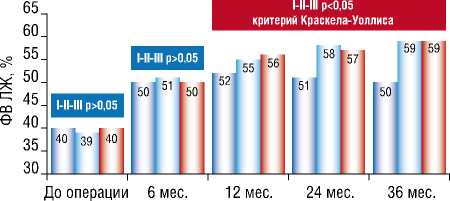
Исходно показатели всех групп пациентов статистически значимо не различались (p = 0,655, критерий Краскела–Уоллиса). В течение 6 месяцев у исследуемых отмечено увеличение ФВ ЛЖ в I группе с 40[35–45]% до 50[46–52]% (p<0,01), во II группе — с 39[36–44]% до 51[47–54]% (p<0,01), в III группе — с 40[36–45]% до 50[46–54]% (p<0,01). Между группами за этот период статистически значимых различий не выявлено. Однако в отдаленном послеоперационном периоде (12–36 месяцев) показатели различались: во II и III группах ФВ ЛЖ статистически значимо увеличилась до 59[54–62]% и 59[55–63]%, соответственно; в контрольной группе ФВ ЛЖ через 36 месяцев после операции составила 50[47–53]% (p<0,05, критерий Краскела–Уоллиса) (Рис. 3).
Изменение перфузии и сократительной функции миокарда ЛЖ (по данным синхро-ОФЭКТ)
Показатели всех групп пациентов до операции не отличались (p = 0,605, критерий Краскела–Уоллиса). Отмечается значимое снижение SRS при контрольном исследовании в течение 6 месяцев: в I группе с 21[19–22] до 10[8–13] баллов (p<0,01), во II группе — с 19[17–22] до 9[7–11] баллов (p<0,01), в III группе — с 20[18–21] до 10[8–12] баллов (p<0,01). В отдаленном послеоперационном периоде (12–36 месяцев) отмечены статистически значимые различия. Через 36 месяцев во II и III группах выявлено улучшение перфузии, показатель SRS снизился до 4[3–7] и 4[2–8] баллов, соответственно, (p<0,01), что значимо отличалось от результатов I группы — 11[6–18] баллов (p<0,05, критерий Краскела–Уоллиса) (Рис. 4).
При оценке показателя сегментного систолического утолщения миокарда (STS), демонстрирующего сокра-
Сроки
I || I группа II группа ■ I III группа
Рис. 3. Динамика ФВ ЛЖ в группах (по данным ЭхоКГ).
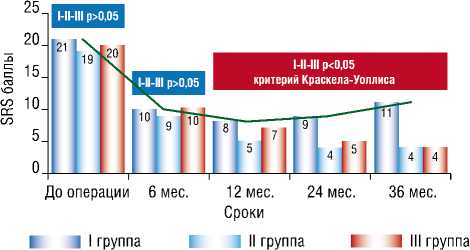
Рис. 4. Динамика SRS в группах (по данным синхро-ОФЭКТ).
тительную способность миокарда ЛЖ, оказалось, что исходно группы были сопоставимы по этому показателю (p = 0,899, критерий Краскела-Уоллиса). В течение 6 мес. после реваскуляризации у пациентов отмечена положительная динамика: в I группе снижение показателя STS с 21[20–23] до 12[10–13] баллов (p<0,01), во II группе — с 22[19–24] до 10[7–13] баллов (p<0,01), в III группе — с 21[19–24] до 8[7–12] баллов (p<0,01). Подобно предыдущим показателям отличия между группами выявлены в отдаленные сроки. Так, в течение 36 месяцев наблюдения STS изменился в I группе до 10[8–14] баллов, во II группе — до 8[5–11] баллов (p<0,01), в III группе — до 7[5–8] баллов (p<0,05, критерий Краскела–Уоллиса) (Рис. 5).
При определении и оценке объема гибернирован-ного миокарда в исследуемых группах, оказалось, что в отдаленные сроки (12–36 месяцев) в I группе выявлено 24[20–29]%, во II группе — 9[5–12]%, в III группе — 10[5–15]% гибернированных зон миокарда ЛЖ.
Оценка качества жизни
Выявлено улучшение качества жизни (согласно опроснику SF–36) у пациентов всех групп. Значимые различия отмечены по следующим показателям:
-
• «Физическое функционирование» (PF): в I группе выявлено увеличение с 28[22–34] до 74[66–80] баллов (p<0,01), во II группе — с 26[20–32] до 86[80–92] баллов (p<0,01), в III группе — с 27 [21–33] до 84 [78–90] баллов (p<0,01);

Борщев Г.Г., Миминошвили Л.Г., Зайниддинов Ф.А. и др.
СРАВНИТЕЛЬНАЯ ОЦЕНКА РЕЗУЛЬТАТОВ КОРОНАРНОГО ШУНТИРОВАНИЯ В СОЧЕТАНИИ С МЕТОДОМ ЭКСТРАКАРДИАЛЬНОЙ РЕВАКУЛЯРИЗАЦИИ МИОКАРДА У ПАЦИЕНТОВ С ДИФФУЗНЫМ ПОРАЖЕНИЕМ ВЕНЕЧНОГО РУСЛА
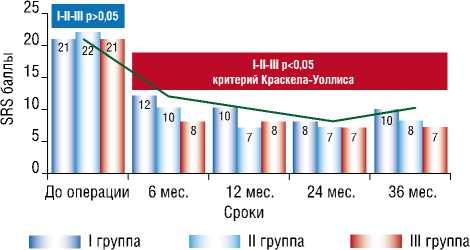
Рис. 5. Динамика STS в группах (по данным синхро-ОФЭКТ).
-
• «Ролевое функционирование, обусловленное физическим состоянием» (RP): в I группе — с 16[10–22] до 76[70–82] баллов (p<0,01), во II группе — с 17[10–24] до 90[85–95] баллов (p<0,01), в III группе — с 15 [10–20] до 92 [88–96] баллов (p<0,01);
-
• «Интенсивность боли» (BP): в I группе — с 24[16–32] до 80[75–85] баллов (p <0,01), во II группе — с 22 [14–30] до 90[85–95] баллов (p<0,01), в III группе — с 25 [20–30] до 92[86–98] баллов (p<0,01).
Выявлено статистически значимое различие между группами по общему показателю качества жизни («Физический компонент здоровья» PH) через 12–36 месяцев после реваскуляризации: 46[42–50] баллов в I группе, 58[54–62] баллов во II группе, 60[56–64] баллов в III группе (p<0,05, критерий Краскела-Уоллиса).
Обсуждение
В настоящее время нет достаточной доказательной базы и общепринятых национальных рекомендаций по хирургическому лечению пациентов с диффузным поражением коронарного русла. Коронарная эндартероэкто-мия в некоторых случаях позволяет получить удовлетворительные результаты лечения больных, которым невозможно добиться полной реваскуляризации другими методами [9], но важно отметить, что эта методика связана с высоким риском развития инфаркта миокарда в перио-перационном периоде, причинами которого, возможно, является активация коагуляционного каскада из-за отсутствия эндотелия на ранних сроках, а также пролиферация миоцитов и соединительной ткани в более позднем периоде, поэтому после эндартерэктомии необходимо строго следовать рекомендациям по антитромбоци-тарной терапии [19].
С момента первых публикаций ТМЛР стала предметом серьезных споров из-за противоречивых результатов эффективности и безопасности ее применения, а также отсутствия объяснений возможных механизмов реваскуляризации. Наблюдаемое во многих исследованиях улучшение клинического состояния пациентов, их качества жизни подвержено высокому риску систематической ошибки и может быть объяснено с точки зрения эффекта плацебо [12]. По данным многих исследо- ваний проведение ТМЛР не влияет на увеличение перфузии и функции миокарда [20–22]. Различий в выживаемости пациентов после выполнения этой методики в сравнении с контрольной группой обнаружено не было, а в некоторых наблюдениях отмечается даже увеличение послеоперационной летальности, поэтому риски, связанные с проведением ТМЛР, перевешивают потенциальную пользу [23]. По мнению ряда ученых, качество доказательств эффективности методики считается низким [12].
В проведенном Meier P. с соавт. мета-анализе 12 исследований с участием 6529 пациентов сделаны выводы, что развитые коллатерали играют важнейшую защитную роль и снижают риск смерти. Так, у пациентов с хорошо развитым внутри- и внесердечным коллатеральным кровотоком риск смерти уменьшался на 36% [24]. Поэтому возможность стимуляции формирования дополнительных коллатералей особенно необходима у пациентов с диффузным поражением коронарных артерий, при невозможности полной прямой реваскуляризации без риска осложнений.
Введение в клиническую практику Ю.Л. Шевченко хирургического метода индукции экстракардиальной реваскуляризации миокарда «ЮрЛеон» открыло новые возможности для лечения больных с диффузным поражением коронарного русла [5].
В нашем исследовании отмечается значимое улучшение клинического состояния, качества жизни и увеличение ФВ ЛЖ у пациентов после дополнения КШ методикой ЮрЛеон в отдаленном послеоперационном периоде по сравнению с контрольной группой. Увеличение показателей сократимости обусловлено значимым улучшением перфузии и восстановлением гибернированного миокарда за счет дополнительного экстракардиального кровоснабжения, особенно в тех зонах, где шунтирование не было выполнено по разным причинам.
Сравнивая между собой модификации одного хирургического метода стимуляции экстракардиальной реваскуляризации миокарда, предложенного Ю.Л. Шевченко, следует отметить, что значимых различий в их эффективности не выявлено, все исследуемые результаты были сопоставимы, однако ЮрЛеон II — технически более сложный метод и требует дополнительного времени для создания липидно-фибринового матрикса (Табл. 3).
Концентрат факторов свертывания крови и тромбоцитов, который находится в липидно-фибриновой матрице приводит к ускорению процессов тромбообразования в зоне хирургической агрессии в ближайшем послеоперационном периоде, способствуя снижению кровоточивости повреждённых тканей и, соответственно, уменьшению отделяемого по дренажам. У пациентов с диффузным поражением коронарного русла и прогнозируемой большой кровопотерей (поздняя отмена антитром-боцитарной терапии перед хирургическим вмешательством, экстренная операция, бимаммарное шунтирова-
Табл. 3. Сравнение техники выполнения двух разных модификаций метода хирургической стимуляции непрямой реваскуляризации
|
Этапы |
ЮрЛеон II |
ЮрЛеон III |
|
Дооперационный |
Заготовка обогащённой тромбоцитами плазмы крови |
– |
|
Интраоперационный |
Извлечение жировой ткани из переднего средостения и эпикарда. Обработка перикарда и эпикарда абразивным материалом. Формирование и фиксация липидно–фибринового матрикса к сердцу. Установка дополнительного перикардиального дренажа |
Обработка перикарда и эпикарда абразивным материалом. Формирование медиастинального жирового лоскута с субтотальной пери-кардэктомией. Установка дополнительного перикардиального дренажа. |
|
Послеоперационный |
Введение на 2 сутки после операции дренажного аспирата, содержащего факторы роста сосудов. |
Введение на 2 сутки после операции дренажного аспирата, содержащего факторы роста сосудов. |
ние, наличие других рисков кровотечений), КШ целесообразно дополнять методикой ЮрЛеон II с применением липидно-фибриновой матрицы.
Ограничениями данного исследования является отсутствие рандомизации, ослепления, а также одноцентровой и ретроспективный характер наблюдения. Отсутствовала возможность анализа данных всех пациентов в установленные сроки, часть пациентов выбыла из исследования. При выявлении новых экстракарди-альных источников существует проблема визуализации, в исследование не включены морфологические данные подтверждения формирования новых экстракардиаль-ных коллатералей. В настоящее время необходимо продолжение исследований.
Заключение
Стимуляция экстракардиального неоангиогенеза при проведении КШ имеет большое значение для обеспечения дополнительного кровоснабжения миокарда в долгосрочном послеоперационном периоде, параллельно с уже сформированными прямыми сосудистыми анастомозами. Достоверно лучшие показатели сократимости и перфузии миокарда, стабильно высокое качество жизни больных в отдаленном послеоперационном периоде позволяют считать КШ, дополненное методикой ЮрЛеон II и ЮрЛеон III, операцией выбора у пациентов с ИБС и диффузным коронарным атеросклерозом.
Список литературы Сравнительная оценка результатов коронарного шунтирования в сочетании с методом экстракардиальной ревакуляризации миокарда у пациентов с диффузным поражением венечного русла
- Акчурин Р.С., Ширяев А.А., Васильев В.П., и др. Диффузное поражение коронарных артерий в коронарной хирургии (аналитический обзор) // Клиническая и экспериментальная хирургия. Журнал имени академика Б.В. Петровского. — 2018. — №6(4). — С.75-81. doi: 10.24411/2308-1198-2018-14011.
- Белаш С.А., Барбухатти К.О. Реконструктивные операции при диффузном коронарном атеросклерозе без эндартерэктомии // Инновационная медицина Кубани. — 2019. — №15(3). — С.53-61. doi: 10.35401/2500-0268-2019-15-3-53-61.
- Белаш С.А., Барбухатти К.О., Шевченко С.С. и др. Отдаленные результаты реваскуляризации миокарда в сочетании с эндартерэктомией при диффузном коронарном атеросклерозе // Грудная и сердечно-сосудистая хирургия. — 2021. — №3(63). — С.188-194. doi: 10.24022/0236-2791-2021-63-3-188-194.
- Курбанов С.К., Власова Э.Е., Саличкин Д.В. и др. Госпитальные и годичные результаты коронарного шунтирования при диффузном поражении коронарных артерий // Кардиологический вестник. — 2019. — №14(1). — С.60-66. doi: 10.17116/Cardiobulletin20191401160.
- Шевченко Ю.Л., Борщев Г.Г. Экстракардиальная реваскуляризация миокарда у больных ИБС с диффузным поражением коронарного русла. — М.: Издательство НМХЦ им. Н.И. Пирогова, 2022.
- Brown RA, Shantsila E, Varma C, et al. Epidemiology and pathogenesis of diffuse obstructive coronary artery disease: the role of arterial stiffness, shear stress, monocyte subsets and circulating mircoparticles. Ann Med. 2016; 48(6): 444-455. doi: 10.1080/07853890.2016.1190861.
- Lozano I, Capin E, de la Hera JM, et al. Diffuse Coronary Artery Disease Not Amenable to Revascularization: Long-term Prognosis. Rev Esp Cardiol (Engl Ed). 2015; 68(7): 631-3. doi: 10.1016/j.rec.2015.02.013.
- Ramasubrahmanyam G, Panchanatheeswaran K, Varma Kalangi TK, et al. Surgical management of diffusely diseased coronary arteries. Indian J Thorac Cardiovasc Surg. 2019; 35(3): 453-460. doi: 10.1007/s12055-018-0776-2.
- Ширяев А.А., Акчурин Р.С., Васильев В.П., и др. Годовые результаты коронарного шунтирования у пациентов с диффузным поражением коронарных артерий // Кардиология и сердечно-сосудистая хирургия. — 2021. — №14(5). — С.413 419. doi: 10.17116/ kardio202114051413.
- Nishigawa K, Fukui T, Yamazaki M, et al. Ten-Year Experience of Coronary Endarterectomy for the Diffusely Diseased Left Anterior Descending Artery. Ann Thorac Surg. 2017; 103(3): 710-716. doi: 10.1016/j.athoracsur. 2016.11.028.
- Mirhoseini M, Cayton M. Revascularization of the heart by laser. J. Microsurg. 1981; 2: 253-260.
- Briones E, Lacalle JR, Marin-Leon I, et al. Transmyocardial laser revascularization versus medical therapy for refractory angina. Cochrane Database Syst Rev. 2015; 2015(2): CD003712. doi: 10.1002/14651858.CD003712.
- Schofield PM, McNab D. National Institute for Health and Clinical. NICE evaluation of transmyocardial laser revascularisation and percutaneous laser revascularisation for refractory angina. Heart. 2010; 96(4): 312-313. doi: 10.1136/hrt.2009.185769.
- Шевченко Ю.Л., Борщев Г.Г., Ульбашев Д.С. Отдаленные результаты коронарного шунтирования, дополненного хирургической стимуляцией экстракардиальной васкуляризации миокарда, у пациентов с диффузным поражением коронарного русла // Комплексные проблемы сердечно-сосудистых заболеваний. — 2023. — №12(1). — С.160-171. doi: 10.17802/2306-1278-2023-12-1-160-171.
- Shevchenko YuL, Borshchev GG, Ulbashev DS. Surgical technique of angiogenesis stimulation (extracardial myocardial revascularization) in patients with coronary artery disease. Cardiology and Cardiovascular Medicine. 2022; 6: 529-535. doi: 10.26502/fccm.92920295.
- Шевченко Ю.Л., Байков В.Ю., Борщев Г.Г. и др. Миниинвазивная торакоскопическая техника стимуляции экстракардиальной васкуляризации миокарда методом ЮрЛеон при диффузном поражении коронарного русла при ИБС // Вестник НМХЦ им. Н.И. Пирогова. — 2022. — Т.17. — №2. — С.103-106. doi: 10.25881/ 20728255_2022_17_2_103.
- Shevchenko YuL, Borshchev GG. Effect of extracardial myocardial revascularization on long-term results of surgical treatment of patients with coronary heart disease. The 12th Annual International Congress of Cardiology-2023. Lisbon, Portugal. 17-19 July 2023.
- Шевченко Ю.Л. Влияние экстракардиальной реваскуляризации миокарда (методика ЮрЛеон) на отдаленные результаты хирургического лечения пациентов с ишемической болезнью сердца // Кардиологический вестник. — 2023. — №18. — С.164.
- Heo W, Min HK, Kang DK, et al. Long Segmental Reconstruction of Diffusely Diseased Left Anterior Descending Coronary Artery Using Left Internal Thoracic Artery with Extensive Endarterectomy. Korean J Thorac Cardiovasc Surg. 2015; 48(4): 285-288. doi: 10.5090/kjtcs.2015.48.4.285.
- van der Sloot JA, Huikeshoven M, Tukkie R, et al. Transmyocardial revascularization using an XeCl excimer laser: results of a randomized trial. Ann Thorac Surg. 2004; 78(3): 875-882. doi: 10.1016/ j.athoracsur.2004.02.073.
- Iwanski J, Knapp SM, Avery R, et al. Clinical outcomes meta-analysis: measuring subendocardial perfusion and efficacy of transmyocardial laser revascularization with nuclear imaging. J Cardiothorac Surg. 2017; 12(1): 37. doi: 10.1186/s13019-017-0602-8.
- Tasse J, Arora R. Transmyocardial revascularization: peril and potential. J Cardiovasc Pharmacol Ther. 2007; 12(1): 44-53. doi: 10.1177/ 1074248406297640.
- Peterson ED, Kaul P, Kaczmarek RG, et al. From controlled trials to clinical practice: monitoring transmyocardial revascularization use and outcomes. J Am Coll Cardiol. 2003; 42(9): 1611-1616. doi: 10.1016/j.jacc.2003.07.003.
- Meier P, Hemingway H, Lansky AJ, et al. The impact of the coronary collateral circulation on mortality: a meta-analysis. Eur Heart J. 2012; 33(5): 614-621. doi: 10.1093/eurheartj/ehr308.


