Сравнительные результаты герниопластики у больных с большими послеоперационными вентральными грыжами
Автор: Чарышкин А.Л., Фролов Андрей Андреевич
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Хирургия
Статья в выпуске: 1, 2014 года.
Бесплатный доступ
Исследовано 123 пациента с грыжами передней брюшной стенки срединной локализации (ширина грыжевых ворот более 15 см), которые сформировались после верхнесрединной, средне-срединной, или средне-нижнесрединной лапаротомии в период с 2003 по 2012 г. Средний возраст оперированных больных составил 64,2±9,3 года. В зависимости от методики операции все исследуемые пациенты были разделены на три группы. Между группами не было выявлено значимых различий по полу, возрасту, характеру сопутствующей патологии. Предложенный способ герниопластики у больных с большими послеоперационными вентральными грыжами повышает качество жизни и снижает риск рецидива заболевания в отдаленном послеоперационном периоде в сравнении с методами inlay-sublay и onlay.
Послеоперационная вентральная грыжа, способ герниопластики
Короткий адрес: https://sciup.org/14112968
IDR: 14112968 | УДК: 617.55-089.844
Gernioplasty comparative results at patients with big postoperative ventral hernias
123 patients with hernias of a forward belly wall, median localization are investigated, width of hernial gate more than 15 cm which were created after average and median laparotomy during the period from 2003 to 2012. Average age of the operated patients made 64,2±9,3 years. Depending on an operation technique all studied patients were divided into three groups. Between groups it wasn't revealed significant distinctions on a sex, age, character of accompanying pathology. The offered way hernioplasty at patients with big postoperative ventral hernias increases quality of life and reduces risk of recurrence of a disease in the remote postoperative period in comparison with the inlay-sublay and on lay methods.
Текст научной статьи Сравнительные результаты герниопластики у больных с большими послеоперационными вентральными грыжами
Введение. Послеоперационные вентральные грыжи (ПОВГ) возникают у 2–20 % больных, перенесших лапаротомию [1, 2, 5, 6].
Летальность после плановых грыжесечений ПОВГ составляет 0,2–0,3 %, после экстренных – от 2 до 8 % [3–5, 8]. У больных старше 60 лет с большими послеоперационными вентральными грыжами и сопутствующими заболеваниями летальность и количество послеоперационных осложнений достигают 16–20 % [7, 9, 10]. У больных после лапаротомии при наличии нескольких факторов риска и сопутствующей патологии возрастает вероятность развития вентральных грыж [11, 12].
Количество больных с осложнениями со стороны послеоперационной раны достигает 18,6 % при применении сетчатых полимерных протезов [7–10].
Абдоминальный компартмент-синдром у больных с послеоперационными вентральными грыжами является одним из грозных осложнений, указывающих на необходимость дальнейшего поиска методов его лечения [3, 4, 6].
Цель исследования. Улучшение хирургического лечения больных с большими послеоперационными вентральными грыжами путем применения разработанного способа герниопластики с использованием имплантата.
Материалы и методы. Работа выполнена в соответствии с основными направлениями программы научных исследований ФГБОУ ВПО «Ульяновский государственный университет» на кафедре факультетской хирургии.
Исследование ретроспективное, проспективное, поисковое. Сроки проведения исследования 2003–2012 гг.
Критерии включения: возраст 18 лет и старше; пол мужской и женский; наличие грыжи передней брюшной стенки, имеющей срединную локализацию, ширину грыжевых ворот более 15 см, сформировавшуюся после верхнесрединной, средне-срединной, или средненижнесрединной лапаротомии; информированное согласие пациентов на операцию.
Критерии исключения: возраст младше 18 лет; послеоперационная грыжа иной локализации, чем срединная (боковая, правой подвздошной области); ширина грыжевых ворот менее 15 см; отказ больного от выполнения операции; инфаркт миокарда; острые нарушения мозгового кровообращения.
В работе представлены результаты обследования и лечения 123 пациентов с ПОВГ, оперированных в хирургических отделениях МУЗ УГКБСМП и ГУЗ УОКБ № 1 г. Ульяновска.
Распределение больных по возрасту и полу представлено в табл. 1.
Распределение пациентов по возрасту и полу, чел. (%)
Таблица 1
|
Младше 45 лет |
45–59 лет |
60 лет и старше |
|
|
Мужчины |
1 (0,8) |
12 (9,8) |
10 (8,1) |
|
Женщины |
9 (7,3) |
38 (30,9) |
53 (43,1) |
|
Всего |
10 (8,1) |
50 (40,7) |
63 (51,2) |
Из табл. 1 видно, что мужчин – 23 (18,7 %), женщин – 100 (81,3 %), преобладание женщин в исследовании соответствует данным литературы, посвященной данной проблеме. Средний возраст оперированных больных составил 64,2±9,3 года.
В работе использовалась SWR-классификация, разработанная J.P. Chevrel и A.M. Rath, принятая на XXI Международном конгрессе герниологов в Мадриде (1999) и рекомендованная в нашей стране на V конференции «Актуальные вопросы герниологии» [3].
Все исследуемые пациенты были с грыжами W4 по SWR-классификации, рецидивные грыжи выявлены у 38 (30,9 %) больных, рецидивирующие – у 17 (13,8 %).
Исследуемые пациенты имели несколько сопутствующих заболеваний, из которых чаще наблюдали гипертоническую болезнь – у 71 (57,7 %) больного, ожирение и повышенную массу тела – у 53 (43,1 %), патологию сердца – у 44 (35,8 %), варикозную болезнь вен нижних конечностей – у 63 (51,2 %), заболевания печени – у 32 (26 %) пациентов.
Для решения поставленных задач были использованы клинико-лабораторные, рентгенологические, эндоскопические, УЗ, статистические методы исследования.
Для выявления динамики изменений внутрибрюшного давления (ВБД) измерение проводили посредством непрямой интравези-кальной тензометрии, начиная с 1-х сут после операции.
Все операции выполняли под эндотрахе-альным наркозом. В качестве сетчатого имплантата во всех группах использовали полипропиленовую сетку, для фиксации имплантата – шовный материал пролен.
В зависимости от методики операции все исследуемые пациенты были разделены на три группы. Первую группу составили 40 па- циентов, оперированных по разработанному способу (проспективное исследование), автор А.Л. Чарышкин (патент РФ на изобретение № 2422105, по заявке № 2010108656, приоритет от 9.03.2010; зарегистрировано 27.06.2011; бюллетень № 18). Метод заключается в следующем. Под эндотрахеальным наркозом с искусственной вентиляцией легких производят иссечение старого послеоперационного рубца с излишками кожи 1 (рис. 1) и при необходимости удаляют жировой фартук. Осторожно вскрывают грыжевой мешок, производят герниолапаротомию. Затем выполняют интраабдоминальный этап операции (разделение сращений, ревизия брюшной полости, по показаниям – выполнение симультанных операций).
По окружности грыжевых ворот создают карман 2 (рис. 1) под мышечно-апоневротическим слоем 3 на протяжении 6–8 см в пред-брюшинном пространстве, отделяя брюшину 4 от мышечно-апоневротического слоя 3 . Рассеченную брюшину 4 грыжевых ворот ушивают непрерывным рассасывающимся швом край в край. На ушитую брюшину 4 помещают сетчатый эндопротез таким образом, чтобы он по окружности занимал сформированный карман 2 и отступал на 6–8 см от края грыжевых ворот.
После имплантации сетчатого эндопротеза в сформированный карман 2 его подшивают к мышечно-апоневротическому слою 3 сзади наперед по периметру симметрично восемью П-образными швами 6 (рис. 2), отступив от края грыжевых ворот на 6–8 см, при этом П-образные швы 6 проходят через мышечно-апоневротический слой 3, нити не завязывают (рис. 2). После этого грыжевые ворота ушивают узловыми швами край в край нерассасывающимися нитями. Ушивать начинают с дистального угла грыжевых ворот, накладывают 2–4 узловых шва, завязывают, затем ушивают проксимальный угол 2–4 узловыми швами, завязывают. Затем завязывают симметрично крайние верхние и нижние ранее наложенные П-образные швы 6, фиксирующие сетчатый эндопротез 5 к мышечно-апоневротическому слою 3. Осуществляют полное симметричное расправление сетчатого эндопротеза 5. Далее накладывают остальные узловые швы, закрывающие грыжевые ворота, таким образом, чтобы лигатуры 7 проходили через сетчатый эндопротез 5. Сетчатый эндопротез 5 фиксируют по средней линии лигатурами 7, проведенными через мышечно-апоневротический слой 3, на всем протяжении грыжевых ворот (рис. 2). По мере закрытия грыжевых ворот узловыми швами последовательно завязывают вначале угловые верхние и нижние П-образные швы. После полного закрытия грыжевых ворот завязывают средние ранее наложенные П-образные швы 6, фиксирующие сетчатый эндопротез 5 к мышечно-апоневротическому слою 3, расположенные справа и слева от грыжевых ворот. Швы накладывают на кожу.
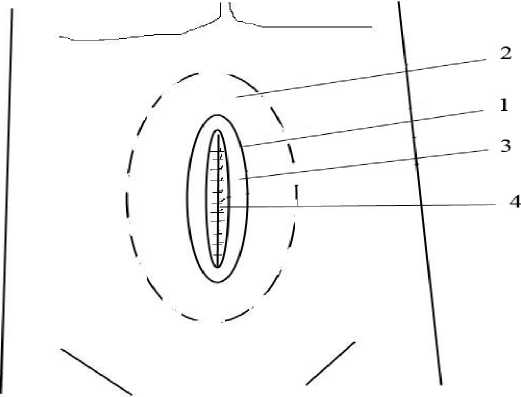
Рис. 1. Иллюстрация рассеченной кожи 1 , кармана 2 под мышечно-апоневротическим слоем 3 и ушитой брюшины
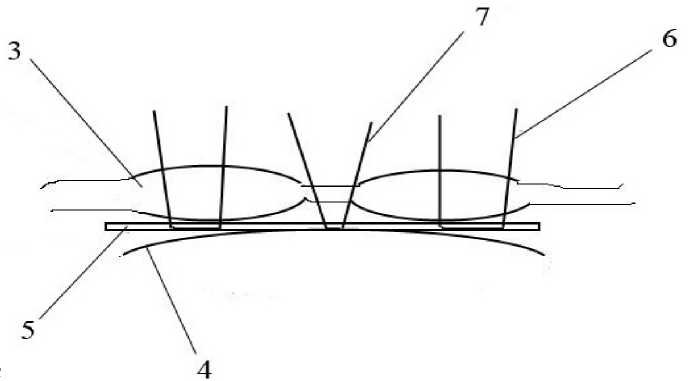
Рис. 2. Иллюстрация подшитого сетчатого эндопротеза 5 П-образными швами 6 .
Сетчатый эндопротез 5 зафиксирован по средней линии к мышечно-апоневротическому слою лигатурами 7
Вторую группу составили 30 пациентов, оперированных по методике В.И. Белоконева inlay-sublay (ретроспективное исследование). Третью группу составили 53 пациента, оперированных по методике В.В. Жебровского onlay (ретроспективное и проспективное исследование).
Все больные давали информированное добровольное согласие на хирургическое вмешательство и проводимое в послеоперационном периоде лечение.
Статистическая обработка результатов производилась с помощью пакета программ Statistica 6. При сравнении полученных параметров использовался t-критерий Стьюдента для независимых парных выборок и χ2-тест. Статистически значимыми признавались различия с уровнем доверительной вероятности не менее 95 % с учетом поправки Бонферро-ни для множественных сравнений.
Результаты и обсуждение. Продолжительность операции во второй группе больных составила 80,1±30,4 мин, в третьей группе – 67,5±24,1 мин. В первой группе длительность выполнения разработанного способа операции составила 63,1±20,4 мин, что на 17 мин меньше, чем во второй группе, и на 4,4 мин меньше, чем в третьей группе (p<0,05).
Продолжительность послеоперационной боли (табл. 2) во второй группе больных – 6,5±0,3 сут, в третьей группе – 5,9±0,5 сут. В первой группе продолжительность боли составила 4,9±0,3 сут, что на 1,6 сут меньше, чем во второй группе, и на 1 сут меньше, чем в третьей группе (p<0,05).
Таблица 2
|
Первая группа (n=40) |
Вторая группа (n=30) |
Третья группа (n=53) |
|
4,9±0,3* |
6,5±0,3 |
5,9±0,5 |
Примечание. * – статистически значимые различия со второй и третьей группами (p<0,05).
Продолжительность послеоперационной боли в группах больных, сут
Во второй группе больных местные воспалительные осложнения со стороны послеоперационной раны выявлены у 9 (30 %), в третьей группе – у 16 (30,2 %) больных. В первой группе местные осложнения наблюдались у 3 (7,5 %) пациентов, что на 22,5 % меньше, чем во второй группе, и на 22,7 % меньше, чем в третьей группе (p<0,05).
Лейкоцитарный индекс интоксикации
(ЛИИ) в третьей группе больных на вторые сутки составил 6,1±0,3; во второй группе – 5,7±0,1, а в первой группе – 4,5±0,2, что значительно меньше, чем в группах сопоставления (р<0,05). На пятые сутки ЛИИ в первой группе был ниже, чем у больных второй и третьей групп, а на десятые сутки во всех группах данный показатель был в пределах нормы (табл. 3).
Таблица 3
|
Группы больных |
ЛИИ после операции |
||
|
2-е сут |
5-е сут |
10-е сут |
|
|
Первая группа (n=40) |
4,5±0,2* |
3,9±0,1* |
2,1±0,1 |
|
Вторая группа (n=30) |
5,7±0,1 |
5,2±0,2 |
2,3±0,2 |
|
Третья группа (n=53) |
6,1±0,3 |
5,1±0,3 |
2,2±0,2 |
Примечание. * – достоверные различия со второй и третьей группами (p<0,05).
Динамика ЛИИ в послеоперационном периоде
Во второй группе больных внутрибрюш-ное давление после операции повышалось до 21,2±0,9 мм рт. ст., в третьей группе – до 22,1±1,3 мм рт. ст., что соответствует 3 сте- пени идиопатической артериальной гипотензии (ИАГ), в первой группе показатели ВБД после операции повышались до 2 степени ИАГ – 19,1±1,0 мм рт. ст. (p<0,05) (табл. 4).
Показатели ВБД после операции, мм рт. ст.
Таблица 4
|
Первая группа (n=40) |
Вторая группа (n=30) |
Третья группа (n=53) |
|
19,1±1,0* |
21,2±0,9 |
22,1±1,3 |
Примечание. * – достоверные различия со второй и третьей группами (p<0,05).
При подготовке к оперативному вмешательству анализы биохимии крови у пациентов во всех группах были в пределах нормы.
У 32 пациентов из 3 исследуемых групп на 2-е сут после операции выявлен холестаз (табл. 5).
Таблица 5
Количество больных с холестазом после операции в исследуемых группах, чел. (%)
|
Первая группа (n=40) |
Вторая группа (n=30) |
Третья группа (n=53) |
|
10 (25) |
8 (26,7) |
14 (26,4) |
Клинические проявления холестаза у пациентов после герниопластики были следующими: чувство тяжести в правом подреберье, горечь во рту, при осмотре наблюдалась незначительная иктеричность склер.
Уровень общего билирубина увеличивался в среднем до 45,4±6,3 мкмоль/л у 32 исследуемых пациентов с холестазом на 2-е сут после операции, билирубинемия была преимущественно за счет прямой фракции билирубина. По группам на 2-е сут после операции показатели общего билирубина распределились следующим образом: в первой группе – 46,1±2,3 мкмоль/л, во второй – 45,8±4,1 мкмоль/л, в третьей – 45,0±6,0 мкмоль/л. Снижение общего билирубина происходило на 10-е сут послеоперационного периода у всех больных, когда он составил в среднем 24,3±3,2 мкмоль/л. По группам снижение общего билирубина на 10-е сут после операции было следующим: в первой группе – 22,1±3,0 мкмоль/л, во второй – 25,1±3,5 мкмоль/л, в третьей – 24,9±2,1 мкмоль/л.
Показатели АлАТ и АсАТ у пациентов с холестазом по группам на 2-е сут после операции: в первой группе – 108,1±10,2 и 74,1±12,8; во второй – 118,1±14,3 и 70,2±10,5; в третьей – 110,4±16,8 и 71,2±14,1 соответственно.
Снижение АлАТ и АсАТ у пациентов с холестазом по группам происходило на 10-е сут после операции и составило: в первой группе – 83,1±10,4 и 39,2±12,1; во второй – 80,3±14,1 и 40,4±14,2; в третьей – 85,1±9,2 и 43,3±10,5 соответственно.
На ультразвуковом исследовании у 32 пациентов с холестазом признаков обструкции желчевыводящих путей не выявлено.
После операции уровень внутрибрюшно-го давления повышался у всех 32 пациентов с холестазом до 3-й степени внутрибрюшной гипертензии, что в среднем составило 21,6±1,2 мм рт. ст. Показатели уровня внут-рибрюшной гипертензии у пациентов с холестазом по группам представлены в табл. 6.
Таблица 6
|
Первая группа (n=10) |
Вторая группа (n=8) |
Третья группа (n=14) |
|
21,0±1,5 |
21,8±0,9 |
21,9±1,8 |
Показатели ВБД после операции у больных с холестазом, мм рт. ст.
Таким образом, проведенные клинические наблюдения и биохимические исследования показали наличие взаимосвязи внутри-брюшной гипертензии и развития холестаза в раннем послеоперационном периоде у больных с послеоперационными вентральными грыжами после герниопластики. По нашему мнению, причиной холестаза у исследуемых пациентов послужили заболевания печени (хронический вирусный гепатит и жировой гепатоз) как предрасполагающие факторы, а 3-я степень внутрибрюшной гипертензии после операции – как производящий фактор.
По данным УЗИ, скопление жидкости различной толщины вокруг имплантата во второй группе наблюдали у 19 (63,3 %) пациентов, в третьей группе – у 46 (86,8 %) пациентов, а в первой группе – только у 5 (12,5 %) больных, что значительно меньше, чем у пациентов в группах сравнения (p<0,01).
Послеоперационный койко-день во второй группе больных составил 16,4±4,2 сут, в третьей группе – 15,9±5,3 сут, а в первой группе – 13,2±2,1 сут, что на 3,2 сут меньше, чем во второй группе, и на 2,7 сут меньше, чем в третьей группе (p<0,05).
В третьей группе был 1 (1,9 %) летальный исход. Больной умер от острой сердечно-сосудистой недостаточности на фоне инфаркта миокарда. В остальных группах летальных исходов не было.
Все пациенты обследованы в сроки от 6 мес. до 1 года.
В первой группе больных после выполнения герниопластики по разработанному способу рецидива заболевания обнаружено не было, во второй группе рецидив выявлен у 2 (6,7 %) пациентов, в третьей группе – у 5 (9,4 %).
При изучении отдаленных результатов по трехбалльной системе оценки во второй группе хорошие результаты отмечены у 21 (70 %) больного, удовлетворительные – у 7 (23,3 %), неудовлетворительные – у 2 (6,7 %), в третьей группе хорошие отдаленные результаты наблюдались у 36 (67,9 %) больных, удовлетворительные – у 12 (22,7 %), неудовлетворительные – у 5 (9,4 %).
В первой группе хорошие отдаленные результаты отмечены у 34 (85 %) больных, что на 15 % больше, чем во второй, и на 17,1 % больше, чем в третьей группе. Удовлетворительные результаты в первой группе получены у 6 (15 %) пациентов, неудовлетворительных результатов не было.
Нами изучены показатели качества жизни (КЖ) у всех исследуемых больных (табл. 7, 8).
Результаты исследования качества жизни показывают, что у пациентов второй группы после герниопластики inlay-sublay и третьей группы, оперированных по методу onlay, в отдаленном послеоперационном периоде отмечается снижение параметров качества жизни. При анализе полученных результатов выявлены достоверно более высокие суммарные показатели физического и психического здоровья у пациентов после герниопластики разработанным способом.
Отдаленные результаты качества жизни (через 1 год после операции) у пациентов, оперированных разработанным способом, показывают стабильность восстановленных клинических показателей: они сохраняют те же улучшенные значения, что наблюдались через шесть месяцев после выполненной операции.
Очевидно, что полученный положительный эффект является результатом применения разработанного способа герниопластики при больших и гигантских послеоперационных грыжах, который изолирует имплантат от подкожно-жировой клетчатки, брюшной полости и способствует снижению риска развития осложнений, рецидива заболевания и улучшению качества жизни.
Таблица 7
|
Параметры КЖ |
Результаты в группах |
|||
|
Первая группа (n=40) |
Вторая группа (n=30) |
Третья группа (n=53) |
||
|
Компонент здоровья |
Шкала |
|||
|
Физический |
ФФ |
84,7* |
80,7 |
80,2 |
|
РФФ |
74,2* |
68,1 |
68,2 |
|
|
Б |
72,1* |
67,2 |
67,3 |
|
|
ОЗ |
58,8* |
52,1 |
51,7 |
|
|
Психологический |
Ж |
59,4* |
53,2 |
53,5 |
|
СФ |
73,1* |
61,7 |
62,3 |
|
|
РЭФ |
72,1* |
67,1 |
67,4 |
|
|
ПЗ |
62,9* |
52,2 |
53,4 |
|
Примечание. * – статистически значимые различия со второй и третьей группами (p<0,05).
Таблица 8
|
Параметры КЖ |
Результаты в группах |
|||
|
Первая группа (n=40) |
Вторая группа (n=30) |
Третья группа (n=53) |
||
|
Компонент здоровья |
Шкала |
|||
|
Физический |
ФФ |
85,1* |
81,1 |
80,3 |
|
РФФ |
74,3* |
68,5 |
68,1 |
|
|
Б |
72,4* |
67,2 |
67,5 |
|
|
ОЗ |
59,1* |
52,3 |
51,9 |
|
|
Психологический |
Ж |
60,1* |
53,5 |
53,7 |
|
СФ |
73,2* |
61,9 |
62,4 |
|
|
РЭФ |
72,4* |
67,1 |
67,6 |
|
|
ПЗ |
63,1* |
52,4 |
53,5 |
|
Примечание. * – статистически значимые различия со второй и третьей группами (p<0,05).
Качество жизни пациентов в отдаленном послеоперационном периоде через 6 мес. после операции (опросник SF-36)
Качество жизни пациентов в отдаленном послеоперационном периоде через 1 год после операции (опросник SF-36)
Выводы:
-
1. Причинами холестаза у больных с большими послеоперационными вентральными грыжами послужили хронический вирусный гепатит и жировой гепатоз как предрасполагающие факторы и 3 степень внутри-брюшной гипертензии после операции – как производящий фактор.
-
2. Разработанный способ герниопласти-ки у больных с большими послеоперационными вентральными грыжами изолирует имплантат от подкожно-жировой клетчатки и брюшной полости, что снижает риск развития местных воспалительных осложнений со стороны послеоперационной раны на 22,5 % в сравнении с методами inlay-sublay и onlay.
-
3. Предложенный способ герниопласти-ки у больных с большими послеоперационными вентральными грыжами повышает суммарные показатели физического и психического здоровья у пациентов в отдаленном послеоперационном периоде в сравнении с методами inlay-sublay и onlay.
-
1. Белоконев В. И. Принципы техники пластики и результаты лечения послеоперационных вентральных грыж срединной локализации / В. И. Белоконев, З. В. Ковалева, С. Ю. Пушкин // Герниология. – 2004. – № 2. – С. 6–12.
-
2. Егиев В. Н. Атлас оперативной хирургии грыж / В. Н. Егиев, К. В. Лядов, П. К. Воскресенский. – М. : Медпрактика – М., 2003. – 228 с.
-
3. Ермолов А. С. О современной классификации послеоперационных грыж живота / А. С. Ермолов, А. В. Упырев, В. А. Ильичев // Герниоло-гия. – 2006. – № 3. – С. 16–17.
-
4. Жебровский В. В. Хирургия грыж живота и эвентраций / В. В. Жебровский. – М. : МИА, 2009. – 440 с.
-
5. Мирзабекян Ю. Р. Прогноз и профилактика раневых осложнений после пластики передней брюшной стенки по поводу послеоперационной вентральной грыжи / Ю. Р. Мирзабекян, С. Р. Добровольский // Хирургия. – 2008. – № 1. – С. 66–71.
-
6. Профилактика осложнений хирургического лечения послеоперационных рецидивных вентральных грыж : методич. рекомендации / С. Р. Добровольский [и др.]. – М., 2007. – 24 с.
-
7. Тимошин А. Д. Концепция хирургического лечения послеоперационных грыж передней брюшной стенки / А. Д. Тимошин, А. В. Юрасов, А. Л. Шестаков // Герниология. – 2004. – № 1. – С. 5–10.
-
8. Усов С. А. Проблема инфекционных осложнений аллопластики инцизионных грыж брюшной стенки : обзор зарубежной литературы последнего десятилетия / С. А. Усов, В. Г. Носов // Бюллетень ВСНЦ СО РАМН. – 2006. – № 6 (52). – С. 221–225.
-
9. Чарышкин А. Л. Метод герниопластики послеоперационных срединных вентральных грыж / А. Л. Чарышкин, М. Н. Васильев // Хирургия. – 2011. – № 9. – С. 15–18.
-
10. Чарышкин А. Л. Способ герниопластики больших и гигантских послеоперационных вентральных грыж / А. Л. Чарышкин, А. А. Фролов // Фундаментальные исследования. – 2013. – № 9 (6). – С. 127–131.
-
11. Study comparing the complication rates between laparoscopic and open ventral hernia repairs / J. M. McGreevy [et al.] // Surg. Endosc. – 2003. – Vol. 17, № 11. – P. 1778–1780.
-
12. Use of prosthetic materials in incisional hernias: our clinical experience / L. Napolitano [et al.]
-
// G. Chir. – 2004. – Vol. 25, № 4. – P. 141–145.
GERNIOPLASTY COMPARATIVE RESULTSAT PATIENTS WITH BIG POSTOPERATIVE VENTRAL HERNIAS
A.L. Charyshkin, A.A. Frolov
Ulyanovsk State University
Список литературы Сравнительные результаты герниопластики у больных с большими послеоперационными вентральными грыжами
- Белоконев В. И. Принципы техники пластики и результаты лечения послеоперационных вентральных грыж срединной локализации/В. И. Белоконев, З. В. Ковалева, С. Ю. Пушкин//Герниология. -2004. -№ 2. -С. 6-12.
- Егиев В. Н. Атлас оперативной хирургии грыж/В. Н. Егиев, К. В. Лядов, П. К. Воскресенский. -М.: Медпрактика -М., 2003. -228 с.
- Ермолов А. С. О современной классификации послеоперационных грыж живота/А. С. Ермолов, А. В. Упырев, В. А. Ильичев//Герниология. -2006. -№ 3. -С. 16-17.
- Жебровский В. В. Хирургия грыж живота и эвентраций/В. В. Жебровский. -М.: МИА, 2009. -440 с.
- Мирзабекян Ю. Р. Прогноз и профилактика раневых осложнений после пластики передней брюшной стенки по поводу послеоперационной вентральной грыжи/Ю. Р. Мирзабекян, С. Р. Добровольский//Хирургия. -2008. -№ 1. -С. 66-71.
- Профилактика осложнений хирургического лечения послеоперационных рецидивных вентральных грыж: методич. рекомендации/С. Р. Добровольский [и др.]. -М., 2007. -24 с.
- Тимошин А. Д. Концепция хирургического лечения послеоперационных грыж передней брюшной стенки/А. Д. Тимошин, А. В. Юрасов, А. Л. Шестаков//Герниология. -2004. -№ 1. -С. 5-10.
- Усов С. А. Проблема инфекционных осложнений аллопластики инцизионных грыж брюшной стенки: обзор зарубежной литературы последнего десятилетия/С. А. Усов, В. Г. Носов//Бюллетень ВСНЦ СО РАМН. -2006. -№ 6 (52). -С. 221-225.
- Чарышкин А. Л. Метод герниопластики послеоперационных срединных вентральных грыж/А. Л. Чарышкин, М. Н. Васильев//Хирургия. -2011. -№ 9. -С. 15-18.
- Чарышкин А. Л. Способ герниопластики больших и гигантских послеоперационных вентральных грыж/А. Л. Чарышкин, А. А. Фролов//Фундаментальные исследования. -2013. -№ 9 (6). -С. 127-131.
- Study comparing the complication rates between laparoscopic and open ventral hernia repairs/J. M. McGreevy [et al.]//Surg. Endosc. -2003. -Vol. 17, № 11. -P. 1778-1780.
- Use of prosthetic materials in incisional hernias: our clinical experience/L. Napolitano [et al.]//G. Chir. -2004. -Vol. 25, № 4. -P. 141-145.


