Сравнительные результаты различных принципов этапной гибридной реваскуляризации миокарда у пациентов с предварительным стентированием венечных артерий и эндоваскулярной коррекцией венечного русла после коронарного шунтирования
Автор: Шевченко Ю.Л., Ермаков Д.Ю., Вахрамеева А.Ю., Баранов А.В.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 2 т.19, 2024 года.
Бесплатный доступ
Обоснование: Этапная гибридная реваскуляризация миокарда (ГРМ) является эффективным методом лечения больных ИБС. В настоящий момент не определен оптимальный порядок выполнения хирургического и эндоваскулярного этапов вмешательства в рамках ГРМ у пациентов с атеросклеротическим поражением КА. Цель: Сравнить ближайшие и отдаленные результаты этапной ГРМ в объеме коронарного шунтирования (КШ) с предшествующим стентированием КА и ЧКВ с последующим КШ. Методы: На ретроспективной основе в исследование включено 97 больных ИБС, которым была проведена этапная ГРМ в ФГБУ «НМХЦ им. Н.И. Пирогова» МЗ РФ с 2014 по 2020 гг. В I группе 48 пациентам было выполнено КШ с последующим ЧКВ (КШ+ЧКВ); во II группе 49 больным сначала было проведено стентирование КА, затем — КШ (ЧКВ+КШ). Средний временной промежуток между 1 и 2 этапами ГРМ составил 87,5±10,6 дней, общий период наблюдения — 36,9±5,8 месяцев. Результаты: Группа КШ+ЧКВ показала несколько более оптимальные 3-летние результаты по сравнению с когортой ЧКВ+КШ в отношении РИМ (20,1% против 24,5%, p = NS) и НЦП (18,5% против 22,3%, p = NS). Число зарегистрированных случаев НВТ у пациентов I и II групп было сходным — 23,1% против 24,0% (p = NS). Частота ИМ, ОНМК, смерти от всех причин достоверно не отличалась в обеих группах и составила 3 (6,3%), 2 (4,2%) и 3 (6,1%), и 3 (6,1%), 3 (6,3%) и 2 (4,1%) случаев в I и II когорте, соответственно (p = NS). Общий удельный вес MACE через 36,9±5,8 мес наблюдения составил 16,7% против 16,3% у пациентов КШ+ЧКВ и ЧКВ+КШ (p = NS). Заключение: Подход к ГРМ с выполнением КШ первым этапом перед ЧКВ показывает несколько большую эффективность и обеспечивает аналогичную безопасность по сравнению со стратегией «ЧКВ до КШ».
Ишемическая болезнь сердца, гибридная реваскуляризация миокарда, коронарное шунтирование, чрескожное коронарное вмешательство
Короткий адрес: https://sciup.org/140307066
IDR: 140307066 | DOI: 10.25881/20728255_2024_19_2_4
Comparative results of various principles of staged hybrid myocardial revascularization in patients with preliminary coronary artery stenting and percutaneous coronary intervention after coronary bypass graft
Background: Staged hybrid coronary revascularization (HCR) is an effective treatment method for patients with CAD. At the moment, the optimal procedure for performing the surgical and endovascular stages of intervention within the framework of HCR in patients with atherosclerotic lesions of the coronary artery (CA) has not been determined. Purpose: To compare the immediate and long-term results of staged HCR in the scope of coronary artery bypass grafting (CABG) with previous CA stenting and PCI followed by CABG. Methods: On a retrospective basis, the study included 97 patients with CAD who underwent staged HCR at the Pirogov Center (Moscow, Russia) from 2014 to 2020. In group I, 48 patients underwent CABG followed by PCI (CABG+PCI); in group II, 49 patients first underwent coronary artery stenting, then CABG (PCI+CABG). The average time interval between the 1st and 2nd stages of breastfeeding was 87.5±10.6 days, the total observation period was 36.9±5.8 months. Results: The CABG+PCI cohort showed slightly better 3-year outcomes compared to the PCI+CABG cohort in terms of relapse of myocardial ischemia (20.1% vs. 24.5%, p = NS) and TLR (18.5% vs. 22.3 %, p = NS). The number of registered cases of VGF in patients of groups I and II was similar — 23.1% versus 24.0% (p = NS). The incidence of MI, stroke, death from all causes did not differ significantly in both groups and was 3 (6.3%), 2 (4.2%) and 3 (6.1%), and 3 (6.1%), 3 (6.3%) and 2 (4.1%) cases in cohorts I and II, respectively (p = NS). The overall proportion of MACE after 36.9±5.8 months of follow-up was 16.7% versus 16.3% in patients with CABG+PCI and PCI+CABG (p = NS). Conclusion: The approach to HCR with CABG performed as the first stage before PCI shows slightly greater effectiveness and provides similar safety compared to the “PCI before CABG” strategy.
Текст научной статьи Сравнительные результаты различных принципов этапной гибридной реваскуляризации миокарда у пациентов с предварительным стентированием венечных артерий и эндоваскулярной коррекцией венечного русла после коронарного шунтирования
Инвазивная прямая реваскуляризация миокарда (ПРМ) — высокоэффективный способ лечения больных ИБС, который позволяет снизить функциональный класс стенокардии напряжения (СН) и, при определенных условиях, не только увеличить продолжительность жизни пациентов, но и улучшить ее качество [1]. Методы ПРМ давно закрепились в мировой и отечественной врачебной практике, доказав свое превосходство над изолированным применением оптимальной медикаментозной те-

Шевченко Ю.Л., Ермаков Д.Ю., Вахрамеева А.Ю., Баранов А.В.
СРАВНИТЕЛЬНЫЕ РЕЗУЛЬТАТЫ РАЗЛИЧНЫХ ПРИНЦИПОВ ЭТАПНОЙ ГИБРИДНОЙ РЕВАСКУЛЯРИЗАЦИИ МИОКАРДА У ПАЦИЕНТОВ С ПРЕДВАРИТЕЛЬНЫМ СТЕНТИРОВАНИЕМ ВЕНЕЧНЫХ АРТЕРИЙ И ЭНДОВАСКУЛЯРНОЙ КОРРЕКЦИЕЙ ВЕНЕЧНОГО РУСЛА ПОСЛЕ КОРОНАРНОГО ШУНТИРОВАНИЯ рапии [1]. Чрескожное коронарное вмешательство (ЧКВ) и коронарное шунтирование (КШ), являясь альтернативными способами инвазивной коррекции поражений венечного русла, имеют свои преимущества и недостатки.
К преимуществам ЧКВ относятся: малая инвазив-ность оперативного вмешательства, короткий восстановительный период, низкий риск инфекционных осложнений, отсутствие потребности в наркотизации пациента. Среди недостатков эндоваскулярной реваскуляризации КА можно отметить более высокую частоту развития неблагоприятных сердечно-сосудистых событий (MACE) в отдаленном периоде после вмешательства у больных с анатомически тяжелым поражением венечного русла и сахарным диабетом (СД) [2; 3].
В свою очередь, КШ позволяет обеспечить хорошие отдаленные резутаты операции у больных ИБС с комор-бидной патологией и стволовым, трехсосудистым поражением КА с высоким баллом шкалы Syntax и Syntax II, а также увеличить выживаемость пациентов с низкой фракцией выброса ЛЖ (ФВ) [1–3]. К недостаткам технологии КШ можно отнести необходимость проведения эндотра-хеального наркоза и экстракорпорального кровообращения в ряде ситуаций, риск кровопотери и отсутствие возможности выполнения максимальной реваскуляризации миокарда из-за анатомических особенностей коронарного русла [4].
Методом, объединяющим преимущества и нивелирующим недостатки обоих способов ПРМ, явилась гибридная реваскуляризация миокарда (ГРМ). ГРМ подразумевает выполнение доступного объема шунтирования КА преимущественно без применения экстракорпорального кровообращения и с обязательным формированием маммаро-коронарного анастомоза (МКШ) левой внутренней грудной артерии (ЛВГА) с ПНА. Иные поражения КА корректируются с помощью ЧКВ с использованием стентов с лекарственным покрытием (СЛП) одномоментно (в условиях гибридной операционной) или в несколько этапов. Основным предиктором позднего достижения комбинированной конечной точки MACE больными после КШ является использование анастомоза ЛВГА-ПНА. 20-летние результаты наблюдения демонстрируют повышение выживаемости пациентов с применением ВГА на 4,4 года дольше, чем при использовании только венозных трансплантатов; меньшее количество повторных операций, поздних инфарктов, ранних рецидивов стенокардии, а также более низкими показатели летальности [5; 6].
Так, выполнение КШ с использованием только ЛВГА в бассейне ПНА («aorta no-touch technique») или с дополнительным осуществлением минимального объема венозного шунтирования позволяет значимо снизить потребность в экстракорпоральном кровообращении, уменьшить риск кровопотери, длительность оперативного вмешательства и количество послеоперационных осложнений [7]. Эндоваскулярная реваскуляризация других бассейнов КА обеспечивает хорошие отдаленные результаты в отношении реци- дива ишемии (РИМ) и MACE, избавляя от необходимости расширения объема хирургических манипуляций при КШ.
Проведение одномоментной ГРМ возможно только в ограниченном количестве кардиохирургических стационаров, оснащенных гибридной операционной. Этапная ГРМ остается эффективной стратегией, обеспечивающей необходимый результат у больных ИБС, обладающей, однако, малой доказательной базой [8; 9; 10]. При этом не определены преимущества и недостатки подходов к этапной ГРМ с предварительным ЧКВ перед КШ и хирургической реваскуляризацией миокарда с последующим стентированием КА. В данной работе мы поставили перед собой задачу сравнить между собой обе методики ПРМ.
Материалы и методы
На ретроспективной основе в исследование было включено 97 пациентов с атеросклеротическим поражением КА, которым была проведена этапная ГРМ. КШ было выполнено в отделении сердечно-сосудистой хирургии, ЧКВ — в отделении рентгенохирургических методов диагностики и лечения Клиники грудной и сердечно-сосудистой хирургии им. Св. Георгия НМХЦ им. Н.И. Пирогова с 2014 по 2020 гг. Пациенты были разделены на 2 группы: в I группу вошли больные ИБС, которым в рамках ГРМ в качестве первого этапа реваскуляризации было выполнено КШ с последующим ЧКВ (КШ+ЧКВ); во II — больные, которым сначала было проведено стентирование КА, затем — коронарное шунтирование (ЧКВ+КШ).
По клинической характеристике пациенты обеих групп между собой достоверно не отличались, за исключением частоты стенокардии напряжения ФК IV (p = 0,02) (Табл. 1). Возраст больных в первой и второй группе в среднем составил 63,3±4,2 и 62,8±5,1 лет соответственно, среди испытуемых преобладали мужчины (66,7% и 69,4%). ОИМ в анамнезе имели 10 (20,8%) и 14 (28,6%) больных, средняя ФВ в группах КШ+ЧКВ и ЧКВ+КШ была 52,8±4,9% и 51,1±5,3%. Большинство па-
Табл. 1. Клиническая характеристика больных
|
Показатель |
Группа I КШ+ЧКВ (n = 48) |
Группа II ЧКВ+КШ (n = 49) |
p |
|
|
Возраст, годы (M±SD) |
63,3±4,2 |
62,8±5,1 |
NS |
|
|
Мужской пол, n (%) |
32 (66,7) |
37 (69,4) |
NS |
|
|
Курение, n (%) |
34 (70,8) |
37 (75,5) |
NS |
|
|
Артериальная гипертензия, n (%) |
41 (85,4) |
39 (79,6) |
NS |
|
|
ХОБЛ, n (%) |
27 (56,3) |
32 (65,3) |
NS |
|
|
ФВ, % (M±SD) |
52,8±4,9 |
51,1±5,3 |
NS |
|
|
ХСН, n (%) |
6 (12,5) |
7 (14,3) |
NS |
|
|
СД, n (%) |
11 (22,9) |
9 (18,4) |
NS |
|
|
ОИМ в анамнезе, n (%) |
10 (20,8) |
14 (28,6) |
NS |
|
|
ОНМК в анамнезе, n (%) |
3 (6,3) |
2 (4,1) |
NS |
|
|
Мультифокальный атеросклероз, n (%) |
4 (8,3) |
3 (6,1) |
NS |
|
|
ФК СН |
ФК II, n (%) |
7 (14,6) |
10 (20,4) |
NS |
|
ФК III, n (%) |
36 (75,0) |
39 (79,6) |
NS |
|
|
ФК IV, n (%) |
5 (10,4) |
0 (0) |
<0,05 |
|

Шевченко Ю.Л., Ермаков Д.Ю., Вахрамеева А.Ю., Баранов А.В.
СРАВНИТЕЛЬНЫЕ РЕЗУЛЬТАТЫ РАЗЛИЧНЫХ ПРИНЦИПОВ ЭТАПНОЙ ГИБРИДНОЙ РЕВАСКУЛЯРИЗАЦИИ МИОКАРДА У ПАЦИЕНТОВ С ПРЕДВАРИТЕЛЬНЫМ СТЕНТИРОВАНИЕМ ВЕНЕЧНЫХ АРТЕРИЙ И ЭНДОВАСКУЛЯРНОЙ КОРРЕКЦИЕЙ ВЕНЕЧНОГО РУСЛА ПОСЛЕ КОРОНАРНОГО ШУНТИРОВАНИЯ циентов в обеих группах страдали СН ФК III (75% больных КШ+ЧКВ и 79,6% испытуемых в группе II).
У 48 больных первой группы при первичной КАГ было выявлено 189 поражений КА, в группе II (n = 49) — 201 значимый стеноз (p = NS). По частоте выявления поражений различных анатомических локализаций больные обеих групп достоверно не отличались (p = NS). У всех пациентов были зарегистрированы гемодинамически значимые стенозы ПНА — 48 (28,2%) и 39 (27,8%) поражений в I и II группах, соответственно. Поражение ствола ЛКА встречалось у 5 (10,4%) больных КШ+ЧКВ и 6 (12,2%) испытуемых с первичным ЧКВ. Основные стволы ОА и ПКА были стенозированы в 19 (11,2%), 22 (12,5%) и 32 (18,8%), 30 (17,0%) случаях в группах с первичным и вторичным КШ, соответственно. В первой и второй когортах частота выявления поражения ЗМЖА при правовенечном и сбалансированном типе коронарного кровоснабжения составила 8,8% против 10,2% (Табл. 2). Все пациенты имели поражение двух и более основных стволов эпикардиальных артерий.
На дооперационном этапе селективная многопроекционная коронароангиография выполнялась на ангиографической установке Toshiba Infinix (Япония) по стандартному протоколу с оценкой полученных результатов двумя независимыми специалистами. Для диагностики ишемии миокарда 73 (88%) пациентам выполнялись нагрузочные пробы. Однофотонная эмиссионная томография миокарда синхронизированная с ЭКГ с 99mТс-технетрилом (Синхро-ОФЭКТ) у 60 (72,3%) больных проводилась по стандартному протоколу: нагрузка-покой. Стресс-ЭхоКГ с физической нагрузкой — у 13 (15,7) больных.
Всем исследуемым пациентам до реваскуляризации была назначена ацетилсалициловая кислота (АСК) (100 мг/сут.) для пожизненного приема. Анти-тромбоцитарная терапия также включала клопидогрел (нагрузочная доза 300 мг, если не принимался ранее; далее 75 мг/сут. в течение 12 мес.). Послеоперационная медикаментозная терапия в обязательном порядке включала статины, ингибиторы ангиотензинпревращающего фермента либо блокаторы рецепторов ангиотензина II, и соответствовала актуальным клиническим рекомендациям.
Критериями включения в исследование явились: стабильная ИБС II–IV ФК; ишемия миокарда, доказанная при помощи нагрузочных проб; двух- и трехсосудистое атеросклеротическое поражение КА с промежуточным и высоким баллом по шкале анатомического риска Syntax.
Критерии исключения из исследования: больные ИБС с сочетанным гемодинамически значимым поражением КА и клапанов сердца, аневризмой ЛЖ, требующей реконструкции, выраженной недостаточностью функции почек, печени, онкологической патологией.
Целью настоящего исследования стало сравнение ближайших и отдаленных результатов этапной гибридной реваскуляризации миокарда в объеме коронарного шунтирования с предшествующим стентированием КА и ЧКВ с последующим КШ.
Табл. 2. Ангиографическая характеристика больных
|
Показатель |
Группа I КШ+ЧКВ (n = 48) |
Группа II ЧКВ+КШ (n = 49) |
p |
|
|
Всего поражений, n (%) |
170 (100,0) |
176 (100,0) |
NS |
|
|
Ствол ЛКА n (%) |
5 (2,9) |
6 (3,4) |
NS |
|
|
Система ПНА |
ПНА, n (%) |
48 (28,2) |
49 (27,8) |
NS |
|
ДА, n (%) |
21 (12,4) |
23 (13,1) |
NS |
|
|
ИМА, n (%) |
2 (1,2) |
2 (1,1) |
NS |
|
|
Система ОА |
ОА, n (%) |
19 (11,2) |
22 (12,5) |
NS |
|
АТК, n (%) |
12 (7,1) |
11 (6,3) |
NS |
|
|
ЗБВ, n (%) |
5 (2,9) |
4 (2,3) |
NS |
|
|
ЗМЖА, n (%) |
5 (2,9) |
7 (4,0) |
NS |
|
|
Система ПКА |
ПКА, n (%) |
32 (18,8) |
30 (17,0) |
NS |
|
ЗБВ, n (%) |
6 (3,5) |
4 (2,3) |
NS |
|
|
ЗМЖА, n (%) |
15 (8,8) |
18 (10,2) |
NS |
|
|
Поражение B2/C, n (%) |
21 (43,8) |
19 (38,8) |
NS |
|
|
Syntax Score, значение (M±SD) |
27,8±5,23 |
28,2±6,1 |
NS |
|
Результаты исследования
Всего в первой и второй группе больным на I этапе ГРМ было скорректировано 87 (51,2%) и 76 (43,2%) поражений КА, соответственно. Больным КШ+ЧКВ выполнялось КШ с наложением 87 (100%) шунтов, из которых 47 (54%) представляли собой маммарные, а 40 (46%) — аутовенозные кондуиты. Шунтирование ПНА с формированием анастомоза ЛВГА-ПНА проводилось 47 (97,9%) испытуемым, 1 пациенту осуществлено КШ ПНА с использованием аутовены по причине гипоплазии ВГА. Всего было сформировано 40 дистальных анастомозов с использованием аутовены: ДА — 10 (11,5%), ИМА — 1 (1,1%), 13 (14,9%) — в системе ОА, 15 (17,2%) — в системе ПКА.
Во второй группе на I этапе ГРМ было имплантировано 125 (100%) стентов. Длина стентированного участка в среднем составила 22,7±7,4 мм, диаметр имплантированного стента — 2,93±0,63 мм. Большинству пациентов запланированный объем ЧКВ был выполнен за один этап эндоваскулярного вмешательства, количество этапов составило 1,37±0,5. Рентгенохирургическая реваскуляризация ПНА и ствола ЛКА целенаправленно не проводилась. ДА и ИМА были стентированы в 15 (8,5%) и 2 (1,1%) случаях, соответственно. При эндоваскулярной реваскуляризации бассейна ОА было выполнено КС в зоне 27 (35,5%) пораженных сегментов КА, при ЧКВ в бассейне ПКА — 32 (42,1%) стенозов.
Продолжительность операции КШ в I группе в среднем составила 271,2±56,9 мин., интраоперационная кровопотеря — 479,5±73,1 мл. Потребность в инотропной и вазопрессорной поддержке возникла у 9 (18,8%) и 26 (54,2%), соответственно. Большинству пациентов (n = 37, 77,1%) реваскуляризация была выполнена на работающем сердце. Продолжительность ЧКВ во II группе была 108,4±36,7 мин., вмешательство осуществлялось трансрадиально у 38 (77,6%) пациентов.
В раннем послеоперационном периоде потребность в инотропной и вазопрессорной поддержке составила 10,4% и 45,8%, соответственно. Кровотечение, которое

Шевченко Ю.Л., Ермаков Д.Ю., Вахрамеева А.Ю., Баранов А.В.
СРАВНИТЕЛЬНЫЕ РЕЗУЛЬТАТЫ РАЗЛИЧНЫХ ПРИНЦИПОВ ЭТАПНОЙ ГИБРИДНОЙ РЕВАСКУЛЯРИЗАЦИИ МИОКАРДА У ПАЦИЕНТОВ С ПРЕДВАРИТЕЛЬНЫМ СТЕНТИРОВАНИЕМ ВЕНЕЧНЫХ АРТЕРИЙ И ЭНДОВАСКУЛЯРНОЙ КОРРЕКЦИЕЙ ВЕНЕЧНОГО РУСЛА ПОСЛЕ КОРОНАРНОГО ШУНТИРОВАНИЯ
Табл. 3. Результаты I этапа гибридной реваскуляризации
|
Показатель |
Группа I КШ+ЧКВ (n = 48) |
Группа II ЧКВ+КШ (n = 49) |
p |
|
Скорректировано поражений, n (%) |
86 (51,2) |
76 (43,2) |
NS |
|
Маммаро-коронарное шунтирование, n (%) |
47 (54,0) |
– |
|
|
Венозные шунты, n (%) |
39 (46,0) |
– |
|
|
Имплантировано СЛП, n (%) |
– |
125 (100,0) |
|
|
Длина стентированного участка, мм (M±SD) |
– |
22,7±7,4 |
|
|
Диаметр имплантированного стента, мм (M±SD) |
– |
2,93±0,63 |
|
|
Количество этапов ЧКВ (M±SD) |
– |
1,37±0,5 |
Локализация формирования дистального анастомоза и установки СЛП
На втором этапе ГРМ в группе I было имплантировано 76 (100,0%) СЛП при эндоваскулярной коррекции 53 (31,2%) коронарных поражений против 125 (100,0%) стентов у пациентов ЧКВ+КШ (p<0,05). Длина стентированного участка в среднем составила 16,4±6,1 мм, диаметр стента — 2,75±0,78. Больные I когорты в среднем перенесли достоверно меньше этапов ЧКВ по сравнению с пациентами ЧКВ+КШ — 1,15±0,56 против 1,37±0,5 (p<0,05). Частота стентирования ДА, ОА и ЗМЖА была достоверно меньше в группе КШ+ЧКВ по сравнению со второй группой — 10 (5,9%) против 5 (2,8%), 10 (5,9%) против 15 (8,5%) и 1 ( 0,6%) против 10 (5,7%), соответственно (p<0,05).
На этапе КШ во II когорте была проведена хирургическая коррекция 74 (42,0%) стенозов венечного русла. В процессе КШ было наложено 49 (27,8%) маммаро-коронарных анастомозов. Достоверно реже по сравнению с группой ЧКВ+КШ проводилась реваскуляризация диагональных ветвей ПНА — 5 (2,8%) против 10 (5,9%) (p<0,05), частота аутовенозного шунтирования других КА в обеих группах не отличалась (p = NS) (Табл. 6).
По интраоперационной характеристике КШ и ЧКВ пациенты обеих групп между собой достоверно не отличались (p = NS) (Табл. 7).
Табл. 4. Интраоперационная характеристика вмешательства I этапа ГРМ
|
Показатель |
Группа I КШ+ЧКВ (n = 48) |
Группа II ЧКВ+КШ (n=49) |
p |
Коронарное шунтирование
|
Продолжительность оперативного вмешательства, мин. (M±SD) |
271,2±56,9 |
– |
|
|
Экстракорпоральное кровообращение, n (%) |
9 (18,8) |
– |
|
|
Инотропная поддержка, n (%) |
9 (18,8) |
– |
|
|
Вазопрессорная поддержка, n (%) |
26 (54,2) |
– |
|
|
Интраоперационная кровопотеря, мл (M±SD) |
479,5±73,1 |
– |
Чрескожное коронарное вмешательство
|
Продолжительность оперативного вмешательства, мин. (M±SD) |
– |
108,4±36,7 |
|
|
Трансрадиальный доступ, n (%) |
– |
38 (77,6) |
Табл. 5. Характеристика периоперационного периода I этапа ГРМ
|
Показатель |
Группа I КШ+ЧКВ (n = 48) |
Группа II ЧКВ+КШ (n = 49) |
|
Средняя кровопотеря за 1–е сутки, мл (M±SD) |
544,4±162,9 |
– |
|
Гемотрансфузия, n (%) |
12 (25,0) |
– |
|
Среднее время послеоперационной ИВЛ, час (M±SD) |
5,9±3,02 |
– |
|
Среднее время пребывания в ОРИТ, час (M±SD) |
25,7±5,99 |
10,8±3,1 |
|
Инотропная поддержка, n (%) |
5 (10,4) |
– |
|
Вазопрессорная поддержка, n (%) |
22 (45,8) |
– |
|
Послеоперационное кровотечение, n (%) |
1 (2,1) |
– |
|
Периоперационный ОИМ, n (%) |
1 (2,1) |
1 (2,0) |
|
ОНМК, n (%) |
– |
– |
|
Послеоперационная летальность, n (%) |
– |
– |
|
Послеоперационный койко-день, (M±SD) |
12,9±6,74 |
3,1±0,1 |
По характеристике периоперационного периода больные обеих групп также между собой достоверно не отличались (p = NS). Ранний послеоперационный период во второй когорте осложнился развитием летального крупноочагового ОИМ, связанного с острым тромбозом шунта ЛВГА-ПНА.
После второго этапа ГРМ у 45 (93,8%) больных I группы и 46 (93,9%) пациентов II группы была клиника стенокардии напряжения 0-I ФК (p = NS). У 2 (4,2%) и 3 (6,1%) испытуемых I и II когорты резидуальная ишемия миокарда была клинически представлена СН II функционального класса, соответственно (p = NS).
В течение 36,9±5,8 мес. наблюдения РИМ несколько чаще регистрировался во второй группе — 10,4% против 12,2%, 16,6% против 18,3% и 20,1% против 24,5% на 1, 2 и 3 году наблюдения, соответственно, однако различия были недостоверны (p = NS) (Табл. 9).
В группе КШ+ЧКВ в первой трети периода наблюдения в 6 (11,1%) случаях развился бинарный РВС и в 4 (10,3%) — НВТ; по показаниям было выполнено стентирование 9 (16,7%) поражений КА и 1 (2,6%) эндоваскулярная реконструкция ВШ. К концу периода наблюдения в I когорте было дополнительно накоплено 3 (5,6%) случая РВС, 1 (1,9%) случай рецидива РВС,
Шевченко Ю.Л., Ермаков Д.Ю., Вахрамеева А.Ю., Баранов А.В.
СРАВНИТЕЛЬНЫЕ РЕЗУЛЬТАТЫ РАЗЛИЧНЫХ ПРИНЦИПОВ ЭТАПНОЙ ГИБРИДНОЙ РЕВАСКУЛЯРИЗАЦИИ МИОКАРДА У ПАЦИЕНТОВ С ПРЕДВАРИТЕЛЬНЫМ СТЕНТИРОВАНИЕМ ВЕНЕЧНЫХ АРТЕРИЙ И ЭНДОВАСКУЛЯРНОЙ КОРРЕКЦИЕЙ ВЕНЕЧНОГО РУСЛА ПОСЛЕ КОРОНАРНОГО ШУНТИРОВАНИЯ
Табл. 6. Результаты II этапа гибридной реваскуляризации
|
Показатель |
Группа I КШ+ЧКВ (n = 48) 170 |
Группа II ЧКВ+КШ (n = 49) 176 |
p |
|
Скорректировано поражений, n (%) |
140 (82,4) |
150 (85,2) |
NS |
|
Маммаро-коронарное шунтирование, n (%) |
47 (27,6) |
49 (27,8) |
NS |
|
Венозные шунты, n (%) |
39 (22,9) |
25 (14,2) |
<0,05 |
|
Имплантировано СЛП, n (%) |
76 (100,0) |
125 (100,0) |
<0,05 |
|
Длина стентированного участка, мм (M±SD) |
16,4±6,1 |
22,7±7,4 |
<0,05 |
|
Диаметр имплантированного стента, мм (M±SD) |
2,75±0,78 |
2,93±0,63 |
<0,05 |
|
Количество этапов ЧКВ (M±SD) |
1,15±0,56 |
1,37±0,5 |
<0,05 |
Локализация формирования дистального анастомоза
|
Ствол ЛКА n (%) |
– |
– |
|
|
Система ПНА ПНА, n (%) |
48 (28,2) |
49 (27,8) |
NS |
|
ДА, n (%) |
10 (5,9) |
5 (2,8) |
<0,05 |
|
ИМА, n (%) |
1 (0,6) |
0 (0) |
NS |
|
Система ОА ОА, n (%) |
– |
– |
|
|
АТК, n (%) |
7 (4,1) |
4 (2,3) |
NS |
|
ЗБВ, n (%) |
2 (1,2) |
0 (0) |
NS |
|
ЗМЖА, n (%) |
4 (2,4) |
4 (2,3) |
NS |
|
Система ПКА ПКА, n (%) |
– |
– |
|
|
ЗБВ, n (%) |
1 (0,6) |
1 (0,6) |
NS |
|
ЗМЖА, n (%) |
14 (8,2) |
11 (6,3) |
NS |
Локализация зоны установки СЛП
|
Ствол ЛКА n (%) |
1 (0,6) |
– |
NS |
|
Система ПНА ПНА, n (%) |
– |
– |
|
|
ДА, n (%) |
10 (5,9) |
15 (8,5) |
<0,05 |
|
ИМА, n (%) |
0 (0) |
2 (1,1) |
NS |
|
Система ОА ОА, n (%) |
8 (4,7) |
14 (8,0) |
<0,05 |
|
АТК, n (%) |
5 (2,9) |
6 (3,4) |
NS |
|
ЗБВ, n (%) |
2 (1,2) |
4 (2,3) |
NS |
|
ЗМЖА, n (%) |
1 (0,6) |
3 (1,7) |
NS |
|
Система ПКА ПКА, n (%) |
22 (12,9) |
19 (10,8) |
NS |
|
ЗБВ, n (%) |
4 (2,4) |
3 (1,7) |
NS |
|
ЗМЖА, n (%) |
1 (0,6) |
10 (5,7) |
<0,05 |
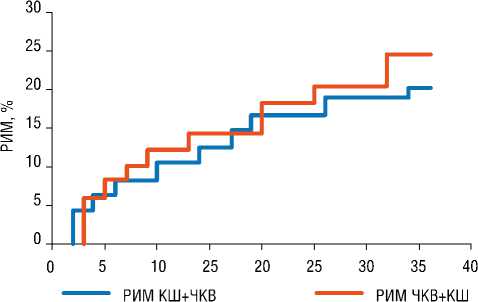
Рис. 1. Рецидив ишемии миокарда. Метод Каплана-Майера.
5 (12,8%) случаев НВТ, по поводу которых была проведена интервенционная реваскуляризация КА в 8 (14,8%) случаях и реканализация окклюзии ВШ у 1 (2,6%) пациента.
Табл. 7. Интраоперационная характеристика вмешательства II этапа ГРМ
|
Показатель |
Группа I КШ+ЧКВ (n = 48) |
Группа II ЧКВ+КШ (n = 49) |
p |
Коронарное шунтирование
|
а |
271,2±56,9 |
281,5±52,2 |
NS |
|
Экстракорпоральное кровообращение, n (%) |
9 (18,8) |
7 (14,3) |
NS |
|
Инотропная поддержка, n (%) |
9 (18,8) |
11 (22,4) |
NS |
|
Вазопрессорная поддержка, n (%) |
26 (54,2) |
25 (51,0) |
NS |
|
Интраоперационная кровопотеря, мл (M±SD) |
479,5±73,1 |
461,9±85,9 |
NS |
Чрескожное коронарное вмешательство
|
Продолжительность оперативного вмешательства, мин. (M±SD) |
117,4±29,6 |
108,4±36,7 |
NS |
|
Трансрадиальный доступ, n (%) |
33 (68,8) |
38 (77,6) |
NS |
Табл. 8. Характеристика периоперационного периода II этапа ГРМ
|
Показатель |
Группа I КШ+ЧКВ (n = 48) |
Группа II ЧКВ+КШ n = 49) |
p |
Коронарное шунтирование
|
Средняя кровопотеря за 1–е сутки, мл (M±SD) |
544,4±162,9 |
538±178,8 |
NS |
|
Гемотрансфузия, n (%) |
12 (25,0) |
14 (28,6) |
NS |
|
Среднее время послеоперационной ИВЛ, час (M±SD) |
5,9±3,02 |
5,7±3,21 |
NS |
|
Среднее время пребывания в ОРИТ, час (M±SD) |
25,7±5,99 |
24,4±5,64 |
NS |
|
Инотропная поддержка, n (%) |
5 (10,4) |
5 (10,2) |
NS |
|
Вазопрессорная поддержка, n (%) |
22 (45,8) |
24 (49,0) |
NS |
|
Послеоперационное кровотечение, n (%) |
1 (2,1) |
1 (2,0) |
NS |
|
Периоперационный ОИМ, n (%) |
1 (2,1) |
1 (2,0) |
NS |
|
ОНМК, n (%) |
– |
– |
NS |
|
Послеоперационная летальность, n (%) |
– |
1 (2,0) |
NS |
|
Послеоперационный койко-день, (M±SD) |
12,9±6,74 |
12,5±5,78 |
NS |
Чрескожное коронарное вмешательство
|
Среднее время пребывания в ОРИТ, час (M±SD) |
10,9±3,05 |
10,8±3,1 |
NS |
|
Периоперационный ОИМ, n (%) |
– |
1 (2,0) |
NS |
|
ОНМК, n (%) |
– |
– |
NS |
|
Послеоперационная летальность, n (%) |
– |
– |
NS |
|
Послеоперационный койко-день, (M±SD) |
3,0±0,1 |
3,1±0,1 |
NS |
Во II группе на 1 году наблюдения было выполнено 13 (17,1%) стентирований КА по поводу 10 (13,2%) случаев бинарного РВС и 3 (12%) случаев НВТ. К концу периода наблюдения дополнительно была проведена реконструкция КА в 9 (11,8%) случаях, в 1 (1,3%) из которых ЧКВ выполнялось в целях коррекции рецидива РВС в средней трети периода наблюдения. Рентгенохирургическое вмешательство на ВШ было проведено 1 (2%) больному II группы (Рис. 2).
К концу периода наблюдения число ИМ, ОНМК, смерти от всех причин достоверно не отличалось в обеих группах и составило 3 (6,3%), 2 (4,2%) и 3 (6,1%),

Шевченко Ю.Л., Ермаков Д.Ю., Вахрамеева А.Ю., Баранов А.В.
СРАВНИТЕЛЬНЫЕ РЕЗУЛЬТАТЫ РАЗЛИЧНЫХ ПРИНЦИПОВ ЭТАПНОЙ ГИБРИДНОЙ РЕВАСКУЛЯРИЗАЦИИ МИОКАРДА У ПАЦИЕНТОВ С ПРЕДВАРИТЕЛЬНЫМ СТЕНТИРОВАНИЕМ ВЕНЕЧНЫХ АРТЕРИЙ И ЭНДОВАСКУЛЯРНОЙ КОРРЕКЦИЕЙ ВЕНЕЧНОГО РУСЛА ПОСЛЕ КОРОНАРНОГО ШУНТИРОВАНИЯ
Табл. 9. Отдаленные осложнения гибридной реваскуляризации
|
Показатель |
Группа I КШ+ЧКВ (n = 48) |
Группа II ЧКВ+КШ (n = 49) |
p |
РИМ
|
1 год, n (%) |
5 (10,4) |
6 (12,2) |
NS |
|
2 года, n (%) |
8 (16,6) |
9 (18,3) |
NS |
|
3 года, n (%) |
10 (20,1) |
12 (24,5) |
NS |
НЦП
|
1 год, n (%) |
6 (11,1) |
10 (13,2) |
NS |
|
2 года, n (%) |
8 (14,8) |
13 (17,1) |
NS |
|
3 года, n (%) |
10 (18,5) |
17 (22,3) |
NS |
НВТ
|
1 год, n (%) |
4 (10,3) |
3 (12,0) |
NS |
|
2 года, n (%) |
7 (17,9) |
5 (20,0) |
NS |
|
3 года, n (%) |
9 (23,1) |
6 (24,0) |
NS |
ИМ
|
1 год, n (%) |
2 (4,2) |
2 (4,1) |
NS |
|
2 года, n (%) |
2 (4,2) |
2 (4,1) |
NS |
|
3 года, n (%) |
3 (6,3) |
3 (6,1) |
NS |
ОНМК
|
1 год, n (%) |
1 (2,1) |
1 (2,0) |
NS |
|
2 года, n (%) |
1 (2,1) |
2 (4,1) |
NS |
|
3 года, n (%) |
2 (4,2) |
3 (6,1) |
NS |
Летальный исход
|
1 год, n (%) |
1 (2,1) |
1 (2,0) |
NS |
|
2 года, n (%) |
2 (4,2) |
2 (4,1) |
NS |
|
3 года, n (%) |
3 (6,3) |
2 (4,1) |
NS |
MACE
Обсуждение
ГРМ занимает все более прочное место в кардиохирургической практике, обладая преимуществами КШ и ЧКВ и будучи лишенной многих их недостатков. Этапная ГРМ представляется эффективной стратегией подхода к реваскуляризации для кардиохирургических стационаров, не оснащенных гибридной операционной. В ряде ситуаций выполнение максимальной реваскуляризации при КШ лимитировано рядом объективных причин, что определяет потребность в проведении ЧКВ перед хирургической коррекцией поражений КА или после шунтирования. ЧКВ также является неотъемлемым компонентом многоэтапного лечения больных ИБС, перенесших КШ, в силу достаточно высокой частоты выявления РИМ и дисфункции венозных кондуитов в послеоперационном периоде.
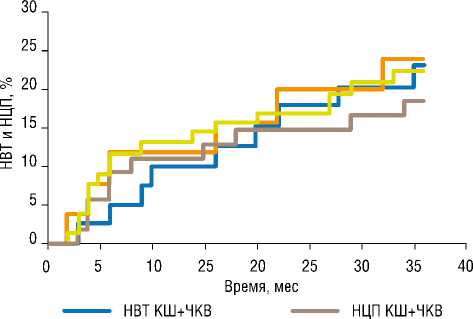
НВТ чкв+кш ----- нцпчкв+кш
Рис. 2. Несостоятельность венозных шунтов и стентированных участков. Метод Каплана-Майера.
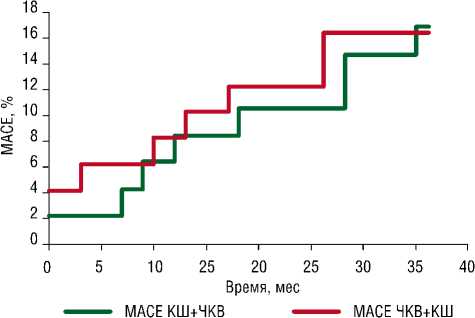
Рис. 3. Неблагоприятные сердечно-сосудистые события. Метод Каплана–Майера.
В настоящем исследовании была проанализирована эффективность и безопасность ГРМ с КШ в качестве первого и второго этапа оперативного лечения больных ИБС. Все больные имели поражение двух и более основных эпикардиальных артерий. В качестве хирургического доступа при КШ у всех пациентов использовалась стандартная срединная стернотомия. У подавляющего большинства больных КШ было выполнено без использования экстракорпорального кровообращения — 81,3% в группе КШ+ЧКВ против 85,7% в группе ЧКВ-КШ (p = NS). По продолжительности оперативного вмешательства (КШ), частоте применения инотропной и вазопрессорной поддержки, а также объему интраоперационной кровопотери разницы выявлено не было (p = NS).
Выполнение КШ или ЧКВ в качестве первого этапа ГРМ приводило к достоверно большему объему запланированной реваскуляризации (исключая бассейн ПНА) соответствующим методом. Так, в группе ЧКВ+КШ было наложено 39 (22,9%) венозных шунтов и установлено 76 стентов против 25 (14,2%) ВШ и СЛП у больных ЧКВ+КШ (p<0,05). При этом, во II когорте средний диаметр установленного стента и длина стентированного

Шевченко Ю.Л., Ермаков Д.Ю., Вахрамеева А.Ю., Баранов А.В.
СРАВНИТЕЛЬНЫЕ РЕЗУЛЬТАТЫ РАЗЛИЧНЫХ ПРИНЦИПОВ ЭТАПНОЙ ГИБРИДНОЙ РЕВАСКУЛЯРИЗАЦИИ МИОКАРДА У ПАЦИЕНТОВ С ПРЕДВАРИТЕЛЬНЫМ СТЕНТИРОВАНИЕМ ВЕНЕЧНЫХ АРТЕРИЙ И ЭНДОВАСКУЛЯРНОЙ КОРРЕКЦИЕЙ ВЕНЕЧНОГО РУСЛА ПОСЛЕ КОРОНАРНОГО ШУНТИРОВАНИЯ участка также были достоверно больше (16,4±6,1 мм и 2,75±0,78 мм против 22,7±7,4 мм и 2,93±0,63 мм, соответственно, p<0,05), что связано с большей частотой реваскуляризации проксимальных сегментов КА и потребности в эндоваскулярной коррекции венечных артерий на всем протяжении зоны поражения (атеросклеротической бляшки). Также больные II группы чаше переносили более 1 этапа ЧКВ — 1,15±0,56 против 1,37±0,5 эпизода эндоваскулярной реваскуляризации (p<0,05).
Необходимо отметить, что частота дисфункции ВШ к концу периода наблюдения несколько превалировала над НЦП, при этом в группе КШ+ЧКВ разность между данными параметрами была выше, чем во II когорте — 18,5% НЦП и 23,1% НВТ против 22,3% НЦП и 24% НВТ (p = NS). Так, применение СЛП II и III поколения в нашем исследовании не уступало или обеспечивало несколько большую эффективность реваскуляризации в отдаленном периоде после ЧКВ по сравнению с венозным шунтированием не-ПНА бассейнов венечного русла.
По частоте периоперационных MACE и периоперационной характеристике в целом больные двух когорт ожидаемо не отличались (p = NS). Частота регистрации дисфункции венозных шунтов в отдаленном периоде наблюдения была одинакова в группах КШ+ЧКВ и ЧКВ+КШ — 23,1% против 24%, соответственно, (p = NS). Удельный вес НЦП недостоверно превалировал во II когорте — 17 (22,3%) случаев против 10 (18,5%) (p = NS), что также предположительно связано с большей средней протяженностью стентированного участка. Клиника РИМ также недостоверно чаще отмечалась у больных группы ЧКВ+КШ к 3 году наблюдения — 24,5% против 20,1% (p = NS), что связано с несколько большей частотой НЦП.
Число неблагоприятных сердечно-сосудистых событий через 36 месяцев достоверно не отличалось — 8 (16,7%) случаев в группе ЧКВ+КШ против 8 (16,3%) случаев MACE во второй когорте (p = NS). Удельный вес ОНМК составил 2 (4,2%) и 3 (6,1%), ИМ — 3 (6,3%) и 3 (6,1%), летальных исходов — 3 (6,3%) и 2 (4,1%) в группе КШ+ЧКВ и ЧКВ+КШ, соответственно, (p = NS).
Заключение
Исходя из полученных результатов исследования, можно сделать следующие выводы:
-
1. Гибридная реваскуляризация сердца выполнением коронарного шунтирования с формированием маммарно-коронарного анастомоза с передней нисходящей артерией преимущественно без экстракорпорального кровообращения, перед эндоваскулярной коррекцией, по сравнению со стратегией «ЧКВ перед КШ», показывает несколько более оптимальные 3-летние результаты в отношении рецидива ишемии миокарда (20,1% против 24,5%, p = NS) и частоты бинарного рестеноза (18,5% против 22,3%, p = NS).
-
2. Гибридная реваскуляризация сердца выполнением коронарного шунтирования с формированием
МКШ преимущественно без ИК первым этапом до ЧКВ и эндоваскулярной реваскуляризацией КА перед КШ одинаково безопасны для больных ИБС и не показывают достоверной разницы в частоте развития сердечно-сосудистых осложнений и смерти от всех причин через 3 года после оперативного вмешательства (16,7% против 16,3%, p = NS).
Список литературы Сравнительные результаты различных принципов этапной гибридной реваскуляризации миокарда у пациентов с предварительным стентированием венечных артерий и эндоваскулярной коррекцией венечного русла после коронарного шунтирования
- Lawton JS, Tamis-Holland JE, Bangalore S, Bates ER, Beckie TM, et al. 2021 ACC/AHA/SCAI Guideline for Coronary Artery Revascularization: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 2022; 145(3): 18-114. doi: 10.1161/CIR.0000000000001038.
- Thuijs DJ, Kappetein AP, Serruys PW, Mohr FW, et al. SYNTAX Extended Survival Investigators. Percutaneous coronary intervention versus coronary artery bypass grafting in patients with three-vessel or left main coronary artery disease: 10-year follow-up of the multicentre randomised controlled SYNTAX trial. Lancet. 2019; 394(10206): 1325-1334. doi: 10.1016/S0140-6736(19)31997-X.
- Brener SJ, Alapati V, Chan D, Da-Wariboko A, Kaid Y, Latyshev Y, et al. The SYNTAX II Score Predicts Mortality at 4 Years in Patients Undergoing Percutaneous Coronary Intervention. J Invasive Cardiol. 2018; 30(8): 290-294.
- Ганюков В.И., Кочергин Н.А., Шилов А.А., Тарасов Р. С., Козырин К.А., Прокудина Е.С. и др. Рандомизированное исследование гибридной коронарной реваскуляризации в сравнении со стандартными аортокоронарным шунтированием и многососудистым стентированием: 5 летние результаты исследования HREVS // Кардиология. — 2023. — №63(11). — С.57-63. doi: 10.18087/cardio.2023.11.n2475.
- Шевченко Ю.Л., Борщев Г.Г., Ульбашев Д.С., Землянов А.В. Выбор кондуитов в коронарной хирургии // Вестник Национального медико-хирургического центра им. Н.И. Пирогова. — 2019. — Т.14. — №1. — С.97-104. doi: 10.25881/BPNMSC.2019.69.57.019.
- Шевченко Ю.Л., Ермаков Д.Ю., Марчак Д.И. Дисфункция коронарных шунтов и стентов после хирургическоий реваскуляризации миокарда больных ИБС: патогенез, факторы риска и клиническая оценка // Вестник Национального медико-хирургического центра им. Н.И. Пирогова. — 2022. — Т.17. — №3. — С.94-100. doi: 10.25881/20728255_2022_17_3_94.
- Algoet M, Oosterlinck W, Balkhy HH. Reply to: Anaortic With No Touch to the Aorta Is a Central Technique to Decrease Invasiveness of CABG. Innovations (Phila). 2023; 18(3): 296. doi: 10.1177/15569845231168615.
- Nenna A, Nappi F, Spadaccio C, et al. Hybrid coronary revascularization in multivessel coronary artery disease: a systematic review. Future Cardiol. 2022; 18(3): 219-234. doi: 10.2217/fca-2020-0244.
- Hannan EL, Wu Y, Cozzens K, Sundt TM, et al. Hybrid Coronary Revascularization Versus Conventional Coronary Artery Bypass Surgery: Utilization and Comparative Outcomes. Circ Cardiovasc Interv. 2020; 13(10): e009386. doi: 10.1161/CIRCINTERVENTIONS.120.009386.
- Giambruno V, Jones P, Khaliel F, Chu MW, et al. Hybrid Coronary Revascularization Versus On-Pump Coronary Artery Bypass Grafting. Ann Thorac Surg. 2018; 105(5): 1330-1335. doi: 10.1016/j.athoracsur.2017.11.019.


