Сравнительный анализ хирургических доступов при выполнении поясничной лимфаденэктомии у больных раком эндометрия
Автор: Алимов В.А., Новикова Е.Г., Греков Д.Н., Лебедев С.С., Багателия З.А., Полякова Н.Ю., Лаевская А.А., Шабунин А.В.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Клинические исследования
Статья в выпуске: 3 т.24, 2025 года.
Бесплатный доступ
Введение. На данный момент роль лимфаденэктомии при первой стадии рака эндометрия (РЭ) отходит на второй план, уступая биопсии сторожевых лимфоузлов. С учетом новых данных об улучшении выживаемости у больных высокого риска лимфогенного метастазирования при проведении полноценной тазовой и поясничной лимфаденэктомии и тенденции к рестадированию данной когорты больных во вторую стадию в соответствии с новой классификацией FIGO 2023 проблема выполнения поясничной лимфаденэктомии вновь становится актуальной. Цель исследования – сравнительный анализ используемых хирургических доступов при выполнении поясничной лимфаденэктомии у больных РЭ с акцентом на недостатки и преимущества каждого. Материал и методы. Ретроспективно произведен анализ историй болезни 122 пациенток, прооперированных в ММКНЦ им. С. П. Боткина по поводу рака эндометрия. В исследование включены пациентки, которым были выполнены хирургические вмешательства в объеме тазовой и поясничной лимфаденэктомии, гистерэктомии посредством четырех хирургических доступов: лапаротомного (n=28), лапароскопического трансабдоминального (n=30), лапароскопического забрюшинного (n=41) и робот-ассистированного забрюшинного (n=23). Проводился сравнительный анализ следующих показателей: индекса массы тела больных, длительности операции, количества удаленных тазовых и парааортальных лимфоузлов, частоты достижения III и IV уровней лимфодиссекции, частоты интраи послеоперационных осложнений, количества койкодней в послеоперационном периоде и частоты переводов в отделение реанимации и интенсивной терапии. Результаты. По сравнению с другими подгруппами хирургические вмешательства, проводимые посредством лапароскопического забрюшинного доступа, характеризовались наименьшей длительностью операции, высокой частотой достижений IV уровня лимфодиссекции и приемлемым уровнем интраи послеоперационных осложнений. Заключение. По данным нашего исследования, наиболее выигрышными характеристиками при выполнении поясничной лимфаденэктомии обладал лапароскопический забрюшинный доступ.
Парааортальная лимфаденэктомия, робот-ассистированная лимфаденэктомия, ретроперитонеальная лимфаденэктомия, забрюшинная лимфаденэктомия, рак эндометрия
Короткий адрес: https://sciup.org/140310571
IDR: 140310571 | УДК: 618.14-006.6:616.428-089 | DOI: 10.21294/1814-4861-2025-24-3-15-26
Comparative analysis of surgical approaches for para-aortic lymphadenectomy in endometrial cancer patients
Background. To date, the role of lymphadenectomy in stage I endometrial cancer has been relegated to the background in favor of sentinel lymph node biopsy. Taking into account the new data on the improved survival in patients at high risk of lymph node metastasis after pelvic and para-aortic lymphadenectomy and the tendency to upstaging in accordance with the new FIGO 2023 classification, the problem of performing para-aortic lymphadenectomy becomes relevant again. The study objective: a comparative analysis of surgical accesses used in performing lumbar lymphadenectomy in endometrial cancer patients with an emphasis on the disadvantages and advantages of each surgical approach. Material and Methods. Medical records of 122 endometrial cancer patients treated at the S. P. Botkin Moscow Medical Scientific Center were retrospectively analyzed. The study included patients undergoing pelvic and para-aortic lymphadenectomy, and hysterectomy through four surgical access methods: laparotomy (n=28), laparoscopic transabdominal (n=30), laparoscopic retroperitoneal (n=41) and robot-assisted retroperitoneal (n=23). The following parameters were compared between the subgroups: body mass index of patients, duration of surgery, number of removed pelvic and para-aortic lymph nodes, frequency of achieving III and IV levels of lymphadenectomy, frequency of intraand postoperative complications, length of hospital stay in the postoperative period, and frequency of transfers to intensive care unit. Results. Compared with other subgroups, surgery performed via laparoscopic retroperitoneal access was characterized by the shortest duration of surgery, high frequency of achieving level IV lymphadenectomy and acceptable level of intraand postoperative complications. Conclusion. Laparoscopic retroperitoneal access was found to have greatest advantageous in performing lumbar lymphadenectomy.
Текст научной статьи Сравнительный анализ хирургических доступов при выполнении поясничной лимфаденэктомии у больных раком эндометрия
В Российской Федерации, по данным национального канцер-регистра за 2023 г., рак эндометрия занял второе место в структуре заболеваемости ЗНО женской репродуктивной системы, уступая лишь раку молочной железы [2]. В 70 % случаев рак эндометрия выявляют на ранних стадиях [1]. Согласно клиническим рекомендациям Минздрава РФ, при I стадии заболевания показано хирургическое вмешательство, объем которого зависит от степени инвазии опухоли в миометрий и ее гистологического типа [3, 4]. Общепризнанным объемом операции является гистерэктомия, тогда как вопрос о роли лимфаденэктомии все еще остается дискуссионным.
Ранее считалось, что лимфаденэктомия при лечении I стадии рака эндометрия выполняет одновременно две функции – лечебную и стадирующую, последняя позволяет определить необходимость и режим адъювантного лечения, что, в свою очередь, улучшает прогноз пациенток. Однако по мере накопления клинических данных наметилась тенденция к деэскалации объема лимфодиссекции при ранних стадиях заболевания. Так, в 2009 г. по результатам двух масштабных рандомизированных исследований (ASTEC study и авторской группы Benedetti Panici et al.) при первой стадии рака эндометрия лимфаденэктомии была отведена исключительно стадирующая роль, в связи с отсутствием влияния на общую и безрецидивную выживаемость. Более того, удаление лимфоузлов было ассоциированно с большей частотой интра- и послеоперационных осложнений. В 2016 г. была внедрена технология биопсии сторожевых лимфоузлов (БСЛУ) с применением флуоресцентной визуализации, в связи с чем встал вопрос о возможности замены лимфаденэктомии на БСЛУ при ранних стадиях заболевания [5]. Уже к 2022 г. авторитетные между- народные медицинские сообщества, такие как ESMO и ESGO, признали БСЛУ полноценной альтернативой лимфаденэктомии при первой стадии рака эндометрия. Рекомендации основывались на высокой чувствительности метода, минимальной инвазивности вмешательства, а также были обусловлены отсутствием новых рандомизированных клинических исследований, которые могли бы свидетельствовать о преимуществах системной лимфодиссекции [6–9].
Впоследствии результаты исследований об отсутствии влияния лимфаденэктомии на выживаемость были подвергнуты критике, основные тезисы которой указывали на погрешности в дизайне исследований и низкий процент пациенток высокого риска в выборке [10, 11]. На данный момент в научной литературе опубликованы данные обсервационных исследований, согласно которым именно полная (тазовая и поясничная) лимфаденэктомия у больных первой стадией рака эндометрия высокого риска лимфогенного метастазирования была ассоциирована со значительным улучшением общей выживаемости по сравнению с БСЛУ [12]. Кроме того, в настоящее время во всем мире проводятся рандомизированные клинические исследования, направленные на изучение терапевтической эффективности системной лимфаденэктомии при начальных стадиях заболевания у пациенток высокого риска [13–15].
В настоящее время подход к лечению первой стадии рака эндометрия высокого риска модифицируется. В 2023 г. FIGO была опубликована новая классификация рака эндометрия, согласно которой определение стадии зависит не только от анатомических характеристик опухоли, но и от гистотипа и мутационного статуса. В соответствии с новой классификацией опухоли с агрессивным гистологическим подтипом с инвазией в миометрий теперь относятся ко второй стадии заболевания, а не к первой, как считалось ранее. Приблизительно 15–20 % пациенток с первоначально диагностированной I стадией подлежат рестадированию, что обусловливает необходимость выполнения лимфаденэктомии в тазовой и поясничной областях [16].
Таким образом, проблема технических аспектов выполнения полноценной лимфаденэктомии до уровня почечных сосудов вновь приобретает актуальность. Из числа хирургических вмешательств, выполняемых у онкогинекологических больных, поясничная лимфаденэктомия считается наиболее сложным этапом с технической точки зрения.
Изначально методика выполнения поясничной лимфаденэктомии в научной литературе обсуждалась лишь при лапаротомном доступе, который обеспечивал необходимую радикальность операции и не требовал специальных лапароскопических навыков. Однако данный доступ был связан со значительной травматизацией тканей, в связи с чем сопровождался высоким риском осложнений и длительным периодом восстановления. Первые сравнительные исследования лапаротомного и лапароскопического доступов при лечении рака эндометрия были опубликованы в 1990-х гг. На начальном этапе внедрения малоинвазивных технологий применялся исключительно трансперитонеальный лапароскопический доступ. Примерно в то же время для парааортальной лимфодиссекции стали использовать и забрюшинный доступ. Одними из первых его начали внедрять онкоурологи при биопсии почек, а впоследствии при выполнении тазовой и поясничной лимфаденэктомии при раке предстательной железы и герминогенных опухолях. Позднее эту методику стали использовать для лечения рака шейки матки. Дальнейшее развитие хирургических технологий привело к внедрению робот-ассистированных вмешательств. Вслед за этим, уже в конце 2000-х гг., онкогинекологи провели первые робот-ассисти-рованные забрюшинные лимфаденэктомии при раке эндометрия и раке шейки матки.
По данным исследований, сравнивающих результаты лимфаденэктомий, выполненных посредством различных хирургических доступов, забрюшинный подход имел ряд преимуществ. Авторы исследований отмечали лучшую визуализацию парааортальных лимфоузлов, удобное расположение инструментов, более низкую частоту периоперационных осложнений и меньшую травматичность вмешательства. Кроме того, с учетом распространенности нарушений жирового обмена у больных раком эндометрия, забрюшинный доступ позволял обеспечивать более полный объем лимфаденэктомии по сравнению с трансбрюшинным подходом, что оценивалось по количеству удаленных лимфоузлов. Однако широкому распространению забрюшинного доступа препятствовали технические сложности при выполнении лимфодиссекции с использованием стандартных инструментов – биполярного коагулятора и ножниц [17, 18].
Развитие хирургического оборудования, представленного инструментами эндоскопического гемостаза нового поколения (биполярными и ультразвуковыми) и новой моделью системы DaVinci Xi, значительно упростило выполнение поясничной лимфодиссекции. Данные технологии позволили использовать универсальные инструменты с возможностью переключения режимов коагуляции и резания, обеспечивающих эффективный гемостаз посредством дозированной подачи энергии в зависимости от свойств коагулируемой ткани на основе измерения тканевого импеданса.
Таким образом, современные технологические достижения создают предпосылки для проведения всестороннего сравнительного анализа эффективности, преимуществ и потенциальных ограничений лапаротомного (ЛТ), лапароскопического трансабдоминального (ЛС), лапароскопического забрюшинного (ЛСЗ) и робот-ассистированного забрюшинного (РАЗ) доступов при выполнении забрюшинной поясничной лимфаденэктомии.
Материал и методы
Материалом для научного исследования послужили 122 истории болезни пациенток с диагнозом рак тела матки I стадии, прооперированных в Московском многопрофильном научно-клиническом центре им. С.П. Боткина за период с 2022 по 2024 г. В исследование включены пациентки, которым были выполнены хирургические вмешательства в объеме тазовой и поясничной лимфаденэктомии, гистерэктомии посредством четырех хирургических доступов: лапаротомного (ЛТ; n=28), лапароскопического трансабдоминального (ЛС; n=30), лапароскопического забрюшинного (ЛСЗ; n=41) и робот-ассистированного забрюшинного (РАЗ; n=23). Схематичные варианты доступов и расстановки троакаров представлены на рис. 1.
При лапаротомных операциях срединный разрез осуществляли от лонного сочленения до мечевидного отростка грудины с обходом пупка слева, использовали ретракторы, моно- и биполярные коагуляторы, инструмент биполярного гемостаза LigaSure Impact. Для выполнения поясничного этапа лимфаденэктомии рассекали брюшину над правым краем аорты на расстоянии от бифуркации правой общей подвздошной артерии до уровня двенадцатиперстной кишки, мобилизовали последнюю кверху до уровня левой почечной вены. Для визуализации парааортальной зоны выполняли мобилизацию сигмовидной и левых отделов ободочной кишки. Лимфаденэктомию выполняли биполярным пинцетом и ножницами.
При лапароскопических операциях, как трансабдоминальных, так и забрюшинных, в качестве биполярного гемостаза применяли LigaSure Blunt 5 мм, классические грасперы и видеоэндоскопи-ческое оборудование фирмы Karl Storz. При лапароскопическом трансабдоминальном доступе для выполнения поясничного этапа лимфаденэктомии аналогичным, как и при лапаротомии, образом рассекали брюшину и выполняли мобилизацию соответствующих органов брюшной полости. После тазового этапа эндоскоп помещали над лоном, рассекали брюшину по ходу правой общей подвздошной артерии и аорты до уровня двенадцатиперстной кишки. Брюшину в проекции последней фиксировали к передней брюшной стенке различными вариантами лифтингов, что обеспечивало адекватную визуализацию в области почечных сосудов.
При забрюшинных доступах, как лапароскопическом, так и робот-ассистированном, троакары устанавливали в проекции левого латерального канала. Инсуффляцию CO2 в забрюшинное пространство проводили до уровня давления 15 мм рт. ст. После введения эндоскопа и визуализации троа-
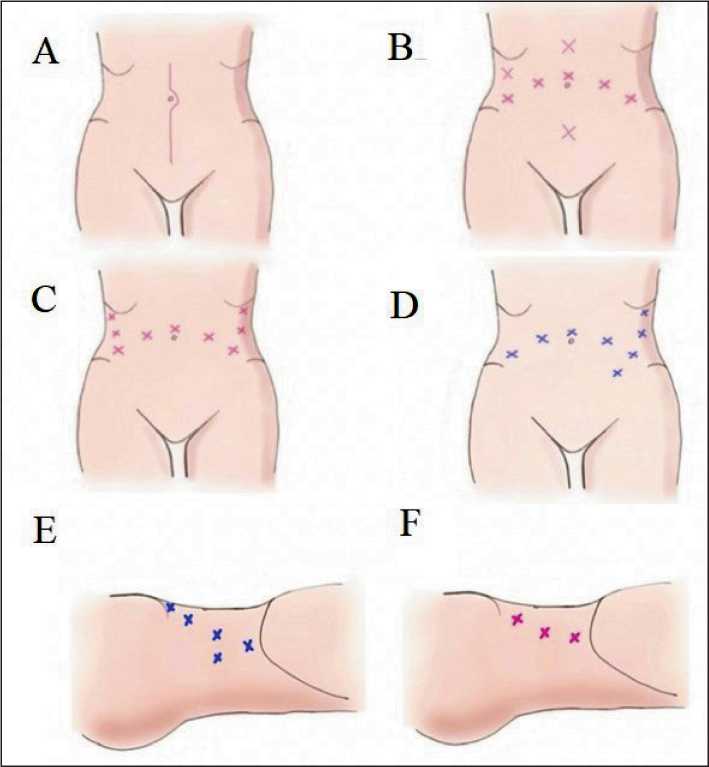
Рис. 1. Расстановка троакаров при различных хирургических доступах.
Примечания: A – лапаротомный доступ, вид сверху;
B – лапароскопический трансабдоминальный доступ, вид сверху; C – лапароскопический забрюшинный доступ, вид сверху; D – робот-ассистированный забрюшинный доступ, вид сверху; E – робот-ассистированный забрюшинный доступ, вид сбоку; F – лапароскопический забрюшинный доступ, вид сбоку; рисунок выполнен авторами
Fig. 1. Trocar placement for different surgical approaches Notes: A – laparotomy approach, top view; B – laparoscopic transabdominal approach, top view; B – laparoscopic retroperitoneal approach, top view; G – robot-assisted retroperitoneal approach, top view; D – robot-assisted retroperitoneal approach, side view; E – laparoscopic retroperitoneal approach, side view; created by the authors каров в забрюшинном пространстве выделяли поясничную мышцу, которая служила основным ориентиром. Далее визуализировали наружную подвздошную артерию и левый мочеточник. Диссекция тканей проводилась по слою между мочеточником и артериальными сосудами последовательно: левой наружной подвздошной артерии, общей подвздошной, аортой – до уровня нижней брыжеечной. Затем отсепаровывали ткани, находящиеся медиально от мочеточника, представляющие собой парааортальую клетчатку с лимфоузлами. Обнаруживали зону конфлю-енции левой гонадной вены в левую почечную. Выполняли лимфаденэктомию парааортально. Затем выделяли аорто-кавальную зону. В случае удобных анатомических соотношений или при робот-ассистированных подходах продолжали операцию с левой стороны. В других случаях выполняли аналогичную переустановку на правую сторону. Использовали тот же слой для диссекции между мочеточником и сосудами. На уровне впадения гонадной вены в нижнюю полую пересекали первую, что освобождало зону для аорто-кавальной и паракавальной лимфаденэктомии справа.
Робот-ассистированные операции выполняли на установке DaVinci Xi. В качестве инструментария были использованы биполярный граспер и монополярные ножницы. Устанавливали один ассистентский троакар, через который осуществляли тракцию окружающих тканей и вакуум-аспирацию.
При оценке уровня лимфодиссекции в исследовании была использована классификация D. Quer-leu 2008 г., представленная на рис. 2.
Оптимальным считалось выполнение парааор-тальной лимфаденэктомии до IV уровня, включающего удаление лимфоузлов до почечных сосудов. В случае технических трудностей процедуру ограничивали III уровнем лимфодиссекции – до нижней брыжеечной артерии.
При каждом хирургическом доступе оценивались следующие показатели: индекс массы тела (ИМТ) больных, длительность операции (мин), количество тазовых и парааортальных лимфоузлов, частота достижения III и IV уровней лимфодиссекции, индекс массы тела больных при соответствующем уровне лимфаденэктомии,
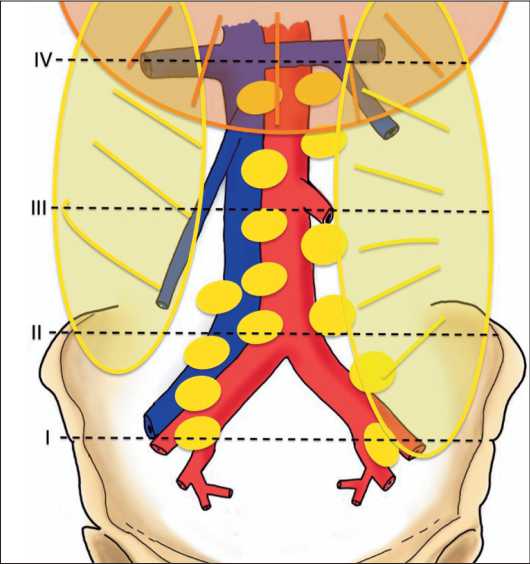
Рис. 2. Уровни лимфаденэктомии в соответствии с классификацией D. Querleu (2008). Примечания: I уровень – до бифуркации общих подвздошных артерий; II уровень – до бифуркации аорты; III уровень – до нижней брыжеечной артерии; IV уровень – до почечных сосудов; I–II уровни соответствуют объему тазовой лимфодиссекции;
III–IV уровни – поясничной лимфодиссекции; рисунок выполнен авторами
Fig. 2. Levels of lymphadenectomy according to D. Querleu 2008 classification. Notes: Level I – to the bifurcation of the common iliac arteries; Level II – to the bifurcation of the aorta; Level III – to the inferior mesenteric artery; Level IV – to the renal vessels; Levels I–II correspond to pelvic lymph node dissection; Levels III–IV – lumbar dissection; created by the authors интра- и послеоперационные осложнения, количество койко-дней в послеоперационном периоде, частота переводов в ОРИТ. Оценку показателей выполнения тазового этапа лимфаденэктомии (I–II уровни) и гистерэктомии не проводили ввиду отсутствия предмета исследования.
Полученные в ходе исследования результаты были подвергнуты статистической обработке. При оценке качественных признаков использовали критерии χ2 Пирсона и Фишера, с последующим применением пост-хок теста при наличии значимых различий. Для количественных признаков применяли U-тест Манна–Уитни для сравнения двух групп и критерий Краскела–Уоллиса для сравнения более двух групп.
Результаты количественных данных были представлены в виде среднего арифметического и стандартной ошибки среднего (X±m), где m – ошибка среднего или квадратичное отклонение. Для медианы приведены значения интерквартильного размаха, минимальные и максимальные значения (min-max) были указаны в соответствующих случаях.
Результаты
В анализируемом исследовании были рассмотрены истории болезни 122 пациенток, средний возраст которых во всей выборке составил 63,8 ± ± 1,3 года. Средний возраст пациенток в каждой подгруппе представлен в табл. 1. Подгруппы пациенток относительно однородны по среднему возрасту.
Результаты исследования показали, что 58,2 % пациенток (n=71) имели различной степени нарушения жирового обмена (ИМТ>30). Самый высокий показатель ИМТ был зафиксирован в группе ЛСЗ и составил 32,8 кг/м2 (рис. 3). При попарном сравнении было установлено, что ИМТ пациенток в группе ЛС доступа был статистически значимо ниже, чем в группе ЛСЗ доступа. Для остальных доступов значимых различий не было выявлено.
Из всей выборки 11,4 % (n=14) больных страдали морбидным ожирением (ИМТ >40). В группе пациенток с морбидным ожирением 9 (64%) были прооперированы ЛСЗ доступом, среди них IV уровень лимфаденэктомии был достигнут у 7 (78,8 %). Одна пациентка была прооперирована РАЗ доступом, с достижением IV уровня лимфаденэктомии. Остальным 4 пациенткам выполнили лапаротомию, из которых у 2 (50 %) был достигнут уровень почечных сосудов. Показатели для пациенток с морбидным ожирением представлены на рис. 4.
Основные результаты оперативных вмешательств, полученные в ходе проведенного исследования при различных хирургических доступах, приведены в табл. 2. В рамках оценки травматичности вмешательства и течения послеоперационного периода помимо частоты осложнений рассчитывалась доля пациенток, нуждающихся в наблюдении в условиях отделения реанимации и интенсивной терапии (ОРИТ).
Òàблицà 1/Table 1
Ñðåдниé вîзðàñт пàциåнтîê в êàждîé пîдгðóппå
Average age of patients in each subgroup
Хирургический доступ/Surgical approach ЛТ/LT ЛС/LS ЛСЗ/LSR РАЗ/RAR
Средний возраст пациенток в подгруппе (лет)/Average age (years) 62,1 ± 1,2 65,1 ± 1,2 64,1 ± 1,4 63,9 ± 1,4
Примечание: ЛТ – лапаротомия; ЛС – лапароскопический трансабдоминальный доступ; ЛСЗ – лапароскопический забрюшинный доступ; РАЗ – робот-ассистированный забрюшинный доступ; таблица составлена авторами.
Note: LT – laparotomy; LS – laparoscopic transabdominal; LSR – laparoscopic retroperitoneal; RAR – robot-assisted retroperitoneal; created by the authors.
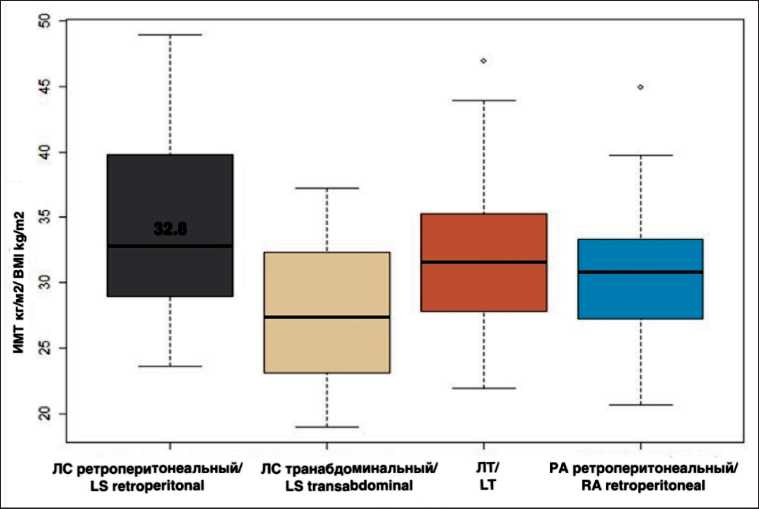
Рис. 3. Уровень ИМТ у пациенток в сравниваемых группах. Примечание: рисунок выполнен авторами
Fig. 3. BMI of patients in comparison groups. Note: created by the authors
^ £ h
§5
И
Лапароскопический ретроперитонеальный/ Laparoscopic retroperitoneal
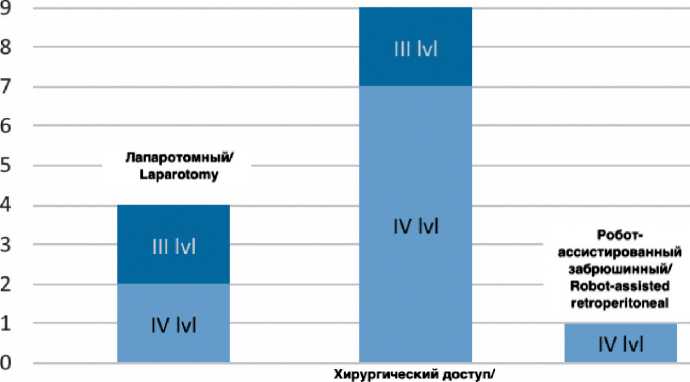
Рис. 4. Распределение пациенток с морбидным ожирением по группам сравнения. Примечание: рисунок выполнен авторами
Fig. 4. Distribution of patients with morbid obesity by comparison groups.
Notes: LT – laparotomy, LSr – laparoscopy retroperitoneal approach, RAr – robot-assisted retroperitoneal approach; created by the authors
Surgical approach
При сравнении длительности оперативных вмешательств наиболее «быстрыми» стали вмешательства, выполняемые ЛСЗ доступом, а наиболее «долгими» – РАЗ. При попарном сравнении выявлены статистически значимые отличия в показателях длительности операций для РАЗ доступа относительно ЛС, ЛСЗ и ЛТ доступов. В среднем длительность робот-ассистированного вмешательства была на 96 мин дольше по сравнению с другими доступами. Следует отметить, что длительность операций при ЛСЗ доступе включала переустановку троакаров с левой стороны на правую – для выполнения лимфаденэктомии парааортальной и паракавальной областей. При РАЗ доступе весь поясничный этап выполняли с левой стороны, что, в свою очередь, не привело к удлинению временных показателей.
При определении технических возможностей по достижению уровней лимфаденэктомии при различных хирургических доступах были получены следующие результаты. С помощью статистического анализа выявлено, что IV уровень лимфодиссекции чаще всего был достижим при ЛСЗ доступе (85,37 %, p-value=0,002) по срав-
Òàблицà 2/Table 2
Пîêàзàтåли îпåðàтивныõ вмåшàтåльñтв в зàвиñимîñти îт õиðóðгичåñêîгî дîñтóпà Surgical parameters depending on a surgical approach
|
Хирургический доступ/Surgical approach |
ЛТ/LT (n=28) |
ЛС/LS (n=30) |
ЛСЗ/LSR (n=41) |
РАЗ/RAR (n=23) |
p-value |
|
|
Длительность операции (мин)/ Duration of surgery (min) |
217 [200; 254] |
215 [180; 250] |
205 [190; 245] |
308* [255; 344] |
<0,001 |
|
|
Уровень лимфодиссекции/ Level of lymphodissection |
III IV |
18 (62,2 %) 10 (35,8 %) |
12 (40 %) 18 (60 %) |
6 (14,6 %)* 35 (85,4 %)* |
7 (30,5 %) 16(69,5 %) |
0,047 0,021 |
|
Средние значения ИМТ у пациенток с III уровнем ЛД/ Average BMI (III level of lymphodissection) |
31,8 (25,5–46,9) |
28,2* (22,6–31,6) |
33,3* (24,5–44) |
30,1 (20–32,4) |
0,095 |
|
|
Средние значения ИМТ у пациенток с IV уровнем ЛД/ Average BMI (IV level of lymphodissection) |
29,6 (26,2–37,9) |
27,5 * (19–35,3) |
31,7 * (19–48,9) |
31,4 (24–44) |
0,018 |
|
|
Кол-во тазовых лимфоузлов/Number of pelvic lymph nodes |
14,7 (6–27) |
13,8 (7–23) |
13,1 (6–26) |
10 (5–20) |
0,412 |
|
|
Кол-во поясничных лимфоузлов/ Number of lumbar lymph nodes |
8,1 (6–24) |
6,6 (5–16) |
8,9 (6–19) |
7 (6–12) |
0,478 |
|
|
Частота перевода в ОРИТ/Frequence of ICU care |
6 (21,4 %) |
2 (6,6 %) |
4 (9,8 %) |
10 (62,5 %)** |
<0,001 |
|
|
Кол-во койко-дней/Days in hospital |
6,9 (4–19) |
4,7 (2–7) |
4,7 (2–13) |
5,3 (3–10) |
0,017 |
|
|
Осложнения интраоперационные/ Intraoperative complications |
1 (3,6 %) |
2 (6,6 %) |
1 (2,4 %) |
1 (4,3 %) |
0,382 |
|
|
Осложнения послеоперационные/ Postoperative complications |
6 (21,4%)*** |
0 |
0* |
1 (4,3%) |
0,006 |
|
Примечания: * – различия, значимые в сравнении с ЛТ доступом; ** – различия, значимые в сравнении с ЛТ и ЛСЗ доступами;
*** – различия, значимые в сравнении с РАЗ доступом; ЛТ – лапаротомия, ЛС – лапароскопический трансабдоминальный доступ, ЛСЗ – лапароскопический забрюшинный доступ, РАЗ – робот-ассистированный забрюшинный доступ; ЛД – лимфодиссекция; таблица составлена авторами.
Note: * – statistically significant differences compared to LT access; ** – statistically significant differences compared to LT and LSZ accesses; *** – statistically significant differences compared to RAZ access; LT – laparotomy, LS – laparoscopic transabdominal, LSR – laparoscopic retroperitoneal, RAR – robot-assisted retroperitoneal; created by the authors.
нению с группой ЛТ. В это же время IV уровень статистически значимо реже наблюдался в группе ЛТ (35,7 %, p-value=0,004). Значимой корреляции между количеством лимфоузлов и методом хирургического доступа выявлено не было.
В свою очередь, при изучении факторов, препятствующих достижению IV уровня лимфаденэктомии, была обнаружена следующая зависимость: в группах ЛТ, ЛС и ЛСЗ средний ИМТ больных был обратно пропорционален доле достижения IV уровня лимфаденэктомии. В то же время в РАЗ подгруппе такого явления не прослеживалось. Исходя из этого, можно предположить, что высокий ИМТ не является ограничивающим фактором при робот-ассистированных операциях, в отличие от ЛС доступов.
Травматичность вмешательства при разных хирургических доступах оценивалась по течению раннего послеоперационного периода, в частности, по необходимости перевода пациентов в отделение ОРИТ. Переводы в ОРИТ статистически значимо чаще наблюдались при РАЗ доступе (62,5 % против 21,4 и 9,7 %, p-value<0,001) по сравнению с ЛСЗ и ЛТ группами. В данной ситуации это связано не столько с травматичностью операции, сколько с ее продолжительностью. Наименьший процент переводов в отделение интенсивной терапии отмечен в группе ЛС.
При анализе течения послеоперационного периода количество койко-дней в послеоперационном периоде для ЛТ, ЛС, ЛСЗ и РАЗ доступов в среднем составило 6 [5;6], 5 [4;5], 5 [3;6] и 5 [4;6] соответственно. При попарном сравнении было установлено, что количество койко-дней для ЛТ было статистически значимо выше, чем для ЛСЗ доступа. Для остальных анализируемых групп значимых различий не выявлено.
Для последовательной оценки произошедших осложнений последние были разделены на интра-и послеоперационные. Среди интраоперационных осложнений при ЛТ зафиксировано одно ранение наружной подвздошной вены, при ЛС – два повреждения нижней полой вены, при РАЗ – один случай ранения наружной подвздошной вены, а при ЛСЗ – один случай пересечения правого мочеточника в верхней трети при диссекции пара-кавального пространства. В каждом случае объем кровопотери не превышал 500 мл, и ни одно из повреждений сосудов не потребовало конверсии. При формировании анастомоза мочеточника на стенте был выполнен местный доступ по переднеподмышечной линии.
В послеоперационном периоде наибольшее количество осложнений зафиксировано при ЛТ доступе (24,9%). Среди них был один эпизод ранней спаечной кишечной непроходимости, одна эвентра-
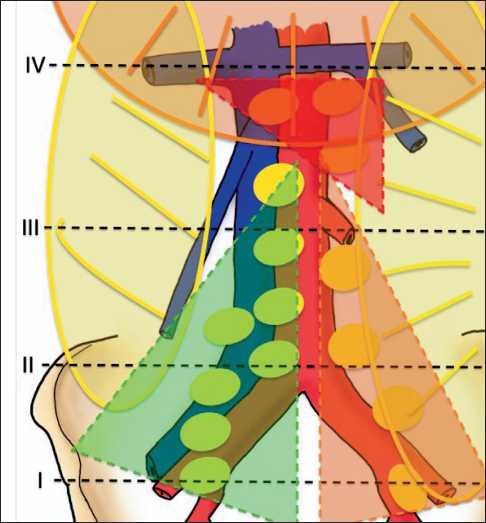
Рис. 5. Доступность зон предполагаемой лимфаденэктомии при трансабдоминальных доступах. Примечания: зеленая зона обозначает наиболее доступную зону; оранжевая – менее доступную зону; красная – труднодоступную; рисунок выполнен авторами
Fig. 5. Accessibility of the areas for proposed lymphadenectomy via transabdominal approaches. Notes: the green area denotes the most accessible area; orange – the less accessible area; red – the difficult to access area; created by the authors ция и четыре случая раневых осложнений (сером). В подгруппах ЛС и ЛСЗ доступов послеоперационных осложнений не было зафиксировано. Различия в частоте послеоперационных осложнений были статистически достоверными. В РАЗ группе произошло одно кровотечение из троакарного порта, объемом 1000 мл, потребовавшее релапароскопии, санации и коагуляции участка кровотечения.
Обсуждение результатов исследования
На данный момент целесообразность выполнения тазовой и поясничной лимфаденэктомии сохраняется у больных 1 стадией рака эндометрия с высоким риском лимфогенного метастазирования. При этом только полноценный объем лимфодис-секции до почечных сосудов приводит к улучшению результатов выживаемости [11–14]. Этот этап хирургического вмешательства стандартизован, однако сложность анатомических соотношений и эргономика доступа не позволяют называть его рутинным.
В особенности это актуально для пациенток с ИМТ свыше 30, доля которых в рамках нашего исследования составила 63,1 %. Таким образом, выбор хирургического доступа, позволяющего достичь IV уровня лимфодиссекции у пациенток с высоким ИМТ, становится значимой хирургической задачей.
При рассмотрении технических аспектов поясничной лимфаденэктомии исследуемые подгруппы целесообразно разделить на две когорты – трансабдоминальные вмешательства, куда входят ЛС и ЛТ, и забрюшинные, включающие ЛС и РА доступы. На рис. 5 представлены зоны расположения лимфоузлов в зависимости от сложности эргономических аспектов, обусловленных анатомическими соотношениями при трансабдоминальных доступах.
Зеленым треугольником обозначена зона пара-кавальных и аортокавальных лимфоузлов, которые при трансабдоминальных доступах достижимы сравнительно легко. После лигирования правой гонадной вены и мобилизации брыжейки восходящего отдела толстой кишки диссекция лимфоузлов возможна в этой области без каких-либо ограничений.
Анатомическая область, обозначенная оранжевым треугольником, в которой находятся лимфоузлы, прилежащие к левым общим подвздошным сосудам, и парааортальная клетчатка до уровня нижней брыжеечной артерии, представляется более трудоемкой для лимфаденэктомии. Это обусловлено необходимостью отдельной широкой мобилизации сигмовидной кишки и работой в узком «окне», ограниченном сверху ее брыжейкой, снизу аортой, а слева нижней брыжеечной артерией. Сложность этого этапа прямо пропорционально повышается с увеличением ИМТ пациентки. Длина нижней брыжеечной артерии в соотношении с выраженным развитием клетчатки брыжейки в этой зоне не позволяет свободно выполнять манипуляции. При этом топография левого мочеточника не всегда очевидна, поскольку его визуализация в средней и верхней трети при развитой жировой клетчатке затруднена.
Наиболее сложной зоной является анатомическая область, обозначенная красным треугольником. При операциях у пациенток с нормальным ИМТ анатомические соотношения позволяют мобилизовать двенадцатиперстную кишку, брыжейку нисходящего отдела толстой кишки, установить ретракторы или лифтинги при ЛС доступах. Основная сложность обусловлена формированием еще одного узкого «окна», ограниченного справа нижней брыжеечной артерией, снизу аортой, слева двенадцатиперстной кишкой, а сверху брыжейкой толстой кишки, что затрудняет безопасное выполнение парааортальной лимфаденэктомии на IV уровне. У больных с высоким ИМТ развитая висцеральная жировая клетчатка, в том числе паранефральная, брыжейка тонкой и толстой кишки дополнительно ограничивают пространство для диссекции и мобилизации анатомических структур.
В отличие от трансабдоминальных при забрюшинных доступах с перестановкой троакаров на правую сторону для паракавальной и аорто-кавальной диссекции узкие пространства, в которых приходилось бы работать со значитель- ными техническими трудностями, практически отсутствуют. Как указано в разделе «Материал и методы», выбор для диссекции слоя между мочеточником и магистральными сосудами позволяет полностью отвести от зоны операции все анатомические структуры. Так, брыжейка с гонадной веной и мочеточником отводятся кверху, а пара-нефральная клетчатка оттесняется в сторону за счет давления газа, что обеспечивает адекватную визуализацию лимфоузлов и пространство для манипуляций (рис. 6).
Отдельно стоит отметить особенности робот-ассистированных операций, которые позволяют осуществлять лимфаденэктомию в паракавальной и аортокавальной зоне без редокинга на правую сторону, за счет артикуляционной подвижности инструментов (рис. 7). В данном случае инструменты вводятся в указанные области через «окна», образованные аортой, нижней брыжеечной артерией и брыжейкой толстой кишки.
Таким образом, забрюшинные доступы более эргономичны для выполнения поясничного этапа лимфаденэктомии по сравнению с трансабдоминальными, что обусловлено анатомическими характеристиками этой области.
По данным нашего исследования, весьма значительные преимущества имел ЛСЗ-доступ. Статистически значимыми преимуществами стали частота достижения IV уровня лимфаденэктомии (85,4 %) и низкий процент осложнений по сравнению с ЛТ.
В ЛСЗ подгруппе была зафиксирована наименьшая продолжительность операций, которая в среднем составила 205 мин. У пациенток данной подгруппы были отмечены наибольшие значения ИМТ (32,8 кг/м2), что в совокупности с высокой частотой (85,4 %) достижения IV уровня лимфо-диссекции косвенно свидетельствует об отсутствии ограничивающего влияния этого фактора при данном доступе. Кроме того, при ЛСЗ доступе зафиксированы низкий процент переводов в ОРИТ (9,8 %), частота интра- и послеоперационных осложнений (2,4 и 0 % соответственно) и короткий срок госпитализации (4,7 койко-дней). Исходя из вышеизложенного, именно лапароскопический забрюшинный доступ можно считать методом выбора при необходимости выполнения поясничной лимфаденэктомии.
При лапароскопическом доступе основным преимуществом является малотравматичность (наиболее низкая частота перевода в ОРИТ после операций – 6,6 %, низкое число осложнений как интра-, так и послеоперационых – 6,6 %). У пациенток данной подгруппы ИМТ накладывал большее количество ограничений на выполнение адекватного объема операций. Cредний ИМТ составил 27,8 кг/м2, а процент достижения IV уровня лимфодиссекции 60 %. Таким образом, данный способ может считаться эффективным и безопас-
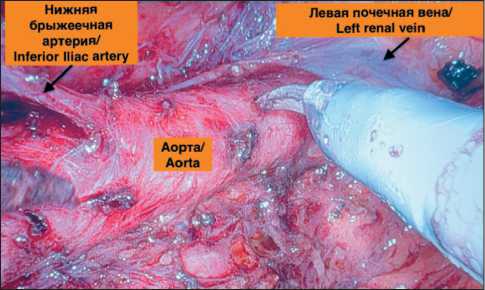
Рис. 6. Фотография парааортальной области при достижении IV уровня лимфодиссекции при робот-ассистированной поясничной лимфаденэктомии. Примечание: рисунок выполнен авторами
Fig. 6. Photo of the paraaortic region upon reaching level IV lymph node dissection during robot-assisted lumbar lymph-adenectomy. Note: created by the authors
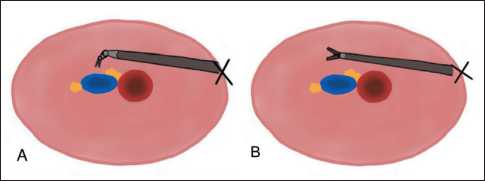
Рис. 7. А – артикуляционные бранши роботических инструментов позволяют манипулировать за аортой в паракавальной зоне; B – при лапароскопических операциях данная зона не удобна для лимфаденэктомии за счет ограничения подвижности инструментов. Примечание: рисунок выполнен авторами
Fig. 7. A – articulating branches of robotic instruments allow manipulation behind the aorta in the paracaval zone;
B – in laparoscopic surgery, this zone is not convenient for lymph-adenectomy due to limited mobility of instruments. Note: created by the authors ным для пациенток без нарушения жирового обмена. Однако у него нет преимуществ перед ЛСЗ доступом, следовательно, его можно рассматривать только как альтернативу последнему.
Лапаротомный доступ характеризовался наименьшим процентом достижения IV уровня лимфаденэктомии, который составил всего 35,7 %, что примерно соответствует доле пациенток без нарушения жирового обмена. Длительность операций в среднем составила 217 мин, что соответствовало средним значениям по всей выборке. Частота переводов пациенток в реанимацию была несколько выше (21,4 %), но без статистически достоверных различий. В данной подгруппе были отмечены более длительный срок госпитализации (6,9 койко-дней) и более высокий уровень интра- и послеоперационных осложнений (3,6 и 21,4 % соответственно). Можно заключить, что данный доступ значительно более травматичен, что в большинстве случаев не позволяет выполнять полный объем вмешательства. Это заставляет рассматривать лапаротомию как нежелательную альтернативу, актуальную только при невозможности выполнения операций малоинвазивным доступом.
При анализе показателей робот-ассистированных операций на первый план выходит значительная длительность хирургических вмешательств. Этим обусловлена высокая частота переводов пациенток в ОРИТ, которая составила 62,5 % и стала наибольшей во всей выборке. Данные показатели имели статистически достоверные отличия от ЛСЗ и других подгрупп. Частота осложнений находилась на среднем уровне. Тем не менее полный объем операций достигали у 68,5 % пациенток, что являлось вторым значимым показателем во всей выборке после ЛСЗ подгруппы. Фактически характеристики, уступающие ЛСЗ доступу, лишь увеличивают стоимость вмешательства. На данный момент, с учетом дороговизны и отсутствия очевидных преимуществ, роль робот-ассистированных операций по сравнению с лапароскопическими не определена. Однако сама по себе возможность выполнения полноценной лимфодиссекции без редокинга за счет артикуляции браншей и несколько лучшая визуализация – уникальные свойства, имеющие перспективу для развития.
Отдельное внимание стоит уделить характеристикам инструментария. При робот-ассистированных операциях применяют комбинацию биполярного граспера с монополярными ножницами, что в случае лапароскопических вмешательств вовсе привело к отказу от забрюшинного доступа на рубеже 2010-х гг. С внедрением новых поколений инструментов (таких как ультразвуковые ножницы


