Сравнительный анализ эффективности простого и многокомпонентного методов щелочной децеллюляризации на примере очистки волокнистого внеклеточного матрикса дермы
Автор: Калмыкова Н.В., Демьяненко И.А., Шевлягина Н.В., Андреевская С.Г., Суслов А.П.
Журнал: Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье @vestnik-reaviz
Рубрика: Морфология. Патология
Статья в выпуске: 1 (25), 2017 года.
Бесплатный доступ
Щелочная децеллюляризация является одним из наиболее распространенных методов получения очищенного внеклеточного матрикса (ВКМ). Тем не менее, в литературе отсутствуют работы, посвященные сравнительному анализу эффективности различных методов щелочной очистки ВКМ. В настоящей работе было проведено сравнительное исследование влияния простого метода децеллюляризации раствором гидроксида натрия и многокомпонентного метода несколькими различными растворами на основе гидроксида натрия и сульфата натрия на биохимические, морфологические и термомеханические характеристики волокнистого внеклеточного матрикса дермы крупного рогатого скота (КРС), а именно быка домашнего Bos taurus taurus. Показано, что оба метода вызывают эффективное удаление клеточных компонентов из ВКМ. Однако в образцах, очищенных многокомпонентным методом выявлено меньшее количество остаточной дцДНК. Результаты морфологического и термомеханического исследований свидетельствуют о том, что применение многокомпонентной децеллюляри-зации по сравнению с простой обработкой гидроксидом натрия приводит к уменьшению дезорганизации волокнистой сети ВКМ с сохранением структуры коллагеновых волокон, а также к увеличению эластичности материала. Полученные данные указывают на большую сохранность нативной структуры децеллюляризированного ВКМ дермы КРС при применении щелочной очистки с использованием растворов, содержащих соли сульфата. По результатам работы можно заключить, что использование многокомпонентного метода является более предпочтительным для осуществления щелочной децеллюляризации дермы КРС.
Децеллюляризация, внеклеточный матрикс, дерма
Короткий адрес: https://sciup.org/14344254
IDR: 14344254 | УДК: 57.085
Comparative analysis of efficiency of simple and multicomponent methods of alkaline decellularization through the example of cleaning of fibered extracellular matrix of derma
Alkaline decellularization is one of the most common methods of obtaining a purified extracellular matrix (ECM). Nevertheless, there are no works in the literature devoted to a comparative analysis of the effectiveness of various methods of alkaline purification of ECM. The present work runs about a comparative study of the effect of a simple method of decellularization with sodium hydroxide solution and a multicomponent method by several different solutions based on sodium hydroxide and sodium sulfate on the biochemical, morphological and thermomechanical characteristics of the fibrous extracellular matrix of cattle dermis, namely, the Bos taurus taurus. It is shown that both methods cause effective removal of cellular components from the ECM. However, in samples purified with a multicomponent method, less residual dsDNA was detected. The results of morphological and thermomechanical studies indicate that the use of multicomponent decellularization in comparison with simple treatment with sodium hydroxide leads to a decrease in the disorganization of the ECM fibrous network, while maintaining the structure of the collagen fibers, and also to an increase in the elasticity of the material. The data obtained indicate a greater preservation of the native structure of the decellularized ECM dermis of cattle with alkaline purification using solutions containing sulfate salts. Based on the results of the work, it can be concluded that the use of a multicomponent method is more preferable for the implementation of alkaline decellularization of the cattle dermis.
Текст научной статьи Сравнительный анализ эффективности простого и многокомпонентного методов щелочной децеллюляризации на примере очистки волокнистого внеклеточного матрикса дермы
Введение. Биологические свойства очищенного от клеточных компонентов внеклеточного матрикса (ВКМ) различных тканей, включающие способность к индукции пролиферации, миграции и дифференцировки клеток, а также к активации процессов ремоделирования собственных тканей организма реципиента, обуславливают интенсивное использование медицинских изделий и препаратов на его основе в регенеративной медицине и пластической хирургии [1]. Описано множество способов децеллюляризации тканей путем разнообразных химических и физических воздействий [2]. С одной стороны, применяемая для очистки ВКМ методика в идеале должна обеспечивать максимальную сохранность его трехмерной ультраструктуры, пространственной топологии и химического состава. Поскольку преобладающим источником для изготовления большинства децеллюляризированых матриксов для медицинского применения являются ксеногенные ткани [3], то процедура получения очищенного ВКМ должна обеспечивать отсутствие реакции отторжения ксенотрансплантата при его имплантации в ткани пациента. В связи с этим распространение получили методики децеллю-ляризации на основе обработки ВКМ растворами на основе щелочей. Щелочные растворы вызывают эффективный гидролиз и солюбилизацию клеточных компонентов, а также белков и гликопротеинов ВКМ, чье присутствие в матриксе может провоцировать неблагоприятный ответ организма реципиента. В то же время использование щелочных растворов может вызывать существенные изменения структурных и термомеханических характеристик матрикса за счет частичных гидролиза и денатурации молекул коллагена, разрушения межмолекулярных сшивок, модификации боковых групп аминокислот, дезорганизации пучков волокон коллагена вследствие чрезмерного набухания [4, 5, 6, 7, 8, 9]. В этой связи при осуществлении децеллюляризации ВКМ щелочами необходимо контролировать pH используемых растворов и продолжительность очистки для обеспечения приемлемых целостности структуры, биологических, химических и физических параметров. Кроме того, в ряде работ предложено вносить в щелочные растворы для очистки соли сульфатов, что препятствует избыточному набуханию пучков волокон коллагена ВКМ [7, 10, 11]. Таким образом, исследования оптимальных условий получения децеллюляризованного ВКМ путем обработки растворами на основе щелочей является актуальными. В то же время в литературе отсутствуют работы, посвященные сравнительному анализу эффективности различных методов щелочной очистки ВКМ, а также их влияния на его морфологию и основные физические характеристики.
Цель исследования. Целью настоящего исследования явилась сравнительная характеристика морфологических, биохимических и термомеханических показателей децеллюляризи-рованного ВКМ сетчатого слоя дермы КРС, полученного путем простой щелочной очистки раствором гидроксида натрия и многокомпонентной щелочной очистки несколькими различными растворами на основе гидроксида натрия и сульфата натрия.
Материалы и методы. Изготовление децеллюляризированного ВКМ. Для изготовления децеллюляризованного ВКМ дермы использовали кожу крупного рогатого скота (КРС), а именно быка домашнего Bos taurus taurus, полученную на предприятии ООО «ПОКС». Забор кожи проводили из чепрачной зоны животных возрастом 16–18 месяцев, имеющих массу шкуры 22–25 кг. Перед химической обработкой кожу промывали водой для удаления механических включений. Затем при помощи доильной машины удаляли гиподерму и сосочковый слой дермы. Полученный сетчатый слой дермы толщиной 4 мм разрезали на лоскуты размером 20×20 см, которые использовали в дальнейшей работе.
Инкубацию фрагментов дермы в растворах проводили при температуре 20 °С в лабораторных стаканах на орбитальном шейкере «SkyLine» (ELMI, Латвия) при 250 об/мин. Соотношение объема растворов к массе образца составляло 20 мл/г.
Процесс децеллюляризации дермы осуществляли двумя различными способами. Каждая экспериментальная группа состояла из четырех лоскутов. Также для исследования использовали четыре фрагмента сетчатого слоя дермы, не прошедшего химическую обработку.
Фрагменты лоскутов первой экспериментальной группы (однокомпонентный метод очистки) обрабатывали раствором 1М NaОH на дистиллированной воде в течение 20-ти часов. При этом каждый час проводили замену раствора на свежий. Затем лоскуты дермы извлекали и промывали дистиллированной водой до достижения pH смыва нейтральных значений.
Лоскуты второй экспериментальной группы (многокомпонентный метод очистки) подвергали последовательной обработке 4-я растворами [12]. Сначала образцы инкубировали в солевом растворе 0,35М NaOH в течение 20 часов, затем 20 часов обрабатывали раствором 1,25М NaOH и 1,5М Na 2 SО 4 и отмывали дистиллированной водой в течение 30 мин. После этого лоскуты помещали в раствор 1,3М Na 2 SO 4 на 20 часов и отмывали дистиллированной водой в течение 30 мин. На заключительном этапе для отмывки от солей образцы обрабатывали раствором 1М H 3 BO 3 на протяжении 20 часов, и отмывали дистиллированной водой до достижения pH смыва нейтральных значений. На всем протяжении химической обработки проводили замену всех растворов на свежеприготовленные каждый час.
По окончании процесса очистки образцы обеих экспериментальных групп лиофильно высушивали на приборе Hetosicc (Дания).
Гистологическое исследование. Для морфологической оценки эффективности удаления клеточных компонентов, а также влияния химической обработки на структуру ВКМ полученные образцы подвергали гистологическому исследованию. Для этого вырезали фрагменты децеллюляризованного различными способами ВКМ, а также сетчатого слоя дермы до обработки, размером 5×5 мм2. Данные фрагменты фиксировали 10 % формалином на фосфатном буфере в течение 72 часов. После этого образцы обезвоживали по стандартной методике и заливали в заливочную среду на основе парафина Histomix Extra (Биовитрум, Россия). На микротоме Microm HM 325 (Thermo Scientific, США) изготавливали гистологические срезы толщиной 3 мкм, которые монтировали на предметные стекла с полилизиновым покрытием. Срезы окрашивали гематоксилином и эозином и заключали под покровное стекло в заливочную среду Bio-Mount (Bio Optica, Италия). Полученные препараты анализировали при помощи микроскопа NikonNi-U (Nikon, Япония). Микрофотографии получали при помощи цифровой камеры Nikon DS-Fi1 (Nikon, Япония), вмонтированной в тринокулярную насадку микроскопа.
Сканирующая электронная микроскопия. Для анализа пространственной структуры образцов ВКМ использовали метод сканирующей электронной микроскопии. Для исследования иссекали фрагменты образцов размером 4×1 мм2, и закрепляли их на алюминиевом столике микроскопа при помощи силикатного клея. Затем образцы анализировали с помощью сканирующего двулучевого электронного микроскопа Quanta 200 3D (FEI Company, USA) с предварительным напылением золотом на модуле “SPI-MODULE Sputter Coater” (SPI Supplies, USA). Толщина слоя золота (проба 999) составила 7 нм. Исследование напыленных образцов проводили в режиме высокого вакуума, при ускоряющем напряжении сканирующего микроскопа 5 кВ. Получали и анализировали изображения перпендикулярно расположенных верхней и боковой поверхностей фрагментов ВКМ. На изображениях верхней поверхности при помощи программы Scadium OLYMPUS (Германия) производили подсчет количества пор и их диаметра на площади образца равной 7,82 мкм2.
Электрофорез в ПААГ в присутствии додецилсульфата натрия по Лэммли. Для качественной оценки целостности α-цепей молекул тропоколлагена проводили исследование полученных децеллюляризованных ВКМ, а также контрольного образца коллагена I типа (Sigma, США) методом электрофореза в ПААГ [13]. Для этого образцы в концентрации 10 мг/мл нагревали при 95 °С в течение 5 мин в 1М Tris-HCl буфере (pH 6,8), содержавшем 10 % SDS, 40 % глицерина 14,5 М 2-меркаптоэтанола и 0,01 % бромфенолового синего. Затем 7 мкл раствора вносили в лунки концентрирующего геля. Образцы подвергали 1,5 часовому электрофоретическому разделению в концентрирующем (5 %) и разделяющем (7,5 %) ПААГ в буфере (pH 8,3), содержавшем 25 mM Tris, 250 mM glycine и 0,1 % SDS. Напряжение и сила тока при этом составляла 80 V, 20 мА и 120 V, 40 мА в концентрирующих и разделяющих гелях соответственно. После разделения гели инкубировали в растворе уксусная кислота /этанол/ вода в соотношении 1:4:5 в течение 15 минут. Затем 20 мин окрашивали в том же растворе с добавлением 0,4 % Coomassie Blue R250. Гель отмывали 60 мин в 5 % уксусной кислоте и инкубировали в дистиллированной воде в течение ночи при постоянном покачивании.
Количественное определение дцДНК в образцах очищенного ВКМ. Содержание дцДНК является показателем, свидетельствующим об эффективности удаления клеточных компонентов при получении очищенного ВКМ [14]. Для количественной оценки дцДНК при помощи набора «ДНК-сорб-С» (АмплиСенс, Россия) проводили выделение тотальной ДНК из фрагментов образцов массой 25 мг. Количество выделенной двухцепочечной ДНК определяли флуориметрически на приборе Qubit 2.0 (Invitrogen, США), используя набор реагентов Qubit dsDNA HS Assay Kit (Invitrogen, США). После этого рассчитывали содержание ДНК в нг/мг сухой массы образца.
Определение термомеханических свойств. Термомеханические свойства являются важным показателем, определяющим возможности применения биосовместимых материалов [15, 16, 17]. Для исследования влияния щелочной децеллюляризации на термомеханические характеристики очищенного ВКМ проводили определение температуры сваривания (Т), удлинения при разрыве, а также предела прочности при растяжении. Определение температуры сваривания проводили на фрагментах образцов, размером 6×0,3 см2 после предварительной инкубации в 10-кратном объеме дистиллированной воды в течение 18 часов при температуре 20 °С при помощи прибора по ГОСТ 938.25-73. Образец насаживали на крючки прибора. В емкость прибора наливали 100 мл дистиллированной воды. Прибор с водой и образцом плотно закрывали крышкой. Затем включали подогрев и определяли Т сваривания двух образцов. За Т сваривания принимали среднее арифметическое результатов испытания двух фрагментов одного образца.
Удлинение при разрыве, а также предел прочности при растяжении анализировали на фрагментах образцов, размером 12×2 см, при помощи разрывной машины РТ-250 (Россия) по ГОСТ 938.11-69. В разрывную машину типа РТ-250 устанавливали образец, зажимая головные части образца между зажимами точно посередине. Во время проведения испытания фиксировали момент появления трещин на поверхности образца, фиксировали величину нагрузки и величину по шкале удлинений при разрыве. Предел прочности при растяжении σ в Па вычисляли по формуле о = -,
F, где P – нагрузка при разрыве (устанавливают по шкале разрывной машины); F – площадь поперечного сечения образца на участке разрыва в м2.
Удлинение при разрыве в процентах вычисляли по формуле:
М
6 = -.
100 ,
где ∆l – удлинение, соответствующее заданному напряжению, мм; l – первоначальная рабо- чая длина образца в мм).
Статистическая обработка результатов. Статистическую обработку результатов проводили с использованием программы STATISTICA 7.0. Данные на диаграммах и таблице представлены в виде среднего арифметического значения ± стандартное отклонение. Для оценки статистической значимости отличий между двумя экспериментальными группами применяли непараметрический критерий Манна-Уитни. Статистически значимыми считали различия при р < 0,05 (на диаграммах и таблице обозначены звездочкой) (табл. 1).
Таблица 1
Термомеханические показатели образцов, полученных методами простой (группа 1) и многокомпонентной очистки (группа 2), а также сетчатого слоя дермы до химической обработки
|
Температура сваривания, °С |
Предел прочности при растяжении, Па |
Удлинение при разрыве, мм |
|
|
Группа 1 |
58,0 ± 0,8 |
1,3 ± 0,2 |
71,2 ± 1,0 |
|
Группа 2 |
60,3 ± 3,0 |
0,3 ± 0,2* |
78,5 ± 2,1* |
|
Дерма |
65,3 ± 1,0 |
5,8 ± 0,1 |
125,5 ± 9,8 |
Примечание: * - p < 0,05 (по сравнению с группой 1).
Результаты, обсуждение. Обработка растворами щелочей известна, как один из наиболее эффективных методов получения децеллюляризированного ВКМ из плотных волокнистых соединительных тканей [9]. В настоящей работе нами было проведено сравнительное исследование влияния одно- и многокомпонентной методик щелочной очистки ВКМ на его основные биохимические, морфологические и термомеханические характеристики. В качестве однокомпонентного метода применяли обработку простым высокощелочным раствором 1М NaOH. Ранее применение данного раствора в сочетании с обработкой трипсином было успешно использовано для децеллюляризации дермы [18]. В качестве сложного многокомпонентного метода использовали методику [12], включающую (1) предварительную обработку ткани слабощелочным раствором 0,35 М NaOH, (2) обработку высокощелочным раствором 1,25 М NaOH и 1,5М Na 2 SО 4 , обработку слабокислыми растворами (3) 1,3 М Na 2 SO 4 и (4) 1 М H 3 BO 3 .
Согласно опубликованным данным, наиболее часто источником децеллюляризированного ВКМ для производства медицинских изделий являются дерма кожи, подслизистая оболочка тонкого кишечника и перикард ксеногенного происхождения [19]. В настоящей работе для данной цели нами был использован сетчатый слой дермы кожи КРС, что обусловлено простотой его получения в необходимых количествах и высокой коммерческой доступностью.
Данные литературы свидетельствуют о том, что наличие остаточных клеточных фрагментов в очищенном ВКМ в значительной степени способствует развитию неблагоприятной тканевой реакции при его имплантации [20]. Гистологическое исследование образцов ВКМ не выявило наличия в них клеток или же клеточных фрагментов как после однокомпонентной, так и после многокомпонентной щелочной очистки (рис. 1). При этом среднее значение содержания дцДНК в образцах составило 13,1 и 7,2 нг/мг сухой массы соответственно (рис. 2). В то же время количество дцДНК в сетчатом слое дермы до децеллюляризации составило в среднем 3295 нг/мг сухой массы (данные не показаны). Содержание дцДНК в очищенном ВКМ в количестве менее 50 нг/мг сухой массы ранее было предложено в качестве критерия эффективной децеллюляризации [1]. Таким образом, результаты как гистологического, так и биохимического исследования свидетельствуют об эффективности удаления клеток из ВКМ дермы кожи обоими методами. В то же время статистический анализ выявил достоверное снижение количества дцДНК в ВКМ, очищенном многокомпонентным методом по сравнению с однокомпонентным, что свидетельствует о более эффективном удалении остаточных клеточных компонентов. Известно, что высокая ионная сила раствора способствует диссоциации ДНК и белков [21]. В связи с этим можно предположить, что наблюдаемое снижение количества остаточной ДНК может быть обусловлено повышением ионной силы растворов за счет внесения в них сульфата натрия.
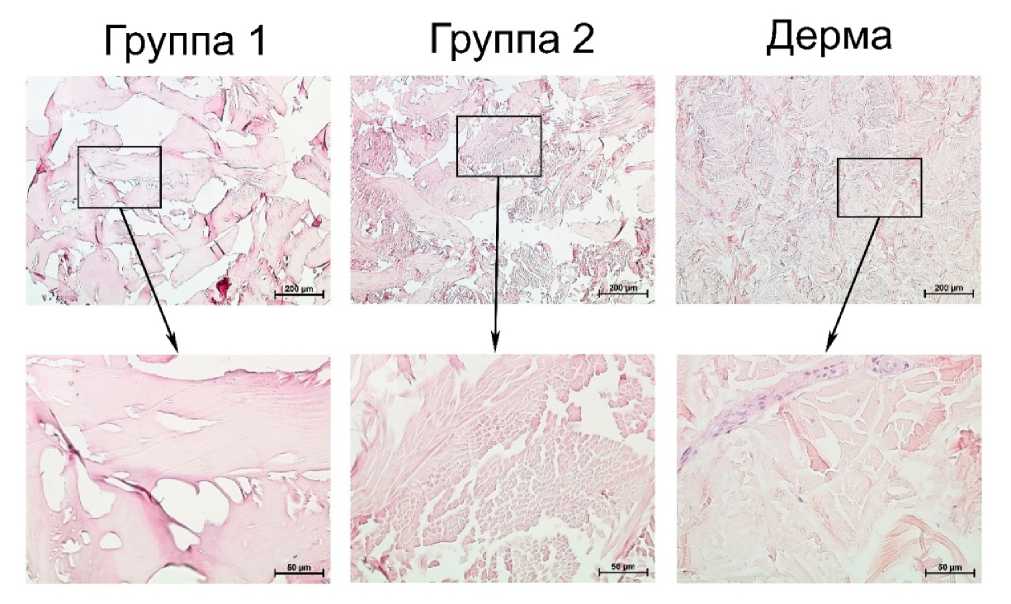
Рис. 1. Репрезентативные микрофотографии поперечных гистологических срезов сетчатого слоя дермы КРС (дерма) и ВКМ, полученных методами простой (группа 1) и многокомпонентной очистки (группа 2). Окрашивание гематоксилном и эозином
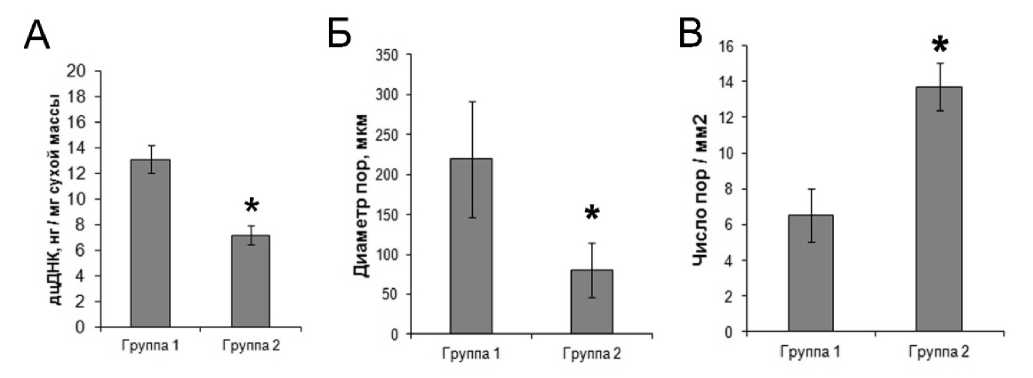
Рис. 2. Содержание дцДНК (А), а также размер (Б) и количество пор (В) во ВКМ, полученных методами простой (группа 1) и многокомпонентной очистки (группа 2): * – p < 0,05 (по сравнению с группой 1)
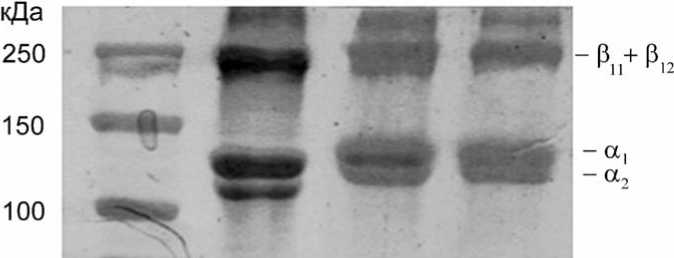
Щелочную децеллюляризацию относят к одному из самых «жестких» методов очистки ВКМ [1, 9]. С одной стороны, гидролизующая активность щелочей обеспечивает иммунологическую безопасность получаемого биосовместимого материала за счет солюбилизации клеточных компонентов и гликопротеинов, содержащих эпитоп галактоза-альфа (1-3)галактоза (aGal) [18]. С другой стороны, чрезмерное воздействие щелочи может привести к гидролизу белков матрикса, что окажет значительное влияние на его структуру и биологические свойства. Анализ результатов электрофоретического разделения полученных образцов очищенного ВКМ в ПААГ в денатурирующих условиях (рис. 3) показал наличие на электрофореграммах полос, характерных для димеров (β полоса – α1α2 или α1α1) и мономеров молекул α цепей тропоколлагена (α1 и α2 полосы), возникающих при разделении коллагена I типа [22]. Полученные данные свидетельствуют о значительном преобладании данного белка в ВКМ, очищенном при помощи обеих методик. Кроме того, в обоих случаях электрофореграммы указывают на отсутствие значительного гидролиза цепей, составляющих молекулы тропоколлагена. Таким образом, используемые методы щелочной децеллюляризации обеспечивают сохранение целостности цепей основного структурного белка ВКМ сетчатого слоя дермы.
Маркер Коллаген Группа 1 Группа 2 I типа
75 <■►
Рис. 3. Результаты электрофоретического разделения в ПААГ образцов ВКМ, полученных методами простой (группа 1) и многокомпонентной очистки (группа 2), а также контрольного образца коллагена I типа (коллаген I типа)
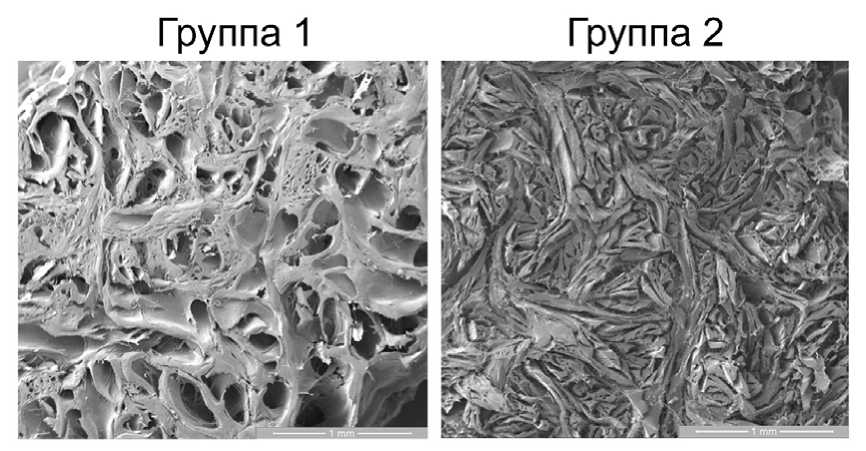
Существенным фактором, влияющим на пространственную топологию очищенного ВКМ, является набухание пучков волокон коллагена, происходящее при обработке щелочными растворами. Процесс набухания обусловлен ионизацией боковых групп цепей тропоколлагена, происходящей в растворе с высоким pH, а также вследствие диссоциации связанных с коллагеном молекул гликозамигликанов [7]. «Щелочное набухание» приводит к увеличению расстояния между пучками волокон коллагена и, как следствие, к «разрыхлению» сети волокнистого компонента ВКМ и увеличению его «пористости». Добавление в щелочной раствор различных солей сульфата известно в качестве способа, позволяющего уменьшить набухание ВКМ [5, 7, 11] за счет связывания большого количества молекул воды при сольватации сульфат ионов. В используемом в настоящей работе многокомпонентном методе щелочной очистки сульфат натрия был добавлен в высокощелочной раствор на втором этапе обработки дермы. После этого образцы инкубировали в растворе, содержащем только сульфат натрия. На заключительном этапе применяли обработку борной кислотой для нейтрализации оставшихся щелочных компонентов и удаления избытка солей [10]. Сравнительное гистологическое исследование полученных образцов очищенного ВКМ показало уменьшение плотности упаковки пучков волокон коллагена по сравнению с интактной дермой (рис. 1), менее выраженное в образцах, подвергнутых многокомпонентной обработке по сравнению с однокомпонентной. Качественный анализ срезов боковых поверхностей данных образцов методом СЭМ также показал увеличение «разрыхления» сети волокон ВКМ после од- нокомпонентной очистки относительно многокомпонентной (рис. 4). Морфологическая структура ВКМ, очищенного обоими методами, была представлена разнонаправленными тяжами пучков коллагеновых волокон со значительно варьирующей толщиной (10–300 мкм). Структура данных тяжей на гистологических препаратах образцов, полученных однокомпонентным методом, была преимущественно гомогенна (рис. 1). В то же время в ВКМ, полученном многокомпонентным методом, в составе тяжей были хорошо различимы волокна, диаметром 1–10 мкм (рис. 1), что соответствует диаметру волокон коллагена [23, 24].
Группа 1
Группа 2
Рис. 4. Репрезентативные микрофотографии срезов боковой поверхности ВКМ, полученных методами простой (группа 1) и многокомпонентной очистки (группа 2). Сканирующая электронная микроскопия
Исследование верхней поверхности образцов методом СЭМ также позволило визуализировать отдельные коллагеновые волокна в составе разнонаправленных пучков ВКМ после многокомпонентной очистки (рис. 5), тогда как пучки в составе ВКМ после однокомпонентной очистки имели преимущественно аморфную структуру (рис. 5). Морфометрический анализ СЭМ-микрофотографий верхней поверхности пластов ВКМ выявил значительные отличия между двумя экспериментальными группами по размерам и количеству пор в материале. Так, средняя величина диаметра пор в образцах, обработанных по многокомпонентной методике (79,9 мкм), была более чем в 2 раза меньше, чем в образцах, очищенных однокомпонентным методом (218,6 мкм), а количество пор на единицу площади, наоборот – в среднем в 2 раза больше (рис. 2).
В целом, результаты морфологического исследования свидетельствуют о том, что щелочная децеллюляризация оказывает значительное влияние на структуру ВКМ дермы. Однако применение многокомпонентного метода обеспечивает лучшую сохранность его волокнистого компонента по сравнению с однокомпонентным. При использовании многокомпонентного метода не происходит дезорганизации структуры коллагеновых волокон в составе пучков, вызываемой, вероятно, «щелочным набуханием» образцов. Менее выраженное «разрыхление» волокнистого матрикса, очевидно, обуславливает уменьшение размера пор и увеличения их числа. Согласно данным литературы, уменьшение структурных элементов трехмерных матриксов способствует увеличению жизнеспособности, ускорению миграции и дифференцировки клеток при культивировании в системе in vitro [25], что связывают с увеличени- ем площади поверхности и, как следствие, количества доступных сайтов связывания с рецепторами клеточных мембран. Также показано, что фибробласты при контакте с матриксом могут связываться с порами широкого диапазона диаметров: от 63 до 150 мкм, но при этом их жизнеспособность увеличивается с уменьшением размера пор материала [26]. Исходя из этого, можно предположить, что структура ВКМ, очищенного многокомпонентным методом будет обеспечивать лучшие кондуктивные свойства материала при использовании его в качестве скаффолда для регенерации соединительной ткани.
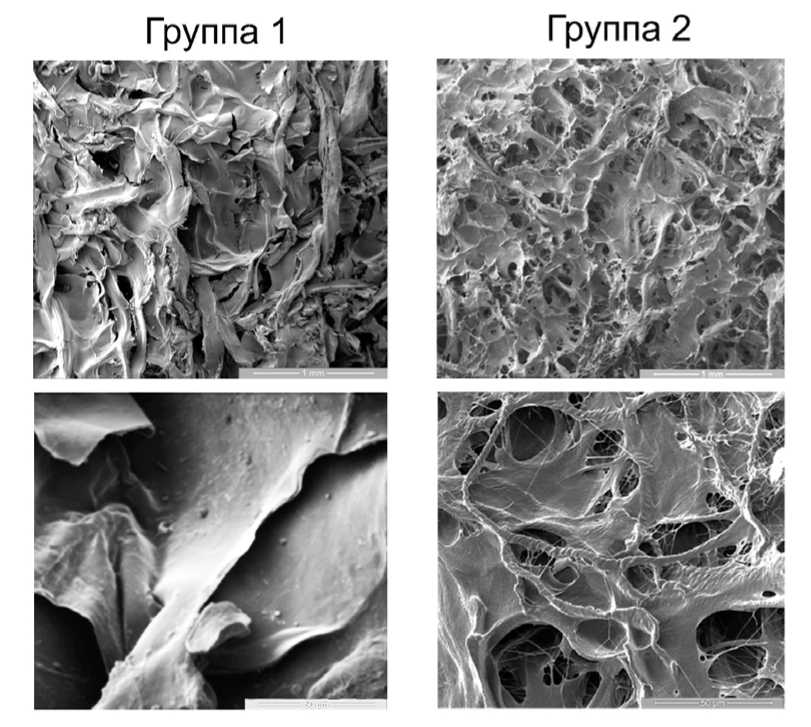
Группа 1
Рис. 5. Репрезентативные микрофотографии верхней поверхности ВКМ, полученных методами простой (группа 1) и многокомпонентной очистки (группа 2). Сканирующая электронная микроскопия
Понижение как термостабильности, так и механических свойств при децеллюляризации главным образом связывают с процессом разрушения и вымывания гликозаминогликанов, входящих в состав гликопротеинов, участвующих в процессе «упаковки» волокон коллагена в пучки [7]. Исследование термомеханических показателей выявило, что оба метода щелочной очистки ВКМ вызывают значительное снижение температуры сваривания, предела прочности при растяжении и удлинения при разрыве по сравнению с интактной дермой (табл. 1).
Очевидно, что данный эффект напрямую связан с обнаруженными структурными изменениями матрикса (рис. 1), вызванными химической обработкой. Сравнительный анализ де-целлюляризованных ВКМ показал уменьшение величины прочности при растяжении и увеличение удлинения при разрыве в образцах, очищенных многокомпонентным методом, по сравнению с однокомпонентным (табл. 1). Вероятно, утолщение и структурная гомогенность пучков волокон коллагена, вызванные «щелочным набуханием», обуславливают большую механическую прочность ВКМ, полученного однокомпонентным методом очистки. В то же время подобная дезорганизация сети волокнистого матрикса приводит к потере его эластичности, проявляющейся в уменьшении удлинения при разрыве.
Выводы. Результаты проведенного исследования свидетельствуют о том, что изученные методики щелочной децеллюляризации ВКМ дермы КРС позволяют эффективно удалить клеточные компоненты, не вызывая гидролиза цепей молекул тропоколлагена. Применение многокомпонентного метода очистки, включающего обработку дермы высокощелочным и отмывочным растворами, содержащими сульфат натрия, позволяет по сравнению с однокомпонентной высокощелочной обработкой: (1) уменьшить количество остаточной ДНК, (2) уменьшить дезорганизацию волокнистой сети ВКМ с сохранением структуры коллагеновых волокон, (3) уменьшить размер и увеличить число пор в материале, (4) снизить потерю его эластичности. Полученные данные указывают на большую сохранность нативной структуры децеллюляризированного ВКМ при данном методе очистки. Можно заключить, что использование многокомпонентной очистки с использованием растворов, содержащих соли сульфата, является более предпочтительным для осуществления щелочной децеллюляризации дермы КРС. Однако применение простого однокомпонентного метода очистки высокощелочным раствором гидроксида натрия может быть оправдано в случае необходимости получения матрикса с более высокими прочностными характеристиками.
Список литературы Сравнительный анализ эффективности простого и многокомпонентного методов щелочной децеллюляризации на примере очистки волокнистого внеклеточного матрикса дермы
- Crapo P.M., Gilbert T.W., Badylak S.F. An overview of tissue and whole organ decellularization processes. Biomaterials. 2011; 32 (12): 3233-3243 DOI: 10.1016/j.biomaterials.2011.01.057
- Badylak S.F., Taylor D., Uygun K. Whole-organ tissue engineering: decellularization and recellularization of threedimensional matrix scaffolds. Annu Rev Biomed Eng. 2011; 13: 27-53 DOI: 10.1146/annurev-bioeng-071910-124743
- Badylak, S.F. Xenogeneic extracellular matrix as a scaffold for tissue reconstruction. Transpl Immunol. 2004; 12: 367-377 DOI: 10.1016/j.trim.2003.12.016
- Goissis G., da Silva Maginador S.V., da Conceigao Amaro Martins V. Biomimetic mineralization of charged collagen matrices: in vitro and in vivo study. Artifical organs. 2003; 27 (5): 437-443.
- Reing J.E., Brown B.N., Daly K.A., Freund J.M., Gilbert T.W., Hsiong S.X., Huber A., Kullas K.E., Tottey S., Wolf M.T., Badylak S.F. The effects of processing methods upon mechanical and biologic properties of porcine dermal extracellular matrix scaffolds. Biomaterials. 2010; 31(33): 8626-8633 DOI: 10.1016/j.biomaterials.2010.07.083
- Sheridan W.S., Duffy G.P., Murphy B.P. Mechanical characterization of a customized decellularized scaffold for vascular tissue engineering. J Mech Behav Biomed Mater. 2012; 8: 58-70 DOI: 10.1016/j.jmbbm.2011.12.003
- Mendoza-Novelo B., Avila E.E., Cauich-Rodnguez J.V., Jorge-Herrero E., Rojo F.J., Guinea G.V., Mata-Mata J.L. Decellularization of pericardial tissue and its impact on tensile viscoelasticity and glycosaminoglycan content. Acta Biomater. 2011; 7: 1241-1248 DOI: 10.1016/j.actbio.2010.11.017
- Tsuchiya T., Balestrini J.L., Mendez J., Calle E.A., Zhao L., Niklason L.E. Influence of pH on extracellular matrix preservation during lung decellularization. Tissue Eng Part C Methods. 2014; 20(12): 1028-1036 DOI: 10.1089/ten.TEC.2013.0492
- Keane T.J., Swinehart I., Badylak S.F. Methods of tissue decellularization used for preparation of biologic scaffolds and in vivo relevance. Methods. 2015; 16(84): 25-34 DOI: 10.1016/j.ymeth.2015.03.005
- Goissis G., Piccirili L., Goes J.C, Plepis A., Das-Gupta D.K. Anionic Collagen: Polymer Composites with Improved Dielectric and Rheological Properties. Artif organs. 1998; 22(3): 203-209.
- Bet M.R., Goissis G., Lacerda C. Characterization of polyanionic collagen prepared by selective hydrolysis of asparagine and glutamine carboxyamide side chains. Biomacromolecules. 2001; 2(4): 1074-1079.
- Patent № 2353397 RF. Biorassasyvaemaja kollagenovaja matrica, sposob ee poluchenija i primenenija. Safojan A.A., Nesterenko S.V., Nesterenko V.G., Alekseeva N.Ju.
- Laemmli, U. K. Cleavage of structural proteins during the assembly of the head of bacteriophage T4. Nature.1970; 227: 680-68.
- Gilbert T.W., Freund J.M., Badylak S.F. Quantification of DNA in biologic scaffold materials. J Surg Res. 2009; 152(1): 135-139 DOI: 10.1016/j.jss.2008.02.013
- Liang H.C., Chang Y., Hsu C.K., Lee M.H., Sung H.W. Effects of crosslinking degree of an acellular biological tissue on its tissue regeneration pattern. Biomaterials. 2004; 25(17): 3541-3552 DOI: 10.1016/j.biomaterials.2003.09.109
- Burger J.W., Halm J.A., Wijsmuller A.R., ten Raa S., Jeekel J. Evaluation of new prosthetic meshes for ventral hernia repair. Surg endosc. 2006; 20(8): 1320-1325 DOI: 10.1007/s00464-005-0706-4
- Gaertner W.B., Bonsack M.E., Delaney J.P. Experimental evaluation of four biologic prostheses for ventral hernia repair. Journal of gastrointestinal surgery. 2007; 11(10): 1275-1285 DOI: 10.1007/s11605-007-0242-8
- Zhang X., Deng Z., Wang H., Yang Z., Guo W. Expansion and delivery of human fibroblasts on micronized acellular dermal matrix for skin regeneration. Biomaterials. 2009; 30(14): 2666-2674 DOI: 10.1016/j.biomaterials.2009.01.018
- Cornwell K.G., Landsman A., James K.S. Extracellular matrix biomaterials for soft tissue repair. Clinics in podiatric medicine and surgery. 2009; 26(4): 507-523 DOI: 10.1016/j.cpm.2009.08.001
- Keane T.J., Londodo R., Turner N.J., Badylak S.F. Consequences of ineffective decellularization of biologic scaffolds on the host response. Biomaterials. 2012; 33(6): 1771-1781 DOI: 10.1016/j.biomaterials.2011.10.054
- Cox B., Emili A. Tissue subcellular fractionation for use in mass-spectrometry-based proteomics. Nat protoc. 2006; 1(4): 1872-1878 DOI: 10.1038/nprot.2006.273
- Deyl Z., Miksil I. Advanced separation methods for collagen parent a-chains, their polymers and fragments. J Chromatogr B. 2000; 739: 3-31.
- Ushiki T. Collagen fibers, reticular fibers and elastic fibers. A comprehensive understanding from a morphological viewpoint. Arch Histol Cytol. 2002; 65(2): 109-126 DOI: 10.1679/aohc.65.109
- Shoulders M.D., Raines R.T. Collagen structure and stability. Annu Rev Biochem. 2009; 78: 929-958. DOI: 10.1146/annurev.biochem.77.032207.120833.
- Stevens M.M., George J.H. Exploring and Engineering the cell surface interface. Science. 2005; 310(5751): 11351138 DOI: 10.1126/science.1106587
- O’Brien F.J., Harley B.A., Yannas I.V., Gibson L.J. The effect of pore size on cell adhesion in collagen-GAG scaffolds. Biomaterials. 2005; 26(4): 433-441 DOI: 10.1016/j.biomaterials.2004.02.052


