Сравнительный анализ коагуляционной активности плазмы крови под влиянием температуры in vitro у пойкилотермных и гомойотермных животных
Автор: Березина Д.И., Фомина Л.Л., Кулакова Т.С., Ткачева Е.С., Попова В.В.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Проблемы терморегуляции
Статья в выпуске: 4 т.60, 2025 года.
Бесплатный доступ
Гемостаз - сложный физиологический процесс, обеспечивающий оптимальное агрегатное состояние крови. На тонкую биохимию процессов свертывания и антикоагуляции в значительной степени влияют отклонения от оптимальной температуры, необходимой для взаимодействия между различными ферментами свертывания. Исследование термического влияния на гемостазиологический профиль животных in vitro помогает понять особенности и патологии гемостаза, приводящие к болезням. Изучение гемостазиологической активности крови при разных температурах также важно для медицины, поскольку коагулопатии исследуются на животных моделях с отличной от человеческой температурой тела. В настоящем исследовании впервые in vitro определены изменения в активности различных путей каскада коагуляции (вторичный гемостаз) у холоднокровных (африканский клариевый сом, обыкновенный карп, радужная форель) и теплокровных (курица, крупный рогатый скот) животных при температурных режимах, моделирующих гипо-, нормо- и гипертермию. Нашей целью стало определение отклонений параметров коагулограммы животных с различным термобиологическим статусом (пойкилотермных и гомойотермных) от температуры инкубации плазмы in vitro. Работа была выполнена в 2023 году. В качестве пойкилотермных животных использовали здоровых особей радужной форели (Oncorhynchus mykiss W., n = 15), африканского клариевого сома (Clarias gariepinus B., n = 10) и обыкновенного чешуйчатого карпа (Cyprinus carpio L., n = 15). В качестве теплокровных животных исследовали здоровых коров айрширской породы ( Bos taurus L., n = 15) в возрасте от 4 до 6 лет на разных стадиях лактации и здоровых кур-несушек (Gallus gallus L., n = 19) породы Rhode Island Red, кросс Hisex Brown в возрасте 2 года. Пробы крови получали в пробирки IMPROVACUTER («Guangzhou Improve Medical Instruments Co., Ltd.», Китай), содержащие 3,8 % раствор цитрата натрия в соотношении 1:9. До взятия крови рыб анестезировали, добавляя в воду гвоздичное масло в дозе 0,033 мл/л и выдерживая в ней в течение 15 мин, затем проводили отбор проб пункцией хвостового гемального канала. У птицы кровь получали пункцией подкрыльцовой вены, у крупного рогатого скота - пункцией хвостовой вены. Бедную тромбоцитами плазму получали в результате центрифугирования крови (центрифуга СМ-6М, «ELMI laboratory technology, Ltd.», Латвия) при 3000 об/мин в течение 20 мин. Для оценки состояния плазменно-коагуляционного гемостаза определяли АЧТВ (активированное частичное тромбопластиновое время), ПВ (протромбиновое время), ТВ (тромбиновое время), активность фибриногена автоматически с помощью коагулометра Thrombostat («Behnk Elektronik GmbH & Co.», Германия) при 37 °С и мануально с использованием термостата медицинского водяного TW-2 («ELMI laboratory technology, Ltd», Латвия) при 46 °C, 43 °C, 40 °C, 28 °C, 24 °C и 18 °C. Антикоагулянтные свойства крови оценивали по активности антитромбина III при тех же температурах. В исследовании применяли реагенты производства ООО «Технология-Стандарт» (Россия) и НПО «РЕНАМ» (Россия). Статистический анализ показал, что при нагревании in vitro коагуляционная система теплокровных животных проявляет тенденцию к гиперкоагуляции, которая варьирует в зависимости от механизмов свертывания. В случае крупного рогатого скота наблюдалась достоверная активация процесса свертывания через тканевые факторы и уменьшение эффективности антикоагулянтных механизмов: ПВ (R = -0,79; p ≤ 0,01) и активность антитромбина (R = -0,8; p ≤ 0,01) на 60 % достоверно зависели от температуры реакционной среды. У птицы было обнаружено усиление свертывания по общему пути (R = -0,8; p ≤ 0,01) с одновременным снижением активности фибриногена (R = -0,8; p £ 0,01), доля влияния температуры в которых составляла соответственно 71 и 39 %. Для пойкилотермных животных (рыбы) достоверно подтверждена разносторонняя термически обусловленная реакция гемостаза. Для карпа была характерна гипокоагуляция посредством снижения тканевой активации свертывания, где значение ПВ (R = 0,8; p ≤ 0,01) на 50 % обусловлено температурой инкубации плазмы. У сома зафиксирован достоверный комплекс гиперкоагуляционных процессов, вызванный повышением активности фибриногена (R = -0,7; p ≤ 0,01) и снижением активности антитромбина (R = -0,8; p ≤ 0,01). При этом следует отметить, что плазменные факторы свертывания крови сома оказались наиболее термолабильны (или видоспецифичны) среди всех изученных видов рыб. В случае форели значимые зависимости выявлены не были. Установлено, что изменение термального режима в стандартизированных для гуманной медицины коагулологических исследованиях влияет на активность того или иного пути активизации свертывания крови у животных in vitro, хотя изменения не являются специфическими для пойкило- и гомойотермных. Полученные данные могут использоваться для разработки коагулологических тестов, адаптированных для биологии, зоологии и ветеринарии.
Гемостаз, кровь, температура, крупный рогатый скот, птица, рыбы
Короткий адрес: https://sciup.org/142246215
IDR: 142246215 | УДК: 636:612.115:57.089 | DOI: 10.15389/agrobiology.2025.4.681rus
Comparing the influence of temperature on the coagulation activity of blood plasma in vitro in poikilothermic and homeothermic animals
Hemostasis is a physiological process that is well-controlled and complex in the body that ensures the optimal state of blood aggregation. Deviations from the optimal temperature for the interaction between the various coagulation enzymes greatly affect the fine biochemistry of coagulation and anticoagulation processes. In vitro studies of thermal effects on the coagulation profile of animals contribute to the study of various features and pathologies of hemostasis that lead to animal diseases. The study of animal blood coagulation activity at different temperatures is crucial for human medicine, as coagulopathies are studied in animal models with body temperatures that differ from human ones. For the first time, changes in the activity of various coagulation cascade pathways (secondary hemostasis) were determined in cold-blooded (African sharptooth catfish, common carp, rainbow trout) and warm-blooded (chicken, cattle) animals under temperature conditions modulating hypo-, normal-, and hyperthermia in vitro. The aim of this study was to evaluate the differences in hemostasis parameters between animals with different thermobiological status when plasma incubation temperature changes in vitro are influenced. The study was conducted in Vologda SDFA in 2023. Healthy rainbow trout (Oncorhynchus mykiss W ., n = 15), African sharptooth catfish (Clarias gariepinus B., n = 10), and common carp (Cyprinus carpio L., n = 15) were used as poikilothermic (cold-blooded) animals. Healthy Ayrshire cows (Bos taurus L., n = 15) at different stages of lactation, 4-6 years old, and healthy hens (Gallus gallus L., n = 19) of the Rhode Island Red breed 2 years old were studied as homoiothermic (warm-blooded) animals. Blood samples were collected in IMPROVACUTER tubes (Guangzhou Improve Medical Instruments Co., Ltd, China) containing 3.8 % sodium citrate solution in a 1:9 ratio. Prior to blood collection, the fish were anesthetized by introducing clove oil into the water at a concentration of 0.033 ml/l and maintaining them in this solution for 15 minutes. Subsequently, samples were obtained through puncture of the caudal hemal canal. In birds, blood was obtained by puncture of the axillary vein, in cattle by puncture of the caudal vein. Platelet-poor plasma was obtained by centrifugation of blood in a CM-6M centrifuge (ELMI laboratory technology, Ltd, Latvia) at 3000 rpm for 20 min. The state of plasma-coagulation hemostasis was evaluated using indicators such as APTT (Activated partial thromboplastin time), PT (Prothrombin time), TT (Thrombin time) and analysis of fibrinogen activity automatically using a coagulometer Thrombostat (Behnk Elektronik GmbH & Co., Germany) at 37 °C, and manually using a medical water thermostat TW-2 (ELMI laboratory technology, Ltd, Latvia) temperatures of 46 °C, 43 °C, 40 °C, 28 °C, 24 °C and 18 °C. The anticoagulation properties of blood were assessed by assessing the activity of Antithrombin III in blood plasma at the same temperatures. The research employed reagents produced by Tekhnologiya-Standart LLC (Russia) and NPO RENAM (Russia). Statistical analysis has shown that when heated in vitro, the coagulation system of warm-blooded animals exhibits a tendency towards hypercoagulation, which can vary depending on the coagulation mechanisms involved. In the case of cattle, there is a significant activation of the coagulation process through tissue factors and a decrease in the effectiveness of anticoagulant mechanisms, namely PT (R = -0.79; p ≤ 0.01) and antithrombin activity (R = -0.8; p ≤ 0,01) are 60% reliable dependent on the temperature of the reaction medium. Birds demonstrate increased coagulation along the common pathway (R = -0.8; p ≤ 0.01) with a simultaneous decrease in fibrinogen activity (R = -0.8; p ≤ 0.01), the proportion of the influence of temperature in which are approx. 71 % and 39 %,, respectively. Fish and other poikilothermic animals reliably confirm a diverse thermally-mediated hemostasis response. Carp was characterized by hypocoagulation by reducing tissue activation of coagulation, where the PT value (R = 0.8; p ≤ 0.01) was 50 % determined by the plasma incubation temperature. Catfish showed a significant array of hypercoagulation processes, resulting from a rise in fibrinogen activity (R = -0.7; p ≤ 0.01) and a decrease in antithrombin activity (R = -0.8; p ≤ 0.01). Among all fish species studied, catfish has the plasma blood coagulation factors that are the most thermolabile or species-specific. There were no significant relationships established for trout. The thermal regime in standard humane medicine coagulological studies has been shown to affect the activation of blood coagulation in animals in vitro, but the changes are not specific to poikilotermic and homoerothermic. The data obtained can be used to develop coagulological tests adapted for biology, zoology and veterinary science.
Текст научной статьи Сравнительный анализ коагуляционной активности плазмы крови под влиянием температуры in vitro у пойкилотермных и гомойотермных животных
Проблема устойчивости и приспособления организма к различным воздействиям окружающей среды остается одной из наиболее значимых в биологии, физиологии и ветеринарии. Среди экологических факторов резкое изменение температуры представляет собой одно из основных препятствий для развития животноводства в различных регионах мира (1). Приоритетным направлением физиологии животных в условиях колебаний температуры служит исследование гемодинамических изменений, возникающих под воздействием излишнего тепла или холода на организм, поскольку система кровообращения играет ключевую роль в теплообмене и, соответственно, в поддержании температурного гомеостаза. Ввиду постоянной температуры тела у млекопитающих, относительно сниженной у рыб и повышенной у птиц, характер изменений гемодинамики в общем и свертывания крови в частности может различаться при температурных воздействиях.
В этой связи изучение закономерностей и механизмов, влияющих на системную и регионарную гемодинамику при экстремальном температурном воздействии, становится одной из важнейших задач современной биологической и ветеринарной науки. Успехи в ее решении могут оказать значительное влияние на разработку методов профилактики и коррекции нарушений гемодинамики в условиях как жаркого, так и холодного климата. Актуальным остается вопрос углубленного исследования механизмов воздействия общего перегревания на различные системы организма, включая систему гемостаза.
Гемостаз — сложный, хорошо контролируемый физиологический процесс, обеспечивающий оптимальное агрегатное состояние крови. Система гемостаза позволяет закрывать поврежденные кровеносные сосуды, поддерживать кровь в жидком состоянии и удалять тромбы после восстановления целостности сосудов (2). Процесс свертывания крови включает в себя агрегацию тромбоцитов, коагуляцию и фибринолиз, также называемые первичным, вторичным и третичным гемостазом. Вторичный гемостаз (коагуляционный) представляет собой каскад протеолитических реакций в плазме крови, главная цель которого — формирование фибринового сгустка (3).
Свертывание крови происходит по одной и той же фундаментальной схеме у всех позвоночных (4), называемой каскадом коагуляции, однако есть и некоторые различия. Гемокоагуляция у рыб (5) и птиц (6, 7) считается результатом функционирования внешней системы свертывания крови, инициируемой, как и у млекопитающих, тканевым тромбопластином, высвобождаемым из поврежденных тканей или слизи. Свертывание крови у млекопитающих зависит главным образом от внутреннего механизма образования тромбопластина из самой крови. Также у птиц внутренний путь существенно изменен, что связано с отсутствием факторов XII и XI (6, 7). У млекопитающих развилось несколько дополнительных регуляторных механизмов каскада, а именно появился крупный белок, называемый аполипопротеином (паралог плазминогена). Каким-то образом этот белок модулирует разрушение тромбов, вмешиваясь в действие плазмина (8).
Нарушение гемостаза, в том числе вторичного, становится патогенетической основой многих болезней и летальных исходов у крупного рогатого скота (9-11), рыб (12), кур (13-15), а также у других животных, в 682
связи с чем актуальна разработка диагностических, профилактических и терапевтических методов нормализации гемостаза. Кроме этого, некоторые рыбы (16), мелкий рогатый скот (17), свиньи (18) и другие животные (19) служат модельными организмами для исследований гемокоагуляции в гуманной медицине, хотя есть мнение, что из-за видозависимых различий в системе гемостаза результаты, полученные на таких моделях, не могут быть напрямую применимы к заболеваниям человека (20).
Температура тела — один из важнейших параметров внутренней среды организма, а также фактор регуляции функционирования живых систем (21). Холоднокровные, также известные как пойкилотермные животные, не могут регулировать температуру своего тела изнутри, поэтому она варьирует в зависимости от окружающей среды. Механизм поддержания гомеостаза у рыб не так совершенен из-за их эволюционного положения, как у теплокровных животных. Поэтому пределы изменения констант внутренней среды организма у рыб шире, чем у теплокровных (22). Напротив, теплокровные, или гомойотермные, животные, включая человека, поддерживают постоянную температуру тела с помощью эндогенных механизмов.
Отклонения от оптимальной температуры в значительной степени влияют на тонкую биохимию процессов свертывания и антикоагуляции, а именно нарушаются взаимодействия между различными ферментами свертывания, клеточными рецепторами и внутриклеточными механизмами (23). Биохимически катализируемые реакции в организме любого животного имеют тенденцию протекать медленнее при низких температурах и быстрее при более высоких температурах, вплоть до того момента, когда белки начинают денатурировать, после чего скорость реакции быстро снижается (24). Некоторые авторы предполагают, что ферменты, принимающие участие в свертывании крови пойкилотермных животных, например рыб, способны работать в более широком диапазоне температур, чем у теплокровных видов, поскольку температура их тела тесно связана с изменчивой температурой воды (25). M. Tavares-Dias с соавт. (26) подчеркивают, что температура совершенно по-разному влияет на время свертывания крови у рыб, обитающих в условиях умеренного, холодного и тропического климата, хотя и подразумевая разницу в количестве тромбоцитов, осуществляющих первичный, а не вторичный гемостаз. Термический стресс значительно снижает экспрессию каскада генов фактора свертывания VII, изоформы антитромбина III, кофактора гепарина 2 и гамма-цепи фибриногена у холодолюбивых рыб (27), что свидетельствует об увеличении проницаемости сосудов и гипокоагуляции, однако для птиц эти эффекты не были подтверждены (28).
Известно, что гипертермия может привести к протромботическому состоянию и к коагулопатии потребления у человека и других млекопитающих, которая проявляется одновременным возникновением ДВС-синдрома (синдром диссеминированного внутрисосудистого свертывания крови) и повышенной склонностью к кровотечениям (23). Глубокая гипотермия вызывает нарушение функции факторов свертывания крови и ингибиторной функции.
Данные, характеризующие функциональное состояние плазменнокоагуляционного звена гемостаза у продуктивных животных под влиянием температуры in vitro, достаточно фрагментарны. В основном работы по термической реактивности процессов свертывания крови посвящены изучению влияния гипер- и гипотермии на лабораторных животных in vivo или характеризуют коагуляционный гемостаз животных, подвергшихся отдельным заболеваниям, связанным с гипо- и гипертермией.
Исследование термического влияния на гемостазиологический про- филь животных in vitro способствует расширению знаний об особенностях функционирования, а также патологиях гемостаза, приводящих к болезням животных (26, 29). Изучение свертывающей активности крови животных при разных температурах также важно для гуманной медицины, поскольку коагулопатии исследуются на животных моделях (жвачные, свиньи, крысы, рыбы) с отличной от человеческой температурой тела (30-32). Помимо этого, могут быть раскрыты особенности адаптации коагуляционной системы крови к биоклиматическим факторам у животных с различающимся термобиологическим статусом.
В настоящем исследовании впервые in vitro определены изменения в активности различных путей каскада коагуляции (вторичный гемостаз) у африканского клариевого сома, обыкновенного карпа, радужной форели, а также у курицы и крупного рогатого скота при температурных режимах, моделирующих гипо-, нормо- и гипертермию.
Нашей целью стало определение отклонений параметров коагулограммы животных с различным термобиологическим статусом (пойкило-термных и гомойотермных) от температуры инкубации плазмы in vitro.
Ìåòîäèêà. Работа выполнена в 2023 году. Эксперименты с животными проводили в соответствии с Руководством Национального института здравоохранения по уходу и использованию лабораторных животных. Программа исследований с использованием животных была одобрена Комиссией по биоэтике ФГБОУ ВО Вологодской ГМХА (протокол ¹ 1 от 21 октября 2023 года).
В качестве пойкилотермных животных использовали здоровых особей радужной форели ( Oncorhynchus mykiss W., n = 15) массой 800-1000 г (без половой идентификации), выращенных в ООО «Аквакультура» (оз. Мотко-зеро, Белозерский р-н, Вологодская обл.), здоровых особей африканского кла-риевого сома ( Clarias gariepinus B., n = 10) массой 200-1000 г (без половой идентификации), выращенных в «АкваБиоЦентре» Вологодской ГМХА им. Н.В. Верещагина, и особей обыкновенного чешуйчатого карпа ( Cyprinus carpio L., n = 15) массой 800-1000 г (без половой идентификации), выращенных в рыбоводческом хозяйстве ООО Рыботоварная фирма «Диана» (Вологодская обл.).
В качестве теплокровных животных исследовали здоровых коров айрширской породы ( Bos taurus L., n = 15) на привязном содержании, в возрасте от 4 до 6 лет, на разных стадиях лактации, с живой массой 400-480 кг, принадлежащих СПК «Агрофирма Красная Звезда» (Вологодский р-н, Вологодская обл.), и здоровых кур-несушек ( Gallus gallus L., n = 19) породы Rhode Island Red, кросс Hisex Brown в возрасте 2 года, массой 1900 г, принадлежащих СХПК «Племптица-Можайское» (пос. Можайское, Вологодская обл.). Птицу содержали в четырехъярусных клетках («Valli S.r.L.», Италия).
Образцы крови получали в пробирки IMPROVACUTER («Guang-zhou Improve Medical Instruments Co., Ltd.», Китай), содержащие 3,8 % раствор цитрата натрия в соотношении 1:9. До взятия крови рыб анестезировали, добавляя в воду гвоздичное масло в дозе 0,033 мл/л (33) и выдерживая в ней в течение 15 мин, затем проводили отбор проб пункцией хвостового гемального канала. У птицы кровь получали пункцией подкрыльцовой вены, у крупного рогатого скота — пункцией хвостовой вены.
Бедную тромбоцитами плазму получали в результате центрифугирования крови (центрифуга М-6М, «ELMI laboratory technology, Ltd.», Латвия) при 3000 об/мин в течение 20 мин.
Для оценки состояния плазменно-коагуляционного гемостаза определяли следующие показатели: АЧТВ (активированное частичное тромбо-684
пластиновое время) — время свертывания плазмы крови в условиях стандартизированной контактной (каолином) и фосфолипидной (кефалином) активации процесса в присутствии ионов кальция; ПВ (протромбиновое время) — время свертывания плазмы крови при добавлении тромбопластина (фактора III, тромбокиназы кроличьего мозга) в присутствии ионов кальция; ТВ (тромбиновое время) — время свертывания плазмы крови под действием человеческого тромбина стандартной активности; активность фибриногена — время свертывания разбавленной в 10 раз цитратной плазмы крови при добавлении избытка человеческого тромбина.
Момент свертывания во всех анализах обнаруживали механическим способом, основанным на измерении времени с момента внесения реагента, запускающего ферментативный процесс свертывания, до момента коагуляции: при 37 ° С на коагулометре Thrombostat («Behnk Elektronik GmbH & Co», Германия), а также мануально с использованием термостата медицинского водяного TW-2 («ELMI laboratory technology, Ltd.», Латвия) при 46 ° C, 43 ° C, 40 ° C, 28 ° C, 24 ° C и 18 ° C.
Были использованы медицинские наборы Тромбо-тест, Техпластин-тест, АПТВ-тест (ООО «Технология-Стандарт», Россия) и Фибриноген-тест (НПО «РЕНАМ», Россия). Антикоагулянтные свойства крови оценивали по активности антитромбина III с помощью Тех-Антитромбин-теста (ООО «Технология-Стандарт», Россия) при тех же температурах. Эту активность тестировали по скорости инактивации человеческого тромбина в плазме крови, подвергнутой тепловому дефибринированию. Все исследования проводили в соответствии с инструкциями к реагентам. Реагенты, используемые в работе, стандартизированы и применяются в диагностике патологий свертывания крови у человека, поэтому любые отклонения в исследованиях in vitro будут влиять на показатели.
Статистический анализ полученных данных осуществляли при помощи программного обеспечения Statistica 10.0 и Microsoft Excel. Данные представлены в виде среднего и стандартной ошибки среднего ( М± SEM). Нормальность распределения данных оценивали при помощи критериев Шапиро-Уилка и Колмогорова-Смирнова. Для оценки достоверности различий параметров между видами в парных независимых выборках использовали критерий Манна-Уитни, для различий параметров при разных температурах в множественных зависимых выборках — критерий Вилкоксона. Силу парной линейной связи между переменными оценивали при помощи непараметрического коэффициента корреляции Спирмана (R). Качественную интерпретацию силы связи между показателями коагулограммы и температурой инкубации плазмы выполняли на основе шкалы Чеддока. Влияние температурного фактора оценивали с помощью теоретического коэффициента детерминации (R2). Проверку статистической значимости коэффициентов корреляции осуществляли с помощью статистического критерия Фишера (однофакторный дисперсионный анализ, One-way ANOVA) (34).
Результаты. Данные, полученные в процессе коагулологических исследований радужной форели, африканского клариевого сома и карпа обыкновенного, подробно представлены в более ранней авторской публикации (35). Область температурного комфорта, представляющая собой оптимальный температурный диапазон для нормального функционирования организма указанных видов, колеблется от 10 до 30 ° C, что меньше стандартной для использованной методики. Ниже представлены наиболее значимые изменения, выявленные при анализе динамики коагулограмм исследованных рыб.
Нарушения конечного этапа свертывания плазмы крови (по общему пути) определяют при помощи измерения тромбинового времени (ТВ), в то время как протромбиновое время (ПВ) характеризует гемокоагуляцию по внешнему пути (путь тканевой активации). У радужной форели наблюдалось ускорение ТВ в 7,1 раз при повышении температуры инкубации с 18 до 43 °C. Исследование ПВ показало, что процесс свертывания крови прекращался либо значительно удлинялся независимо от того, повышалась или понижалась температура инкубации. Эффективность внутреннего (путь контактной активации) и общего путей свертывания, оцениваемая по АЧТВ, при 18 °C в 2,2 раза (p < 0,05) превышала длительность при 37 °C, в то время как при 43 °C коагуляционная активность не проявлялась. Активность фибриногена — показатель, отражающий способность превращения фибриногена в фибрин под влиянием человеческого тромбина в условиях разной температуры. Повышение температуры инкубации до 37 °C в сравнении с 24 °C у форели приводило к ускорению преобразования фибриногена на 33 % (p < 0,05).
Можно заключить, что коагуляционная активность плазмы у форели повышается под влиянием термического фактора по общему и контактному путям. При этом некоторые факторы внутреннего и внешнего путей проявляют термолабильность или видоспецифичность.
Изменения скорости ТВ и ПВ в ответ на повышение температуры у африканского клариевого сома in vitro отмечено не было. Максимальная продолжительность АЧТВ наблюдалась при 18 ° C и с увеличением температуры до 43 ° C оно сократилось в 4,4 раза (p < 0,05). Подобная зависимость отмечена для активности фибриногена, которая была значительно снижена при низких температурах, тогда как при температурах выше общеупотреби-мой (37 ° C) процесс превращения фибриногена в фибрин ускорился в 10,5 раза (p < 0,05). Активность антитромбина III отражает способность этого белка инактивировать факторы свертывания. Антикоагуляционные свойства крови у сома при 28 ° C были в 80,3 раза активнее (p < 0,05), чем при температуре инкубации 37 ° C.
Таким образом, под влиянием температуры у сома проявляется комплекс гиперкоагуляционных процессов за счет контактной активации свертывания, увеличения активности фибриногена и снижения антикоагуляционной активности. По неактивности тестов, характеризующих общий и внешний пути, следует предположить, что некоторые факторы сома обладают видоспецифичностью или термолабильностью. В крупном обзоре гемостатической системы рыб M. Tavares-Dias с соавт. (26) также упоминается, что внешний путь активации коагуляции у этих животных может содержать термолабильные факторы свертывания крови.
Наиболее продолжительное время формирования фибринового сгустка под влиянием экзогенного тромбина у карпа обыкновенного отмечалось при оптимальной для теста температуре 37 ° C, в то время как при охлаждении до 18 ° C и нагревании до 43 ° C это время уменьшалось соответственно в 49 и 6 раз (p < 0,05). ПВ увеличивалось в 29 раз (p < 0,05) при переходе от низких к высоким температурам. Напротив, АЧТВ укорачивалось втрое с повышением температуры инкубации, достигая минимума при 40 ° C (p < 0,05). Скорость преобразования фибриногена в фибрин линейно снижалась на 32,4 и повышалась на 43,3 % (p < 0,05) относительно показателя при 37 ° C вследствие изменения температуры соответственно до 18 ° C и 43 ° C. Максимальную активность антитромбина III у карпа наблюдали в интервале температур от 18 до 24 ° C, тогда как самая низкая активность фиксировалась в диапазоне от 37 до 43 ° C.
Исходя из полученных данных, можно утверждать, что для вторичного гемостаза карпа характерен комплекс гипо- и гиперкоагуляционных процессов, зависящих от температуры. Активность факторов общего пути сначала снижалась, а затем усиливалась, тогда как по пути тканевой активации шел противоположный процесс. Свертывание по внутреннему пути, как у других исследованных рыб, ускорялось, антикоагуляционная система была весьма нестабильна.
Оптимальная температура физиологических реакций у коров айр-ширской породы составляла ~ 40 ° C, что было больше стандартной для использованной методики.
Время образования фибринового сгустка под влиянием человеческого тромбина (ТВ) с постепенным нагревом плазмы до 43 ° C сократилось относительно изначального в 2,8 раза (р < 0,05), хотя изменения носили ступенчатый, а не линейный характер (табл. 1). Сходная тенденция наблюдалась при изучении ПВ: оно сокращалось в 3,6 раза (р < 0,05) при тепловом воздействии. Эффективность внутреннего пути свертывания крови (АЧТВ) в условиях пониженной температуры (18 ° C) была самой низкой, тогда как при повышении температуры инкубации до 28 ° C стремительно увеличилась в 13 раз (р < 0,05). При дальнейшем нагреве до 43 ° C эффективность свертывания снижалась постепенно, тем не менее, все еще оставалась в 4 раза выше (р < 0,05), чем при 18 ° C (р < 0,05). Активность фибриногена изменялась аналогичным образом, составив разницу между значением при 18 ° C и значениями при 28 ° C и 43 ° C соответственно в 14,6 и 5,2 раза (р < 0,05). Антитромботическая активность плазмы крови крупного рогатого скота демонстрировала обратно пропорциональное снижение в зависимости от увеличения температуры инкубации, было отмечено ее уменьшение от 18 ° C к 43 ° C в 13,3 раза (см. табл. 1).
Следует подчеркнуть, что скорость свертывания по общему и контактному путям прямолинейно увеличивалась с повышением температуры инкубации плазмы, при этом падала активность антитромбина. Факторы пути контактной активации и активность фибриногена были неустойчивы как к низкой, так и к высокой температуре.
Как и у крупного рогатого скота, температура тела птицы превышала стандартную для медицинской методики. Для нормального протекания физиологических процессов она должна составлять 41-42 ° C.
Активность различных механизмов плазменного гемостаза у исследованных птиц варьировала в зависимости от температуры (табл. 2). ТВ сокращалось прямо пропорционально увеличению интенсивности нагрева плазмы, наблюдалась разница в 4,6 раза относительно значения при 18 ° C. Изменения продолжительности ПВ у кур были достаточно разнонаправ-лены при нагреве реакционной среды, при этом самая короткая продолжительность отмечалась при термальном минимуме (18 ° C) и максимуме (46 ° C), а самая продолжительная — при 28 и 43 ° C. Анализируя динамику активности внутреннего пути гемостаза, можно выделить высокую продолжительность АЧТВ при 28 ° C по сравнению с другими температурными режимами, где колебания были незначительными. Самым коротким оказалось ТВ при 37 ° C. При росте температуры с 18 ° C до 43 ° C активность фибриногена у птиц снижалась почти линейно в 15,6 раза (р < 0,05), в то время как антитромбин, наоборот, демонстрировал увеличение антикоагуляционных способностей в 5,7 раза (р < 0,05).
-
1 . Коагулограмма коров ( Bos taurus L.) айрширской породы при различных температурах инкубации плазмы ( n = 15, ̱ SEM, Вологодская ГМХА им. Н.В. Верещагина, 2023 год)
|
Показатель |
Температура, °С |
|||||
|
18 |
24 |
28 |
37 |
40 |
43 |
|
|
ТВ, с |
50,09±6,22cdg |
61,47±5,43cdg |
33,61±3,61abg |
26,54±1,74abfg |
45,17±4,63dg |
18,01±2,11abcdf |
|
ПВ, с |
89,51±12,79bcdfg |
48,61±3,40afg |
52,69±2,31afg |
55,13±13,68ag |
34,57±1,68abcg |
24,88±2,58abcdf |
|
АЧТВ, с |
353,09±14,89bcdfg |
98,80±6,84acdf |
27,00±4,33abdfg |
62,83±2,34abc |
64,31±6,85abc |
88,91±29,19ac |
|
Активность фибриногена, с |
130,15±27,00bcdfg |
39,79±3,80acdfg |
8,89±0,84abdfg |
12,46±1,20abcfg |
23,90±5,67abcd |
24,77±5,45abcd |
|
Активность антитромбина III, с |
65,99±6,79cdf |
39,67±6,12cdf |
14,41±1,97abf |
10,53±0,44ab |
10,11±0,22abc |
4,95±1,35 |
Примечание. ТВ — тромбиновое время, ПВ — протромбиновое время, АЧТВ — активированное частичное тромбопластиновое время. a, b, c, d, f, g Различия с аналогичным параметром достоверны (p < 0,05) соответственно при 18 ° С, 24 ° С, 28 ° С, 37 ° С, 40 ° С, 43 °С.
-
2 Коагулограмма кур-несушек ( Gallus gallus L.) породы Rhode Island Red, кросс Hisex Brown при различных температурах инкубации плазмы ( n = 19, ̱ SEM, Вологодская ГМХА им. Н.В. Верещагина, 2023 год)
Показатель
Температура, °С
18
28
37
43
46
|
ТВ, с |
149,97±11,32bcdf |
91,83±5,72acdf |
46,39±1,74abf |
45,52±1,64abf |
32,43±3,65abcd |
|
ПВ, с |
29,33±6,37bcd |
209,78±34,24acf |
83,13±15,36abdf |
154,64±41,71acf |
43,71±13,99bcd |
|
АЧТВ, с |
84,72±15,23b |
231,31±31,41acdf |
64,56±7,67b |
78,82±12,41b |
86,86±17,56b |
|
Активность фибриногена, с |
25,35±4,99bcdf |
102,79±9,86af |
93,88±9,75af |
109,15±11,27af |
395,60±32,99abcd |
|
Активность антитромбина III, с |
11,81±2,62bcdf |
47,18±9,19a |
33,13±3,35a |
41,91±12,54a |
67,98±31,18a |
Примечание. ТВ — тромбиновое время, ПВ — протромбиновое время, АЧТВ — активированное частичное тромбопластиновое время. a, b, c, d, f , g Различия с аналогичным параметром достоверны (p < 0,05) соответственно при 18 ° С, 28 ° С, 37 ° С, 43 ° С, 46 ° С.
Обобщая выявленные изменения, следует выделить нестабильность активности коагуляции по внешнему и внутреннему путям при меняющемся температурном режиме. Схожим с крупным рогатым скотом образом происходила гиперкоагуляция по общему пути, а также отмечалась активация антикоагулянтной системы. Эти данные подтверждают, что тенденции к усилению свертывания при гипертермии и его ослаблению при гипотермии, указанные в работах на человеке и других млекопитающих (18, 19, 23, 30), справедливы и для крупного рогатого скота.
Корреляционно-регрессионный и однофакторный дисперсионный анализ (One-way ANOVA) показали, что степень влияния температурного фактора на изучаемые параметры у животных с различным термобиологическим статусом неодинакова.
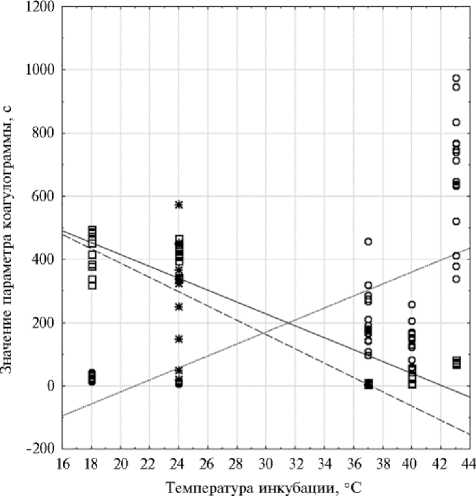
Согласно шкале Чеддока, были обнаружены значимые корреляционные связи у двух видов рыб: у карпа наблюдалась прямая корреляция между температурой и ПВ (R = 0,8; p ≤ 0,01), в то время как у сома отмечалась обратная связь между температурой и активностью фибриногена (R = - 0,7; p ≤ 0,01) и антитромбина III (R = - 0,8; p ≤ 0,01) (рис. 1).
В случае форели значимые корреляционные зависимости установлены не были. Опираясь на выявленные корреляции и теоретический коэффициент детерминации (R2), было установлено, что ПВ у карпа на 50 % обусловлено температурой инкубации плазмы. Что касается активности фибриногена и антитромбина III у сома, то влияние температурного фактора составило соответственно 77 % и 52 % (см. рис. 1).
Ч, 1 "х 2 "«Ц 3
Рис. 1. Регрессионная модель корреляции между отдельными параметрами коагулограммы и температурой инкубации плазмы у пойкилотермных животных: 1 — поле корреляции между протромбиновым временем и температурой инкубации плазмы у обыкновенного чешуйчатого карпа Cyprinus carpio L. ( n = 15; p ≤ 0,01), 2 — поле корреляции между активностью фибриногена и температурой инкубации плазмы у африканского клариевого сома Clarias gariepinus B. ( n = 10; p ≤ 0,01), 3 — поле корреляции между активностью антитромбина III и температурой инкубации плазмы у африканского клариевого сома ( n = 10; p ≤ 0,01) (Вологодская ГМХА им. Н.В. Верещагина, 2023 год).
Коэффициент детерминации показал, что у крупного рогатого скота
ПВ и активность антитромбина на 60 % достоверно зависели от температуры реакционной среды, при этом эмпирическое корреляционное отношение (R) составило соответственно - 0,79 (p ≤ 0,01) и - 0,80 (p ≤ 0,01), что свидетельствует об отрицательной обратной связи высокой силы (рис. 2).
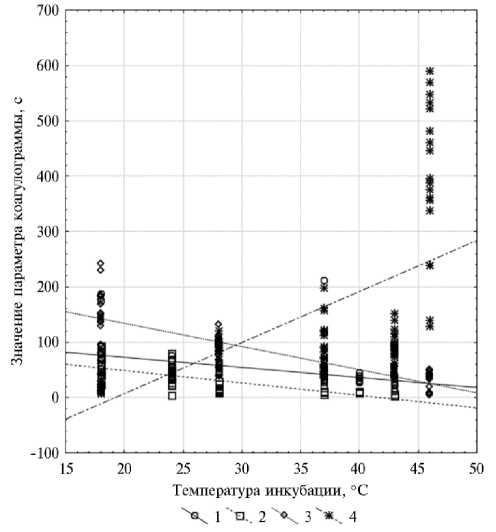
Рис. 2. Регрессионная модель корреляции между отдельными параметрами коагулограммы и температурой инкубации плазмы у гомойотермных животных: 1 — поле корреляции между протромбиновым временем и температурой инкубации плазмы у коров ( Bos taurus L.) айрширской породы ( n = 15; p ≤ 0,01), 2 — поле корреляции между активностью антитромбина III и температурой инкубации плазмы у коров айрширской породы ( n = 15; p ≤ 0,01), 3 — поле корреляции между тромбиновым временем и температурой инкубации плазмы у кур-несушек ( Gallus gallus L.) породы Rhode Island Red, кросс Hisex Brown ( n = 19; p ≤ 0,01), 4 — поле корреляции между активностью антитромбина III и температурой инкубации плазмы у кур-несушек породы Rhode Island Red, кросс Hisex Brown ( n = 19; p ≤ 0,01) (Вологодская ГМХА им. Н.В. Верещагина, 2023 год).
При исследовании кур было надежно установлено, что температурные условия оказывают значительное влияние на ТВ (R = - 0,8; p ≤ 0,01) и активность фибриногена (R = 0,8; p ≤ 0,01), с коэффициентами детерминации, равными соответственно 71 и 39 %. Обнаруженные связи могут быть классифицированы как обратная и прямая корреляции высокой степени (см. рис. 2).
Тепловой стресс — один из самых дорогостоящих в сельском хозяйстве внешних факторов, негативно влияющих на здоровье животных, их производительность и качество продукции. Еще 20 лет назад ежегодные экономические потери в мясной и птицеводческой промышленности США из-за теплового стресса оценивались соответственно в 369 млн долларов и 128 млн долларов, а в свиноводческой промышленности в 900 млн долларов (36). Один из элементов патогенеза этого состояния — нарушение свертывания крови. Существующие исследования теплового стресса фиксируют увеличение активности некоторых элементов каскада свертывания (37) и инициацию коагулопатических изменений, способствующих развитию ДВС-синдрома при гипертермии у коров и свиней (38, 39). Повышение свертывающей активности крови рыб, аналогичное млекопитающим, было также 690
зафиксировано в результате воздействия на них теплового стресса (40, 41). Эти данные подчеркивают важность коагулологических исследований в ветеринарии с целью создания специализированных диагностических методов для животных, что необходимо для профилактики и терапии жизнеугрожающих состояний. Для достижения этих целей немаловажно изучение базовых принципов работы каскада коагуляции в результате воздействия на него термического фактора у животных с различным термобиологическим статусом.
В некоторых медицинских исследованиях есть данные о реактивности системы вторичного гемостаза при воздействии высоких температур у животных in vivo (19, 30, 42) и in vitro (43), в основном это млекопитающие. Известно, что гипертермия оказывает активирующее влияние на коагуляционное звено системы гемостаза на фоне угнетения физиологических антикоагулянтов и фибринолиза, характеризующих так называемую коагулопатию потребления. Схожую гемостазиологическую картину в текущем исследовании мы наблюдали у крупного рогатого скота. При этом результаты, полученные С.В. Москаленко с соавт. (43), подтверждают также отмеченную нами термически обусловленную денатурацию белков каскада свертывания, в результате чего фиксируются гипокоагуляционные сдвиги.
Есть фрагментарные исследования, в которых упоминается температурная зависимость гемокоагуляции у рыб in vitro. В частности, сообщалось, что скорость свертывания цельной крови или плазмы увеличивается при нагреве, после чего процесс свертывания инактивируется (44-46). Также предполагается наличие двух или более термолабильных факторов свертывания крови у рыб, что нашло подтверждение в рамках настоящего исследования.
Механизм активации коагуляции in vivo, вызванной гипертермией, частично выяснен: экспериментальные исследования указывают на решающую роль эндогенного тканевого фактора в инициации свертывания крови (23), тогда как увеличение свертывающей активности крови в текущем исследовании также указывало на увеличение активности ферментативных процессов в плазме.
О воздействии низких температур на гемостатические показатели сведений в литературе гораздо меньше, и они более противоречивы. При изучении влияния гипотермии на крыс (47), собак (48, 49), свиней (18) регистрировали выраженную тромбинемию и угнетение фибринолитической активности плазмы. Также гипотермия действует как естественная стратегия выживания у некоторых млекопитающих, впадающих в спячку: под влиянием низкой температуры у них происходит ингибирование фактора Х каскада коагуляции (50). Мы зафиксировали уменьшение коагуляционной способности плазмы крови у некоторых исследованных животных в условиях пониженной температуры.
В настоящее время диагностику нарушений системы гемостаза у животных проводят, используя методики, заимствованные из гуманной медицины (51), в частности клоттинговые методы с использованием коагуло-метра, который поддерживает температуру инкубации исследуемой плазмы 37 °С. K.E. Russell с соавт. (14), изучавшие птиц, предполагают, что температура инкубации плазмы не влияет на результаты, однако, учитывая подтвержденную зависимость коагуляционной активности плазмы от температуры в настоящем исследовании, стандартные клоттинговые тесты при использовании их в биологической и ветеринарной науке, вероятно, требуют модернизации с учетом оптимальной для видов температуры. К аналогичному выводу пришли авторы, изучавшие попугаев (52, 53). Наши результаты подтверждаются изменением активности тех или иных путей вторичного гемостаза при модуляции гипертермии in vitro у мышей (43) и при гипотермии in vitro у человека (54).
Авторы настоящего исследования признают, что работа имеет несколько ограничений. Во-первых, некоторые активаторы свертывания, такие как тромбопластин (тканевый фактор), видоспецифичны для рыб (26) и птиц (7, 14, 14, 52-55), с чем могут быть связаны отклонения в клоттин-говых тестах (например, длительность ПВ). В результате такие тесты могут неточно отражать истинный статус коагуляции. Также в связи с измененным путем контактной активации использование АЧТВ не может считаться корректным для применения у птиц. Аналогичные результаты получены в исследованиях, фокусирующихся на клинико-диагностической характеристике коагулограмм у птиц (13, 56). Во-вторых, следует помнить, что клинически важный гемостаз происходит in vivo и что такие параметры, как время кровотечения и время свертывания цельной крови, у некоторых видов животных могут быть более надежными показателями коагулопатии, чем результаты коагулологического анализа, поскольку в нем отсутствует клеточный вклад в регуляцию гемостаза, обеспечиваемый стенками сосудов и эндотелиальными клетками. Тем не менее, наряду тромбоэластографией, определением содержания факторов свертывания и генетическими тестами, коагулограмма как комплексный гематологический анализ позволяет наиболее точно охарактеризовать функционирование отдельных звеньев и путей системы плазменной коагуляции. В настоящее время эта методика достаточно доступна с учетом технологических и экономических возможностей лабораторий и широко используется в ветеринарной медицине (57, 58, 59) и биологических исследованиях (15, 27, 55).
Полученные экспериментальные данные, описывающие реактивность системы вторичного гемостаза в ответ на термический фактор, показывают гипотетическую некорректность применения медицинских тестов с постоянной температурой инкубации плазмы 37 ° С в исследованиях физиологии животных с высокой вариативностью температуры внутренней среды. Активность свертывания у исследованных животных в условиях избыточного тепла или холода претерпевала изменения, вызванные вариабельностью в активности разных механизмов плазменного гемостаза in vitro, несмотря на схожесть базового строения каскада коагуляции у позвоночных и вопреки тому, что они обладают различным резервом приспособленности к температурам окружающей среды (пойкило- и гомойотермные). Дисперсионный анализ показал степень температурного влияния на показатели их коагулограмм.
Мы предполагаем, что одними из возможных причин динамики гемостатической картины при умеренно высоких температурах становится возрастание ферментативного потенциала, например тромбина, что ранее экспериментально подтверждалось (23). При экстремальных температурах активация свертывания крови дополнительно также может усиливаться или снижаться за счет протеолитического расщепления белковых факторов, например того же тромбина, фибриногена или антикоагулянтов. При более низких температурах физиологические взаимодействия между белками плазмы, вероятно, замедляются (23). При этом животные с различным термобиологическим статусом, исследованные нами, могли иметь неодинаковую эволюционную толерантность гемостатических белков к термическому воздействию, и указанные процессы происходили у них с различной интенсивностью ввиду того, что действие каждого из факторов свертывания ограничено определенным температурным диапазоном. Для уточнения указанной дисфункции вторичного гемостаза требуются дальнейшие исследования.
Полученные нами данные могут стать основой для создания специализированных тестов в области гемостазиологии, нацеленных на потребности биологии, зоотехнии и ветеринарной науки. Обнаруженные закономерности будут способствовать углублению знаний об устойчивости физиологических систем животных к высоким и низким температурам, а также стимулировать разработку биоиндикаторов термического стресса.
Итак, на основе сравнительного анализа экспериментальных и статистических данных было установлено, что изменение термального режима в стандартизированных для гуманной медицины коагулологических исследованиях влияет на активность того или иного пути активизации свертывания крови у животных in vitro, хотя изменения не являются специфическими для пойкило- и гомойотермных. Вследствие этого можно сделать вывод, что стандартные клоттинговые тесты при их использовании в биологической и ветеринарной науке, вероятно, требуют модернизации с учетом оптимальных для видов температуры и реагентов. Корреляционный анализ показал, что при нагревании in vitro система вторичного гемостаза теплокровных животных проявляет тенденцию к гиперкоагуляции, варьирующую в зависимости от механизмов свертывания. У крупного рогатого скота наблюдалась активация процесса свертывания через тканевые факторы и уменьшение эффективности антикоагулянтных механизмов. У птиц, в свою очередь, было продемонстрировано усиление свертывания по общему пути с одновременным снижением активности фибриногена, что, вероятно, связано с усилением превращения фибриногена в нерастворимый фибрин. Для пойкилотермных животных (рыбы) достоверно подтверждена термически обусловленная реакция гемостаза, имеющая свои особенности. Для карпа была характерна гипокоагуляция посредством снижения тканевой активации свертывания. У сома зафиксирован достоверный комплекс гиперкоагуляционных процессов, вызванный повышением активности фибриногена и снижением активности антитромбина. При этом следует отметить, что плазменные факторы свертывания крови сома наиболее термолабильны (или видоспецифичны) среди всех изученных видов рыб. В случае форели значимые зависимости установлены не были. Полученные данные могут использоваться для разработки коагулологических тестов, адаптированных для биологии, зоологии и ветеринарии. Выявленные закономерности также послужат основой для более глубокого понимания термоустойчивости организма животных и разработки биомаркеров термического стресса.


