Стентирование пищевода в курации дисфагии у онкологических больных
Автор: Стручкова Е.Ю., Мударисов Р.Р., Мерцалов А.С., Шитиков Е.А., Могильницкий И.Е., Воронцов А.В., Бархатова И.В., Фомина М.Н., Стручков В.Ю., Фомин В.С.
Журнал: Московский хирургический журнал @mossj
Статья в выпуске: 3 (55), 2017 года.
Бесплатный доступ
В статье анализирован опыт паллиативного лечения 160 пациентов с дисфагией ввиду непроходимости пищевода. У 139 пациентов стентирова- ние выполнялось в плановом порядке, а 21 больной оперирован по экстренным показаниям вследствие прогрессирующей дисфагии 3-4степени. По результатам лечения анализированы осложнения, а также оптимизирован алгоритм селекции, подготовки пациентов к операции, а также ведению послеоперационного периода у коморбидных пациентов. На основании проведенного нами анализа следует признать эндоскопическое стентиро- вание ведущим методом паллиативного лечения больных раком пищевода, осложненного дисфагией. В настоящее время по накоплению опыта имеется тенденция к увеличению медианы выживаемости больных неоперабельным раком пищевода, которым было выполнено эндоскопическое стентирование опухолевой стриктуры.
Непроходимость пищевода, оbstruction of the esophagus, паллиативное лечение, эндоскопическое стентирование
Короткий адрес: https://sciup.org/142212748
IDR: 142212748 | УДК: 616.33-073.75
Текст научной статьи Стентирование пищевода в курации дисфагии у онкологических больных
Актуальность
Основной причиной развития дисфагии проксимальных отделов желудочно-кишечного тракта следует считать первичный местно-распространенный рак пищевода, который в структуре онкологических заболеваний занимает 16-е место. Ежегодно в России регистрируется до 7700 – 7800 больных раком пищевода, при этом ранние стадии диагностируются не более чем у 5% больных [1]. Возрастная кривая диагностики подобных состояний соответствует 50 лет и более, а доля коморбидных пациентов с запущенной стадией рака пищевода составляет 60-70% [1,2]. Дисфагия, как основной клинический симптом распространенного рака пищевода и кардиального отдела желудка, возникает при сужении просвета на 50-75% и более. При этом средняя продолжительность жизни пациентов с тяжелой опухолевой дисфагией колеблется в пределах 90 - 173 суток [2,3], что указывает на особую актуальность проблемы в XXI веке.
Даже после радикальной операции у 20% больных диагностируются местные рецидивы опухоли в зоне анастомоза с полной или частичной обтурацией просвета [4]. К сожалению, у подавляющего большинства пациентов, об- ращающихся за помощью, паллиативные методы являются ведущими в лечении стенозирующего рака пищевода (в случаях нерезектабельности опухоли, а также при местном рецидиве). Основной задачей паллиативной помощи следует считать уменьшение дисфагии и повышение качества жизни. Для этого используются различные методы (в том числе эндоскопические), выбор которых определяется индивидуально, с учетом стадии опухолевого процесса, клинической симптоматики, возраста, общего состояния пациента и коморбидного фона.
К традиционным методам лечения инкурабельных онкологических больных с дисфагией относятся: хирургическая операция с наложением открытой или лапароскопической гастростомы, а реже чрезкожной эндоскопической гастростомы (при сохранении просвета для проведения эндоскопа) с последующей химиолучевой терапией. Гастростомия, устраняя симптомы дисфагии, лишает пациентов возможности естественного приема пищи, ухудшает качество жизни, нарушает усваивание продуктов питания и является дополнительной психологической травмой. В связи с этим для устранения дисфагии и восстановления питания через рот
продолжают совершенствоваться и разрабатываться новые методы лечения.
История внедрения и применение эндопротезирования верхних отделов желудочно-кишечного тракта насчитывает более 120 лет активных поисков оптимальных «вставок», технических нюансов, а также методик имплантации и «фиксации» стентов в просвете органов.
Бесспорно, революционным шагом стало открытие дантистом Stent C. термопластичного материала для получения отпечатков зубов, чьи свойства позволили использовать его для изготовления дигестивных эндопротезов («стентов») [5].
Первое описание эндоскопического введения расправляющихся металлических спиральных стентов принадлежит Frimberger Е. (1983г.) и изначально стентирование применялось для облегчения дисфагии лишь у больных со стенозирующим раком пищевода. В 1993 г. Cwikiel W. сообщил об использовании покрытого силиконом эндопротеза при доброкачественной стриктуре пищевода в эксперименте, а в последующем и в клинической практике у 5 больных [6]. В дальнейшем с развитием и совершенствованием технологий расширялись показания к стентированию верхних отделов желудочно-кишечного тракта [7].
На сегодняшний день к применению эндоскопического стентирования имеются нижеприведенные группы показаний [8, 9]:
-
1. злокачественные нерезектабельные стенозирующие опухоли пищевода, кардии, выходного отдела желудка, двенадцатиперстной кишки с дисфагией II-IV степени (подготовитель-
- ный этап к химиолучевому или хирургическому лечению, а у инкурабельных больных – как самостоятельный метод паллиативного лечения, альтернативный гастростомии);
-
2. прорастание (компрессия) злокачественными опухолями смежных органов;
-
3. рецидив опухоли в области анастомоза после оперативного лечения;
-
4. эзофагореспираторные свищи;
-
5. несостоятельность анастомозов после операции;
-
6. доброкачественные стриктуры пищевода и анастомозов при рефрактерности к другим неоперативным методам лечения;
-
7. перфорации пищевода (в том числе ятрогенные);
-
8. гемостаз при кровотечении из варикозно расширенных вен пищевода [10,11].
Среди противопоказаний следует выделять абсолютные и относительные. Абсолютным противопоказанием к установке эндопротезов является крайне тяжелое состояние пациента, обусловленное прогрессированием основного заболевания. Среди относительных противопоказаний следует выделить нециркулярные стриктуры, препятствующие «за-якориванию» стента; стриктуры с выраженным изгибом, а также стриктуры с локализацией на расстоянии менее 2 см от верхнего пищеводного сфинктера.
Техника установки стентов
Нарушения проходимости и целостности стенки верхних отделов желудочно-кишечного тракта являются ур-гентными состояниями и диктуют необходимость решения
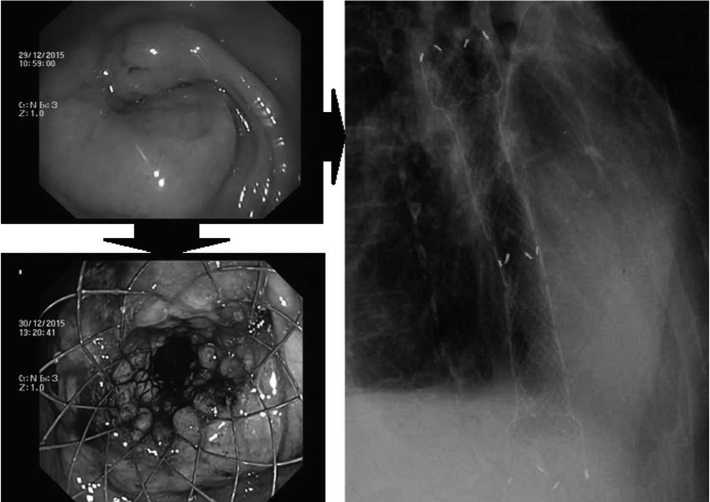
Рис. 1. Порядок выполнения стентирования
«проблемы» в кратчайшие сроки с минимальной инвазив-ностью для больного, что в полной мере реализуется применением саморасширяющихся стентов.
На сегодняшний день можно выделить несколько методов установки саморасправляющихся стентов в пищеводе и кардиальном отделе желудка:
-
1. Под прямым рентгеноскопическим контролем без использования эндоскопической техники с или без предварительной баллонной дилатации через доставочное устройство стента.
-
2. Эндоскопический метод установки стентов под прямым рентгенотелевизионным контролем (рис. 1). На сегодняшний день, наиболее часто используемый способ стентирования верхних отделов желудочно-кишечного тракта (имеет абсолютные показания при извитом ходе стенозированного отдела пищевода, желудка или зоны послеоперационного анастомоза).
-
3. Эндоскопическая установка стента без прямого рентгеноскопического контроля. В связи с исключением лучевой нагрузки на пациента медперсонал имеет все большие перспективы для широкого применения современной видеоэн-доскопической техники малого диаметра. Среди основных условий безопасного применения данной техники стентирования - обязательная предварительная реканализация (бужирование или баллонная дилатация), позволяющая выполнить эндоскопический осмотр дистальной границы стеноза пищевода или желудка.
-
4. Интраоперационная установка стента под мануальным контролем. Применяется крайне редко при паллиативных и циторедуктивных операциях.
Материалы и методы
В данной работе приведен анализ 160 паллиативных имплантаций стентов при опухолевой стриктуре пищевода, проведенных как по экстренным показаниям, так и при плановом обращении больных. Анализу подвергнут 5-лет-ный опыт стентирования опухолевых стриктур пищевода и кардии желудка в эндоскопических отделениях Рязанского областного онкодиспансера (РООД) и ГКБ№52 ДЗМ.
Пациенты с неоперабельными стенозирующими формами рака пищевода и кардиального отдела желудка в большинстве случаев страдают различными сопутствующими заболеваниями, тяжесть которых нарастает на фоне нарушения питания и обезвоживания организма. Ежегодно около 50-63 больных со стенозирующими опухолями пищевода и кардии поступают в ГКБ №52 по наряду скорой помощи с жалобами на невозможность проглотить даже воду или с клиникой ЖКК. В условиях скоропомощного стационара подготовку больных к эндоскопическому лечению необходимо проводить быстро и коррекция нарушений функций сердечно-сосудистой системы, водно-электролитного баланса, белкового и энергетического дефицита осуществля- ется как до стентирования (не более 24 часов), так и после него.
До и во время проведения эндоскопического вмешательства на пищеводе, в зависимости от его сложности и длительности, кроме местной анестезии, мы считаем целесообразным усиливать анестезирующий эффект комбинацией малых доз гипнотиков и анальгетиков (диприван и др.) в субнаркотических дозах. В послеоперационном периоде в течение до 72 часов для купирования болевого синдрома показано использование анальгетических препаратов и обязательно щадящей жидкой диеты.
В настоящее время мы отдаем предпочтение саморас-правляющимся эндопротезам. Они представляют собой сетчатую конструкцию, покрытую полимерной пленкой, способную, благодаря упругости, расширяться после установки в просвете пищевода. На подготовительном этапе стентирования в 13% случаев для расширения просвета пищевода мы использовали либо балонную дилятацию, либо электрореканализацию. Выбор методики определялся индивидуально.
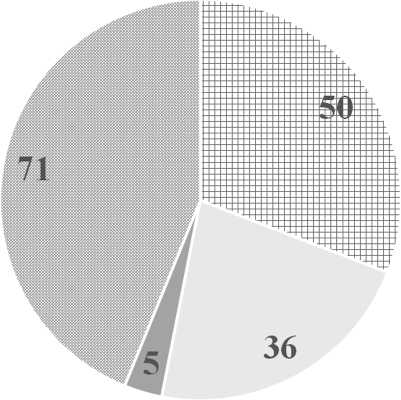
Все 160 стентирований выполнялись как в плановом порядке (139) так и в 21 наблюдении по экстренным показаниям. Патология, при которой проводилось эндопротезирование пищевода, представлена в диаграмме 1. В нашей работе использованы несколько линеек стентов различных производителей, подробная характеристика которых приведена в диаграмме 2.
Возраст больных колебался от 49 до 85 лет (Mср 63,1 года). Нутритивная поддержка пациентов после стентирования заключалась в использовании сбалансированных по незаменимым макронутриентам питательных жидких смесей типа НУТРИЗОН и НУТРИДРИНК, в течении недели рекомендовалась механически, термически и химически щадящая диета с ограничением объёма пищи. В последующем ограничения в питании касались только структуры и химического состава пищи: она должна быть механически щадящей, не вызвать обтурацию стента крупным пищевым комком, а также по отношению к материалу стента пища должна быть не агрессивной.
Результаты и их обсуждение
После стентирования во всех случаях устранялась дисфагия. Больные получали возможность приема сбалансированного полноценного питания через рот. У всех пациентов в течение ближайшего послеоперационного периода отмечены боли в грудной клетке, однако у большинства (94%) болевой синдром являлся незначительным и лишь у 6% потребовал использования наркотических анальгетиков. Из 160 больных только у 6 пациентов наблюдалась миграция стента, при этом во всех наблюдениях была проведена успешная репозиция стента.
-
В 100% наблюдений отмечены улучшение общего состояния, стабилизация и умеренный прирост массы тела.
Диаграмма 1.Характеристика показаний к стентированию
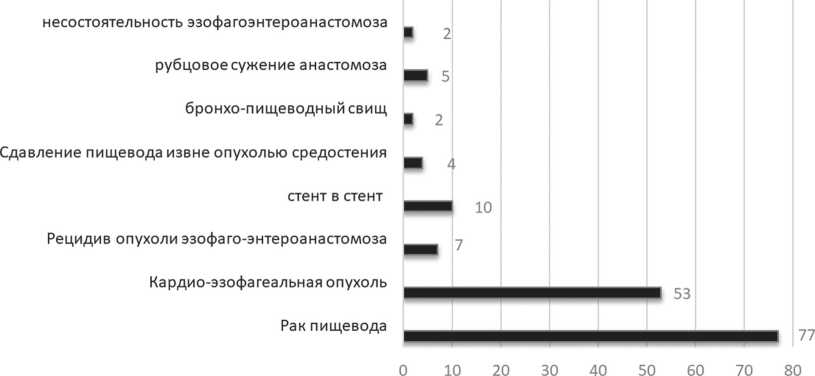
Диаграмма 2Характеристика использованных стентов
-
# М.І.Тесһ (Корея)
Endo-
Аех(Германия)
-
■ Gsebar (Китай)
е Boston Scientific
(США)
При контрольном комплексном обследовании месяц спустя отмечалась проходимость стента, его полное раскрытие и корректное позиционирование (рис. 2). Максимальная продолжительность жизни оперированных нами больных с протезированием пищевода по поводу бластоматозного процесса составила 20 мес.
Как правило выписка из стационара после проведения эндостентирования производилась на 2-3 сутки после контрольного рентгенологического исследования – контроля раскрытия, проходимости и правильного позиционирования импланта.
В ходе нашей работы нами отмечен ряд осложнений, которые подлежат отдельному детальному разбору и анализу. Из осложнений, связанных с реканализацией и стентированием пищевода, во всех случаях отмечалась боль за грудиной разной интенсивности в первые 5-7 дней после установки стента. Интенсивность боли зависела от протяженности и степени исходного стеноза пищевода. После полного рас-
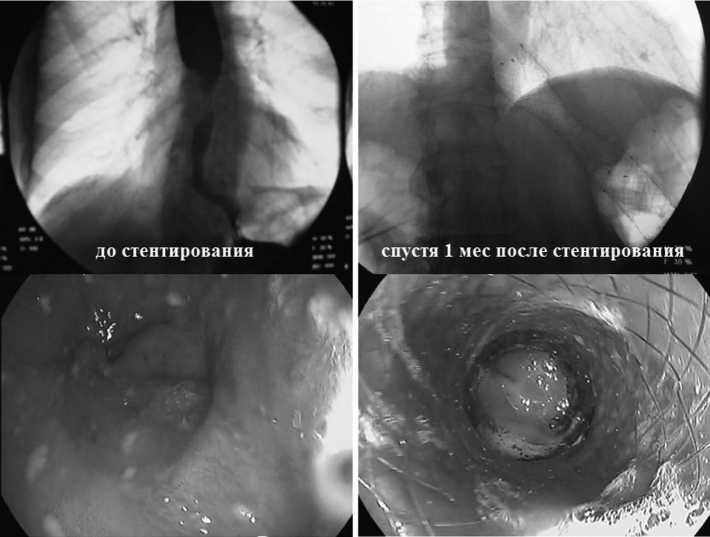
Рис. 2. Кардиоэзофагиальный рак до и после стентирования
правления стента в течение 7 дней болевой синдром полностью исчезал или значительно ослабевал, приема сильнодействующих обезболивающих средств не требовалось.
Кровотечение мы наблюдали у 3 пациентов, поступивших к нам по наряду скорой помощи с диагнозом желудочно-кишечное кровотечение. Этим пациентам были установлены частично покрытые стенты по поводу опухолевой стриктуры нижней трети пищевода от 11 до 14 месяцев назад. Причиной кровотечения явилась травматизация стенки пищевода и опухолевой ткани разрушенными фрагментами стентов. Факторами риска развития кровотечения являлся выраженный экзофитный компонент опухоли, предшествовавшая лучевая и/или химиотерапия, а также качество установленного стента. В нашем случае кровотечение было успешно остановлено во всех наблюдениях применением аргоплазменной и/или радиоволновой коагуляции без рецидива в процессе дальнейшего наблюдения. В одном наблюдении нами отмечена компрессия трахеи после установки стента в пищевод, что незамедлительно было устранено путем стентирования трахеи. Можно считать фактором риска компрессии трахеи высокую радиальную расширяющую силу и анатомическое расположение стриктуры или стеноза выше уровня карины. Компрессия трахеи развивается довольно быстро и лечебные мероприятия (или удаление ранее установленного стента или установку трахеального стента) должны проводиться немедленно, что нами и было выполнено.
Дистальная миграция стента в желудок (при раке кардии) и тонкую кишку (при рецидиве рака желудка после гастрэктомии) наблюдалась у 6 пациентов в сроки до 24 часов после стентирования. По данным литературы при применении пищеводных стентов миграция наблюдается от 5% при непокрытых и до 35% при использовании полностью покрытых стентов [12,13]. При этом частота дислокаций регистрируется в 2,5 раза чаще при экзоорганной компрессии пищевода, чем при его опухолевом поражении [4]. Предрасполагающими факторами для миграции стента считаются: короткая протяженность стриктуры и её выраженная извитость (локализация в области эзофагогастрального перехода, в области анастомоза), предшествующие лучевая и/или химиотерапия [14].
В нашем анализе проведен детальный разбор причин миграции. У одной больной был установлен непокрытый стент по поводу сужения средней трети пищевода извне опухолью средостения. Причина миграции нами видится в предварительной балонной дилятации просвета перед стентированием и меньший чем нужно диаметр стента (ошибка обусловлена опасностью развития компрессии трахеи и органов средостения). Произведена успешная репозиция. У 3-х пациентов миграция в дистальном направлении покрытых стентов явилась следствием активной перистальтики. Конечно, переоценка своих возможностей и небольшой опыт эндоскопистов по данной методике являются причиной возникновения таких осложнений. Пожалуй, только в
1-м случае миграция стента была обусловлена патологией, во всех остальных случаях - это наш недостаточный (на тот момент) опыт при освоении методики эндоскопического эндопротезирования при опухолевых стриктурах.
Возможные пути предотвращения миграции нами видятся в использовании частично покрытых стентов большого диаметра, коаксильной установкой двух стентов (покрытый в просвет непокрытого). При парциальной миграции стент может быть репонирован эндоскопически под обязательным рентгенологическим контролем. В случае полной проксимальной миграции стент подлежит удалению с установкой нового. При полной дистальной миграции хирургические вмешательства, направленные на удаление стента, осуществляются только при появлении симптомов непроходимости или нарушения целостности пищеварительного тракта (перфорация кишки). Во всех случаях нами выполнена репозиция стентов успешно и продолжено паллиативное лечение.
У 10 больных через 6-18 месяцев произошло прорастание и врастание опухоли в стент по проксимальному или дистальному краям с рецидивом дисфагии. Всем выполнена имплантация в зону стеноза второго стента (стен в стент). Частота возникновения осложнения такого рода по данным литературы в случае использования пищеводных стентов отмечается до 18% [15]. Причиной развития подобных осложнений в большинстве наблюдений следует считать прогрессирование онкологического процесса. Причиной прорастания покрытых стентов является разрушение мембраны покрытия. В литературе описаны два возможных механизма разрушения полиуретановой мембраны: повреждение при установке стента и разрушение мембраны пищеварительными ферментами и соляной кислотой (в результате рефлюкса). Этим можно объяснить более высокую частоту прорастания покрытых пилородуоденальных стентов по сравнению с пищеводными и отсутствие данного осложнения при использовании резистентного покрытия (политетрафторэтилен, нейлон) [15].
Установка стентов при опухолевых стриктурах - как правило, паллиативная помощь и если говорить о последующей лучевой терапии, то следует признать ее негативное последствие по отношению к импланту: усиление болевого синдрома и диспептических расстройств, температурная реакция, ухудшение состояния больных. Это связано с материалами из которых состоит стент (45%-титана и 55 % никеля). Титан-металл радионегативный, не накапливает излучение, что нельзя сказать о никеле. Последний накапливает в себе излучение и является, таким образом, источником дополнительной лучевой нагрузки на ткани, провоцируя и усугубляя лучевые повреждений пищевода и окружающих органов его тканей.
На основании проведенного нами анализа следует признать эндоскопическое стентирование ведущим методом паллиативного лечения больных раком пищевода, осложненного дисфагией. В настоящее время по накоплению опыта имеется тенденция к увеличению медианы выживаемости больных неоперабельным раком пищевода, которым было выполнено эндоскопическое стентирование опухолевой стриктуры.
Наличие или отсутствие отдаленных метастазов не оказывает существенного влияния на тактику паллиативного лечения, в котором ведущее место принадлежит внутрипросветным манипуляциям.
Заключение
Использование современных методов малоинвазивного лечения открывает перспективы для проведения полноценной паллиативной терапии инкурабельных больных с распространенным, стенозирующим раком пищевода, кардии и пилородуоденальной зоны. При выборе того или иного метода внутрипросветной эндоскопической хирургии и терапии следует исходить из опыта врача-эндоскописта, материально-технического оснащения, индивидуальных особенностей и общего состояния пациента, а также стадии, локализации и распространенности опухолевого процесса.
Несмотря на очевидные преимущества данного метода лечения, ряд вопросов остаётся спорным. До сегодняшнего дня дискутабельной является возможность применения стентов и их переносимость пациентами при высоком расположении злокачественных стриктур пищевода. Также остаётся неопределенным влияние на частоту осложнений проводимой лучевой и/или химиотерапии. Новейшие технические разработки – рассасывающиеся стенты, стенты с импрегнацией радиоактивными изотопами и т.д. возможно, позволят улучшить длительность и качество жизни пациентов, но до их внедрения в широкую практику необходимы проспективные контролируемые исследования.
осковский фургический урнал
Список литературы Стентирование пищевода в курации дисфагии у онкологических больных
- Чиссов ВИ, Старинский ВВ, Петрова ГВ. Злокачественные новообразования в России в 2006 году (заболеваемость и смертность). М.; 2008
- Соколов ВВ, Павлов П.В., Чиссов В.И., Вашакмадзе Л.А., Бойко А.В. Методы реканализации и стентирования при стенозирующем раке пищевода, желудка и 12-перстной кишки (Обзор литературы). Сибирский онкологический журнал. 2012; 5:64-73
- Соколов В.В., Филоненко Е.В., Карпова Е.С., Мамон-тов А.С., Козлов В.В. Эндоскопическая реканализация и стентирование при раке пищевода у больных с дисфагией III-IV степени. Вестник Московского oнкологического общества. 2004; 12: 7
- Хрусталева М.В., Годжелло Э.А. Выбор способа эндоскопического протезирования бластоматозных поражений пищевода, кардии и пищеводных анастомозов саморасправляющимися стен-тами. Вестник хирургической гастроэнтерологии. 2011; 2:14-24
- Venkatachala M, Richard KА. Placement of Conventional and Expandable Stems for Malignant Esophageal Stenoses. Tech. in Gastrointest. Endosc. 2001; 3(3):166-175
- Cwikiel W, Willén R, Stridbeck H, Lillo-Gil R, von Holstein CS. Self-expanding stent in the treatment of benign esophageal strictures: experimental study in pigs and presentation of clinical cases. Radiology. 1993; 187:667-671
- Dua KS, Kozarek R, Kim J, Evans J, Medda BK, Lang I, Ho-gan WJ, Shaker R. Self expanding metal esophageal stent with anti-reflux mechanism. Gastrointest Endosc. 2001; 53:603-613
- Hindy P, Hong J, Lam-Tsai Y, Gress F. Comprehensive Review of Esophageal Stents Gastroenterology & Hepatology. 2012; 8(8):526-534
- Sharma P, Kozarek R Role of Esophageal Stents in Benign and Malignant Diseases Am J Gastroenterol. 2010; 105:258-273
- Escorsell A, Bosch J. Self-expandable metal stents in the treatment of acute esophageal variceal bleeding. Gastroenterol Res Pract 2011;2011:910986
- Pontone S, Giusto M, Filippini A, Cicerone C, Pironi D, Merli M. Hemostasis in uncontrolled esophageal variceal bleeding by self-expanding metal stents: a systematic review. Gastroenterology and Hepatology From Bed to Bench. 2016;9(1):6-11
- Adam A Esophageal Stents Cardiovascular Interventional. Radiology. 2001; 1:112-113
- Siddiqui A, Spechler SJ, Huerta S. Surgical Bypass Versus Endoscopic Stenting for Malignant Gastroduodenal Obstruction: A Decision Analysis. Dig Dis Sci. 2007; 52:276-281
- Molina-Infante J, Fernandez-Bermejo M, Perez-Gallardo B. Removal of a migrated covered metallic stent through an esophageal stricture, with multiple endoloops. Endoscopy. 2010; 42(2):Е268-E269
- Jung GS. Malignant Gastric Outlet Obstructions: Treatment by Means of Coaxial Placement of Uncovered and Covered Expandable Nitinol Stents J Vasc Interv Radiol. 2002; 13:275-283.


