Стереотаксическая лучевая терапия при почечно-клеточном раке. Опыт и непосредственные результаты
Автор: Степанович Е.А., Демешко П.Д., Поляков С.Л., Минайло И.И.
Журнал: Злокачественные опухоли @malignanttumors
Статья в выпуске: 3S1 т.12, 2022 года.
Бесплатный доступ
Цель: Оценить выживаемость пациентов, страдающих почечно-клеточным (ПКР) раком I ст., подвергнутых стереотаксической аблационной лучевой терапии (САЛТ). Материал и методы: В исследование включены 22 пациента, которым в РНПЦ ОМР им. Н. Н. Александрова в период 2018–2022 гг. была проведена САЛТ по поводу впервые выявленной опухоли почки. Общее число облученных опухолей составило 25. Критериями включения в исследования явились: рак почки I стадии, наличие противопоказаний к хирургическому лечению, или отказ от хирургического лечения, а также высокий риск развития послеоперационных осложнений. В исследование включались пациенты с размером образований ≤ 5 см. Лечение осуществлялось на аппарате TrueBeam STx (Varian Medical Systems, США). Предписанная доза составила 48 Гр за 4 фракции, биологически эффективная доза (BED) α / β 3 Гр = 240 Гр, BED α / β 10 Гр = 105 Гр. Конечными точками исследования являлись кумулятивная инцидентность (КИ), скорректированная (СВ) и общая выживаемость (ОВ). Результаты: В 24 случаях при первичном контроле был достигнут локальный контроль заболевания (в 2 в виде полной регрессии, в 15 в виде стабилизации заболевания, в 7 случаях — частичная регрессия опухоли). У 1 пациента был отмечен продолженный рост опухоли и дальнейшее системное прогрессирование заболевания. При оценки локального контроля, медиана наблюдения которого составила 24 месяца, 4-летняя кумулятивная инцидентность составила 4,2 %. Вместе с тем, у 2 пациентов имело место прогрессирования заболевания с развитием отдаленных метастазов, безметастатическая выживаемость составила 86,2 %. За период наблюдения (медиана 24 месяца) умерло 3 человека, все — от причин, не связанных с раком почки. 4-летняя скорректированная выживаемость составила 100 %, общая выживаемость — 85,2 %. Выводы: Полученные предварительные результаты свидетельствуют о том, что стереотаксическая лучевая терапия может быть использована у неоперабельных пациентов, однако необходимо более глубокое изучение отдаленных результатов после проведенного лечения на большей когорте пациентов.
Почечно-клеточный рак, стереотаксическая лучевая терапия, общая выживаемость
Короткий адрес: https://sciup.org/140295817
IDR: 140295817 | DOI: 10.18027/2224-5057-2022-12-3s1-57-61
Текст научной статьи Стереотаксическая лучевая терапия при почечно-клеточном раке. Опыт и непосредственные результаты
Стандартом лечения рака почки I стадии в настоящее время является хирургический метод, позволяющий достигнуть 95% безрецидивной выживаемости при медиане наблюдения 5 лет и более. Для неоперируемых пациентов с небольшими первичными опухолями альтернативным подходом является аблация опухоли, а также стереотаксическая аблационная лучевая терапия (САЛТ) [1, 2, 3]. Стереотаксическая лучевая терапия или стереотаксическая лучевая терапия — метод крупнофракционной (гипо-фракционированной) дистанционной лучевой терапии, заключающийся в высокоточной доставке дозы излучения к мишени внутри тела пациента за одну или несколько фракций и характеризующийся резким спадом (градиентом) дозы на границе облучаемого объема [4].
Хотя радиочастотная абляция и криоабляция являются альтернативными вариантами локального лечения, САЛТ может быть предпочтительным подходом при лечении более крупных (до 5 см в диаметре), центрально расположенных опухолей с близким прилежанием к сосудам или мочеточнику, поскольку инвазивные методы местной абляции в указанной ситуации могут приводить к образованию стриктур, свищей и кровотечению [5]. Более того, поскольку САЛТ является неинвазивным методом лечения, то может иметь преимущества перед другими альтернативными местными методами лечения у пациентов с наличием противопоказаний к проведению оперативного лечения.
Безопасная реализация данной методики возможна при наличии соответствующего современного радиологического оборудования, включая возможность изготовления фиксирующих устройств, предлучевой подготовки с использованием 4-D компьютерной томографии (КТ) для оценки смещения мишени во время дыхания или синхронизации с ним, а также специализированных стереотаксических линейных ускорителей электронов с возможностью проведения облучения с управлением по изображениям (стереоскопический рентгеновский контроль за позиционированием пациента/мишени или компьютерная томография в коническом пучке).
Целью настоящего исследования явилось оценка непосредственных и отдаленных результатов применения САЛТ у неоперируемых пациентов с локализованным раком почки.
МАТЕРИАЛ И МЕТОДЫ
В проспективное исследование включено 22 пациента в возрасте от 60 до 80 лет (медиана возраста — 70 лет), которым в РНПЦ ОМР им. Н. Н. Александрова в период 2018–2022 гг. была проведена САЛТ по поводу впервые выявленной опухоли почки. Общее число облученных опухолей составило 25. Критериями включения в исследования явились: рак почки I стадии, наличие противопоказаний к хирургическому лечению, или отказ от хирургического лечения, а также высокий риск развития послеоперационных осложнений. В исследования включались пациенты с размером образований ≤ 5 см.
У шестерых пациентов диагноз почечно-клеточного рака был верифицирован гистологически после проведения трепан-биопсии образования под ультразвуковым контролем. У 16 пациентов верификация не выполнялась ввиду отсутствия технической возможности проведения биопсии (высокий риск повреждения прилегающих органов), в указанных случаях диагноз новообразования устанавливался мультидисциплинарным консилиумом на основе типичной картины при КТ-ангиографии.
Предлучевая подготовка пациентов заключалась в изготовлении фиксирующего устройства в виде вакуумного матраца с применением пневмокомпрессии для уменьшения подвижности органов брюшной полости во время дыхания.
4-D КТ, совмещенная с КТ-ангиографией проводилась на сканере DISCOVERY IQ (GE, США) с применением методики Real-time Position Management (RPM) system (Varian, США), заключавшейся в получении серий синхронизованных по дыханию изображений, отражающих все фазы дыхательного цикла.
Клинический объем облучения (CTV) включал макроскопическую опухоль, определяемую на сгенерированной из 4-D изображений композитной серии, отражающей амплитуду движения опухоли во время дыхания (внутренний целевой объем [internal target volume, ITV]). Планируемый объем облучения (PTV) получали изометрическим расширением CTV на 3 мм (рис. 1).
Предписанная доза составила 48 Гр за 4 фракции, биологически эффективная доза (BED) α/β 3 Гр = 240 Гр, BED α/β 10Гр = 105 Гр.
Дозиметрическое планирование проводилось с помощью системы «ECLIPSE», ARIA (Varian Medical System, США) по методике VMAT с предписанием дозы на изоцентр согласно рекомендациям ICRU 62 [4] (рис. 2).
В соответствии с требованиями программы гарантии качества лучевой терапии во всех случаях выполнялась дозиметрическая верификация плана лечения. С этой целью создавался индивидуальный верификационный план, который затем проверялся на линейном ускорителе с использованием системы OCTAVIUS 4D (с последующим сравнением полученного объемного дозного распределения с запланированным). Для оценки совпадения дозных распределений применялся метод гамма-индексирования.
Реализация курса ЛТ проводилась на специализированном стереотаксическом линейном ускорителе электронов TrueBeam STx (Varian Medical Systems, США) с применением управления процессом ЛТ по изображениям (IGRT) (КТ в коническом пучке). Облучение осуществлялось с перерывом между фракциями в 48 часов.
Локальный контроль оценивался по данным КТ-ангиографии (в двух случаях МРТ-ангиографии в ввиду наличия противопоказаний к введению рентгенкон-трастных средств) 1 раз в 6 мес. Оценка эффекта проведенного лечения осуществлялась по системе критериев RECIST 1.1 по данным контрольных томографических исследований, выполненных не ранее, чем через 3 месяца после окончания лучевого лечения. Были использованы следующие критерии оценки эффекта: а) полный ответ — исчезновение очага; б) частичный ответ — регрессия очага на 30% и более; в) стабилизация — отсутствие динамики; г) прогрессирование — увеличение размеров очага на 20% и более. Критерием достижения локального контроля считали стабилизацию или частичный эффект.
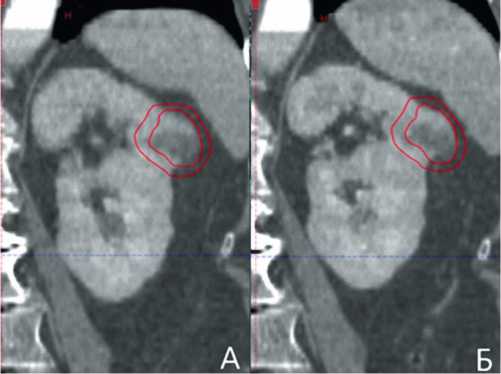
Рисунок 1. Оконтуривание клинического и планируемого объемов облучения (А — фаза выдоха; Б — фаза вдоха).
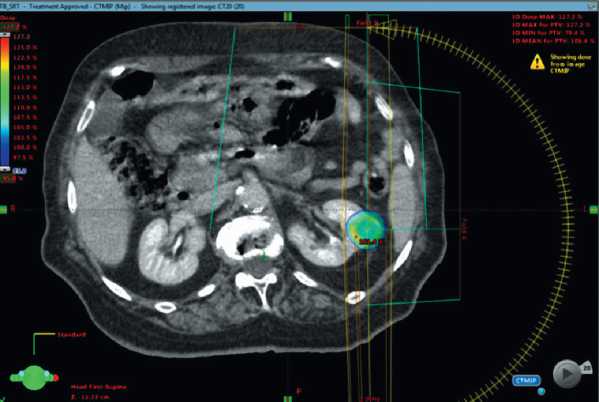
Рисунок 2. Типичный план облучения по методике VMAT.
Отдаленные результаты оценены по показателям кумулятивной инцидентности, скорректированной и общей выживаемости.
РЕЗУЛЬТАТЫ
Все пациенты завершили запланированный курс лечения, перерывы между фракциями сверх запланированных отсутствовали. У 6 из 22 (27%) пациентов отмечены явления острой гастроинтестинальной токсичности по классификации CTCAE 4.0 в виде тошноты I ст. выраженности у 5 пациентов (тошнота, потеря аппетита без изменений в приеме пищи) и рвоты у 1 пациента (рвота не более 2 раз в сутки). Указанные проявления у большинства пациентов развивались к окончанию курса лечения и купировались в течение 1–2 недель.
Общее число облученных первичных опухолей составило 25. В 24 случаях при первичном контроле был достигнут локальный контроль заболевания (у 2 в виде полной регрессии, у 15 в виде стабилизации заболевания, в 7 случаях — частичная регрессия опухоли). У 1 пациента был отмечен продолженный рост опухоли и дальнейшее системное прогрессирование заболевания.
На рис. 3 приведен пример полной регрессии опухоли левой почки через 1,5 года после стереотаксического облучения.
При оценки локального контроля, медиана наблюдения которого составила 24 месяца, 4-летняя кумулятивная инцидентность составила 4,2%. Вместе с тем, у 2 пациентов имело место прогрессирование заболевания с развитием отдаленных метастазов, безметастатическая выживаемость составила 86,2%.
За период наблюдения (медиана 24 месяца) в группе первичных пациентов умерло 3 человека, все — от причин, не связанных с раком почки. 4-летняя скорректированная выживаемость составила 100%, общая выживаемость — 85,2%.
ОБСУЖДЕНИЕ
Традиционно ПКР считается нечувствительной к облучению опухолью, что подтверждается исследованиями in vitro и in vivo. Сравнение различных клеточных линий in vitro показало, что ПКР относится к числу наиболее радиорезистентных новообразований [6]. Поскольку известно, что клетки ПКР демонстрируют низкое соотношение a/b (что подтверждается результатами исследования клоногенной выживаемости клеточных линий RCC Caki-1 и A498, показавших соотношение a/b 6,9 и 2,6 соответственно [7]), более высокие очаговые и суммарные дозы, применяемые при гипофракционированной лучевой терапии (в том числе САЛТ), могут преодолеть внутреннюю радиорезистентность ПКР. При более высоких дозах облучения альтернативные механизмы гибели клеток ПКР, такие как церамид-индуцированный апоптоз, становятся превалирующими [8]. Апоптоз эндотелиальных клеток, основанный на церамидном пути, считается важным механизмом действия крупнофракционной лучевой терапии
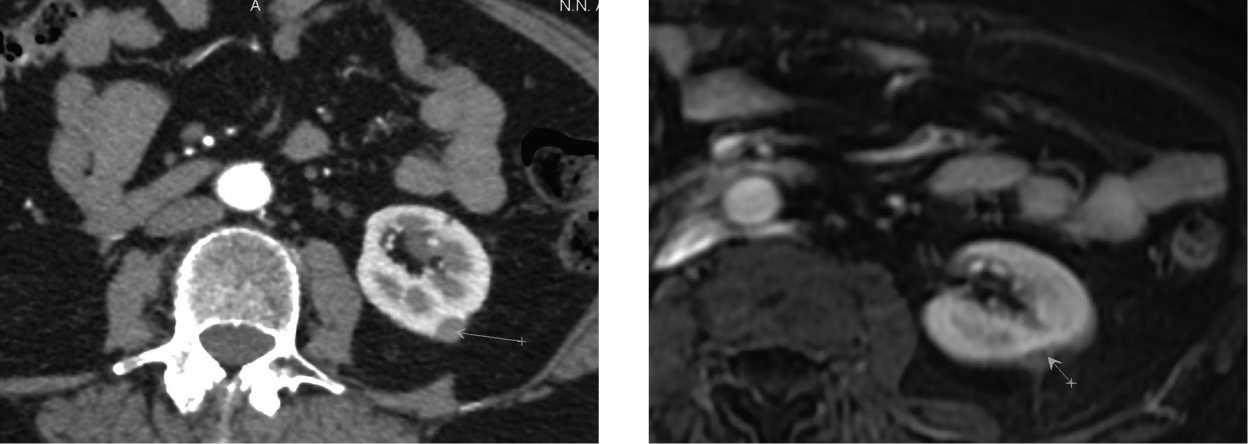
Рисунок 3. Картина полной регрессии опухоли при сроке наблюдения 1,5 года. А — Компьютерная томография до лечения; Б — Магнитно-резонансная томография после облучения.
РОССИЙСКИЙ
ОНКОЛОГИЧЕСКИЙ КОНГРЕСС-2022
XXVI
при опухолях с высокой васкуляризацией, к которым в том числе относится ПКР [8].
На молекулярном уровне секреторная форма кислой сфингомиелиназы перемещается во внеклеточную часть клеточной мембраны и превращает сфингомиелин в про-апоптотический белок церамид посредством ферментативного гидролиза [9]. Тот факт, что кислая сфингомиелиназа, особенно ее секреторная форма, преимущественно экспрессируется в эндотелиальных клетках, объясняет высокую чувствительность эндотелия к керамид-инду-цированному апоптозу [10]. Исследования in vivo, сравнивавшие линии мышей с инактивированной и интактной сфингомиелиназой показали, что в первом случае у мышей определялся повышенный порог индуцированного облучением эндотелиального апоптоза при проведении однократного облучения в дозе 20 Гр [11]. В клиническом плане важная роль сфингомиелиназы в отношении ответа опухоли после САЛТ была продемонстрирована в исследовании Sathishkumar S. et al. [12]: у 75 % пациентов с частичным или полным ответом опухоли после САЛТ наблюдалось значительное повышение уровня сфингомиелиназы в сыворотке крови.
Учитывая высокую иммуногенность, ПКР, индуцированная лучевой терапией иммуногенная гибель клеток может вызывать абскопальный эффект, приводящий к элиминации отдаленных метастазов. Имеется несколько сообщений о случаях абскопального эффекта при метастатическом ПКР после локальной лучевой терапии [13–17]. В небольшой серии случаев с 4 пациентами, опубликованной Wersäll P.J. et al., все пациенты, у которых наблюдался абскопальный эффект, жили более 5 лет, демонстрируя длительный противоопухолевый ответ [13]. Проводимое в настоящее время исследование II фазы направлено на изучение профиля безопасности и эффективности (общая выживаемость, время до местного прогрессирования, выживаемость без отдаленного прогрессирования) САЛТ и пемброли-зумаба при олигометастатическом ПКР (NCT02855203).
Согласно полученным нами результатам, стабилизация процесса была получена у 15 из 25 облученных опухолей (60%), частичная регрессия была достигнута в 7 случаях (28%), полная регрессия у 2 пациентов, при этом у 1 пациента был отмечен продолженный рост опухоли. Результаты нашего исследования коррелируют с данными других работ. Так, по данным исследования M. Staehler [et al.], частота полных, частичных ответов и стабилизации процесса после проведения однафракционного радиохирургического лечения в дозе 25 Гр составила соответственно 20%, 57% и 23% при медиане наблюдения 28,1 месяца. [18]. В исследовании McBride S. M. et al. [19] применена сходная с использованной нами схема фракционирования дозы (48 Гр за 3 фракции), при которой частота локального контроля в течение 12 месяцев составила 94% (полная регрессия в 7% случаев, частичная регрессия, стабилизация и продолжение роста — в 14%, 73% и 7%, соответственно), при этом не было отмечено случаев токсичности II и выше степени тяжести. В срок наблюдения, соответ- ствовавший 36,7 месяца было отмечено всего 2 местных рецидива. Svedman С. et al. [20] применили САЛТ по схеме 30 Гр за 3 фракции у 7 пациентов с опухолями единственной почки, средний объем образований составил 42 мл (от 4 до 60 мл). Авторы отмечают удовлетворительные отдаленные результаты лечения (медиана наблюдения составила 54 месяца) — был выявлен только один местный рецидив, по поводу которого было выполнено повторное облучение, при этом только у двух пациентов (включая случай ре-облучения) развилось умеренное снижение функции почек (повышение уровня креатинина на 25% выше нормы) при периоде наблюдения более 4 лет.
Основным ограничением данного исследования является небольшое число пациентов и относительно короткий период наблюдения (медиана — 15 месяцев), вместе с тем результаты демонстрируют возможность применения данного метода у пациентов, не подходящих для других методов локального лечения, что требует дальнейшего изучения в проспективном исследовании.
ЗАКЛЮЧЕНИЕ
Применение экстракраниальной стереотаксической лучевой терапии при раке почки у пациентов с наличием противопоказаний к хирургическому лечению, или отказе от хирургического лечения, а также имеющим высокий риск развития послеоперационных осложнений характеризуется удовлетворительными непосредственными и отдаленными результатами. Полученные предварительные результаты свидетельствуют о том, что стереотаксическая лучевая терапия может быть альтернативным методом лечения у неоперабельных пациентов с первичным локализованным раком почки и позволяет достичь высоких цифр локального контроля и удовлетворительно переносится.
Необходимо более глубокое изучение отдаленных результатов после проведенного лечения на большей когорте пациентов. Дальнейшее исследование необходимо и для определения оптимальных доз и режима фракционирования, а также для разработки надежных методик оценки эффекта.
Список литературы Стереотаксическая лучевая терапия при почечно-клеточном раке. Опыт и непосредственные результаты
- Percutaneous ablation or minimally invasive partial nephrectomy for cT1a renal masses? A propensity score-matched analysis / L. Bianchi [et al.] // Int J Urol .- 2022 .- Vol. 29, № 3 .- P. 222-228.
- European Association of Urology Guidelines on Upper Urinary Tract Urothelial Carcinoma : 2020 Update / M. Rouprêt [et al.] // Eur. Urol .- 2021 .- Vol. 79 (1) .- P. 62-79.
- Роль стереотаксической лучевой терапии при почечно-клеточном раке / П. Д. Демешко [и др.] // Онколог. журн .- 2019 .- Т. 13, № 1 .- С. 110-116.
- Stereotactic ablative radiation therapy for oligoprogressive renal cellcarcinoma / J. E. Schoenhals [et al.] // Adv. Radiat. Oncol .- 2021 .- Vol. 6 (5) .- P. 100692.
- Stereotactic body radiotherapy for primary renal cell carcinoma and adrenal metastases / G. Kothari [et al.] // Chin. Clin. Oncol .- 2017 .- Vol. 6 (Suppl 2) .- P. 17.
- Deschavanne, P. J. A review of human cell radiosensitivity in vitro / P. J. Deschavanne, B. Fertil // Int. J. Radiat. Oncol. Biol. Phys .- 1996 .- Vol. 34 .- P. 251-266.
- Radiobiologic studies of radioimmunotherapy and external beam radiotherapy in Vitro and in Vivo in human renal cell carcinoma xenografts / S. Ning [et al.] // Cancer .- 1997 .- Vol. 80 .- P. 2519-2528.
- Radiotherapy for renal-cell carcinoma / G. De Meerleer [et al.] // Lancet Oncol .- 2014 .- Vol. 15 .- P. 170-177.
- Kolesnick, R. Radiation and ceramide-induced apoptosis / R. Kolesnick, Z. Fuks // Oncogene .- 2003 .- Vol. 22 .- P. 5897-906.
- Human vascular endothelial cells are a rich and regulatable source of secretory sphingomyelinase. Implications for early atherogenesis and ceramide-mediated cell signaling / S. Marathe [et al.] // J. Biol. Chem .- 1998 .- Vol. 273 .- P. 4081-4088.
- Tumor response to radiotherapy regulated by endothelial cell apoptosis / M. Garcia-Barros Science .- 2003 .- Vol. 300 .- P. 1155-1159.
- Elevated sphingomyelinase activity and ceramide concentration in serum of patients undergoing high dose spatially fractionated radiation treatment : implications for endothelial apoptosis / S. Sathishkumar [et al.] // Cancer. Biol. Ther .- 2005 .- Vol. 4 .- P. 979-986.
- Regression of non-irradiated metastases after extracranial stereotactic radiotherapy in metastatic renal cell carcinoma / P. J. Wersall [et al.] // Acta. Oncol .- 2006 .- Vol. 45 .- P. 493-497.
- The abscopal effect of radiation therapy / D. J. Craig [et al.] // Future. Oncol .- 2021 .- Vol. 17 (13) .- P. 1683-1694.
- The abscopal effect : a review of pre-clinical and clinical advances / J. R. Janopaul-Naylor [et al.] // Int. J. Mol. Sci .- 2021 .- Vol. 22 (20) .- P. 11061.
- The abscopal effect in the era of checkpoint inhibitors / O. Kodet [et al.] // Int. J. Mol. Sci .- 2021 .- Vol. 22 (13) .- P. 7204.
- Abscopal effect in the radio and immunotherapy / A. M. Pevzner [et al.] // Radiat. Oncol. J .- 2021 .- Vol. 39 (4) .- P. 247-253.
- Single fraction radiosurgery for the treatment of renal tumors / M. Staehler [et al.] // J. Urol .- 2015 .- Vol. 193, № 3 .- P. 771-775.
- McBride, S. M. A phase 1 dose-escalation study of robotic radiosurgery in inoperable primary renal cell carcinoma / S. M. McBride, A. A. Wagner, I. D. Kaplan // Int. J. Radiat. Oncol. Biol. Phys .- 2013 .- Vol. 87, № 2 - P. 84.
- A prospective phase II trial of using extracranial stereotactic radiotherapy in primary and metastatic renal cell carcinoma / C. Svedman [et al.] / / Acta. Oncol.- Vol. 45, № 7.- P. 870-875.


