Стимуляция неоангиогенеза у больных с облитерирующим атеросклерозом артерий нижних конечностей
Автор: Корымасов Е.А., Казанцев А.В.
Журнал: Хирургическая практика @spractice
Рубрика: Оригинальные исследования
Статья в выпуске: 1, 2017 года.
Бесплатный доступ
Представлены результаты применения аутологичных прогениторных клеток костного мозга для стимуляции неоангиогенеза у 42 больных с дистальной формой облитерирующего атеросклероза артерий нижних конечностей, при невозможности выполнения реконструктивной операции. Пациенты были распределены в 3 группы по 14 человек: I группа - больные, которым вводились аутологичные прогениторные клетки CD 133+; во II группе вводилась лейкоцитарная фракция клеток костного мозга (CD 34+); III группа (плацебо) - больные, которым был введен физиологический раствор. Полученный препарат вводили в мышцы внутренней и внешней поверхности голени. Оценка результатов по шкале Rutherford показала, что в 1 и 2 группах пациентов, получивших клеточный материал, наблюдается статистически значимое улучшение клинического состояния по сравнению с 3 группой «плацебо» (p
Хроническая ишемия нижних конечностей, трансплантация стволовых клеток, костный мозг, предшественники эндотелиоцитов
Короткий адрес: https://sciup.org/142211697
IDR: 142211697 | УДК: 616.34-007.43-031:611.957]-089.844
Stimulation of neoangiogenesis in patients with atherosclerosis obliterating arteries of lower extremities
The results of neoangiogenesis has been studied for the treatment of 42 patients with arterial atherosclerosis occlusive disease of lower extremities who are not candidates for treatment surgical. We studied the results in the 3 groupies including 14 patients in the each. Autological progenitor cells (CD 133+) were transplanted in I-st group. Leucocytes bone morrow cells (CD 34+) were transplanted in II group. The patients of III group was injected isotonic solution as a placebo. All of solutions were injected in internal and external muscles of shin. We appreciated our clinical results in Rutherford's scale. In conclusion, we observed what the improvement of clinical condition in patients (with a transplantation of CD 133+ and CD 34+ of I and II groups) was trustworthy by Mann-Whitney's criterion.
Текст научной статьи Стимуляция неоангиогенеза у больных с облитерирующим атеросклерозом артерий нижних конечностей
Введение Материалы и методы
В последнее время среди больных с облитерирующим атеросклерозом артерий нижних конечностей увеличивается удельный вес поражения бедренно-подколенно-берцового сегмента [1]. Выбор хирургической тактики у таких пациентов является наиболее трудной задачей современной ангиохирургии, особенно при развитии критической ишемии: применение методов прямой реваскуляризации возможно лишь у 40-70% больных. Основной причиной невозможности выполнения и неудовлетворительных результатов реконструктивных операций является этажность поражения с преимущественной окклюзией артерий голени [1–3]. Единственным выходом в таких ситуациях являются различные методы непрямой реваскуляризации, направленные на развитие коллатерального кровообращения. Одним из перспективных методов стимуляции неоангиогенеза является клеточная терапия [4, 5] и генно-инженерные технологии [3, 6]. Немногочисленные исследования демонстрируют эффективность клеточной трансплантации в плане восстановления кровоснабжения мышц [6–9].
Целью исследования явилось изучение эффективности применения аутологичных прогениторных клеток костного мозга у больных с облитерирующим атеросклерозом артерий нижних конечностей.
В исследование включены 42 пациента (мужчины) с облитерирующим атеросклерозом артерий нижних конечностей, в возрасте от 46 до 69 лет (средний возраст 57±1,8 лет). Длительность заболевания составила от 1 года до 16 лет (в среднем 5,8±4,17 лет). У всех больных была II Б стадия заболевания по классификации А.В. Покровского, дистанция безболевой ходьбы 10-50 м, поражение бедренно-подколенно-берцового сегмента, невозможность выполнения реконструктивной операции. У 15 больных ранее была выполнена поясничная симпатэктомия, реваскуляризирующая остеоперфорация большеберцовой кости, ампутация пальцев стопы (у 3 больных с 2 сторон). Протокол исследования прошел экспертизу в Комитете по биоэтике и был утвержден Ученым Советом ФГБОУ ВО «СамГМУ Минздрава РФ». У всех пациентов получено письменное информированное согласие на участие в исследовании.
Всем больным в соответствии с протоколом выполняли общеклинические лабораторные исследования, цветное дуплексное картирование артерий нижних конечностей с измерением лодыжечно-плечевого индекса, тредмил-тест, трансфеморальную артериографию нижних конечностей.
По дизайну данное исследование является рандомизированным, двойным слепым, плацебо-контролируемым, ограниченной клинической апробацией метода. Все пациенты путем рандомизации были распределены в 3 группы по 14 человек.
В I группу вошли больные, которым вводились аутологичные прогениторные клетки CD133+. Во II группу вошли пациенты, которым вводилась лейкоцитарная фракция клеток костного мозга. В III группу (плацебо) включены больные, которым был введен физиологический раствор. Ни врач, ни больной не знали, какой препарат применялся для лечения («двойное слепое» исследование). Все пациенты получали одинаковую “базовую” медикаментозную терапию (пентоксифиллин, реополиглюкин, никотиновая кислота).
Забор костного мозга осуществлялся в операционной под наркозом путем пункции передних и задних остей подвздошных костей. Далее костный мозг подвергали обработке методом двойного центрифугирования с целью получения лейкоцитарной фракции клеток костного мозга. Выделение CD133+ клеток проводили методом иммуно-магнитной сепарации с использованием реагентов “Miltenyi Biotec”. У пациентов III группы (плацебо) выделенную лейкоцитарную фракцию клеток костного мозга подвергали программному замораживанию и хранили для дальнейшего использования в дьюарах с жидким азотом при температуре -196°С. Полученный препарат вводили в мышцы по латеральной и медиальной поверхности голени в 10 точек на каждой конечности, по 1,5 мл в каждую точку.
В I группе количество введенных ядросодержащих клеток на 1 конечность составило (2,12 + 1,23)×109; CD133+ клеток (1,26±0,12)×106. Во II группе среднее количество введенных в одну конечность ядросодержащих клеток составило (4,65+1,00)×109 и CD133+ (1,84±0,11)×106.
Осложнений после общего обезболивания, трепанации подвздошной кости и введения препарата не отмечено ни у одного из пациентов.
Результаты и обсуждение
Период наблюдения пациентов составил 12 месяцев. Информация о вводимом препарате была раскрыта после окончания обследования всех пациентов через 6 месяцев. В этот же период пациентам III группы была возвращена лейкоцитарная фракция клеток костного мозга, забранная во время основного этапа исследования.
Оценка клинических исходов произведена по рекомендованным стандартам, опубликованным международным обществом кардиоваскулярной хирургии Rutherford et al. (1997) (табл. 1). Оценка эффективности лечения проводилась отдельно для каждой конечности, в которую был введен препарат.
Таким образом, в I и II группах пациентов, получивших прогениторные клетки, наблюдается статистически значимое улучшение клинического состояния по сравнению с III группой – плацебо (p<0,001 по критерию Манна-Уитни).
По результатам тредмил-теста до лечения дистанция безболевой ходьбы у больных в среднем составила 45,2±11,09 м. Через 1, 6 и 12 месяцев дистанция безболевой ходьбы увеличилась во всех группах и составила: в I группе 111,1±42,71 м, 132,1±85,59 м, 135,0±86,27 м соответственно, во II группе 66,1±33,64 м, 125,4±87,24 м, 130,0±88,89 м соответственно, в
III группе – 61,8±20,90 м, 64,3±41,27 м, 75,0±43,98 м. соответственно. Отмечено статистически значимое увеличение дистанции безболевой ходьбы у пациентов I и II группы по сравнению с группой “плацебо” (p<0,005). Статистически значимых отличий в динамике безболевой ходьбы между I и II группами не обнаружено.
Таблица 1
Изменения в клиническом статусе больных по шкале Rutherford
|
Критерий шкалы |
I группа CD133+ 20 конечностей |
II группа СD34+ 17 конечностей |
III группа плацебо 23 конечности |
|
+2 умеренное улучшение |
45% 9 конечностей |
47% 8 конечностей |
4,3% 1 конечность |
|
+1 минимальное улучшение |
35% 7 конечностей |
41,2% 7 конечностей |
17,5% 4 конечности |
|
0 без изменений |
10% 2 конечности |
5,9% 1 конечность |
56,5% 13 конечностей |
|
–1 незначительное ухудшение |
10% 2 конечности |
5,9% 1 конечность |
13% 3 конечности |
|
–2 умеренное ухудшение |
0 |
0 |
8,7% 2 конечности |
|
Манн-Уитни |
р>0,1 |
р<0,001 |
|
Ангиография нижних конечностей выполнялась всем пациентам до лечения и через 6 месяцев после введения клеточного материала. Оценка ангиограмм проводилась отдельно для каждой конечности в баллах, в зависимости от степени развития коллатеральной сети [4]: 0 (отсутствие развития коллатералей), +1 (незначительное развитие коллатералей), +2 (умеренное развитие коллатералей), +3 (богатое развитие коллатералей). Результаты анализа ангиограмм представлены на рис.1.
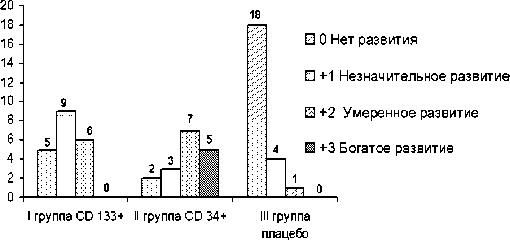
Рис 1. Оценка результатов ангиографии через 6 мес
Среди больных, которым вводили клеточный материал (I и II группы), число пациентов с “незначительным”, “умеренным” и “богатым” развитием коллатералей было больше по сравнению с пациентами III группы (различия статистически значимые: p<0,001 по критерию Манна-Уитни).
Полученные предварительные ближайшие результаты лечения больных со II Б стадией облитерирующего атеросклероза артерий нижних конечностей весьма обнадеживающие. Отсутствие статистически значимых отличий между результатами в I и II группах, при наличии клинического улучшения, позволяет в дальнейшем использовать для лечения только лейкоцитарную фракцию клеток костного мозга. Однако для окончательной оценки необходимо изучение отдаленных результатов лечения, а также дозозависимости эффекта.
Как и любой новый метод лечения со временем находит свое применение, так и предложенный способ займет свое место в арсенале лечения больных с облитерирующим атеросклерозом артерий нижних конечностей.
Заключение
Применение аутологичных прогениторных клеток костного мозга эффективно и безопасно у больных со II Б стадией облитерирующего атеросклероза артерий нижних конечностей. Данный метод лечения целесообразен у пациентов с дистальной формой облитерирующего атеросклероза артерий нижних конечностей, у которых нет возможности выполнения реконструктивной операции, а также у больных, которым уже была выполнена реконструктивная операция или непрямая реваскуляризация, но отмечается прогрессирование ишемии конечности. Предложенный метод лечения можно рекомендовать для многоцентровых клинических испытаний.
Список литературы Стимуляция неоангиогенеза у больных с облитерирующим атеросклерозом артерий нижних конечностей
- Савельев В. С., Кошкин В. М. Критическая ишемия нижних конечностей. М.: Медицина. 1997; 160.
- Покровский А. В. Клиническая ангиология: руководство для врачей. М.: Медицина. 2004; 2: 184 -197.
- Константинов Б.А.,Бочков Н.П.,Гавриленко А.В.Воронов Д.А. и др. Отдаленные результаты лечения хронической ишемии нижних конечностей с использованием генно-инженерных конструкций с геном ангиогенина. Анналы хирургии. 2005; 3: 23 -26.
- Шевченко Ю. Л. Медико-биологические и физиологические основы клеточных технологий в сердечно-сосудистой хирургии. СПб: Наука; 2006; 287.
- Смолянинов А. Б., Пыхтин Е. В., Булгин Д. В., Томонага М. Клеточные технологии в лечении терминальной стадии хронической ишемии нижних конечностей. Клеточная трансплантология и тканевая инженерия. 2007; 2: 3: 40 -46.
- Гавриленко А. В., Воронов Д. А., Фомичева И. И. Генно-инженерные технологии стимуляции ангиогенеза в лечении хронической ишемии нижних конечностей. Анналы хирургии. 2005; 4: 5 -8.
- Бокерия Л. А., Георгиев Г. П., Голухова Е. 3., Еремеева М. В., Ким А.И. и др. Клеточные и интерактивные технологии в лечении врожденных и приобретенных пороков сердца и ишемической болезни сердца. Вестник РАМН. 2004; 9: 48 -55.
- Canizo M. C., Lozano F., Gonzalez-Porras J. R., Barros M. et al. Peripheral endothelial progenitor cells (CD133+) for therapeutic vasculogenesis in a patient with critical limb ischemia. One year follow-up. Cytotherapy. 2007; 9: 1: 99 -102.


