Строение диоксиматов триарилсурьмы и оценка степени заполнения координационной сферы атома металла
Автор: Ефремов А.Н., Шарутина О.К., Шарутин В.В.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Неорганическая химия
Статья в выпуске: 4 т.16, 2024 года.
Бесплатный доступ
На основании данных рентгеноструктурного анализа (РСА) ряда диоксиматов триарилсурьмы Ar3Sb(ON=CHR)2 проведено сравнительное описание их молекулярных структур и установление особенностей строения. В молекулах диоксиматов триарилсурьмы наблюдаются внутримолекулярные контакты Sb···N (2,728(4)-2,900(6) Å), которые иногда меньше примерно на 1 Å суммы ван-дер-ваальсовых радиусов атомов-партнеров (3,61 Å). Сокращенное расстояние Sb×××N не сопровождается ожидаемым удлинением связей N-O в иминокси-группе и не зависит от длин связей Sb-O. Однако укорочение расстояний Sb···N коррелирует с уменьшением валентного угла NOSb. В структурах, содержащих метоксигруппы в арильных лигандах при атоме сурьмы, наблюдаются внутримолекулярные взаимодействия типа Sb···OMe. В диоксиматах триарилсурьмы, содержащих разные арильные лиганды при атоме сурьмы, но одинаковые оксиматные зависимости геометрических параметров координационного узла [SbO2C3] от природы арильных лигандов не наблюдается, но в некоторых структурах имеет место закономерное удлинение внутримолекулярных расстояний Sb···N. Впервые в программе Solid-G для диоксиматов триарилсурьмы проведена количественная оценка степени заполнения координационного пространства атома сурьмы в модели телесных углов лигандов (G-параметр) с учетом геометрии молекул в кристаллическом состоянии по результатам РСА, который составил 80,19-85,70 %. Максимальное насыщение координационной сферы (90,93 ) имеет место в структуре, где наблюдаются внутримолекулярные взаимодействия Sb···OMe. В бис(μ3-2-оксибензальдоксимато-О,O',N)-(μ2-оксо)-тетраарил)дисурьме, где 2-гидроксибензальдоксиматный лиганд является тридентатным мостиковым, а атомы сурьмы гексакоординированы, степень заполнения координационного пространства превышает 90 %.
Диоксиматы триарилсурьмы, молекулярная структура, рентгеноструктурный анализ, стерический фактор, координационная сфера, g-параметр
Короткий адрес: https://sciup.org/147246053
IDR: 147246053 | УДК: 546.865+547.47+548.312.5 | DOI: 10.14529/chem240409
Structure of triarylantimony dioximates and assessment of the metal atom coordination sphere occupation degree
On the basis of the X-ray diffraction analysis data for a number of triarylantimony dioximates Ar3Sb(ON=CHR)2, comparative description of their molecular structures and evaluation of structural features have been carried out. In the triarylantimony dioximate molecules, the Sb···N intramolecular contacts are observed (2.728(4)-2.900(6) Å), which are sometimes smaller by approximately 1 Å than the sum of the van der Waals radii of the partner atoms (3.61 Å). The shortened Sb···N distance is not accompanied by the expected lengthening of the N-O bonds in the iminoxy group and does not depend on the Sb-O bond lengths. However, the shortening of the Sb···N distances correlates with a decrease in the NOSb bond angle. In structures, containing methoxy groups in aryl ligands at the antimony atom, the intramolecular interactions of the Sb···OMe type are observed. In triarylantimony dioximates, containing different aryl ligands at the antimony atom, but identical oximate ligands, no dependences of the [SbO2C3] coordination unit geometric parameters on the nature of aryl ligands are observed, but in some structures there is a regular elongation of the Sb···N intramolecular distances. For the first time in the Solid-G program for triarylantimony dioximates, the quantitative assessment of the antimony atom coordination sphere occupation degree in the model of ligand solid angles (G-parameter) has been carried out, taking into account the molecular geometry in the crystalline state according to the X-ray diffraction analysis results, which amounts to 80.19-85.70%. The maximum coordination sphere occupation (90.93%) occurs in the structure where the Sb···OMe intramolecular interactions are observed. In bis(μ3-2-oxybenzaldoximato-O,O',N)-(μ2-oxo)-tetraaryl)disantimony, where the 2-hydroxybenzaldoximate ligand is tridentate, it is a bridging one, while the antimony atoms are hexacoordinated, the coordination sphere occupation degree exceeds 90%.
Текст научной статьи Строение диоксиматов триарилсурьмы и оценка степени заполнения координационной сферы атома металла
Органические соединения сурьмы(V) представляют интерес с фундаментальной точки зрения, поскольку для них характерны разнообразные структуры, в которых проявляются внутри- и межмолекулярные взаимодействия. К таким соединениям относятся диоксиматы триарилсурьмы, в молекулах которых наблюдаются внутримолекулярные взаимодействия атома металла с атомами азота оксиматных лигандов. Однако диоксиматы триарилсурьмы в литературе представлены относительно небольшим рядом соединений [1–17], при этом большинство из них являются производными трифенил-, три( орто -толил)- и три( мета -толил)сурьмы. Диоксиматы три( пара -толил)- и трис (5-бром-2-метоксифенил)сурьмы представлены единичными примерами, диоксиматы трис (4-фторфенил)- и трис (3-фторфенил)сурьмы ранее не были известны.
Установлено, что объем лигандов, окружающих центральный атом в элементоорганических соединениях, влияет на их реакционную способность. Одним из методов оценки заполнения координационного пространства центрального атома лигандами в металлоорганических комплексах является расчет G-параметра, который характеризует стерические размеры лигандов и может быть использован как для уже синтезированных комплексов, так и для предсказания возможности получения неизвестных соединений [18]. Расчет G-параметра для диоксиматов триарилсурмы ранее не проводился.
Экспериментальная часть
Расчет степени заполнения координационной сферы атома металла всеми лигандами (G-параметр, %), доля координационного пространства, занимаемого каждым лигандом на расстоянии в 2,28 Å от атома металла (параметр G 2,28 , %), а также перекрывания телесных углов лигандов (G γ , %) проводили в программе Solid-G [18]. Погрешность рассчитанных параметров составила ±0,02 %.
Файл с расширением .xyz , необходимый для расчетов в программе Solid-G , формировали с помощью программ OLEX2 [19] и SHELXL/PC [20].
Расчет искомых параметров проводили очередностью команд, отображаемых в интерфейсе программы Solid-G :
-
1. Select Atom – выбор центрального атома, относительно которого будут проводиться расчёты всех параметров.
-
2. Identify Ligands – определение лигандов, связанных с центральным атомом.
-
3. Calculate Angles – запуск расчетов телесных углов и G-параметров.
-
4. Start Viewer – визуализация рассчитанных G-параметров лигандов.
Методики синтеза соединений 1-13 и рентгеновские эксперименты кристаллов осуществлены ранее и опубликованы в работах [21–24].
Расчет G-параметров проведен с учетом геометрии молекул в кристаллическом состоянии по результатам РСА.
Рентгеноструктурный анализ (РСА) кристаллов соединений проведен на автоматическом четырехкружном дифрактометре D8 QUEST фирмы Bruker (Mo Kα-излучение, λ = 0,71073 Å, графитовый монохроматор) при 293 К. Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены с помощью программ SMART и SAINTPlus [25]. Все расчеты по определению и уточнению структур выполнены с помощью программ SHELXL/PC [20] и OLEX2 [19]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Положение атомов водорода уточняли по модели наездника (Uизо(H) = 1,2Uэкв(C)). В некоторых структурах отдельные фрагменты молекул, сольватные молекулы растворителя были разупорядочены при условиях ограничений на их геометрию и параметры колебаний эллипсоидов смещений. Заселенности разупорядоченных атомов были вычислены автоматически. В кристалле соединения 11 присутствуют два типа кристаллографически независимых молекул (а и б). Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№№ 1465384 (1), 1062231 (2), 1059962 (3), 1060054 (4), 2178726 (5), 1471842 (6), 1465109 (7), 1471948 (8), 1060387 (9), 2064391 (10), 1820147 (11), 1834110 (12), 1835929 (13); ; . Основные длины связей и валентные углы соединений 1–10 приведены в табл. 1, соединений 11–13 – в табл. 2.
Таблица 1
Основные геометрические параметры молекул диоксиматов триарилсурьмы Ar 3 Sb(ON=CHAr') 2
|
№ |
Ar, Аr' |
Интервал изменения φ(СSbС), град. |
φ(NOSb), град. |
Ср. знач. d (Sb–C), Å |
d (Sb–О), Å |
d (N–О), Å |
d (Sb···N), Å |
|
1 |
p -Tol, С 6 Н 4 Br-2 |
116,1(2)–122,3(2) |
109,1(2), 109,3(2) |
2,107(4) |
2,072(3), 2,075(3) |
1,372(5), 1,386(5) |
2,841(3), 2,844(4) |
|
2 |
p -Tol, С 6 Н 4 OH-2 |
118,3(1)–121,0(1) |
107,9(2), 108,2(2) |
2,103(4) |
2,081(2), 2,086(2) |
1,387(3), 1,402(3) |
2,839(4), 2,850(3) |
|
3 |
p -Tol, С 6 Н 4 NO 2 -2 |
116,3(2)–123,4(2) |
102,7(2), 109,2(2) |
2,104(4) |
2,069(3), 2,071(3) |
1,381(5), 1,390(4) |
2,728(4), 2,849(3) |
|
4 |
p -Tol, С 4 Н 3 O |
116,2(2)–123,8(3) |
108,6(5), 109,6(4) |
2,114(6) |
2,075(5), 2,076(5) |
1,372(8), 1,374(10) |
2,831(7), 2,847(6) |
|
5 |
p -Tol, С 4 Н 2 O-NO 2 -5 |
117,4(5)–121,5(4) |
108,5(3), 115,3(7) |
2,121(8) |
2,083(4), 2,109(2) |
1,381(7), 1,369(2) |
2,840(5), 2,900(6) |
|
6 |
3-FC 6 H 4 , С 6 Н 4 Br-2 |
117,5(2)–122,6(2) |
110,3(2), 112,1(2) |
2,111(4) |
2,062(3), 2,068(3) |
1,385(5), 1,391(4) |
2,865(4), 2,883(4) |
|
7 |
3-FC 6 H 4 , С 6 Н 4 OH-2 |
119,6(2)–120,2(1) |
111,4(2), 111,4(2) |
2,106(5) |
2,081(3), 2,081(3) |
1,397(4), 1,397(4) |
2,900(1), 2,900(1) |
|
8 |
4-FC 6 H 4 , С 6 Н 4 Br-2 |
117,5(2)–122,7(2) |
112,1(3), 110,0(3) |
2,113(5) |
2,108(6), 2,112(5) |
1,384(6), 1,385(6) |
2,884(6), 2,860(5) |
|
9 |
4-FC 6 H 4 , С 6 Н 4 NO 2 -2 |
116,2(1)–122,9(1) |
104,0(2), 110,5(2) |
2,113(3) |
2,065(2), 2,085(2) |
1,382(4), 1,391(3) |
2,765(3), 2,866(3) |
|
10 |
2-MeO-5-BrC 6 H 3, С 6 Н 4 Br-2 |
115,2(2)–125,2(2) |
112,3(3), 112,9(3) |
2,122(6) |
2,069(3), 2,072(3) |
1,372(6), 1,374(5) |
2,887(4), 2,895(4) |
Таблица 2
Основные геометрические параметры молекул бис ( μ 3 -2-оксибензальдоксимато-О,O',N)-( μ 2 -оксо)- тетракис (арил)дисурьмы 11–13
|
№ |
Ar |
φ(СNO), град. |
Интервал изменения d (Sb–C), Å |
d (Sb–Oмост), Å |
d (Sb–Oоксимат.), Å |
d (Sb–Oокси), Å |
d (Sb···N), Å |
|
11а |
p -Tol |
115,7(2) |
2,108(7)-2,128(6) |
1,943(3) |
2,101(4) |
2,016(4) |
2,257(3) |
|
12 |
3-FC 6 H 4 |
115,7(2), 115,0(2) |
2,117(3)-2,136(3) |
1,948(2), 1,954(2) |
2,076(2), 2,097(2) |
2,002(2), 2,010(2) |
2,257(3), 2,230(3) |
|
13 |
4-FC 6 H 4 |
115,7(2), 115,0(2) |
2,130(6)-2,139(7) |
1,954(4), 1,958(4) |
2,094(5), 2,082(4) |
2,015(5), 2,019(4) |
2,257(3), 2,230(3) |
Обсуждение результатов
В мол е к у ла х д и о к с и ма то в три а ри лс у рьмы 1 – 10 атом сурьмы имеет координацию тригональной бипирамиды с а томами к и с лорода оксиматных лигандов в аксиальных п оложе н и ях [21–23] (рис. 1). Молек ул ы с оеди н е н ия 7 симметричны и содержат винтовую ось четвертого порядка, проходящую через атомы Sb (1) , С ( 11 ) , С ( 14 ) .
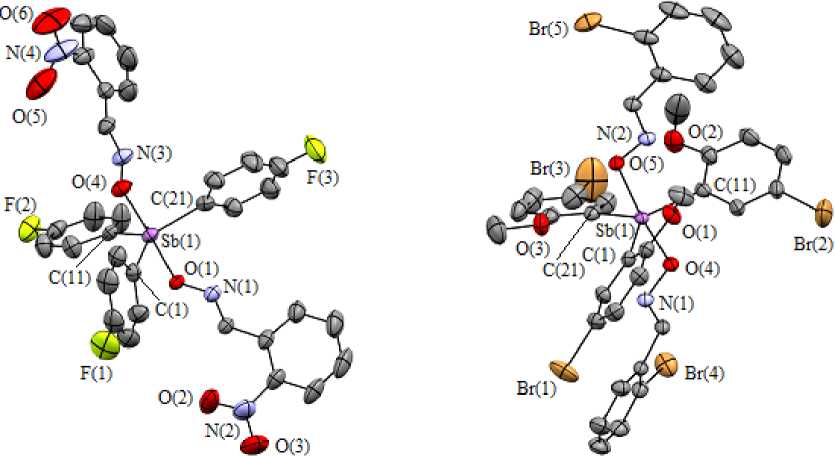
Рис. 1. Молекулярные структуры 9 (слева) и 10 (справа) (атомы водорода не приведены)
В 1 – 10 суммы э к в а то ри альн ы х угл ов CSbC равны 360º (в пределах погрешности экспери мента) , зн а че н и я и н д и видуальн ы х углов отклоняются от теоретического не бол е е, чем на 5º. Аксиальные углы OSbO б ли з ки к и деа льн ому ( 180º) (уменьшение не более, чем на 10º).
Фрагменты SbC3 в с трукту ра х диоксиматов триарилсурьмы практически плоские. Наибольшие расстояния Sb···[С 3 ] н а б люд аю тс я в с тру к ту ра х 5 и 10 и составляют 0,068 и 0,073 Å соответственно. В молекуле 7 атом Sb р а с п о ла г а е тс я в п л ос к ос ти [ С 3 ].
В интервале 2,103(4)– 2 , 122(6) Å находятся средние значения длин связей Sb–C. При этом наибо л ь шие з нач ения наб л юдают ся в м о л ек ул ах 5 (среднее значение 2,121(8) Å ) и 10 (2,122(6) Å ) . Расстояния Sb–O и зме н яю тс я в н еш и ро к ом д иа п азон е ( 2, 0 62( 3 ) - 2,112(5) Å) и незначительно (не более чем на 0,062 Å) п р е в ышаю т с у мму к ов але н т н ых рад и у с ов Sb и O (2,05 Å [26]). Длины связей Sb–C в о в с е х струк т у ра х п ревы ша ю т ра сс тоя н и я Sb–O, т. е. экваториальные лиганды при атом е с у рьмы р а с п ол ож ен ы д а л ьш е , че м ак с и альные , что является особенностью строения диок-симатов триарилсурьмы.
В молекулах 1 – 10 н аблюд а ю тс я в н у три моле к у лярн ые к он та к т ы Sb···N (2,728(4)–2,900(6) Å), кот оры е ин ог д а м еньш е п ри ме рн о на 1 Å суммы ван-дер-ваальсовых радиусов атомов-партнеров (3,61 Å [27 ] ) . С ок ращ е н ное рас с тоян и е Sb ⋅⋅⋅ N не сопровождается ожидаемым удлинением связей N–O и н е за в и с и т от дли н с в язе й Sb–O. Однако укорочение расстояний Sb···N приводит к уменьшению валентного угла NOS b.
Расстояния Sb···OMe в стру к ту ре 10 составляют 3,035(4), 3,074(6) и 3,165(5) Å, что не превышает сумму ван-дер- в аальс ов ых радиусов атомов металла и кислорода (3 , 58 Å) [27]. Данные зн а чени я н е мн ого боль ш е а на логи чных в трис (5-бром-2-метоксифенил)сурьме (2,985(1), 3,051(1), 3,052(1) Å) [28].
А н а л и з д а н н ых геоме трических параметров диоксиматов триарилсурьмы, сод е р жа щ и х р аз н ы е а ри льн ы е ли га н ды п ри а томе с у рьмы, н о од и н а к ов ые окс и ма тн ые , п озв оляет сделать вывод о том, что за в и с и мос ти геоме три че ск их п а рам е тров к оорд и н а ц ион н ого узл а [SbO 2 C 3 ] от природы ари льн ых ли г а н д ов н е н аб лю да ется. В структурах с одинаковыми оксиматными ли г а н д а ми и м е ет мес то н е к ото рое у д ли н е ни е в н у три моле к у лярн ых ра с с тоян и й Sb···N в ряду молекул 1 , 8 , 6 , 10 . В соединении 10, с о д е р ж а щ е м ме токс и гру п п у в о 2-м положении и бром в 5-м положении, обсуждаемые расстояния са м ые д ли н ные в ряд у бис (4-бром-бензальдоксиматов) триарилсурьмы.
Р анее было п о к а за н о, что 2-гидроксибензальдоксим в присутствии пероксида водорода реаг иру е т с три фе н и лс у рьмой с об ра зов а н и е м д и ок с има та три фе н и лс у рьмы [ 2], а с трис (5-бром-2-мет окс ифе н и л)с у рьмой ре а к ц и я и д е т п о д ру гой с хе ме , д а в а я бис ( μ 3 -2-оксибензальдоксимато-О,O',N)-( μ 2 -оксо)- тетракис (5-б ром -2-метоксифенил)дисурьму [29]. Мы установили, что взаимодействие трис (3-фторфенил)- и трис (4-метилфенил)сурьмы с этим же оксимом в присутствии трет - бути л гидроп е рокс ид а п ри в од и т к о б ра зов а н ию с оед и н е н и й 7 и 2 соответственно. При проведении реакций с 30%-ны м в од н ым ра с тв ором п е рок с ид а в одоро да 2-гидроксибензальдоксим п рояв ляе т б и фун к ц и он а л ьн ые с в ойства. С повышением степени окисления атома сурьмы наблюдаетс я рас ще п ле н и е од н о й с в язи Sb–C, при этом продуктом реакции является биядерный сурьма-о рга н ическ и й к омпл е кс , в к отором а томы ме т алла ш е с ти коорд и н и ров а ны [24].
Пред п олага е м ый н а ми меха н и зм р е а к ц и и можно представить схемой:
Ar3Sb + H2O2
OH
Ar 3 Sb
OH
HON=CHC6H4OH-2 OH
----------------> Ar3Sb
- H 2 O
ON=CHC6H4OH-2
Ar3Sb(OH)ON=CHC6H4OH-2
- H 2 O
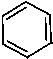
HO
Ar
N
Ar O
/ уO I Ar
O Ar Ar
- 2 ArH
Схема 1
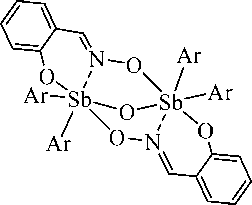
Характер 2- о к с и б е н за л ьдок с и ма тн ы х лига н д ов в м оле к у ла х 11 - 13 определяется как триден-татны й , за с че т с в языв а ни я с од н и м и з а томов Sb через атом кислорода иминоксигруппы, а с другим – ч е ре з атом к и сл орода ги д роксильной группы и координационной связи Sb···N (рис. 2–4).
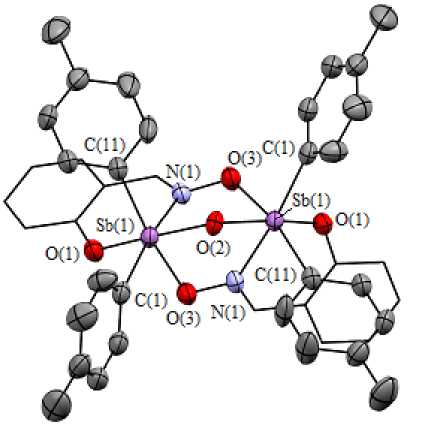
Рис. 2. Молекулярная структура 11а (атомы водорода и сольватная молекула толуола не приведены)
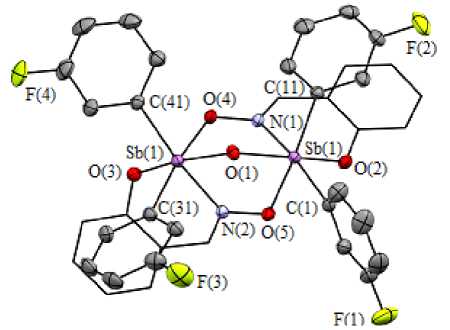
Рис. 3. Молекулярная структура 12 (атомы водорода не приведены)
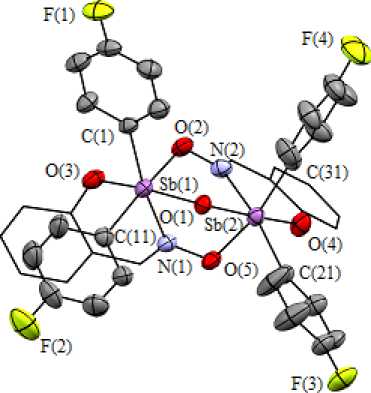
Рис. 4. Молекулярная структура 13 (атомы водорода не приведены)
Координация атомов м ет а лла в 11 - 13 искаженная октаэдрическая: транс -углы составляют 162,0(2)º-172,2(2)º. Дли ны с в язе й Sb-C варьируют в интервале 2,108(7)- 2,139(7) Å. Три типа расстояний Sb-О н ес коль к о ра зли чаю тс я : Sb–O(N=C) – 2,076(2) - 2,097(4) Å; Sb-О мост – 1,943(3) 1,958(4) Å; Sb–O(C Ar ) – 2, 002( 2 ) - 2,020(4) Å. Достаточно короткие расстояния Sb···N (2,230(3) 2,267(5) Å при сумме ван-дер- в аа льс ов ых р а д и у с о в Sb и N 3,61 Å [27]) являются доказательством си льн ого не в а ле н тн о го в за и модействия, которое вызывает уменьшение у глов CNO (до 115,0(2)º - 116,2(5)º) п о с р а в н е н и ю с 12 0 º.
Э лек трон ны е э ф фек ты за ме с ти те ле й в а ри льных радикалах при атоме металла не являются ф а к тором, вл и я ющ и м н а и с к аже н и е в а ле н тных у глов и д ли н у с в язе й Sb-О в 11 - 13 . Наиболее короткие расстояния Sb-С н а б л ю даю тс я в молекуле 11 , содержащей пара -толильные лиганды.
Ра с с т оян и е меж д у а том а ми с у рьмы жесткого [2.2.1]гептанового фрагмента составляет 3,361(2) - 3,378(1) Å, что зн а чи те льно ме ньше у дв ое н ного в а н -дер-ваальсового радиуса Sb (4,12 Å [27]).
На осно ван ии данны х РС А впервые была проведена количественная оценка ст ер ич еског о ф а ктора в молекулах дио ксим ат о в триарилсурьмы по степени заполнения координацио нно й сф ер ы ат о м а сур ь м ы в м о дел и т е л есны х углов лигандов и выявлена взаимосвязь с нал ич ием вн ут р и м о ле кул я р ны х в з аим о действи й , пр иво дящих к искажению геометрических характерист ик м о л екул .
Параметр G (%) ха рак те р и зует процент заполнения координационной сф е р ы а тома ме т а л л а в се ми ли га н д а ми с у че том об ла с те й п е р е к р ыв а н и я (G γ , %) телесных углов двух и более лигандов. Параметр G 2,28 (%) оценив а ет с тепень заполнения координационного простр а н с тв а лигандом на расстоянии в 2,28 Å о т а т ома металла, что позволяет сравнить между собой вк лад р а зн ых ли га ндов в заполнение коорд и на ц и онн ой с ф е ры це н тра л ьн ого а том а .
Согласно расчетам степень заполнения координационного пространства центрального атома (G-параметр) в диоксиматах триарилсурьмы 1-9 составляет 80,19 - 85,70 % (табл. 3). Параметр G 2,28 (Ar) практически одинаков во всех структурах и не зависит от наличия заместителей в арильных группах, поэтому заполнение координационной сферы в 1-9 определяется оксиматны-ми лигандами и расстояниями Sb ⋅⋅⋅ N. Так, в группах или парах соединений с одинаковыми окси-матными лигандами ( 1 , 6 , 8 ; 2 , 7 и 3 , 9 ) наибольшие значения параметра G 2,28 для оксиманых лигандов имеют место в 1 , 2 и 3 , где расстояния Sb ⋅⋅⋅ N наименьшие (2,841(3), 2,844(4) Å в 1 ; 2,839(4), 2,850(3) в Å 2 ; 2,728(4), 2,849(3) в Å 3 ). В структуре 10 более полное насыщение координационной сферы (90,93 %) обеспечивается, напротив, арильными лигандами, которые формируют внутримолекулярные взаимодействия Sb···OMe.
В структурах 11–13 , в которых оксиматный лиганд является тридентатным мостиковым, а атомы сурьмы гексакоординированы, степень заполнения координационного пространства превышает 90 % (G ср. 93,89 % 11 , 92,30 % 12 , 91,81 % 13 ).
Таблица 3
Значения параметров G и G 2,28 для молекул диоксиматов триарилсурьмы Ar 3 Sb(ON=CHAr') 2
|
№ |
Ar, Аr' |
G, % |
G 2,28 (Ar), % |
G 2,28 (ON=CHAr'), % |
|
1 |
p -Tol, С 6 Н 4 Br-2 |
83,55 |
15,25, 15,33, 15,27 |
14,02, 14,00 |
|
2 |
p -Tol, С 6 Н 4 OH-2 |
85,70 |
15,28, 15,33, 15,33 |
15,24, 15,10 |
|
3 |
p -Tol, С 6 Н 4 NO 2 -2 |
84,60 |
15,28, 15,24, 15,27 |
14,09, 14,94 |
|
4 |
p -Tol, С 4 Н 3 O |
83,56 |
15,51, 15,36, 15,32 |
13,58, 13,66 |
|
5 |
p -Tol, С 4 Н 2 O-NO 2 -5 |
80,19 |
15,30, 15,41, 15,33 |
13,68, 13,62 |
|
6 |
3-FC 6 H 4 , С 6 Н 4 Br-2 |
82,51 |
15,31, 15,23, 15,35 |
13,69, 13,83 |
|
7 |
3-FC 6 H 4 , С 6 Н 4 OH-2 |
82,95 |
15,36, 15,57, 15,35 |
14,66, 14,66 |
|
8 |
4-FC 6 H 4 , С 6 Н 4 Br-2 |
82,32 |
15,17, 15,32, 15,37 |
13,66, 13,85 |
|
9 |
4-FC 6 H 4 , С 6 Н 4 NO 2 -2 |
83,58 |
15,30, 15,35, 15,36 |
13,93, 14,74 |
|
10 |
2-MeO-5-BrC 6 H 3, С 6 Н 4 Br-2 |
90,93 |
18,08, 17,97, 17,67 |
13,65, 13,74 |
Выводы
С учетом геометрии молекул в кристаллическом состоянии (по данным РСА) впервые проведен количественный расчет степени заполнения координационной сферы атома сурьмы лигандами (G-параметр, %) в диоксиматах триарилсурьмы, что позволяет оценить стерический фактор. G-параметр в молекулах 1-9 варьирует в пределах 80,19 - 85,70 %. Установлено, что арильные группы, не имеющие координирующих центров, способных образовывать невалентные взаимодействия с атомом сурьмы, вносят примерно одинаковый вклад в насыщение координационной сферы центрального атома, и поэтому G-параметр определяется, главным образом, вкладами ок-симатных лигандов. Насыщение координационного пространства центрального атома в соединении 10 (G 90,93 %) обусловлено арильными лигандами, которые образуют внутримолекулярные невалентные взаимодействия Sb···OМе. Заполняемость координационной сферы металла в соединениях 11–13 , в которых атомы сурьмы гексакоординированы, превышает 90 %.
Список литературы Строение диоксиматов триарилсурьмы и оценка степени заполнения координационной сферы атома металла
- Sharutin V.V., Molokova O.V., Sharutina O.K. et al. // Russ. J. Gen. Chem. 2004. V. 74, No. 10. Р. 1485. DOI: 10.1007/s11176-005-0041-4.
- Sharutin V.V., Sharutina O.K., Molokova O.V. // Russ. J. Inorg. Chem. 2012. V. 57, No. 6. P. 832. DOI: 10.1134/S0036023612010226.
- Gupta A., Sharma R.K., Bohra R. et al. // Polyhedron. 2002. V. 21. P. 2387. DOI: 10.1016/S0277-5387(02)01155-5.
- Yin H, Quan L., Li L. // Inorg. Chem. Commun. 2008. V. 11. P. 1121. DOI: 10.1016/j.inoche.2008.06.017.
- Dodonov V.A., Gushchin A.V., Gor'kaev D.A. et al. // Russ. Chem. Bull. 2002. V. 51. P. 1051. DOI: 10.1023/A: 1019634307064.
- Sharutin V.V., Sharutina O.K., Molokova O.V. et al. // Russ. J. Coord. Chem. 2002. V. 28, No. 7. P. 464. DOI: 10.1023/A:1016293009968.
- Sharutin V.V., Sharutina O.K., Molokova O.V. et al. // Russ. J. Gen. Chem. 2001. V. 71, No. 8. P. 1243. DOI: 10.1023/A: 1013220911661.
- Sharutin V.V., Sharutina O.K., Artem'eva E.V. et al. // Bull. South Ural State Univ. Ser. Chem. 2014. V. 6, No. 2. P. 5. EDN: SAUKZV
- Sharutin V.V., Sharutina O.K., Artem'eva E.V. et al. // Russ. J. Inorg. Chem. 2015. V. 60, No. 2. P. 170. DOI: 10.1134/S0036023615020138.
- Sharutin V.V., Sharutina O.K., Gabitova D.M. et al. // Russ. J. Inorg. Chem. 2017. V. 62, No. 1. Р. 55. DOI: 10.1134/S003602361701017X.
- Sharutin V.V., Sharutina O.K., Artem'eva E.V. et al. // Russ. J. Gen. Chem. 2016. V. 86, No. 12. P. 2671. DOI: 10.1134/S1070363216120161.
- Sharutin V.V., Sharutina O.K., Artem 'eva E.V. et al. // Bull. South Ural State Univ. Ser. Chem. 2015. V. 7, No. 2. P. 17. EDN: TQIWUT
- Sharutin V.V., Sharutina O.K., Artem 'eva E.V. et al. // Bull. South Ural State Univ. Ser. Chem. 2016. V. 8, No. 2. P. 61. DOI: 10.14529/chem160207.
- Artem'eva E.V., Makerova M.S., Sharutin V.V. et al. // Bull. South Ural State Univ. Ser. Chem. 2017. V. 9, No. 2. P. 50. DOI: 10.14529/chem170207.
- Молокова О.В. Оксиматы тетра- и триарилсурьмы. Синтез и строение: дис.... канд. хим. наук. Благовещенск, 2001. 118 с.
- Sharutin V.V., Poddel'sky A.I., Sharutina O.K. // Russ. J. Coord. Chem. 2020. V. 46. P. 663. DOI: 10.1134/s1070328420100012.
- Cambridge Crystallographic Database. Release 2023. UK: University of Cambridge.
- Guzei I.A., WendtM. // Dalton Trans. 2006. V. 33. P. 3991. DOI: 10.1039/b605102b.
- Bruker. SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Displaying Crystal Structures from Diffraction Data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Dolomanov O.V., Bourhis L.J., Gildea R.J. et al. // J. Appl. Cryst. 2009. V. 42. P. 339. DOI: 10.1107/S0021889808042726.
- Шарутин В.В., Шарутина О.К., Ефремов А.Н. // Бутлеровские сообщения. 2016. Т. 47. С. 145. EDN: XHTWFD
- Sharutin V.V., O.K. Sharutina, A.N. Efremov // Russ. J. Coord. Chem. 2017. V. 43. Р. 526. DOI: 10.1134/S1070328417080073.
- Ефремов А.Н. // Вестник ЮУрГУ. Серия «Химия». 2022. Т. 14. С. 34. DOI: 10.14529/chem220403.
- Sharutin V.V., Sharutina O.K., Efremov A.N. et al. // Russ. J. Inorg. Chem. 2019. V. 64. Р. 597. DOI: 10.1134/S0036023619050188.
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Cordero B., Gómez V., Platero-Prats A.E. et al. // Dalton Trans. 2008. V. 21. P. 2832. DOI: 10.1039/B801115J.
- MantinaM., Chamberlin A.C., Valero R. et al. // J. Phys. Chem. A. 2009. V. 113. P. 5806. DOI: 10.1021/jp8111556.
- Sharutin V.V., Senchurin V.S., Sharutina O.K. et al. // Russ. J. Gen. Chem. 2011. V. 81. Р. 2102. DOI: 10.1134/S1070363211100100.
- Sharutin V.V., Sharutina O.K. // Russ. J. Inorg. Chem. 2014. V. 59. P. 1263. DOI: 10.1134/S0036023614110229.


