Строение кристаллов комплексного соединения хлорида марганца с треонином, полученных методом медленного выпаривания
Автор: Абдуллаева Ж.Д., Джумаева Ж.Ш.
Журнал: Бюллетень науки и практики @bulletennauki
Рубрика: Химические науки
Статья в выпуске: 6 т.10, 2024 года.
Бесплатный доступ
Кристаллы комплексных соединений применяются в технике, оптике, медицине, фармации, в обработке поверхностей и т. д. Изучение кристаллической структуры комплексных соединений важен, поскольку они широко используются в промышленности и обладают механическими, термическими и рядом других ценных свойств. Проведено изучение кристаллической структуры комплексного соединения хлорида марганца с аминокислотой треонин, а также изучение физико-химических и биологических свойств. Для синтеза комплексного соединения был применен метод медленного выпаривания. Состав образованных кристаллов соединения был проанализирован рентген дифракционным и спектроскопическими структурными анализами. Исследована структура комплексного соединения MnCl2×C4H9NO3 хлорида марганца и аминокислоты треонин. В результате исследования было установлено что кристаллическая структура соединения MnСl2×C4H9NO3 относится к орторомбической сингонии с пространственной симметрией P212121.
Хлорид марганца (ii) четырехводный, треонин, медленное выпаривание, ик-спектр, кристаллическая структура
Короткий адрес: https://sciup.org/14130168
IDR: 14130168 | УДК: 546.212:546.47 | DOI: 10.33619/2414-2948/103/01
Structure of manganese chloride and threonine crystals formed by slow vaporization method
Crystals of complex compounds are used in technology, optics, medicine, pharmacy, surface treatment, etc. The study of the crystal structure of complex compounds is important because they are widely used in industry and exhibit mechanical, thermal and a number of other valuable properties. Study of the crystal structure of complex compound of manganese chloride with the amino acid threonine, as well as the study of its physicochemical and biological properties. For the synthesis of complex compound, the method of slow evaporation was used. The composition of the formed crystals of the compound was analyzed by X-ray diffraction and spectroscopic structural analyses. the structure of the complex compound MnCl2×C4H9NO3 manganese chloride and the amino acid threonine was studied. As a result of the study, it was established that the crystal structure of the compound MnCl2×C4H9NO3 belongs to the orthorhombic system with space symmetry P212121.
Текст научной статьи Строение кристаллов комплексного соединения хлорида марганца с треонином, полученных методом медленного выпаривания
Бюллетень науки и практики / Bulletin of Science and Practice
УДК 546.212:546.47
Биологическое значение хлорид марганца MnCl 2 ×4H 2 O широко изучается в медицине на предмет его влияния на биологическую активность [1, 2] в качестве нейронального контрастного агента для усиленной магнитно-резонансной томографии а также в исследованиях координационной химии [3, 4]. Контрастные вещества на основе хлорида марганца применяются при магнитно-резонансной томографии (МРТ) для лечения пациентов с очаговыми поражениями печени и тяжелыми нарушениями функции почек из-за его эффективного положительного усиления контраста [5].
Марганец в хелатированной форме малотоксичен и широко используется в качестве контрастного вещества в клинике, инъекционным контрастным веществом Mn(II) является дипиридоксальдифосфат марганца (II) (Mn-DPDP) для визуализации печени [6].
В условиях периодической культуры на жидкой питательной среде добавление в последнюю хлорида марганца (II) ведет к изменениям расщепления четырех белков-субстратов «нейтральными» протеиназами мицелия и культуральной жидкости P. ostreatus [7].
L-треонин, протеиногенная α-аминокислота, включена во все белки, усиливает рост тканей, улучшает энергетический обмен в мышечных клетках и активирует иммунную систему. L-треонин — незаменимая кислота для человека и животных. Его суточная норма, рекомендованная Всемирной организацией здравоохранения (ВОЗ), составляет 15 мг для человека на кг веса. Треонин является жизненно важным компонентом белков и ферментов, играя решающую роль в синтезе белка в организме. В фармацевтике он может входить в состав препаратов, направленных на обеспечение специфических аминокислотных профилей для пациентов с определенными заболеваниями или тех, кто находится в процессе выздоровления. Треонин является важной биоактивной молекулой, которая оказывает жизненно важное посредническое воздействие на синтез белка, энергетический обмен и усвоение питательных веществ. Многие предыдущие исследования были сосредоточены на потребностях, физиологических функциях и путях метаболизма Thr. Сообщалось, что соответствующие уровни Thr в рационе могут способствовать росту животных, усиливать иммунную функцию и поддерживать здоровье кишечника .
Материалы и методы исследования
Комплексное соединение MnСl 2 ×C 4 H 9 NO 3 хлорида марганца с аминокислотой треонин было получено методом медленного выпаривания. ИК-спектроскопией определены основные колебательные частоты комплексного соединения. Изучено расположение кристаллических плоскостей и установлена структура монокристаллов комплексного соединения MnСl 2 ×C 4 H 9 NO 3 хлорида марганца с треонином.
Результаты и обсуждение
Состав полученных комплексных соединений идентифицирован рентген дифракционным и ИК-спектроскопическим анализами. Пространственные изомеры хлорида марганца (II) тетрагидрата [MnCl 2 (H 2 O) 4 ] показаны на Рисунке 1.
В ИК-спектре формированного комплексного соединения MnСl2×C4H9NO3 пики при 3212, 3220, 2931 см-1 в длинноволновой области соответствуют валентному колебанию аминогруппы. Полоса поглощения валентного колебания карбоксильной группы (νasСОО-) сдвинута на 60 см-1, т. е. смещается от 1620 см-1 до 1585 см-1 и 1617 см-1 в область более низких частот, что подтверждает образование комплекса через атом кислорода карбоксильной группы.
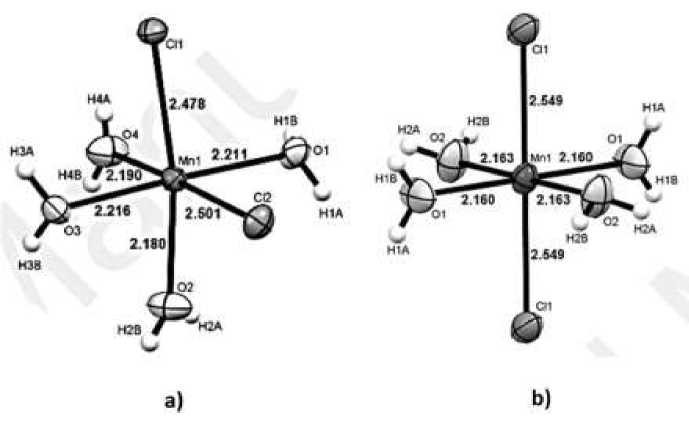
Рисунок 1. Транс- и цис- комплексы хлорида марганца тетрагидрата [MnCl 2 (H 2 O) 4 ] в а) α -, cis-[MnCl 2 (H 2 O) 4 ] и b) β -, trans-[MnCl 2 (H 2 O) 4 ] формах
Колебательные частоты ИК-спектроскопии комплексного соединения хлорида марганца с треонином MnСl 2 ×C 4 H 9 NO 3 даны в Таблице.
Таблица
ОСНОВНЫЕ КОЛЕБАТЕЛЬНЫЕ ЧАСТОТЫ ИК-СПЕКТРА КОМПЛЕКСНОГО СОЕДИНЕНИЯ ХЛОРИДА МАРГАНЦА С ТРЕОНИНОМ MnСl 2 ×C 4 H 9 NO 3 (см-1)
|
Отнесение |
C 4 H 9 NO 3 |
MnСl 2 ×C 4 H 9 NO 3 |
|
v as (NH 2 ) |
— |
2931,42 |
|
v s (NH 2 ) |
2974,51 |
2595,34 |
|
v as (COO-) |
1620,11 |
1585,64 |
|
v s (COO-) |
1413,29 |
1394,64 |
|
δ as (NH 2 ) |
— |
1028,3 |
|
δ s (NH 2 ) |
1028,37 |
715,26 |
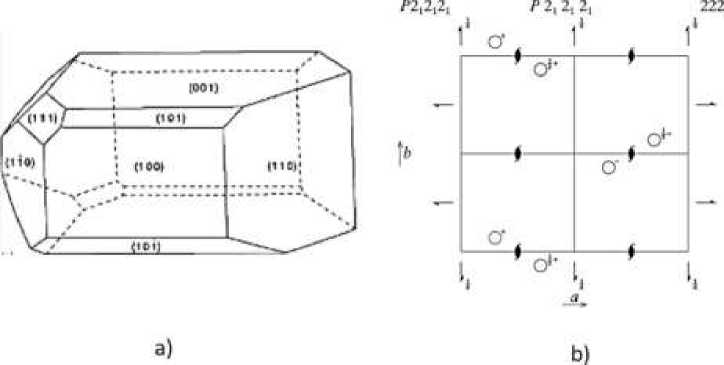
Рисунок 2. а) Расположение кристаллических плоскостей комплексного соединения
MnСl 2 ×C 4 H 9 NO 3 ; b) Установлено, что структура монокристаллов комплексного соединения
MnСl2×C4H9NO3 хлорида марганца с треонином относится к орторомбической сингонии с пространственной симметрией P2 1 2 1 2 1 .
Выводы
Были определены пики поглощения спектров формированного комплексного соединения MnСl 2 ×C 4 H 9 NO 3.
Изучено расположение кристаллических плоскостей и установлена структура монокристаллов комплексного соединения MnСl 2 ×C 4 H 9 NO 3 хлорида марганца с треонином которая относится к орторомбической сингонии с пространственной симметрией P2 1 2 1 2 1 .
Список литературы Строение кристаллов комплексного соединения хлорида марганца с треонином, полученных методом медленного выпаривания
- Zhao F., Cai T., Liu M., Zheng G., Luo W., Chen J. Manganese induces dopaminergic neurodegeneration via microglial activation in a rat model of manganism // Toxicological sciences. 2009. V. 107. №1. P. 156-164. DOI: 10.1093/toxsci/kfn213
- Martinek P., Kula E., Hedbávný J. Reactions of Melolontha hippocastani adults to high manganese content in food // Ecotoxicology and environmental safety. 2018. V. 148. P. 37-43. DOI: 10.1016/j.ecoenv.2017.10.020
- Grünecker B., Kaltwasser S. F., Peterse Y., Sämann P. G., Schmidt M. V., Wotjak C. T., Czisch M. Fractionated manganese injections: effects on MRI contrast enhancement and physiological measures in C57BL/6 mice // NMR in Biomedicine. 2010. V. 23. №8. P. 913-921. DOI: 10.1002/nbm.1508
- Bouteiller H., Pasturel M., Lemoine P. On the Crystal Structures of the Polymorphs of Manganese (II) Chloride Tetrahydrate: α-MnCl2×4H2O and β-MnCl2×4H2O // Journal of Chemical Crystallography. 2021. V. 51. P. 311-316. DOI: 10.1007/s10870-020-00856-z EDN: WJTTYA
- Bernardino M. E., Weinreb J. C., Mitchell D. G., Small W. C., Morris M. Safety and optimum concentration of a manganese chloride-based oral MR contrast agent // Journal of Magnetic Resonance Imaging. 1994. V. 4. №6. P. 872-876. DOI: 10.1002/jmri.1880040620
- Pan D., Schmieder A. H., Wickline S. A., Lanza G. M. Manganese-based MRI contrast agents: past, present, and future // Tetrahedron. 2011. V. 67. №44. P. 8431-8444. DOI: 10.1016/j.tet.2011.07.076 EDN: PHWBDV
- Жук О. Н., Ильючик И. А., Кульгавеня А. Д., Никандров В. Н. Влияние хлорида марганца (II) на протеолитическую активность гриба вешенка обыкновенная (Pleurotus ostreatus) при глубинном культивировании // Вестник Полесского государственного университета. Серия природоведческих наук. 2017. №2. С. 62-68. EDN: YLAFSZ


