Структура микробных сообществ наземных соляных сооружений Пермского края
Автор: Кузнецова М.В., Маммаева М.Г., Кириченко Л.В., Шишкин М.А., Демаков В.А.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 2, 2020 года.
Бесплатный доступ
Изучено разнообразие микробных сообществ наземных соляных сооружений (НСС), расположенных в лечебно-профилактических и санаторно-курортных учреждениях Пермского края. Установлено, что абиотические соляные поверхности всех НСС контаминированы микроорганизмами, при этом выявлена достоверная разница между сильвинитовыми (86.5% положительных проб) и галитовыми (47.4%) сооружениями. Численность жизнеспособных клеток бактерий, в том числе стафилококков, также была выше в сильвинитовых сооружениях, чем в галитовых. На основании бактериологического исследования и анализа нуклеотидных последовательностей гена 16S рРНК изолированные штаммы стафилококков отнесены к следующим видам: Staphylococcus epidermidis -42.3% (n=11), S. aureus и S. saprophyticus - по 19.2% (n=5), S. simulans - 7.7% (n=2), и по одному штамму S. cohnii urealyticum, S. hominis, S. warneri - 3.8%. Видовой состав микробиоценозов поверхностей, определенный методом газовой хроматографии-масс-спектрометрии, включал представителей 18 родов, относящихся к трем крупным филумам Actinobacteria, Firmicutes и Proteobacteria. Актинобактерии были доминирующими в обоих типах НСС. Среди фирмикутов в сильвинитовых НСС превалировали представители рода Clostridium - 63.8% общего количества бактерий, тогда как в галитовых их было в два раза меньше - 32.1%. Содержание кокковой микробиоты, напротив, было почти в 3 раза выше в галитовых сооружениях. Выявленные количественные и качественные показатели микробиоты НСС дополняют представления о структуре микробных сообществ в условиях высокой соляной нагрузки и антропогенного влияния.
Наземные соляные сооружения, микробиоценоз, газовая хроматография-масс-спектрометрия
Короткий адрес: https://sciup.org/147229641
IDR: 147229641 | УДК: 579.63:614.7 | DOI: 10.17072/1994-9952-2020-2-120-127
Structure of microbial communities of the artificial salt constructions of the Perm region
The diversity of microbial communities the artificial salt constructions (ASC) located in the medical-preventive and sanatorium institutions of the Perm region was studied. It was found that the surfaces of the abiotic salt of all ASC were contaminated with microorganisms, and a significant difference was found between the constructions of sylvinite (86.5% of positive samples) and halite (47.4%). The number of viable bacteria, as well as staphylococci, were also higher in sylvinite constructions than in halite ones. Based on bacteriological research and analysis of the 16S rRNA gene nucleotide sequences, the isolated staphylococcus strains belong to the following species: Staphylococcus epidermidis - 42.3% (n=11), S. aureus and S. saprophyticus - 19.2% (n=5), S. simulans - 7.7% (n=2) and one strain of S. cohnii urealyticum, S. hominis, S. warneri - 3.8%. The species composition of microbiocenoses formed on surfaces determined by gas chromatography-mass spectrometry included representatives of 18 genera belonging to the three main phylums: Actinobacteria, Firmicutes and Proteobacteria. Actinobacteria (Actinomyces, Corynebacterium, Nocardia, Propionibacterium, Rhodococcus, etc.) were dominant in both groups ASC. Among Firmicutes, representatives of the genus Clostridium predominated in sylvinite ASC - 63.8% of the total number of bacteria, while in halite they were half as many - 32.1%. The content of coccal microbiota, in contrast, in halite constructions was almost 3 times higher than in sylvinite. Identified quantitative and qualitative indicators of the microbiota of the ASC complement the understanding of the constructions of microbial communities under conditions of high salt load and anthropogenic impact.
Текст научной статьи Структура микробных сообществ наземных соляных сооружений Пермского края
нообразия» [Akhtar et al., 2008]. Возрастание интереса к изучению структуры сообщества микроорганизмов в условиях повышенного засоления среды, с одной стороны, вызвано необходимостью понимания механизмов их длительного выживания в «неростовых» высокоминерализованных природных или искусственных системах [Ventosa et al., 2014]. Другая причина обусловлена прикладным значением – возможностью выделения среди представителей гало-фильных и/или галотолерантных бактерий потенциально перспективных источников биологически активных соединений: ферментов, полимеров, органических веществ с противоопухолевой или антимикробной активностью [Akhtar et al., 2008: Chen et al., 2010; da Silva et al., 2015]. Например, галофильные микроорганизмы различных таксономических групп, продуцирующие вещества с цитотоксической активностью, выделены из образцов рассолов и твердых галогенных образований (отложений каменной соли) на руднике Сипакира (Zipaquirá, Колумбия) [DiazCardenas et al., 2017]. Кроме того, отдельные штаммы или консорциумы солеустойчивых бактерий с высокой биодеградирующей активностью могут быть использованы для утилизации органических отходов, при разработке новых технологий очистки промышленных вод и стоков в условиях засоления [Пастухова и др., 2010; Ястребова, Кошелева, Плотникова, 2016].
Сегодня активно обсуждаются вопросы влияния антропогенного воздействия на микробиоценозы естественных или искусственных пещер [Ikner et al., 2007; Kelly et al., 2009; Engel, 2010]. Обнаружение представителей нормальной или патогенной микробиоты человека, как правило, связывают с интенсивностью антропогенной нагрузки на подземное сооружение. Оказалось, что почти все карстовые источники в юго-западной части штата Иллинойс (США) имеют высокие показатели встречаемости представителей Escherichia coli , Enterococcus spp., Staphylococcus spp. [Kelly et al., 2009]. Известно, что соли обладают угнетающим действием на микроорганизмы, однако многими исследователями выявлена высокая обсеменен-ность воздуха различных соляных сооружений. Ряд публикаций посвящены изучению распространения биологического фактора в подземных шахтах для добычи соли, солелечебницах, а также в санаторных зонах пещер [Akhtar et al., 2008; Frączek, Gorny, 2011; Frączek, Gorny, Ropek, 2013; Gebarowska et al., 2018].
В настоящее время, как в России, так и за рубежом, для лечения и профилактики различных видов соматических и инфекционных заболеваний широко применяются наземные соляные сооружения (НСС) [Sandu et al., 2011; Физиологогигиеническая ..., 2013; Rashleigh, Smith, Roberts, 2014; Zając et al., 2014]. Воздушная среда и абиотические поверхности НСС, используемые для со- летерапии пациентов с заболеваниями органов дыхательной системы, представляют искусственную экосистему, в которой могут накапливаться и персистировать бактерии антропогенного происхождения, обладающие природной солеустойчивостью [Федотова, Горовиц, Баранников, 2005]. Показано, что микробная контаминация воздуха во время сеанса солетерапии составляет от 130‒200 микроорганизмов на 1 м3 [Stirbu, Stirbu, Sandu, 2012]. Дальнейшее выживание микроорганизмов в этих условиях возможно, в первую очередь, на абиотических поверхностях данных сооружений, тем не менее, исследований, направленных на изучение биоразнообразия НСС, в доступной нам литературе не обнаружено.
Цель исследования – изучить структуру микробных сообществ, сформированных на соляных абиотических поверхностях НСС.
Материал и методы
Материал
За период 2017‒2018 гг. исследованы 11 объектов, включающих 7 сильвинитовых и 4 галитовых НСС, расположенных в лечебно-профилактических и санаторно-курортных учреждениях Пермского края. Стены и пол шести сильвинитовых сооружений были облицованы шлифованными соляными блоками, одного – прессованной солеплиткой. Потолок всех сооружений выполнен из деревянных панелей с напылением из природного сильвинита. Галокамеры в основном были выполнены методом напыления соляного материала на ограждающие поверхности с его подсыпкой на пол. В одном из четырех галитовых сооружений для отделки стен и пола использовались шлифованные соляные блоки. Срок эксплуатации соляных сооружений варьировал от 5 месяцев до 24 лет и, в среднем, составлял для сильвинитовых – 11.1±2.8, для галитовых – 2.6±1.8 лет. Показатели всех гигиенических параметров НСС: уровень радиационного фона, концентрации легких отрицательных и положительных аэроионов, микроклимата были в пределах допустимых значений существующих нормативных документов для обоих типов сооружений.
Методы исследования
Для изучения микробного пейзажа образцы проб (n = 71, не менее шести для каждой камеры) отбирали с соляных поверхностей (S = 0.5 м2) сухим способом. Высевы проводили на универсальные (кровяной агар, среда Луриа-Бертани, «Amresco», США) и селективные (солевой агар с маннитом, среда Мак-Конки, среда Сабуро, ООО «ЦФГС», Россия) агаризованные среды методом прямого высева. Уровень бактериальной обсемененности оценивали по общему микробному числу (ОМЧ), отдельно учитывали количество стафилококков, представителей семейства Enterobacteriaceae и кандид. Идентификацию выделенных микроорганизмов осуществляли согласно Приказу МЗ СССР № 535 от 22.04.1985 г. Окончательную идентификацию штаммов стафилококков проводили на основании анализа нуклеотидной последовательности гена 16S рРНК, которую получали с использованием бактериальных праймеров 515F (5′-gtgccagcmgccgcggtaa) и 1391R (5′-gacgggcggtgwgtrca), как описано [Baker et al., 2003], и определяли с применением набора реактивов Big Dye Terminator Cycle Sequencing Kit на автоматическом секвенаторе Genetic Analyser 3500XL («Applied Biosystems», США). Поиск гомологичных последовательностей производили по базе данных GenBank .
Реконструирование таксономического состава до рода/вида проводили после химического извлечения высших жирных кислот, альдегидов, стери-нов и хроматографического разделения пробы методом газовой хроматографии‒масс-спектрометрии (ГХ-МС) согласно [Верховцева, Осипов, 2008] с использованием системы Agilent 6890/5973N («Agilent», США). Липидные компоненты экстрагировали методом кислого метанолиза в 0.4 мл 1 М NaCl в метаноле в течение одного часа при температуре 80°С. Сухой остаток обрабатывали 20 мкл N,O-бис (триметилсилил)-трифторацетамида в течение 15 мин., затем 1‒2 мкл полученной смеси разбавляли гексаном 1:1 и использовали для анализа. Хроматограммы снимали в режиме программирования температуры от 130 до 320°С со скоростью 5°С в мин. Для количественных измерений в качестве внутреннего стандарта использовали тридейтеро-тридеканоат. Результаты анализировали с помощью штатной программы обработки данных и формировали рапорт о реконструированном по биохимическим маркерам составе микробного сообщества.
Статистический анализ данных проводили с использованием программ Microsoft Office Excel и STATISTICA 10. Показатели представлены в виде среднего арифметического и его ошибки (M± m ). Достоверность различий средних величин определяли с помощью t -критерия при уровне достоверности p < 0.05. При сравнении качественных признаков для выявления статистически значимых различий определяли χ² или χ² с поправкой Йейтса.
Результаты и их обсуждение
Методом прямого высева установлено, что абиотические соляные поверхности всех сооружений были контаминированы микроорганизмами. Количество положительных проб варьировало от 20 до 100%, в среднем составив 76.1%, при этом выявлена достоверная разница между сильвинито- выми (86.5%) и галитовыми (47.4%) сооружениями (р = 0.0006). Численность жизнеспособных клеток бактерий, адгезированных на поверхностях, в сильвинитовых сооружениях (4.97E+03±1.32E+04 КОЕ/м2) также была выше, чем в галитовых (1.74E+02±1.68E+02 КОЕ/м2). Уровень обсеме-ненности стафилококками в сильвинитовых сооружениях составил 55.8% (3.11E+02±2.32E+02 КОЕ/м2), тогда как в галитовых – 10.5% (детектированы только в двух пробах), и разница была статистически значима (р = 0.0007). Энтеробактерии встречались в двух сильвинитовых сооружениях, и только в образцах, отобранных с поверхности пола. Жизнеспособные кандиды не выявлены ни в одной пробе.
Получены чистые культуры штаммов стафилококков (n = 26) и проведена их видовая идентификация. Большинство изолированных штаммов принадлежали к виду Staphylococcus epidermidis, в пяти сооружениях обнаружен S. aureus, в единичных пробах – S. warneri, S. simulans, S. cohnii urealyticum и S. saprophyticus. Идентификация отдельных штаммов стафилококков на основании анализа нуклеотидной последовательности гена 16S pPНК показала, что в пяти случаях (19.2%) видовая принадлежность не соответствовала бактериологической идентификации. В результате сравнения нуклеотидной последовательности ам-плифицированных фрагментов гена 16S рРНК изолятов и известных последовательностей гена 16S рРНК типовых штаммов стафилококков распределение выделенных бактерий оказалось следующим: S. epidermidis – 42.3%, S. aureus – 19.2%, S. saprophyticus – 19.2%, S. simulans – 7.7%, и по одному штамму S. cohnii urealyticum S. hominis, S. warneri – 3.8%. Важно, что в настоящее время представители рода Staphylococcus и, в первую очередь, S. aureus рассматриваются как основные «индикаторные бактерии человека», наряду с эше-рихиями и термотолерантными бациллами [Lavoie, Northup, 2006]. Микробиологический анализ, проведенный польскими учеными в двух соляных шахтах «Величка» («Wieliczka») и «Польковице-Серошовице» («Polkowice–Sieroszowice»), одна из которых является старейшей туристической достопримечательностью и спелеолечебницей, а другая – современной промышленной шахтой, выявил, что содержание отдельных видов стафилококков, в частности S. aureus, S. epidermidis, S. haemolyticus или S. saprophyticus, от общего количества бактерий и грибов в шахтах составляет от 1 до 5% [Gebarowska et al., 2018]. Кроме того, штаммы различных видов стафилококков, за исключением S. saprophyticus, были выделены в лечебнице «Соляные копи Бохня» («Kopalnia Soli Bochnia», Польша) [Frączek, Gorny, Ropek, 2013], хотя необходимо отметить, что в упомянутых работах куль- туры изолировали из воздушной среды подземных соляных сооружений. В данном исследовании мы получили сходные показатели и по видовому составу, и по показателю обсемененности: в сильвинитовых сооружениях доля стафилококков от общего количества микроорганизмов (показатель ОМЧ) составила 4.2, в галитовых – 2.3%. Обращает внимание, что S. aureus был выделен только в сооружениях из сильвинита.
Культуральные методы, помимо явных преимуществ (простота выполнения, доступность используемых средств, экономичность) имеют ряд недостатков, связанных с отсутствием универсальной питательной среды, на которой могли бы расти все микроорганизмы, представленные в данной пробе. Кроме этого, большинство микроорганизмов являются некультивируемыми, и, как следствие, малоизученными. Чтобы обойти некоторые ограничения традиционных методик, исследователи используют молекулярные методы, основанные на выделении и анализе нуклеиновых кислот (в основном ДНК) или маркеров клеточной стенки (жирных кислот, альдегидов, спиртов и т.д.) из различных образцов без культивирования микроорганизмов [Верховцева, Осипов, 2008; Engel, 2010].
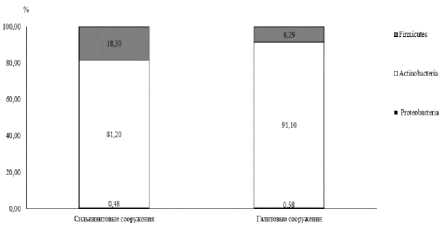
По данным ГХ–МС, в отличие от метода прямого высева, общее количество микроорганизмов было существенно выше и достоверно не различалось: 1.84E+08±7.73E+07 и 1.46E+08±6.46E+07 клеток/м2 в сильвинитовых и галитовых сооружениях, соответственно. Анализ видового состава позволил определить представителей 18 родов, относящихся к трем крупным филумам Actinobacteria, Firmicutes и Proteobacteria (рисунок, А). Актинобактерии ( Actinomyces , Corynebacterium , Nocardia , Propionibacterium , Rhodococcus и др.) были доминирующими в обеих группах: 81.2% в сильвинитовых и 91.1% в галитовых сооружениях (рисунок, Б). Среди фирмикутов в сильвинитовых НСС превалировали представители рода Clostridium ( C. ramosum, C. propionicum ) – 63.8% от общего количества бактерий, тогда как в галитовых их было в два раза меньше – 32.1% (рисунок, В).
Содержание кокковой микробиоты, напротив, было почти в 3 раза выше в галитовых НСС (21.1%), чем в сильвинитовых (7.4%). Бактерии рода Staphylococcus обнаружены во всех соляных сооружениях, представители Streptococcus – в семи из десяти. Протеобактерии выявлены почти в 30% проб, но их доля в микробном спектре не превышала 0.6% от всех микроорганизмов. Более того, детектированы маркеры представителей только 4 таксонов, при этом бактерии родов Alcaligenes и Campylobacter обнаружены только в сильвинитовых НСС. В целом можно отметить, что в сильвинитовых НСС структура микробного сообщества более разнообразная, чем в галитовых. Это может быть связано с более благоприятными условиями для выживания бактерий, так как соли K+ менее токсичны для прокариотов, чем соли Na+, а также с более длительным сроком эксплуатации сильвинитовых сооружений.
А
Proponibaeieriiiin
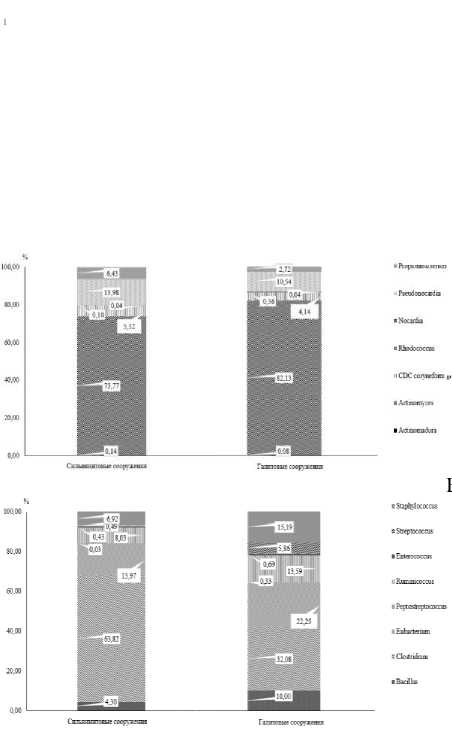
Доли филумов в структуре микробных сообществ НСС (А) и таксономическое распределение представителей внутри филумов Actinobacteria (Б) и Firmicutes (B)
Б
ICDC corynefonn groups
Принимая во внимание отличающиеся условия и методы, использованные для характеристики микробных сообществ в других исследованиях, можно констатировать, что биоразнообразие НСС было существенно меньше, чем принято обнаруживать в соленых озерах [Han et al., 2017], природных пещерах [Engel, 2010] или соляных шахтах [Chen et al., 2007; Diaz-Cardenas et al., 2017]. В большинстве исследований по изучению микробиоценозов в высокоминерализованных средах филумы Actinobacteria, Firmicutes и Proteobacteria являлись доминантными, но их распределение существенно различалось [Chen et al., 2010; Frączek, Gorny, 2011; Claverías et al., 2015; Diaz-Cardenas et al., 2017; Han et al., 2017]. По мнению некоторых ученых, бациллы представляют группу микроорга- низмов, которая более распространена в солесодержащих средах по сравнению с другими таксономическими группами [Akhtar et al., 2008; DiazCardenas et al., 2017]. Биоаэрозольный состав в соляных сооружениях также может способствовать преимущественному распространению осмотоле-рантных бактерий, таких как Bacillus spp. и различные представители семейства Micrococcaceae [Akhtar et al., 2008; Frączek, Gorny, Ropek, 2013; Gebarowska et al., 2018]. В нашем исследовании доля представителей родов Bacillus и Micrococcus оказалась существенно меньше, чем в природных экосистемах или искусственных соляных шахтах. Более значимое представительство отмечено у клостридий, некоторые виды которых входят в состав нормофлоры человека. Что касается протеобакте-рий, наиболее многочисленной и распространенной в соляных шахтах группе бактерий [Chen et al., 2007; Diaz-Cardenas et al., 2017; Han et al., 2017], то они практически не встречались на абиотической поверхности исследованных НСС, а их доля не превышала 0.6% от общего числа микроорганизмов. Доминирующими обитателями в обоих типах сооружений оказались представители рода Actinomyces. Эти микроорганизмы широко распространены в почве и воде, могут выявляться в воздухе как индикаторы загрязнения рабочей и жилой среды. Считается, что их появление в закрытых пространствах связано с повышенной влажностью воздуха [Frączek, Kozdroj, 2013]. Они были обнаружены в большом количестве в соляных шахтах различных регионов мира, а их доля в общем объеме бактерий варьировала от 2 до 15% [Xiao et al., 2007; Diaz-Cardenas et al., 2017; Gebarowska et al., 2018]. Выявленное нами доминирование актинобактерий и, в первую очередь, рода Actinomyces, которые являются сапрофитами человека и в этом качестве обнаруживаются в ротовой полости, тонзиллярных «пробках», верхних дыхательных путях, бронхах и других биотопах, также может служить показателем того, что человеческий фактор является определяющим при формировании микробиоценоза НСС.
Заключение
Естественные или искусственно созданные подземные и наземные соляные сооружения часто специализируются на лечении заболеваний органов дыхания, таких как хронические инфекции верхних и нижних дыхательных путей, аллергия, астма, бронхоэктатическая болезнь. Существует широкое медицинское свидетельство того, что условия внутренней среды в этих сооружениях оказывают полезное влияние на здоровье человека, особенно в случае респираторных заболеваний. Благодаря бактериостатическому эффекту соли, количество и видовой состав микроорганизмов в соляных сооружениях существенно отличаются от других биотопов. Способность бактерий колонизировать абиотические соляные поверхности и сохраняться в НСС ранее не изучалась.
Метод ГХ–МС позволил реконструировать таксономический состав сильвинитовых и галитовых НСС. Идентифицированы представители 18 родов, отнесенные к филумам Actinobacteria, Firmicutes, Proteobacteria, доли которых не различались в двух группах. Полученные данные о значительной численности представителей Actinomyces , обитающих на соляных абиотических поверхностях НСС, позволяют предположить, что они могут быть тем пулом клеток, который «помогает» другим бактериям сохраняться в жизнеспособном состоянии в условиях высокоминерализованной среды. Выявленные количественные и качественные показатели микробиоты соляных сооружений дополняют представления о структуре микробных сообществ в условиях высокой соляной нагрузки и антропогенного влияния. На наш взгляд, больший массив исходных данных о микробной структуре НСС позволит лучше понять распределение микроорганизмов в этой среде обитания и выявить отличительные микробные группы, составляющие постоянных и транзиторных участников экосистемы. В медицинском аспекте, бактериологическим методом выявлена высокая выживаемость как грампо-ложительных, так и грамотрицательных бактерий в условиях повышенной солености. Обнаружена высокая обсемененность поверхностей жизнеспособными стафилококками, включая патогенный S. aureus , которые являются возбудителями оппортунистических инфекций, что необходимо учитывать при разработке методов оптимизации факторов внутренней среды НСС.
Работа выполнена в рамках государственного задания АААА-А19-119112290009-1.
Список литературы Структура микробных сообществ наземных соляных сооружений Пермского края
- Верховцева Н.В., Осипов Г.А. Метод газовой хроматографии-масс-спектрометрии в изучении микробных сообществ почв агроценоза // Проблемы агрохимии и экологии. 2008. № 1. С. 51-54.
- Пастухова Е.С. и др. Бактерии-деструкторы ортофталевой кислоты, выделенные из отходов калийного производства // Вестник Пермского университета. Сер. Биология. 2010. Вып. 3. С. 253-262.
- Федотова М.Ю., Горовиц Э.С., Баранников В.Г. Особенности микрофлоры воздушной среды соляных микроклиматических палат // Пермский медицинский журнал. 2005. Т. 22, № 3. С. 118-121.
- Физиолого-гигиеническая концепция спелео-солелечения / под ред. В. А. Черешнева и др. Екатеринбург, 2013. 183 с.
- Ястребова О.В., Кошелева И.А., Плотникова Е.Г. Структурно-функциональная характеристика бактериального консорциума, выделенного из техногенных почв верхнекамского месторождения солей // Вестник Пермского университета. Сер. Биология. 2016. Вып. 3. С. 253-262.
- Akhtar N. et al. Biodiversity and phylogenetic analysis of culturable bacteria indigenous to Khewra salt mine of Pakistan and their industrial importance // Brazilian Journal of Microbiology. 2008. Vol. 39, № 1. P. 143-150.
- Baker G.C. et al. Review and reanalysis of domain-specific 16S primers // Journal of Microbiological Methods. 2003. Vol. 55, № 3. P. 541-555
- Chen Y.G. et al. Phylogenetic diversity of culturable bacteria in the ancient salt deposits of the Yiping-lang Salt Mine, P.R. China // Acta Microbiologica Sinica. 2007. Vol. 47, № 4. P. 571-577.
- Chen L. et al. Phylogenetic analysis and screening of antimicrobial and cytotoxic activities of moderately halophilic bacteria isolated from the Weihai Solar Saltern (China) // World Journal of Microbiology & Biotechnology. 2010. Vol. 26, № 5. P. 879-888. doi: s11274-009-0247-4
- Claverias F.P. et al. Culturable diversity and antimicrobial activity of Actinobacteria from marine sediments in Valparaiso bay, Chile // Frontiers in Microbiology. 2015. Vol. 6, № 737. P. 1-11. doi: 10.3389/fmicb.2015.00737
- da Silva F.S. et al. Unexplored Brazilian oceanic island host high salt tolerant biosurfactant-producing bacterial strains // Extremophiles. 2015. Vol. 19, № 3. P. 561-572. doi: 10.1007/s00792-015-0740-7.
- Diaz-Cardenas С. et al. Microbial diversity of saline environments: searching for cytotoxic activities // AMB Express. 2017. № 7. P. 223.
- Engel A.S. Microbial Diversity of Cave Ecosystems // Geomicrobiology: Molecular and Environmental Perspective. 2010. P. 219-238.
- Frqczek K., Gorny R.L. Microbial air quality at Szczawnica sanatorium, Poland // Annals of Agricultural and Environmental Medicine. 2011. Vol. 18, № 1. P. 63-71.
- Frqczek K., Gorny R.L., Ropek D. Bioaerosols of sub-terraneotherapy chambers at salt mine health resort // Aerobiologia. 2013. Vol. 29, № 4. P. 481-493.
- Frqczek K., Kozdroj J. Assessment of airborne Acti-nomycetes in subterranean and earth sanatoriums // Ecological Chemistry and Engineering S. 2013. Vol. 20, № 1. P. 151-161.
- Gebarowska E. et al. Comparative analysis of airborne bacteria and fungi in two salt mines in Poland // Aerobiologia. 2018. Vol. 34, № 2. P. 127-138.
- Han R. et al. Microbial community structure and diversity within hypersaline Keke Salt Lake environments // Canadian Journal of Microbiology. 2017. Vol. 63, № 11. P. 895-908. doi: 10.1139/cjm-2016-0773.
- Ikner L.A. et al. Culturable microbial diveristy and the impact of tourism in Kartchner Caverns, Arizona // Microbial Ecology. 2007. Vol. 53, № 1. P. 30-42.
- Kelly W.R. et al. Bacteria contamination of ground-water in a mixed land-use karst region // Water Quality, Exposure and Health. 2009. Vol. 1, № 2. P. 69-78.
- Lavoie K.H, Northup D.E. Bacteria as indicators of human impact in caves // In: Rea GT (ed) 7th National Cave and Karst Management Symposium, Proceedings. NICKMS Steering Committee, Albany, NY. 2006. P. 40-47.
- Rashleigh R., Smith S.M., Roberts N.J. A review of halotherapy for chronic obstructive pulmonary disease // International Journal of Chronic Obstructive Pulmonary Disease. 2014. Vol. 9. P. 239-246.
- Sandu I. et al. The effects of salt solions on the health of human subjects // Present Environment and Sustainable Development. 2011. Vol. 5, № 2. P. 67-88.
- Stirbu C., Stirbu C., Sandu I. Impact assessment of saline aerosols on exercise capacity of athletes // Procedia - Social and Behavioral Sciences. 2012. Vol. 46. P. 4141-4145.
- Ventosa A. et al. The Santa Pola saltern as a model for studying the microbiota of hypersaline environments // Extremophiles. 2014. V. 18. P. 811-824.
- Xiao W. et al. Prokaryotic microbial diversity of the ancient salt deposits in the Kunming Salt Mine, P.R. China // Acta Microbiologica Sinica. 2007. Vol. 47, № 2. P. 295-300.
- Zajqc J. et al. Salt caves as simulation of natural environment and significance of halotherapy // Annals of Agricultural and Environmental Medicine. 2014. Vol. 1, № 21. P. 124-127.


