Структурная организация микрососудистого русла тонкой кишки
Автор: Кудряшова Валентина Николаевна, Маркова Валерия Игоревна, Моисеева Татьяна Васильевна
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 3 т.22, 2014 года.
Бесплатный доступ
Данные о структурной организаций микрососудистого русла тонкой кишки практически отсутствуют. Это связано с тем, что значительная часть информации о нём получена инъекционными способами, не позволяющими выявить гистоструктуру стенки микрососудов. Методические трудности и до настоящего времени ограничивают возможности изучения микрососудистого русла тонкой кишки в различные периоды её функциональной деятельности, функционального покоя и на высоте кишечного пищеварения. Цель работы: получить новые достоверные данные о структурной организации микрососудистого русла тонкой кишки сочетанным методом интра-экстрасосудистой импрегнации солями серебра. Полученные данные позволили выявить в различных отделах тонкой кишки диапазон пищеварительной реакции микрососудистого русла. Эти данные несомненно имеют не только теоретическое но и клиническое значение.
Тонкая кишка, микрососудистое русло, методы выявления
Короткий адрес: https://sciup.org/143176999
IDR: 143176999
Structural organization of the small intestine microvasculature
Data on the structural organization microvasculature of the small intestine are very scarce. This results from the fact that major part of these data have been obtained by means of injection which does not allow to detect the histostructure of the microvessel wall. To the present day, these methodological difficulties have been restricting the studies of microvasculature of the small intestine at different periods of its functional activity, at functional rest and at the height of intestinal digestion. The aim of the work: obtaining new valid data on the structural organisation of the small intestine microvasculature by the combined method of intra- and extravascular argentation. The obtained data have made it possible to find a range of microvasculature digestive reactions in various intestine parts. These data are evidently of both theoretical and clinical value.
Текст научной статьи Структурная организация микрососудистого русла тонкой кишки
Введение. Через тонкую кишку осуществляется передвижение значительных масс жидкости. Коэффициент капиллярной фильтрации в ней составляет 0,10 мл/мин (мм.рт.ст)/100г ткани [1] или в 30 раз выше, чем в капиллярах скелетных мышц. В связи со способностью реабсорбции белков и их составных частей, тонкая кишка рассматривается как «большой нефрон», ее содержимое сравнивается с первичной мочой, а резорбирующий эпителий – с эпителием почечных канальцев. Кроме того, в тонкой кишке осуществляется тесный контакт внутренней среды организма с окружающей его внешней средой. В ней происходит «переход чужих веществ из внешней среды в свою внутреннюю среду организма» [2, с. 145]. На основе концепции о гоместатированной энтеральной среды [2] и новой информации о механизмах ее формирования [3] был сформулирован важный вывод о том, что «биологический смысл совокупностей функций пищеварительной системы заключается в формировании плазмы крови» [3, с. 187].
Цель исследования - получить новые достоверные данные о структурной организации ми-крососудистого русла тонкой кишки сочетанным методом интра-экстрасосудистой импрегнации солями серебра. Полученные данные позволили выявить в различных отделах тонкой кишки диапазон пищеварительной реакции микрососудистого русла. Эти данные несомненно имеют не только теоретическое но и клиническое значение.
Материал и методы исследования. Работа проведена на беспородных собаках (n=7) обоего пола массой 12-18 кг, содержавшихся в виварии Самарской ветеринарной клинике «Друг» (главный врач – доцент В.А.Ваньков). Обращение с животными регламентировалось Международными и Российскими этическими нормативами. Материалом исследования служили препараты тонкой кишки инъецированные слабыми растворами азотнокислого серебра [4, 5] с предварительным повышением аргирофилии стенки кровеносных и лимфатических микрососудов перфузией раствора Ba(OH)2 [6]. Дальнейшие манипуляции: 1) фиксация фрагментов тонкой кишки в 15% раство-
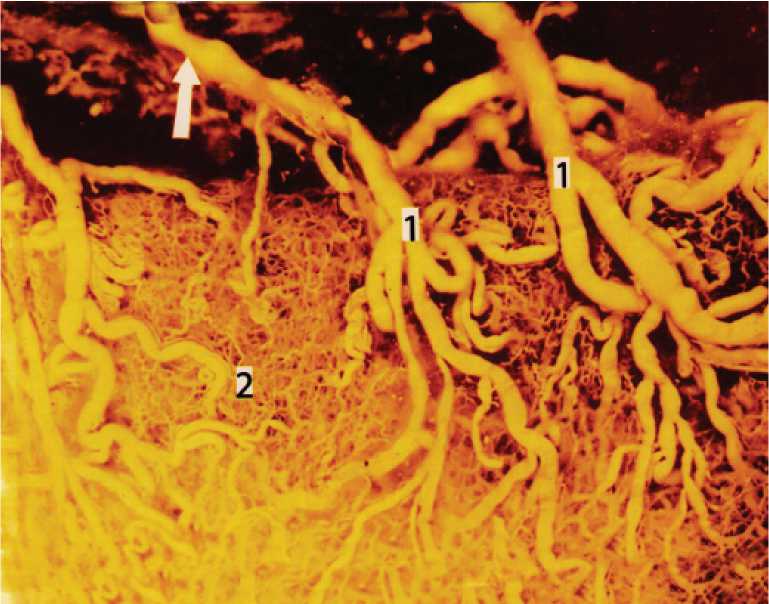
Рис. 1. Прямые артерии (1) с выраженной флюктуацией (1) вступающие в стенку (2) тонкой кишки собаки. Импрегнация по И.И.Маркову. Тотальный препарат. Ув. 16.
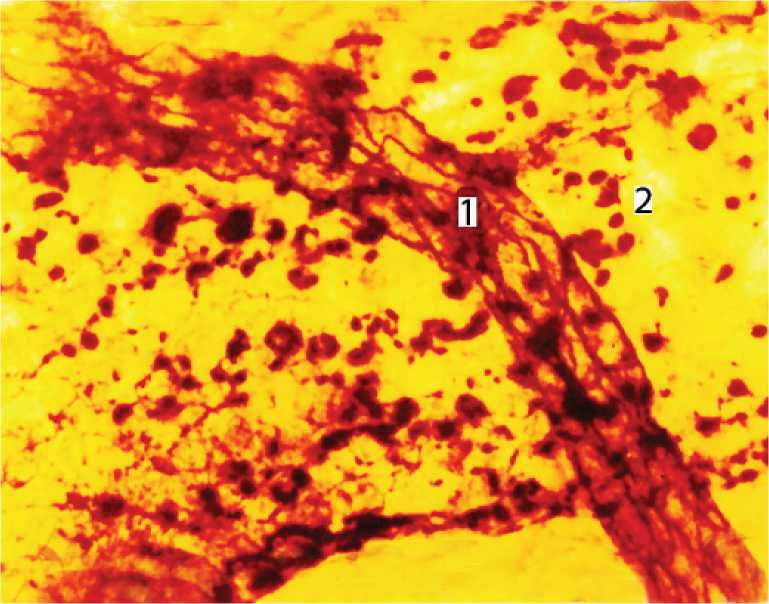
Рис. 2. Расположение венулы (2) на стенке лимфатического микрососуда (1) в подслизистой основе тонкой кишки собаки. Импрегнация по И.И.Маркову. Ув. 200.
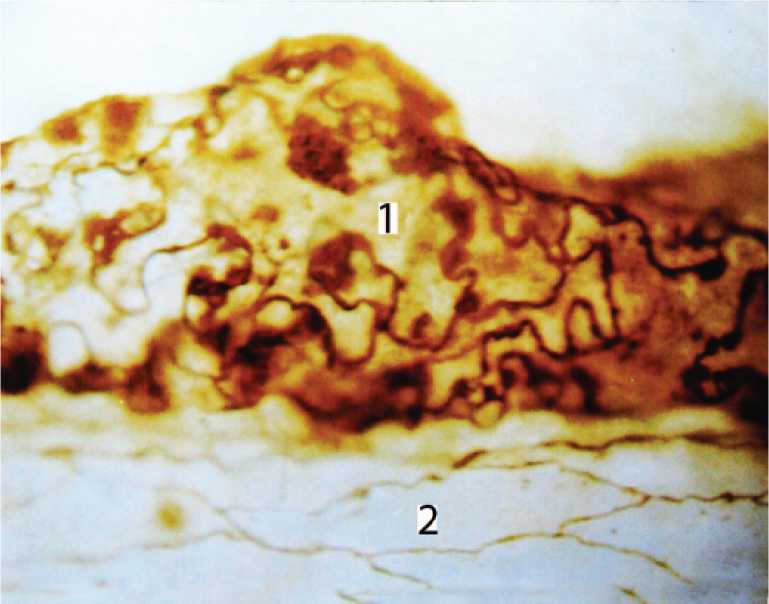
Рис. 3. Лимфо-венозный контакт в межмышечной микрососудистой сети. 1) лимфатический микрососуд; 2) вена. Импрегнация по И.И.Маркову. Ув. 200.
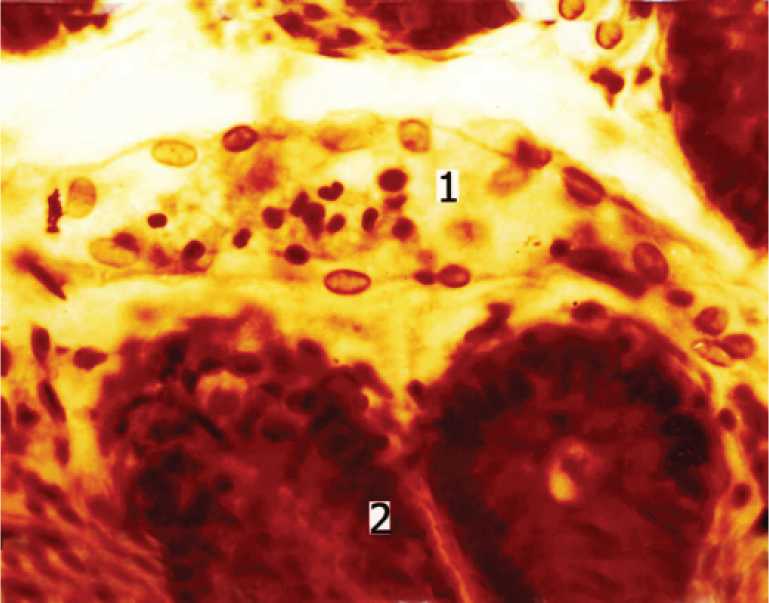
Рис. 4. Лимфатический капилляр (1) в слизистой оболочке тонкой кишки собаки сочетанная импрегнация по В.И.Кошеву. Ув. 200.
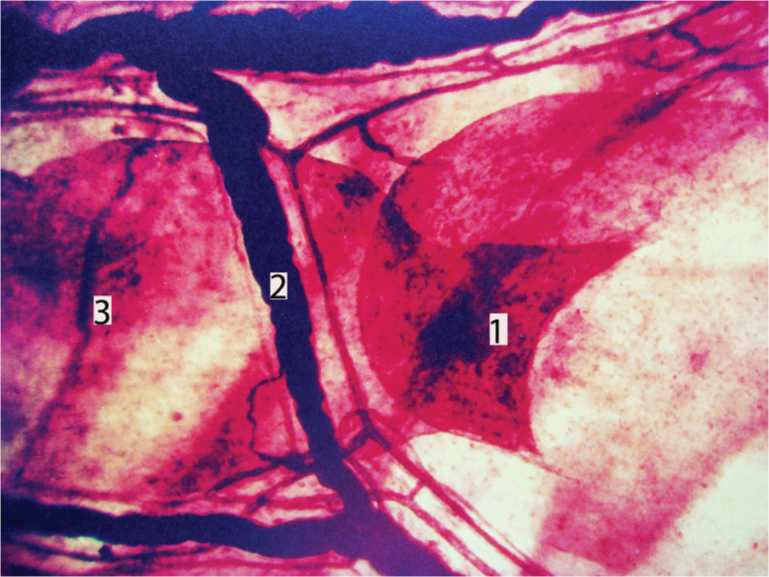
Рис. 5. Лимфатический микрососуд (3) в подслизистой основе тонкой кишки собаки. 1) клапан; 2) нервный ствол. Импрегнация по В.И.Кошеву. Ув. 200.
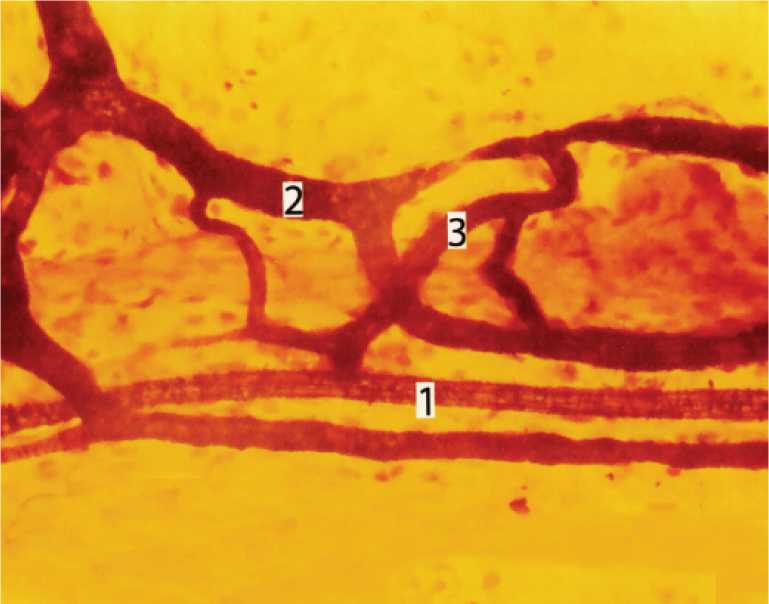
Рис. 6. Артериоло-венулярный анастомоз (3) в межмышечной микросо-судистой сети тонкой кишки собаки. 1) артериола; 2) венула. Импрегнация по И.И.Маркову. Ув. 200.
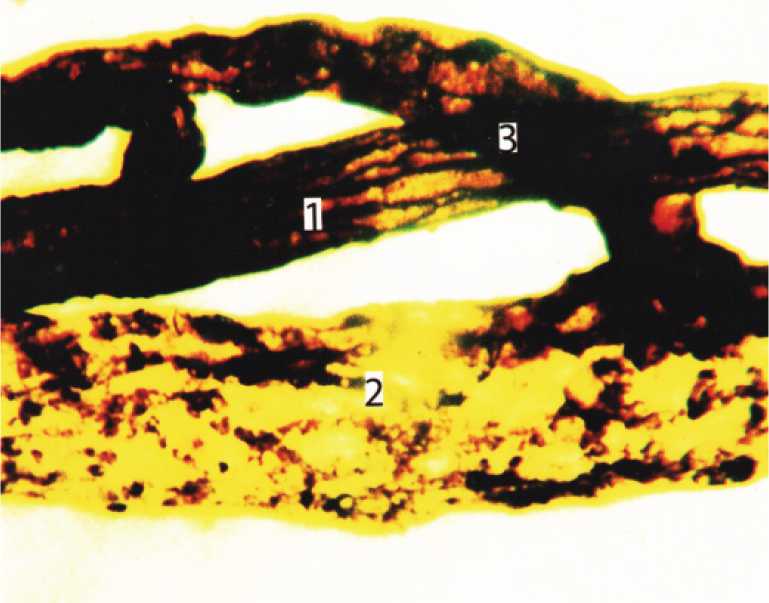
Рис. 7. Артериоло-венулярный анастомоз (3) в подслизистой основе тонкой кишки сытой собаки. 1) артериола; 2) венула. Импрегнация по И.И.Маркову. Ув. 200.
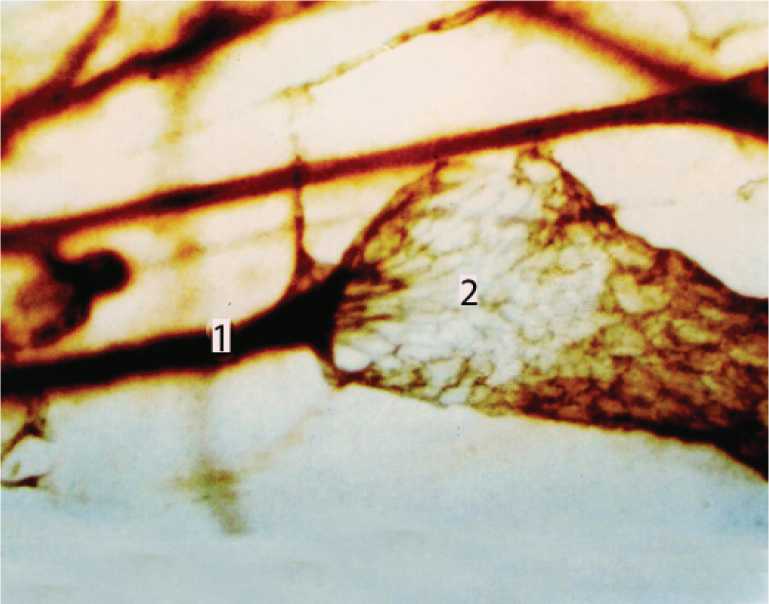
Рис. 8. Артериоло-венулярный анастомоз в подслизистой основе тонкой кишки голодной собаки. 1) артериола; 2) венула. Импрегнация по И.И.Маркову. Ув. 100.
ре аметанального формалина; 2) приготовление замороженных срезов или тотальных расслоенных препаратов стенки кишки; 3) импрегнация в растворе азотнокислого серебра (от 1% до 10%).
Результаты исследования и их обсуждение. Прямые артерии вступают в стенку тонкой кишки, а прямые вены и лимфатические сосуды выходят из нее через мышечные «ворота» в продольном слое мышечной оболочки [4]. Причем, достаточно часто одни мышечные «ворота» пропускают только артерии, другие – только вены. По гистоструктуре прямые артерии – это артерии мышечного типа, а по гидродинамическим понятиям – это конфузоры. На препаратах (рис. 1) удалось зафиксировать флюктуации просвета прямых артерии, т.е. они по всей вероятности, функционируют как перистальтические периферические насосы [7]. На фронтальных срезах тонкой кишки достаточно демонстративно выявляются взаимоотношения мышечных «ворот» с проходящими через них сосудами. Значительный диапазон просвета этих сосудов – от полной их компрессии до значительного расширения – свидетельствует о влияние на них сократительной активности продольного слоя мышечной оболочки. В стенке тонкой кишки сформированы три параллельно включенных в кровоток микрососудистых сети: подсерозная, межмышечная и подслизистая. Все они имеют один общий источник формирования – прямые артерии. Геометрия артериальных ветвлений в каждый из микрососудистых сетей различна. В подслизистой основе – это система аркад, а межмышечной и подсерозной сетях – система тройников.
Радиусы аркад и углы тройников в одних и тех же участках сетей у голодных и сытых животных всегда различны. Это связано с тем что во время перистальтики кишки радиусы и углы периодически изменяются: при растяжении ее – увеличиваются, а при сокращении – уменьшаются. Введенное в физиологию понятие – коэффициент капиллярной фильтрации [8] – зависит от двух параметров: числа функционирующих капилляров и проницаемости стенки микрососудов. Оценка морфофункционального состояния микрососу-дистого русла тонкой кишки путем одновременного выявления функционирующих и закрытых микрососудов [4] на гистологических препаратах позволяет судить о состоянии этих двух параметров. Использование слабых растворов азотнокислого серебра (0,05%) в качестве маркера проницаемости не противоречит современным взглядам на значение морфологических методов в исследование транскапиллярного обмена [9]. Коэффициент выхода маркера через стенку венул подслизистой основы у голодных собак составлял 46% (отношение длины проницаемого участка к длине венулы). У сытых собак (через 90 мин после кормления) – коэффициент увеличивался до 97%. При этом межэндотелиальные граница микрососудов становились широкими, грубыми, а цитоплазма эндотелиоцитов гомогенно импрегни-ровалась серебром. В связи с увеличением проницаемости кровеносных микрососудов и выходу раствора азотнокислого серебра из кровеносного русла происходит резорбции его лимфатическими микрососудами. На этом принципе и основан способ импрегнации внутриорганных лимфатических микрососудов [5], позволивший получить новые данные об их топографии, гистоструктуре и взаимоотношениях с кровеносными микрососудами. Особенности гематолимфатических отношений – расположение кровеносных микрососудов на стенке лимфатических микрососудов, отсутствие между ними посредника – рыхлой соединительной ткани – позволяют сбрасывать в лимфатическое русло значительные объемы ультрафильтрата плазмы крови, а не интерстициальной жидкости (рис. 2, 3).
Избыточный объем первичной лимфы обеспечивает эффективный дренаж лимфоцитов русла тонкой кишки. Появление в первичной лимфе лимфацитов – объясняется переходом их из венул в лимфатические капилляры (рис. 4) и посткапилляры. Значительная часть лимфатического русла подслизистой основы представлена лимфатическими посткапиллярами (рис.5) со сложным клапанным аппаратом. Это не складки эндотелия, а инвагинат узкого конца дистального лимфатикса в расширенный конец проксимального его сегмента. При этом формируется дубликатура эндотелия в виде уплощенной воронки, которая свободно свисает в просвет лимфатического микрососуда в виде лепестка со щелевидным просветом [6]. В органах, выполняющих фазные функции, в том числе и в тонкой кишке, существуют артериоло-вену-лярные анастомозы [10]. Артериоло-венулярные анастомозы формируются за счет разнообразных по форме связей, не имеющих капиллярного сегмента. Через анастомозы осуществляется постоянный кровоток. Об этом свидетельствует постоянное их выявление при интрасосудистой импрегнацией (рис. 6). В стенке тонкой кишки голодных собак в связи с функциональной редукцией капиллярного русла выявляется большое количество прямых пре-посткапиллярных сообщений. Создается иллюзия многочисленных вне-капиллярных путей кровотока. Однако при докра-ске этих препаратов гематоксилином выявляются нефункционирующие капилляры, ответвляются от этих прямых путей кровотока. В стенке тонкой кишки временно закрытых артериоло-венулярных анастомозов нет ни у сытых (рис. 7), ни у голодных (рис. 8) собак.
Заключение. Механизмы, обеспечивающие пищеварительный гомеостаз в тонкой кишке, значительно сложнее механизмов, поддерживающих газовый гомеостаз [11]. Именно поэтому структурная организация ее микрососудистого русла является достаточно сложной. Считается, что основным и постоянным «вызовом» гемеостазу является прием пищи [12]. Однако до настоящего времени существуют различные концепции возникновения функциональной гиперимии слизистой оболочки тонкой кишки. Среди них наиболее обоснована концепция о гидролизатах белка и жира как стимуляторов желудочно-кишечных гормонов [13]. Концепция о регулирующем влиянии мышечной оболочки на кровоток в стенке тонкой кишки [14] не получила в свое время должной оценки, а позже вообще была отвергнута [15-17]. Наши данные указывают на то, что функциональное состояние тонкой кишки оказывает прямое воздействие на проходящие через ее мышечные «ворота» кровеносные и лимфатические сосуды, формируя простые по конструкции перистальтические насосы. Они аналогичны «венозным помпам» нижних конечностей и «лимфатическому сердцу» грудного протока.
Кроме того, кровеносные микрососуды стенки тонкой кишки во время перистальтики подвергаются периодической деформации. При этом в микрососудистом русле возникают участки с переменным гидродинамическим сопротивлением, функционирующие как микронасосы. Согласно уравнениям механики жидкости, изменение углов и радиусов дуг в ответвлениях трубопроводов приводит к увеличению или уменьшению гидродинамических потерь в трубопроводах в значительном диапазоне (до 60 раз) [18].
Особое значение в поддержании адекватного кровотока в тонкой кишке имеют артерио-ло-венулярные анастомозы и особые интимные гематолимфатические отношения. Артериоловенулярные анастомозы способствуют снижению периферического сосудистого сопротивления, возникновению феномена быстрого заполнения вен [19] и выраженной дилататорной сосудистой реакции при механическом раздражении слизистой оболочки тонкой кишки [20]. Сочетание шлюзовой и нутритивной функции – предполагает участие артериоло-венулярных анастомозов в запуске восходящей дилятации верхней брыжеечной артерии при усилении моторной деятельности тонкой кишки при пищеварении. Наличие артериоло-венулярных в микрососудистом русле тонкой кишки есть биологическая целесообразность, формирование их происходит поздно и филогенезе, и в онтогенезе [21].
Список литературы Структурная организация микрососудистого русла тонкой кишки
- Richardson D.R. Compression of autoregulatory escape and autoregulation in the intestinal vascular bed / D.R.Richardson, P.C.Johnson // Amer. J. Physiol., 1969, v 217, p. 586 - 590.
- Синещеков А.Д. Биология питания сельскохозяйственных животных/ М. Колос, 1965, 399 с.
- Алиев А.А. Липидный обмен и продуктивность жвачных животных/ М. Колос, 1980, 381 с.
- Марков И.И. Морфологические аспекты хронической ишемии желудочно-кишечного тракта /Изд. Саратовского ун-та. Самара, 1991, 167 с.
- Марков И.И. Импрегнация внутриорганного лимфатического русла по Ранвье /И.И.Марков // Арх. анат., 1985, № 6, с. 77 - 79.
- Эндолимфососудистая контрактильная трабекулярная система: Монография // В.И.Кошев, Е.С.Петров, И.И.Марков и др. - Самара, 2010, 193 с.
- Титов В.Н. Анатомические и функциональные основы эндотелий-зависимой вазодилятации, оксид азота и эндотелин. Артериолы мышечного типа как перистальтические насосы / В.Н. Титов // Усп. совр. биол., 2010, № 4, с. 360 - 380.
- Landis E.M. Heteroposity of the capillary wall as indicated by cinematography analysis of the passage of dyes / E.M.Landis //Ann. N. Y. Acad. Sci., 1964, v 116, p. 765 - 770.
- Чернух А.М. Микроциркуляция / А.М.Чернух, П.А.Александров, О.В.Алексеев // М.Медицина, 1975, 456 с.
- Baez S. Microcirculation in the intramural vessees of the small intestine in the rat / S.Baez // The Microcirculation, Univ. Jllinois Press "Urbana", 1959, p. 114 - 128.
- Гальперин Ю.М., Лазарев П.И. Пищеварение и гомеостаз / М. Наука, 1986, 304 с.
- Bloom S.R. Glucagon a stress hormone / S.R.Bloom//Postgraduabe Med. J., 1973, v. 49, p. 607 - 612.
- Fara J.W. Jntestinal hormones in mesenteric vasodilatation after intraductonalagents/J.W.Fara, E.H.Rubinsten//Amer. J. Physiol., 1972, v. 223, p. 1067 - 1070.
- Beneke R. Anatomische Folgen reflectorischer Angiospasmen /R.Beneke//München. Ved. Ztschr., 1931, Bd. 78, S. 1831 - 1840.
- Chou C.C. Localization of mesenteric hyperemie durind digestion in dog/ C.C.Chou, Y.M.Yu //Amer. J. Physiol., 1974, v. 230, p. 42 - 47.
- Grayson J. The measurement of intestinal blood flow in man / J.Grayson // J. Physiol., 1951, v. 114, p. 419 - 434.
- Grander H.J. Jntrinsic regulation of intestinal oxygenation in the anesthetized dog/ H.J.Grander, C.P.Norris//Amer. J. Physiol., 1979, v. 239, p. 248 - 251.
- Лойцянский Л.Г. Механика жидкости и газа / М.Наука, 1987, 840 с.
- Сигал М.З. Интраорганная гемодинамика в полых органах при операциях в брюшной полости / Казань, 1980, 234 с.
- Shepherd A.P. Jntestinal capillary blood flow during metabolic hyperemia /A.Shepherd//Amer. J. Physiol., 1979, v. 237, p. 548 - 554.
- Куприянов В.В. Пути микроциркуляции/Кишинев, Картя Молдовенякэ, 1969, 260 с.


